Professional Documents
Culture Documents
Gentechnologia
Gentechnologia
Uploaded by
Nagy DóraCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Gentechnologia
Gentechnologia
Uploaded by
Nagy DóraCopyright:
Available Formats
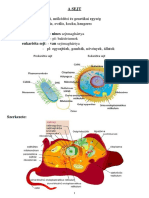
Gntechnolgia
s
fehrjemrnksg
elektronikus-jegyzet
szerzk: Az ELTE Biokmiai Tanszk Munkakzssge
Alexa Anita (12. s 13. fejezet), Fodor Krisztin (3. s 9. fejezet),
Garai gnes (4. s 5. fejezet), Glatz Gbor (6. s 7. fejezet),
Radnai Lszl (1. s 2. fejezet), Rapali Pter (11. fejezet),
Szakcs Dvid (8.. 16. s 17. fejezet), Vrkuti Boglrka (15. fejezet),
Zeke Andrs (10. s 14. fejezet)
szerkeszt: Nyitray Lszl
szakmai lektor: Vrallyay va
Budapest, 2013
2
Gntechnolgia s fehrjemrnksg
rtk: Az ELTE Biokmiai Tanszk munkakzssge
Alexa Anita (12. s 13. fejezet), Fodor Krisztin (3. s 9. fejezet),
Garai gnes (4. s 5. fejezet), Glatz Gbor (6. s 7. fejezet),
Radnai Lszl (1. s 2. fejezet), Rapali Pter (11. fejezet),
Szakcs Dvid (8.. 16. s 17. fejezet), Vrkuti Boglrka (15. fejezet),
Zeke Andrs (10. s 14. fejezet).
szerkesztette: Nyitray Lszl (nyitray@elte.hu)
lektorlta: Vrallyai va
Ksznetnyilvnits: Az elektronikus jegyzet a TMOP-4.1.2.A/1-11/-1-2011-0073 ( E-learning
termszettudomnyos tartalomfejleszts az ELTE TTK-n) s a TMOP 4.2.4.A/1-11-1-2012-0001 (Nemzeti
Kivlsg Program - Hazai hallgati, illetve kutati szemlyi tmogatst biztost rendszer kidolgozsa s
mkdtetse orszgos program; tmogatott: Vrkuti Boglrka) plyzatok tmogatsval kszlt.
Szerzi jog 2013 ELTE TTK Biolgiai Intzet. E knyv kutatsi s oktatsi clokra szabadon
hasznlhat. Brmilyen formban val sokszorostsa a jogtulajdonos rsos engedlyhez kttt.
3
ELSZ 11
1. A GNTECHNOLGIA TRTNETNEK MRFLDKVEI 13
1.1. Az rktanyag felfedezstl a genetikai kd megfejtsig 13
1.1.1. A DNS felfedezse s a klibaktrium lersa 13
1.1.2. A DNS rktanyag szerepnek tisztzsa 14
1.1.3. A DNS kettshlix felfedezse, a genetikai kd megfejtse 15
1.2. A DNS manipullsra alkalmas enzimek felfedezse 17
1.3. A rekombinns DNS technika megjelense 18
1.4. Hibridizcin alapul technikk megjelense 19
1.5. A szekvenlstl a genom korszakig s tovbb 20
1.5.1. A polimerz lncreakci felfedezse 21
1.5.2. Gntechnolgiai eljrsok magasabbrend szervezetekben 21
1.6. Tovbbi olvasnival a fejezethez 22
2. A GNTECHNOLGIA ALAPJA: MOLEKULRIS KLNOZS 23
2.1. In vitro rekombinci 23
2.2. Rekombinns DNS ltrehozsa 24
2.3. Molekulris klnok kialaktsa 25
2.4. Tovbbi olvasnival a fejezethez 26
3. DNS MDOST ENZIMEK S FELHASZNLSUK 27
3.1. DNS-polimerzok 27
3.1.1. A DNS-polimerz I s a Klenow-fragmentum 29
3.1.2. T4 DNS-polimerz 30
3.1.3. T7 DNS-polimerz 30
3.1.4. Hstabil DNS-polimerzok 31
3.1.4.1. Taq-polimerz 31
3.1.4.2. Pfu-polimerz 31
3.1.4.3. Phusion-polimerz 31
3.1.5. Reverz transzkriptz 32
3.2. Nuklezok 32
3.2.1. Restrikcis endonuklezok 32
3.2.1.1. I-es tpus restrikcis endonuklezok 33
3.2.1.2. II-es tpus restrikcis endonuklezok 33
3.2.1.3. III-as tpus restrikcis endonuklezok 34
3.2.1.4. IV-es tpus restrikcis endonuklezok: 34
3.2.2. Egyb nuklezok 35
3.2.2.1. S1-nuklez 35
3.2.2.2. Dezoxiribonuklez (DN-z) I 35
3.3. DNS-ligzok 35
3.4. Vgmdost enzimek 36
3.4.1. Terminlis transzferz 36
3.4.2. Alkalikus foszfatz 37
3.4.3. T4 polinukleotid-kinz 38
4
3.5. Tovbbi olvasnival a fejezethez 38
4. ALAPMDSZEREK S REKOMBINNS DNS KONSTRUKCIK TERVEZSE 39
4.1. Alapmdszerek 39
4.1.1. A DNS tiszttsa s analzise 39
4.1.1.1. Oldatok, reagensek 39
4.1.1.2. Plazmid DNS preparls 40
4.1.1.3. A DNS koncentrci meghatrozsa 41
4.1.2. Glelektroforzis 41
4.1.2.1. Agarz glelektroforzis 41
4.1.2.2. Poliakrilamid glelektroforzis (PAGE) 43
4.1.2.3. A DNS-ek mretnek meghatrozsa 43
4.1.2.4. DNS-ek izollsa agarz glbl 44
4.1.2.5. Restrikcis trkpezs 45
4.1.3. Hibridizcis technikk s nukleinsav prbk 46
4.1.3.1. Nukleinsav prbk ellltsa s jellse 46
4.1.3.2. Southern-blot (lenyomat) technika s az RFLP mdszer 47
4.1.3.3. Northern-blot 49
4.1.3.4. In situ hibridizci, kariotipizls 49
4.1.3.5. DNS-chip (microarray) technika 50
4.2. Rekombinns konstrukcik tervezse 51
4.2.1. Az inszert ellltsa 52
4.2.1.1. Genomilis DNS inszert 52
4.2.1.2. mRNS izolls s cDNS inszert 53
4.2.2. A vektor elksztse 53
4.2.3. Ligls 54
4.2.4. TA/Topo-klnozs 55
4.2.5. Ligls-fggetlen klnozs 56
4.2.6. Restrikcis hasts nlkli ligls rekombincival (attB, attP) 57
4.3. Gnbeviteli eljrsok 57
4.3.1. Transzformls 57
4.3.2. Transzfektls 58
4.3.3. Elektroporci 58
4.3.4. Infekci 59
4.3.5. Gnpuska 59
4.4. Tovbbi olvasnival a fejezethez 59
5. DNS SZEKVENLS 60
5.1. Kmiai szekvenls: radioaktv vgjellt templt 60
5.2. Enzimatikus szekvenls: lnctermincis mdszer 60
5.2.1. Manulis lnctermincis szekvenls 61
5.2.2. Automata fluoreszcens szekvenls 63
5.3. j-genercis szekvenls 65
5.3.1. Piroszekvenls 65
5.3.2. Illumina/Solexa szekvenls 67
5.3.3. SOLiD (Sequencing by Oligonucleotid Ligation and Detection) 68
5.3.4. TSMS (True Single Molecule Sequencing: Valdi egymolekuls szekvenls) 68
5.3.5. SMRT (Single Molecule Real-time: Egymolekuls valsidej) szekvenls 69
5.4. Tovbbi olvasnival a fejezethez 69
6. POLIMERZ LNCREAKCI (PCR) 70
5
6.1. A PCR lpsei 70
6.1.1. Denaturls 70
6.1.2. Anellls 71
6.1.3. Polimerizci/lnchosszabbts (extenzi) 71
6.2. A PCR reakci komponensei 72
6.2.1. PCR templt 73
6.2.2. PCR enzimek 73
6.2.3. PCR primerek 74
6.2.4. Egyb PCR komponensek 74
6.3. A PCR termk (amplikon) detektlsa s kvantitatv PCR 75
6.3.1. Agarz s poliakrilamid glelektroforzis 75
6.3.2. Vals idej (real-time) vagy kvantitatv (q-) PCR 75
6.4. A PCR az alapkutatsban 77
6.4.1. A PCR termk (amplikon) klnozsa s klnozs PCR-rel 77
6.4.2. Szekvenls PCR kszlkben 77
6.4.3. Mutagenezis 78
6.4.3.1. Random (error prone: hibt ejt) PCR mutagenezis 78
6.4.3.2. Helyspecifikus mutagenezis PCR-rel 78
6.4.4. Reverz transzkripcis (RT-) PCR 78
6.4.5. Tovbbi PCR mdszerek (random, fzis, multiplex, fszkes s inverz) 79
6.5. PCR az alkalmazott kutatsban 81
6.5.1. Orvosi diagnosztika 81
6.5.2. Igazsggyi orvostan (DNS ujjlenyomat) 82
6.5.3. s-PCR 82
6.6. Tovbbi olvasnival a fejezethez 83
7. VEKTOR-GAZDA RENDSZEREK 84
7.1. A vektorok ltalnos jellemzi 85
7.1.1. Klnoz s expresszis vektorok 85
7.1.2. Antibiotikum rezisztencia gnek 86
7.2. Plazmid vektorok 87
7.2.1. A plazmidok ltalnos jellemzi 87
7.2.2. A pBR322 vektor 88
7.2.3. A pUC vektorcsald 89
7.2.3.1. A kk-fehr szelekci 90
7.2.4. Fgmidok 91
7.3. Bakteriofg vektorok 92
7.3.1. -fg vektorok 92
7.3.2. M13-alap vektorok 93
7.4. Kozmidok 94
7.5. Mestersges kromoszmk (PAC, BAC, YAC, HAC) 94
7.6. leszt s egyb eukarita vektorok s gazdasejtek 95
7.7. Tovbbi olvasnival a fejezethez 96
8. REKOMBINNS DNS KNYVTRAK 97
8.1. A knyvtrak tpusai 97
8.2. Genomilis DNS knyvtrak 97
6
8.2.1. A genomilis knyvtrak ltrehozsrl ltalban 97
8.2.2. Knyvtr vektorok 99
8.2.3. -fg knyvtrak 99
8.2.3.1. -fg knyvtrak ltrehozsa 100
8.2.3.2. -fg knyvtrak szaportsa, a knyvtr fenntartsa 102
8.2.3.3. A -fg knyvtrak szrse (szkrnelse) plakk hibridizcival 102
8.2.4. Kozmid knyvtrak 104
8.2.4.1. Kozmid knyvtrak ltrehozsa 104
8.2.4.2. Kozmid knyvtrak szaportsa, a knyvtr fenntartsa 105
8.2.4.3. A kozmid knyvtrak szrse kolnia hibridizcival 105
8.2.5. Mestersges kromoszma knyvtrak (BAC s YAC) 106
8.2.5.1. Mestersges bakterilis kromoszma (BAC) knyvtrak ltrehozsa 106
8.2.5.2. BAC knyvtrak szrse s fenntartsa 107
8.2.5.3. leszt mestersges kromoszma (YAC) knyvtrak s ltrehozsuk 107
8.2.5.4. YAC knyvtrak fenntartsa s szrse 108
8.2.5.5. A BAC s YAC rendszerek sszehasonltsa 108
8.2.6. Genomilis knyvtrak felhasznlsi terletei 108
8.3. cDNS knyvtrak 108
8.3.1. cDNS knyvtrak ltrehozsa 109
8.3.2. cDNS knyvtrak szrse s fenntartsa 110
8.3.3. cDNS knyvtrak felhasznlsi terletei 110
8.4. Tovbbi olvasnival a fejezethez 110
9. GENOM PROJEKTEK 111
9.1. A genomszekvenls alapjai 111
9.1.1. Trkpezs 111
9.1.2. Genomszekvenls trkp-alap mdszerrel 113
9.1.3. A shotgun mdszer 114
9.2. Egy plda: a Haemophilus influenzae baktrium szekvencijnak meghatrozsa 114
9.2.1. A lefedettsg (coverage) jelentsge 116
9.2.2. Paired-end szekvenls 117
9.3. A Humn Genom Projekt (HGP) 117
9.3.1. Nehzsgek a humn genom vizsglatban 118
9.3.2. Elindul a HGP 118
9.3.3. Megjelenik egy versenytrs 119
9.3.4. A humn genom vzlatos (draft) szekvencija 119
9.3.5. 2003-ra elkszl a szekvencia 119
9.3.6. A szekvenls technikjnak fejldse 120
9.3.7. Etikai krdsek avagy kinek a DNS-t hasznltk a szekvenlshoz? 120
9.4. Tovbbi genom projektek 120
9.5. Tovbbi olvasnival a fejezethez 121
10. BEVEZETS A BIOINFORMATIKBA 122
10.1. Bioinformatikai adatbzisok 122
10.1.1. Bibliogrfiai gyjtemnyek 122
10.1.2. DNS szekvencia-adatbzisok: GenBank s Ensembl 122
10.1.3. Fehrje-szekvencia adatbzisok: UniProt 123
10.1.4. Az "omikk" vilga. Fajonknti adatbankok. 124
10.1.5. Szerkezeti s funkcionlis adatbzisok 125
10.2. Szekvencia-illesztsek s egyb fontos algoritmusok 126
10.2.1. Pronknti szekvencia-illesztsek (pairwise alignments) 126
7
10.2.2. A szekvencia-illeszts paramterei 127
10.2.3. A BLAST algoritmus 127
10.2.4. Szekvenls ellenrzse illesztsekkel. Plazmid szerkesztk 128
10.2.5. Tbbszrs illesztsek (multiple alignments). A Clustal programcsomag 129
10.2.6. Evolcisan konzervlt elemek azonostsa 129
10.2.7. Automatizlt mdszerek a szekvencik elemzsre 130
10.2.7.1. Pontozmtrixok (PSSM: Position Specific Scoring Matrices). Logk 130
10.2.7.2. Rejtett Markov-modellek (HMM: Hidden Markov Models) 131
10.2.7.3. Neurlis hl mdszerek (Neural net) 132
10.2.7.4. A Bayes-statisztika s a dntselmlet alapjai (Bayesian inference) 133
10.3. Nukleinsavak tulajdonsgainak jslsa 133
10.3.1. Leolvassi keretek s gnek jslsa 133
10.3.2. Gn meghatrozs cDNS alapjn. Eukarita gnek analzise 134
10.3.3. DNS s RNS szerkezetek jslsa. Oligonukleotid tervezs 134
10.3.4. Nukleinsavak "olvadspontja" 135
10.4. Fehrjk tulajdonsgainak jslsa 136
10.4.1. A fehrjk egyszer fizikai tulajdonsgainak becslse. Reverz transzlci 136
10.4.2. Lineris motvumok keresse fehrjkben (s nukleinsavakban) 137
10.4.3. Fehrjeszerkezetek jslsa. Rendezett s rendezetlen rgik 138
10.5. In silico szerkezeti analzisek 139
10.5.1. Makromolekulk grafikai megjelentse 139
10.5.2. Homolgia-modellezs s in silico dokkols 141
10.6. A predikcis mdszerek pontossga 141
10.6.1. Egy predikci "jsgt" ler paramterek. Optimlis dntsek. 141
10.6.2. Adatbzisok minsge: elsdleges s msodlagos hibk 142
10.6.3. Ellenrztt adatbzisok. Ellentmond ksrleti eredmnyek kezelse 143
10.6.4. Mikor hasznljunk jslsokat? 143
10.7. Tovbbi olvasnival a fejezethez 143
11. IN VITRO MUTAGENEZIS 144
11.1. Nem-irnytott in vitro mutagenezis mdszerek 144
11.1.1. Muttor baktrium sejtvonalak 145
11.1.2. Hibt ejt (error prone) PCR mutagenezis 145
11.2. Helyspecifikus in vitro mutagenezis mdszerek 146
11.2.1. DNS kazetta mutagenezis 146
11.2.2. Szelektv templt lebontson alap mutagenezis mdszerek 147
11.2.2.1. Kunkel mutagenezis 147
11.2.2.2. QuickChange mutagenezis 149
11.2.2.3. GeneEditor mutagenezis 151
11.2.3. PCR alap irnytott mutagenezis mdszerek 152
11.2.3.1. Megaprimer PCR mutagenezis 152
11.2.3.2. Overlapping PCR mutagenezis 153
11.3. Tovbbi olvasnival a fejezethez 154
12. IN VITRO S PROKARITA EXPRESSZIS RENDSZEREK 155
12.1. In vitro expresszis rendszerek 155
12.1.1. Az in vitro transzlcis rendszer komponensei 155
12.1.2. Elnyk s htrnyok 157
12.1.3. Alkalmazsok 158
12.2. Prokarita expresszis rendszerek 158
12.2.1. Bakterilis promterek s a riboszma kthely 159
8
12.2.1.1. Promterek 159
12.2.1.2. Riboszma kthely (RBS) 162
12.2.2. A prokarita fehrje expresszi optimalizlsa 162
12.2.2.1. Az indukcis krlmnyek optimalizlsa 164
12.2.2.2. Expresszis trzsek (BL21pLysS, BL21pLysE, Rosetta, BL21Star, stb.) 165
12.2.2.3. Promter optimalizls 165
12.2.2.4. Koexpresszi 165
12.2.3. Fzis rekombinns konstrukcik 166
12.2.3.1. GST-cmke 167
12.2.3.2. MBP-cmke 167
12.2.3.3. Polihisztidin-cmke 167
12.2.3.4. Egyb cmkk 168
12.2.3.5. A fzis cmkk eltvoltsa 169
12.2.4. Rekombinns fehrjk termelse s izollsa 170
12.2.4.1. Indt (starter) kultra elksztse 170
12.2.4.2. Az expresszis kultra nvesztse s indukcija 170
12.2.4.3. A sejtek sszegyjtse (harvesting) 171
12.2.4.4. A sejtek feltrsa 171
12.2.4.5. Izolls oldhat frakcibl 172
12.2.4.6. Preparls zrvnytestbl (inclusion body) 172
12.2.4.7. Izolls periplazmbl 172
12.2.5. A prokarita expresszi elnyei, htrnyai 173
12.3. Tovbbi olvasnival a fejezethez 173
13. EUKARITA EXPRESSZIS RENDSZEREK 174
13.1. leszt expresszis rendszer 174
13.1.1. Az expresszis kazetta 175
13.1.2. Szelekcis markerek 176
13.1.3. Szekrci 176
13.1.4. Poszttranszlcis mdostsok 176
13.1.5. Az expresszi lpsei 176
13.1.6. leszt expresszis vektorok s rendszerek 177
13.1.7. Az leszt expresszis rendszer elnyei s htrnyai 178
13.2. Bakulovrus expresszis rendszer 179
13.2.1. Bac-to-Bac rendszer 179
13.2.2. Kzvetlen bakulovrus (Direkt Bac) rendszer 180
13.2.3. A bakulovrus rendszer elnyei s htrnyai 181
13.3. Emls expresszis rendszer 181
13.3.1. Emls expresszis vektorok 181
13.3.1.1. Emls promterek s enhanszerek 181
13.3.1.2. Transzkripci terminci s poliadenilcis szignl 183
13.3.1.3. Splicing szignl 184
13.3.1.4. Transzlci inicicis (Kozak-) szekvencia 184
13.3.1.5. Szelekcis markerek 185
13.3.1.6. Az emls expresszis vektorok tpusai 185
13.3.1.7. Stabil vagy tranziens transzfekci 187
13.3.2. Sejtvonalak 188
13.3.3. Gnbevitel emls sejtbe 189
13.3.4. Induklhat emls expresszis rendszerek 189
13.3.4.1. A Tet-represszoron alapul indukcis rendszerek 190
13.4. Egyb eukarita expresszis rendszer 191
13.4.1. Dictyostelium discoideum expresszis rendszer 191
13.4.2. Drosophila melanogaster expresszis rendszer 192
13.5. Eukarita sejttenyszts 192
9
13.6. Tovbbi olvasnival a fejezethez 193
14. CLZOTT GNMDOSTS (GN-TARGETING) MDSZEREK 195
14.1. Bevezets 195
14.2. DNS hibajavts s homolg rekombinci 195
14.3. Gn-targeting konstrukcik ellltsa 198
14.3.1. A recombineering alapjai. A Red rekombincis rendszer 198
14.3.2. Gateway klnozs 199
14.3.3. Targeting vektorok tervezse 200
14.3.4. A gn-targeting konstrukcik elksztse 202
14.4. A targeting-konstrukci bejuttatsa a clszervezetbe 202
14.4.1. Sejtek s sejtvonalak transzfektlsa. Emls embrik manipulcija 202
14.4.2. Stabil transzfekci. Transzgnek clzs nlkli bevitele 204
14.4.3. Nvnyi s gomba sejtek transzformlsa. Homolg rekombinci nvnyekben 204
14.4.4. Nvnyek genetikai mdostsa Ti plazmid segtsgvel 205
14.5. Knock-out s knock-in technikk 206
14.5.1. Homing endonuklezok. Cre/Lox s Flp/Frt rendszerek 206
14.5.2. Clszekvencira tervezett hast enzimek. Cink-ujjas s TALE-nuklezok 208
14.5.3. Gnkits (knock-out) s j gnek clzott beptse (knock-in) 210
14.5.4. Feltteles gnkits, gnjavts 211
14.5.5. Genetikai elemek beptse transzpozonok segtsgvel 212
14.5.5.1. A transzpozonok molekulris biolgija 212
14.5.5.2. Genetikai mdosts transzpozonokkal 214
14.5.5.3. Transzpozonok gntechnolgiai alkalmazsai 214
14.6. Gncsendests (knock-down) RNS interferencival 215
14.7. Stabil episzomlis rendszerek 217
14.8. Tovbbi olvasnival a fejezethez 218
15. TRANSZGENIKUS LLNYEK. GNTERPIA 219
15.1. A transzgenikus llnyek tpusai s felhasznlsuk 219
15.1.1. Transzgenikus mikrobk 219
15.1.2. Transzgenikus nvnyek 221
15.1.2.1. Transzgenikus nvnyek ellltsa 221
15.1.2.2. Transzgenikus nvnyek a mezgazdasgban s az lelmiszeriparban 223
15.1.2.3. Transzgenikus nvnyek a gygyszeriparban, vegyiparban, a krnyezeti iparban 224
15.1.3. Transzgenikus llatok az alapkutatsban s a gygyszatban 225
15.1.3.1. Xenotranszplantci s xenogn sejtterpia a gygyszatban 226
15.1.3.2. Emberi betegsgek llatmodelljei: KO (knock-out) egerek 227
15.1.3.3. Transzgenikus llatok az lelmiszeriparban 231
15.1.3.4. Transzgenikus llatok a gygyszeriparban: humn fehrjk ellltsa 231
15.1.3.5. Transzgenikus llatok a krnyezetvdelem szolglatban 232
15.2. Gnterpia 232
15.3. A transzgenikus llnyek felhasznlsnak tudomnyetikai s krnyezetbiztonsgi krdsei 234
15.4. Tovbbi olvasnival a fejezethez 234
16. IRNYTOTT EVOLCIS TECHNIKK 236
16.1. Az irnytott evolcis megkzeltsrl ltalban 236
10
16.2. Knyvtrksztsi technikk 238
16.2.1. PCR alap knyvtrksztsi eljrsok 238
16.2.1.1. Hibt ejt (error-prone) PCR 238
16.2.1.2. Szexulis PCR 238
16.2.2. Helyspecifikus mutagenezisen alapul eljrsok 239
16.2.2.1. Teltsi mutagenezis 240
16.2.2.2. Mutcikkal tzdelt (spiked) oligonukleotidok hasznlata 241
16.2.2.3. Megszabott kodonokat hordoz (tailored) oligonukleotidok hasznlata 241
16.3. Szelekcis eljrsok 242
16.3.1. In vitro szelekcis mdszerek 242
16.3.1.1. Riboszma-bemutats 242
16.3.1.2. mRNS-bemutats 242
16.3.2. A fg-bemutats 243
16.3.3. Rekombinns fehrje knyvtr bemutatsa s szelekcija l sejtek felsznn 245
16.3.3.1. Fehrjk irnytott evolcija baktrium sejtek felsznn 245
16.3.3.2. Fehrjk irnytott evolcija leszt sejtek felsznn 246
16.4. Tovbbi olvasnival a fejezethez 246
17. KLCSNHATSOK KIMUTATSA GNTECHNOLGIAI MDSZEREKKEL 247
17.1. Az leszt kt-hibrid rendszer bemutatsa 247
17.2. Az leszt kt-hibrid rendszer gyengesgei 248
17.3. Hasonl alapokon mkd technikk 249
17.3.1. Fordtott kt-hibrid rendszerek 249
17.3.2. Egy-hibrid rendszerek 249
17.3.3. Hrom-hibrid rendszerek 250
17.3.4. Tovbbi olvasnival a fejezethez 251
18. FGGELK 252
11
Elsz
A gntechnolgia s fehrjemrnksg cm elektronikus jegyzet elssorban a mesterkpzsben
molekulris szint biolgit tanul egyetemi hallgatk szmra kszlt, de brmely, a rekombinns DNS
technolgia irnt rdekld hallgat, vagy mr vgzett kutat szmra is hasznos informcikat tartalmaz.
Mivel a jegyzet f clkznsge mesterszint kpzsben tanul, felttelezzk, hogy az olvas korbban mr
sikeresen elvgzett biokmia, genetika s mikrobiolgia kurzusokat. Ezen tuds nlklzhetetlen a
jegyzetben lert mdszerek elmleti htternek megrtshez.
A jegyzet szerkezett s tartalmt az ELTE-n idestova tbb mint hsz ve tantott gntechnolgia trgy
oktatsa sorn szerzett tapasztalatok alapjn lltottuk ssze. Ezton fejezem ki ksznetemet ma mr
nyugdjas kollgmnak, Szilgyi Lszlnak, aki sok vig oktatta a gntechnolgia trgyat, aki az elsk
kztt alkalmazta a Biokmiai Tanszken a gntechnolgiai mdszereket a kutatmunkjban, s akivel
kzsen alaktottuk ki a trgy tematikjt. Mivel a jegyzetrsban kzremkd szerzgrda minden tagja az
ELTE Biokmia Tanszk fiatal munkatrsa, ahol hagyomnyosan fehrjetudomnnyal foglakozunk, ezrt a
knyv hangslyozottan biokmikusi szemlletre pl. Ebbl a tnybl addik, hogy a
fehrjetudomnyban ltalunk is hasznlt gntechnolgiai mdszereket nagyobb rszletessggel trgyaljuk,
viszont nem megynk bele mlyen pldul a gntechnolgiban nlklzhetetlen mikrobilis s eukarita
sejttenysztsi mdszerek rszletezsbe. Szintn kevesebb teret szentelnk a molekulris genetikai,
funkcionlis genomikai, molekulris sejtbiolgiai, molekulris mikrobiolgiai, virolgiai, nvnybiolgiai
s ms molekulris szint biolgiai kutatsokban alkalmazhat specilis mdszerek bemutatsnak.
A jegyzet cme is a biokmikus szemlletre utal, hiszen a fehrjemrnksg a fehrjetudomny rsze.
Ennek, a neve alapjn alkalmazott tudomnygnak a clja valamilyen szempontbl jobb, hasznosabb
fehrjk ellltsa. De nem csak alkalmazott tudomnyrl van sz, hiszen a fehrjk szerkezet-funkci
sszefggseinek vizsglata ma mr legnagyobb rszt rekombinns fehrjkkel trtnik, s sokszor a
fehrjelncokat kdol DNS szekvencijnak megvltoztatsn keresztl (in vitro helyspecifikus
mutagenezissel) igyeksznk megrteni a fehrje biolgiai szerept s mdszertani megkzeltsben ekkor is
fehrjemrnksget mvelnk. A jegyzetnek nem clja egy szisztematikus fehrjemrnksg trgy lersa,
ezrt nem foglalkozunk rszletesen azokkal a konkrt tervezett fehrjkkel, amelyeket a gntechnolgia
ezen ga mig ellltott. A hangsly a fehrjemrnksghez szksges gntechnolgiai eljrsok lersn
lesz. Igen alaposan trgyaljuk a rekombinns fehrjk ellltsnak lehetsgeit (expresszis rendszerek) s
a szerkezet megvltoztatsnak lehetsgeit (mutagenezis mdszerek). Kln fejezetet szentelnk az
irnytott evolci izgalmas lehetsgeket megteremt mdszereinek bemutatsra. Bizonyos
rtelemben a fehrjemrnksg termkei azok az egyre nagyobb szmban felhasznlsra kerl
fehrjegygyszerek is, amelyek ellltsval, ha nem is rszletekbe menen, de szintn foglalkozunk.
A gntechnolgia a biotechnolgiai iparg rsze. Nem trgya a jegyzetnek a gntechnolgia ipari
alkalmazsainak mlyebb trgyalsa, mivel hangslyozottan a biolgus kutatkpzsben rsztvev
hallgatkat cloztuk meg. Ennek ellenre gy vljk, hogy a vegysz, biomrnk, bionikai, orvosi s
biotechnolgia szakemberkpzs terletn is haszonnal forgathat jegyzetet kap kzhez az olvas.
Elektronikus jegyzetrl lvn sz, igyekeztnk az ebbl a tnybl add lehetsgeket kihasznlni. A
jegyzet nagyszm kereszthivatkozs, internetes hivatkozst tartalmaz. Az utbbiak segtsgvel az olvas a
jegyzet ismeretanyagt messze meghalad, a tanuls hatkonysgt nvel tovbbi temrdek informcihoz
juthat hozz. A mdszerek gyakorlatban trtn hasznlhatsgt segti a jegyzetbe integrlt nhny
videofilm, de ezt a clt szolglja egyes mdszerek praktikus szempontokat is megemlt lersa. Jegyzetnk
elmleti anyag teht nem tartalmaz rszletes gyakorlati recepteket, br tbb helytt hiperhivatkozsok
formjban ilyen weboldalakat is elrhet az olvas.
Szerkezett tekintve a jegyzet egy, a gntechnolgia trtnett a szkebb rtelemben vett molekulris
biolgia (a nukleinsavak kutatsa) trtnetvel egytt felvzol fejezettel kezddik. A gntechnolgia
alapjt jelent molekulris klnozs bemutatsa utn sorra vesszk a terlet mvelshez szksges
12
eszkzket s alapmdszereket. Bemutatjuk a DNS manipulci enzimeit, a DNS molekulk
szeparlshoz szksges elektroforzis technikkat, a nlklzhetetlen hibridizcis s szekvenl
mdszereket, a klnozshoz hasznlhat vektorok tpusait. Sorra vesszk a rekombinns DNS
tervezsnek egyes lpseit, a klnozsi stratgikat, a DNS konstrukcik sejtbe juttatsi mdszereit
(gnbevitel), az in vitro DNS felszaportst lehetv tev polimerz lncreakci alapjait s felhasznlsi
terleteit. Trgyaljuk a klnbz gnknyvtrakat, bemutatjuk a genom projektek mdszertani httert
s nhny konkrt genom programot is (kiemelten a Humn Genom Programot). Igen alapos s rszletes
fejezet foglalkozik a gntechnolgia mvelshez szintn nlklzhetetlen bioinformatika relevns
terleteivel s alkalmazsaival. A fehrjemrnksg trgykrbe elssorban az in vitro mutagenezist s
az sszes lehetsges expresszis rendszert (in vitro, prokarita, eukarita gazdasejtek, transzgenikus
llnyek) ismertet fejezetek tartoznak. Kln fejezetet szentelnk az igen fontos n. gn targeting
(clzott gnbeviteli) mdszereknek, amelyek segtsgvel organizmus szinten mdosthatunk clzottan
egy-egy gnt (knock-out, knock-in technika), illetve a nem tl rgen felfedezett RNS csendests jelensgt
(knock-down) kihasznlva tehetnk tnkre egy-egy mRNS molekult. Szintn kln fejezet foglalkozik a
transzgenikus llnyek ellltsnak httervel, s nhny GMO pldval a mikroorganizmusok, a
nvnyek s az llatok krbl de nem prblunk tfog lerst adni errl a terletrl. Rviden bemutatjuk
a ma mg inkbb jvbeni alkalmazst jelent gnterpis eljrsok alapjait. Vgl sort kertnk a mr
emltett irnytott evolcis mdszerek bemutatsra s ismertetnk nhny specifikus, a
fehrjetudomnyban alkalmazott gntechnolgiai n. interakcis mdszert is. Az egyes fejezetek vgn a
tmhoz kapcsold nhny szakirodalmi forrst, tovbbi olvasnivalt sorolunk fel.
Bzunk benne, hogy az e-jegyzetnk elri a megfelel clkznsget, s mind egyetemi hallgatk, mind a
gntechnolgia irnt rdekl szakemberek hasznosnak talljk majd az elektronikus oldalak lapozgatst. Az
egyik f clunk, hogy a hallgatink a Gntechnolgia kurzus vizsgakvetelmnyt az e-jegyzet
hasznlatval knnyebben s eredmnyesebben teljestsk. A msik f clunk, hogy az olvas ne csak
elmleti httranyagknt hasznlja az e-jegyzetet, hanem a ksrleti munkjnak megtervezshez s
kivitelezshez is hasznosthat informcikat talljon benne, legyen sz laboratriumi gyakorlatokrl,
tudomnyos dikkri s szakdolgozati munkrl vagy gntechnolgiai mdszerek hasznlatt megkvn
alap- s alkalmazott kutatsi projektekrl.
Budapest, 2013. mjus
Nyitray Lszl, szerkeszt
13
1. A gntechnolgia trtnetnek mrfldkvei
A gntechnolgia szletst megelzte a DNS szerepnek s szerkezetnek megismerse, az rklds
molekulris mechanizmusainak feltrsa. Ezrt az albbi trtneti ttekintst a DNS felfedezsnl kezdjk,
s a nukleinsav biokmia mrfldkveinek (s a kulcs ksrletek) felvzolsn t jutunk el azoknak a
mdszereknek a lersig, amelyek lehetv tettk az els rekombinns DNS ltrehozst. ttekintjk a
technolgia fejldst jelz f mdszertani jtsokat, azt a fejldst, ami az egyes gnek vizsglattl
elvezetett a genom projektekig s a nagy teresztkpessg mdszerek megjelensig.
1.1. Az rktanyag felfedezstl a genetikai kd megfejtsig
1.1.1. A DNS felfedezse s a klibaktrium lersa
A gntechnolgia kialakulshoz, a rekombinns DNS technikk megjelenshez vezet ton az els fontos
lpst Friedrich Miescher (1844-1895) tette meg 1869-ben a DNS felfedezsvel. Miescher a leukocitk
kmiai sszettelt vizsglta. A sejtmagokbl egy savban oldhatatlan, viszont lgban oldd, magas foszfor
tartalommal jellemezhet anyagot sikerlt elklntenie, ami a fehrjkkel ellenttben hkezels hatsra
nem csapdott ki az oldatbl. Ksbb ugyanezt az anyagot sikerlt izollnia gy is, hogy pepszines
kezelssel lebontotta a mintban tallhat fehrjket. A fehrjktl eltr sszettel s viselkeds, valamint a
protez kezelssel szembeni rezisztencia arra mutattak, hogy Miescher egy j, korbban ismeretlen anyagot
tallt. Ezt a sejtmagokra jellemz anyagot nukleinnek nevezte el.
1.1. bra: Friedrich Miescher
Theodor Escherich (1857-1911), nmet gyermekorvos s mikrobiolgus a blrendszer baktriumflrjt
vizsglva szmos addig ismeretlen baktriumot azonostott, kzttk egy Gram-negatv, fakultatv anaerob
baktriumot, melynek a Bacterium coli commune nevet adta. Eredmnyeit 1886-ban publiklta. A halla
utn Escherichia coli nevet kapott baktrium napjainkra a gntechnolgiai kutatsok s a gntechnolgiai
ipar egyik legfontosabb eszkzv vlt, melyben knny tenyszthetsge, gyors osztdsa (idelis
krlmnyek kztt 20 percenknt osztdik), egyszer genetikai manipullhatsga jtszottak szerepet.
1.2. bra: Theodor Escherich arckpe s az Escherichia coli elektronmikroszkpos kpe
(mrete 2 x 0,5 m)
14
1.1.2. A DNS rktanyag szerepnek tisztzsa
Frederick Griffith (1879-1941) brit bakteriolgus, a tdgyulladst (pneumonia) okoz Streptococcus
pneumoniae baktriumot vizsglva 1928-ban felfedezte a transzformci jelensgt. A baktrium kt trzst
hasznlta fel ksrletei sorn, melyeket a telepek morfolgija alapjn tudott elklnteni: a sima trzs (S:
smooth) s a durva trzs (R:, rough). Az S-trzs kpes tdgyulladst okozni, mg az R-trzs nem.
Egerekbe injektlva a baktriumokat az S-trzs esetn a kialakul tdgyullads az egr pusztulst okozza,
mg az R-trzs esetn az egr tll. Amikor Griffith hkezelssel elpuszttotta az S-trzsbe tartoz
baktriumokat, majd egerekbe injektlta az gy nyert anyagot, az egerek nem betegedtek meg. Ha azonban
az elpuszttott S-trzshz l R-trzsbe tartoz baktriumokat kevert, az egr megbetegedett s elpusztult,
annak ellenre, hogy nmagban az R-trzs s az ellt S-trzs is rtalmatlannak bizonyult a korbbi
ksrletekben. Az elpusztult egerek szervezetben mindkt trzs jelenltt ki tudta mutatni. Az elpuszttott
baktriumokbl kikerl anyagok teht talaktottk valamilyen mdon az rtalmatlan R-trzsbe tartoz
baktriumokat, vagyis a fertzs kpessge taddott. Griffith a jelensget transzformcinak nevezte el.
(Ma mr tudjuk, hogy az S-trzsbe tartoz baktriumok rendelkeznek egy poliszacharid burokkal, mely
vdelmet biztost a gazdaszervezet immunrendszere ellen. Az R-trzs esetn ez hinyzik. A fertzs
kpessge, vagyis a poliszacharid burok ltrehozshoz szksges genetikai informci, a hkezels sorn
psgben megmaradt, majd az R-trzs baktriumai ltal a klvilgbl felvett DNS molekulk kzvettsvel
jutott t a korbban fertzni nem kpes sejtekbe.)
1.3. bra: Frederick Griffith s Griffith transzformcis ksrlete (GNU Free Documentation License, szerz:
Madeleine Price Ball)
A transzformcirt felels, vagyis a genetikai informcit hordoz anyag kmiai termszetnek azonostsa
Oswald Avery (1877-1955), Colin MacLeod (1909-1972) s Maclyn McCarty (1911-2005) munkjnak
ksznhet. Az 1944-ben publiklt ksrletben Griffith kutatsaihoz hasonlan k is a Pneumococcus
baktrium R- s S-trzseit hasznltk. Az S-trzsbl sikerlt izollniuk a transzformcirt felels anyagot.
Klnbz kmiai mdszerekkel vizsglva a prepartumot kimutattk, hogy az nagy valsznsggel DNS-
bl ll, s nem tartalmaz fehrjket. (Akkoriban a fehrjket tartottk a genetikai informci hordozjnak.)
Ezt kveten klnbz enzim prepartumokkal kezeltk az anyagot (pl. protez, RN-z, DN-z).
Transzformcit csak akkor nem tapasztaltak, ha a prepartumnak DN-z aktivitsa volt. Egyb enzimek
viszont nem gtoltk transzformcit.
15
1.4. bra: Oswald Avery
Avery s munkatrsai eredmnyeit akkoriban a tudomnyos kzvlemny egy rsze kritikusan fogadta,
mivel logikusabbnak tnt a 20 fle aminosavbl ll fehrjkrl felttelezni, hogy rktanyagknt
funkcionlnak. A perdnt ksrletet 1952-ben Alfred Hershey (1908-1997) s Martha Chase (1927-2003)
hajtottk vgre, akik T2 bakteriofggal ksrleteztek. A fgrszecskkrl ismert volt, hogy fehrje burokkal
rendelkeznek, melynek belsejben DNS tallhat. Kihasznlva, hogy a fehrjealkot aminosavak a DNS-sel
ellenttben tartalmaznak knt, viszont nem tartalmaznak foszfort, Hershey s Chase szelektven jellhette
radioaktv kn (
35
S) s foszfor (
32
P) izotpok felhasznlsval a fehrjeburkot s a DNS-t. Ehhez olyan
baktriumokon szaportottk a fgokat, melyek vagy
35
S, vagy
32
P tartalm tptalajon nvekedtek. Az ilyen
mdon jellt fgrszecskkkel azutn olyan baktriumokat fertztek, melyek jelletlen tptalajon
nvekedtek. A
35
S izotp nagyrszt a baktriumsejteken kvl maradt, mg a
32
P a sejtek belsejbe kerlt,
vagyis fertzskor a fg DNS bejutott a sejtekbe, mg a fehrjeburok elemei nem. Radsul a fertzs utn
jonnan kpzd fgrszecskk a
32
P-t megrkltk a szli genercitl, mg a
35
S-t nem.
Eredmnyeik elismersekppen Hershey (Max Delbrck-kel s Salvador Luria-val megosztva, akik szintn
bakteriofgokkal vgzett ksrleteikben a replikci s a mutci problmakrt vizsgltk) 1969-ben
fiziolgiai s orvostudomnyi Nobel-djat kapott.
1.5. bra: Alfred Hershey s Martha Chase
1.1.3. A DNS kettshlix felfedezse, a genetikai kd megfejtse
A gntechnolgia szempontjbl kulcsfontossg esemny volt a DNS szerkezetnek felfedezse, amely
James D. Watson (1928-) s Francis H. C. Crick (1916-2004) nevhez fzdik. Watson s Crick a DNS
kettshlix modelljt Maurice Wilkins (1916-2004) s Rosalind Franklin (1920-1958) rntgendiffrakcis
adatai alapjn lltotta fel 1953-ban. A modell helyesen felttelezte, hogy a DNS kt, egymssal ellenttes
irnyba fut szlat tartalmaz. Az Erwin Chargaff (1905-2002) ltal megfigyelt szablyok alapjn (az
adenin s a timin, tovbb a citozin s a guanin arnya megegyezik a DNS-ben) helyesen feltteleztk azt is,
hogy a szlak kztti kapcsolatot a bzisok kztt specifikus mdon kialakul hidrogn-ktsek jelentik.
16
Watson s Crick modellje rvilgtott a DNS megkettzdsnek mechanizmusra is: mivel brmelyik szl
bzissorrendje egyrtelmen meghatrozza a msik szl bzissorrendjt, a kt szl elvlasztsval nem vsz
el informci. Az elvlasztott szlak mintaknt (templtknt) szolglhatnak j, komplementer szlak
szintzishez. gy kt j kettshlixhez jutunk, melyeknek csak az egyik szla jonnan szintetizlt. Ezt a
mechanizmust szemikonzervatv replikcinak nevezzk.
Watson, Crick s Wilkins 1962-ben fiziolgiai s orvostudomnyi Nobel-djat kapott a DNS szerkezetnek
felfedezsrt. Rosalind Franklin, akinek a hozzjrulsa az eredmnyekhez szintn kulcsfontossg volt,
sajnos nem rszeslhetett ebben az elismersben, ugyanis ngy vvel korbban, 1958-ban elhunyt.
1.6. bra: A. James Watson (balra fent), Francis Crick (balra lent); Watson, Crick s a DNS kettshlix modellje
(jobbra fent); A Rosalind Franklin ltal ksztett DNS szl-diffrakcis felvtel, mely az egyik kulcsfontossg
bizonytk volt a modell helyessgt illeten (jobbra lent).
A DNS szerkezetnek megismersvel azonban mg mindig nyitva maradt egy nagyon fontos krds:
milyen mdon hasznosul a DNS molekulban trolt genetikai informci a sejtekben, vagyis hogyan kpes a
DNS a fehrjelncok szintzist kdolni? Marshall Nirenberg (1927-2010) volt az els, aki sikereket rt el
a genetikai kd megfejtse tern. Ksrleteihez E. coli sejtek citoplazmjt hasznlta fel, melyben jelen volt
a fehrjeszintzishez szksges minden komponens. A minthoz szintetikus RNS-t (poli-U) s a 20
fehrjealkot aminosav kzl egyet-egyet radioaktvan jellve adott. Megfigyelte, hogy poli-U templt
esetn csak a fenilalanin pl be a fehrjelncba. Tovbbi szintetikus RNS molekulkkal is elvgezte a
ksrletet; ekkor ms-ms aminosavak pltek be. Har Gobind Khorana (1922-2011) rvid
oligonukleotidok szintzist kombinlta enzimatikus mdszerekkel, gy kpes volt ellltani olyan RNS
polimereket, melyekben kett, hrom, illetve ngy nukleotid egysg ismtldtt. Ezeket Nirenberg
ksrleteihez hasonlan sejtmentes expresszis rendszerben tesztelte. Kt nukleotid szablyos ismtldse
esetn a polipeptidlncba kt fle aminosav plt be, szablyosan vltakozva. Hrom nukleotid esetn
egyetlen aminosavbl ll szablyos polimer jelent meg. Ngy bzis szablyos ismtldse ngy aminosav
szablyosan ismtld polimert eredmnyezte. Mindez igazolta, hogy a genetikai kdban egy aminosavat
hrom bzis definil, tovbb, hogy a bzishrmasok nem fednek t.
Nirenberg, Khorana s Holley (az utbbi a tRNS-t fedezte fel) 1968-ban a genetikai kd megfejtsrt
megkapta a Nobel-djat.
17
1.2. A DNS manipullsra alkalmas enzimek felfedezse
Az rktanyag kmiai termszetnek, szerkezetnek megismerse, valamint a genetikai kd megfejtse
mellett a gntechnolgia kialakulshoz szksges volt a DNS manipullsra alkalmas enzimek
felfedezse is. Az egyik legfontosabb enzim a DNS szintzisrt felels DNS-polimerz, amit Arthur
Kornberg (1918-2007) fedezett fel 1957-ben. Kornberg munkssgt 1959-ben Nobel-djjal jutalmaztk
(Severo Ochoa-val megosztva, aki elszr bizonytotta, hogy kmcsben RNS-t is lehet szintetizlni)
1.7. bra: Arthur Kornberg
Werner Arber (1929-) a bakterilis restrikcis-modifikcis rendszer vizsglatval 1962-ben olyan
enzimeket fedezett fel, melyek nlkl a rekombinns DNS technolgia nem jhetett volna ltre. Arber a
bakteriofgok gazdasejt specifitsnak okait vizsglta. Megfigyelte, hogy az E. coli K12 trzsben
felszaportott bakteriofgok alacsony hatsfokkal fertznek egy msik trzset, az E. coli B-t, s fordtva: az
E. coli B-ben szaportott fgok rossz hatkonysggal fertznek meg E coli K12-es trzset. Ha viszont
megtrtnik a keresztfertzs az jonnan termelt fgok mr jl szaporodnak az j gazdasejtben s alacsony
hatsfokkal fertzik az eredeti gazdasejtet, amiben korbban jl szaporodtak. Arber felfedezte, hogy a
jelensg htterben a DNS metilcija (modifikci), s endonuklezok ltali, metilcitl fgg hastsa
ll.
A restrikcis-modifikcis rendszernek teht kt eleme van: egy restrikcis endonuklez s egy annak
megfelel, DNS-metilz enzim. A restrikcis endonuklez specifikusan felismer egy 4-8 bzisnyi DNS
szekvencit s hastja a DNS mindkt szlt. A mdost metilz ugyanebben a szekvenciban metill egy
adenint (az aminocsoporton), vagy egy citozint (az 5. sznen vagy az aminocsoporton). A restrikcis
endonuklez nem tudja elhastani az gy mdostott szekvencit. A kt enzim egyttesen van jelen a sejtben,
s jelenltk trzs-specifikus. A baktrium DNS-e a metilznak ksznheten llandan metillt, teht
vdve van a restrikcis endonuklez mkdsvel szemben. A klvilgbl, pl. egy fgbl szrmaz DNS
feltve hogy nem ugyanabbl a baktrium trzsbl rkezik nincs metillva ugyanezeknl a specifikus
szekvenciknl, ezrt a restrikcis endonuklezok nagy valsznsggel elhastjk s gy lebomlik.
Az els restrikcis endonuklezt Hamilton Smith (1931-) s Daniel Nathans (1928-1999) izollta az
1960-as vek vgn. Nathans 1972-ben elsknt hasznlta a restrikcis enzimeket genetikai trkpezsre.
(Az SV40 vrus restrikcis trkpezst vgezte.) Napjainkra mr tbb ezer restrikcis enzimet ismernk,
melyek tbb szz klnbz szekvencia specifikus elhastst teszik lehetv. Arber, Smith s Nathans a
restrikcis endonuklezokkal vgzett kutatsokrt 1978-ban megkapta a Nobel-djat.
Martin Gellert (1929-) fedezte fel a DNS-ligz nev enzimet 1967-ben, amely kpes a DNS molekulk
vgeit foszfodiszter ktsekkel kovalensen sszekapcsolni, ezzel megteremtve a lehetsgt a klnbz
forrsokbl szrmaz DNS molekulk egyestsnek, gy a rekombinns DNS molekulk ellltsnak.
18
1.8. bra: Werner Arber, Hamilton Smith s Daniel Nathans (HS arckpe: Creative Commons License, szerz: Jane
Gitschie; DN arckpnek forrsa: National Library of Medicine)
1.3. A rekombinns DNS technika megjelense
Az els, valdi rekombinns DNS molekulk ltrehozsa az 1972-ben trtnt meg. Paul Berg (1926-)
elsknt dolgozott ki egy enzimekre pl mdszert, kt, klnbz eredet DNS molekula (SV40 vrus s
-fg) egyestsre. A cirkulris DNS molekulkat restrikcis endonuklezzal hastotta. A lineris DNS-t
terminlis dezoxiribonukleotid-transzferz enzimmel kezelte, mely enzim a ktszl DNS egyik szlt kpes
meghosszabbtani a szubsztrtknt adott dNTP-kel. Csak egyfle monomert adva az enzim egyszl,
homopolimer farkat kszt a DNS-en (pl. dATP esetn poli-A). A ktfle forrsbl szrmaz DNS
molekuln gy egymssal komplementer (poli-A s poli-T) tlnyl vgeket tudott ltrehozni, melyek
Watson-Crick fle bzisprosodssal felismertk egymst. A DNS lncok egyestshez ezutn DNS-
polimerzt s DNS-ligzt hasznlt. Munkssgt 1980-ban Nobel-djjal jutalmaztk.
Stanley Cohen (1935-) 1973-ban E. coli sejtek transzformcijra dolgozott ki hatkony eljrst, mellyel
plazmidokat (extrakromoszomlis, cirkulris, ktszl DNS molekulk, melyek nllan replikldnak)
tudott bejuttatni a sejtekbe. A baktriumok a plazmidon tallhat antibiotikum rezisztencia gn hatsra
ellenllv vltak az antibiotikummal szemben; annak jelenltben is tudtak nvekedni. Cohen a kvetkez
vben Herbert Boyer-rel (1936-) egyttmkdve ltrehozott egy rekombinns plazmidot kt msik
plazmid restrikcis endonuklez kezels hatsra ltrejtt darabjaibl. A fragmentumokat DNS-ligz
segtsgvel illesztettk ssze. Az j plazmiddal sikerlt E. coli sejteket transzformlni, melyek mind a kt
kiindulsi molekultl szrmaz gnt (antibiotikum rezisztencia) hordoztk. Ezzel amellett, hogy
rekombinns DNS-t hoztak ltre, demonstrltk azt is, hogy a plazmidok vektorknt (hordoz DNS)
hasznlhatk, vagyis ms forrsbl szrmaz DNS darabok beljk illeszthetk, majd stabilan
fenntarthatk E. coli sejtekben, ahol a plazmid jelenltre a rajta tallhat antibiotikum rezisztencia gnek
segtsgvel lehet szelektlni. Herbert Boyer s Robert Swanson 1976-ban megalaptottk a Genentech
nev cget, mely a gntechnolgiai ipar kezdett jelentette. A Genentech a rekombinns DNS technika
gyakorlati alkalmazst valstotta meg. A legels sikeres fejleszts a humn inzulin hormon E. coli
baktriumban trtn termeltetse volt 1978-ban (Humulin nven kerlt forgalomba 1982-ben.)
1.9. bra: Paul Berg, Herbert Boyer s Stanley Cohen
19
A rekombinns DNS technika megjelense azonban a tudomnyos kzvlemny jelents rszben
aggodalmakat is keltett. Felismertk a klnbz eredet DNS molekulk sszekapcsolsval ltrehozhat
j vrusok illetve baktriumok veszlyeit. Az ilyen mestersgesen sszelltott genommal rendelkez
llnyek igen komoly humn egszsggyi kockzatot jelenthetnek. Emellett a laboratriumbl kikerlve
elre meg nem jsolhat hatsuk lehet ms llnyekre is. Paul Berg az els rekombinns DNS molekula
ltrehozjaknt 1974-ben javasolta, hogy a veszlyekre val tekintettel egszen addig ne folytassanak
ksrleteket rekombinns DNS-sel, amg a megfelel szablyozs s a biztonsgi elrsok meg nem
szletnek. A krds megvitatsra 1975 februrjban megszervezte a hress vlt Asilomar-konferencit. A
ksrletek felfggesztse (moratrium) vgl 16 hnapig, a megfelel biztonsgi elrsok s irnyelvek
kidolgozsig tartott.
1.4. Hibridizcin alapul technikk megjelense
Julius Marmur (1926-1996) s Paul Doty (1920-2011) a DNS h hatsra bekvetkez denaturcijt
vizsgltk az 1960-as vek elejn, mely munkval igen komoly befolyst gyakoroltak a rekombinns DNS
technolgia fejldsre. Hkezels hatsra a DNS kt szla elvlik egymstl, s a minta fnyelnyelse
megn (260 nm-es hullmhossz krnykn a bzisok elnyelik az UV sugrzst). A jelensg hiperkrm
effektus nven ismert. A hmrsklet cskkentsvel a DNS minta renaturldik, vagyis egymssal
komplementer szekvencik esetn a hidrognktsek jra kialakulnak a megfelel bzisprok kztt. A
DNS denaturci, renaturci (klnbz eredet, de komplementer szekvencival rendelkez szlak esetn
hibridizci) jelensgt szmtalan, a mai napig hasznlatos mdszer kihasznlja, gy pldul az Edwin
Southern (1938-) ltal 1975-ben kidolgozott s rla elnevezett Southern-blot (lenyomat) mdszer. A
Southern-blot egy adott szekvencival rendelkez DNS molekula specifikus kimutatsra szolgl eljrs.
(A hasonl elven mkd kimutatsi eljrst RNS minta esetn Northern-blotnak nevezzk.)
Michael Smith (1932-2000) a helyspecifikus mutagenezis mdszernek kidolgozsrt (1978), mg Kary
Mullis (1944-) a polimerz lncreakci (PCR: Polymerase Chain Reaction) mdszernek megalkotsrt
(1983) kapott Nobel-djat 1993-ban. Mindkt mdszer kihasznlja a DNS lncok hibridizcis kpessgt.
Smith a X174 bakteriofg cirkulris, egyszl DNS-nek rvid szakaszaival komplementer szintetikus
oligonukleotidokat szintetizlt, melyeket gy tervezett meg, hogy mind az 5-, mind a 3-vgeik
hibridizltak a fg DNS egy-egy szakaszval, m a kzps szakasz mutcit tartalmazott. DNS-polimerz
segtsgvel ezutn a hibridizlt oligonukleotid 3-vgtl egszen annak 5-vgig szintetizlta a
komplementer DNS lncot, majd DNS-ligzzal egyestette az j szl vgeit. Az gy keletkezett cirkulris
DNS-nek teht csak az j szla hordozta a mutcit. A DNS-t baktriumokba juttatva a keletkez fgok egy
rsze az eredeti, mg ms rsze a mutns szekvencit hordozta. Ezzel a mdszerrel teht clzottan, brmely
kt ismert szekvenciarszlet kztt mutci hozhat ltre. A polimerz lncreakci esetn egy ktszl
DNS molekula (templt) tetszleges szakaszrl kszthetnk specifikus mdon nagyszm msolatot. A
szakaszt kt, a templt DNS egy-egy szlhoz hibridizl szintetikus oligonukleotid jelli ki. A mdszer
felfedezst az 1.5.1. fejezetben rszletezzk.
A DNS hibridizci jelensgt hasznlja ki a nagy teresztkpessg ksrletek elvgzsre alkalmas
DNS-chip (DNS microarray) technolgia is, amelyeknek egyik els vltozatt Stephen Fodor 1991-ben
fejlesztette ki. A DNS-chip lnyege, hogy egy szilrd hordoz felsznn in situ kovalens ktssel kapcsoltan
oligonukleotid prbkat szintetizlnak fotolitogrfiai eljrssal mikroszkopikus mret foltokban, elre
meghatrozott elrendezsben. Adott terleten csak egyfle oligonukleotid tallhat, melynek ismert a
szekvencija. Tbb tzezer ilyen folt is lehet egyetlen chip felsznn. Az gy ltrehozott szintetikus prbkat
felhasznlhatjuk pldul arra, hogy sok gn expresszis szintjt egyidejleg, prhuzamos mdon
meghatrozzuk.
20
1.5. A szekvenlstl a genom korszakig s tovbb
A DNS bzissorrendjnek meghatrozsra elsknt Frederick Sanger (1918-) dolgozott ki ltalnosan
hasznlhat eljrst 1975-ben. A DNS-t felpt nukleotidokat szelektv mdon adta klnbz
reakcielegyekhez, melyekben a szekvenland DNS-sel komplementer szl szintzist DNS-polimerz
enzim vgezte. A szintzis lellt ott, ahov az enzimnek a hinyz nukleotidot be kellett volna ptenie (ez
volt az n. plusz-mnusz mdszer). Walter Gilbert (1932-) s Allan Maxam (1942-) 1977-ben
kidolgozott egy alternatv eljrst, amelyben a DNS szlakat klnbz reagensekkel a ngyfle nukleotid
utn specifikusan elhastotta (kmiai szekvenls). A ltrejv termkek elvlasztsa poliakrilamid glen, a
fragmentumok kimutatsa pedig radioaktivits alapjn trtnt.
Ugyanebben az vben Sanger is kidolgozott egy j eljrst, melyben ismt a DNS-polimerz enzimet
hasznlta fel a DNS szekvenlsra. A DNS szintzis in vitro zajlik, ha van a reakcielegyben DNS-
polimerz, templt DNS, a templthoz hibridizlt oligonukleotid (primer; a 3-OH vg szksges a DNS
szintzishez!), s dNTP (a ngy fle dezoxinukleotid: dATP, dCTP, dGTP, dTTP). A DNS-polimerz enzim
kpes dNTP analgokat is szubsztrtknt elfogadni. gy pldul a 2,3-didezoxinukleozid-trifoszft
(ddNTP) analgok is beplnek, de mivel ezeknek nincs 3-OH csoportja, a tovbbi szintzis lell. A
mdszer ezrt a lnctermincis szekvenls elnevezst kapta (hvjuk mg enzimatikus-, didezoxi- vagy
Sanger-mdszernek is). Sanger ngy klnll reakcielegyet lltott ssze, ugyanazzal a templt DNS-sel.
Mindegyik reakcielegy tartalmazta a ngyfle dezoxi-nukleotidot, viszont a didezoxi-nukleotidok kzl
csak egyet-egyet. Az jonnan szintetizldott szlakat glelketroforzissel szeparlta s az n. szekvenl
ltrt autoradiogramon tudta leolvasni. Sanger az ltala kidolgozott mdszerrel elsknt hatrozta meg egy
termszetben elfordul DNS molekulnak, a X174 bakteriofg teljes genomjnak (5375 bp)
szekvencijt. Ezzel elkezddtt a genomszekvenlsok korszaka. Sanger s Gilbert 1980-ban a DNS
szekvenls mdszereinek kidolgozsrt kmiai Nobel-djat kapott. Sanger esetn ez mr a msodik Nobel-
dj volt; az elst a fehrjeszekvenlsrt kapta 1958-ban.
1.10. bra: Frederick Sanger
Kezdetben csak kisebb genomok szekvenlsa trtnt meg: 1983-ban a -fg (48 kbp), majd 1995-ben a
Haemophylus influenzae (1,9 Mbp) baktrium, ami az els teljes prokarita genom megismerst
jelentette. Az E. coli genom szekvencijt 1997-re ismertk meg (4,6 Mbp, ~4.300 gn). Az eukaritk
krbl az leszt (Saccharomyces cerevisiae) volt az els, melynek a teljes genom szekvencija 1996-ra
kszlt el (12 Mbp, 5885 gn). A Caenorhabditis elegans genomjnak szekvenlsa 1998-ban fejezdtt be
(97 Mbp, 19100 gn). A humn genom (3x10
9
bp, ~23 ezer gn) szekvenlsa (Humn Genom Program)
2004-ben fejezdtt be (mindssze 14 v munkval), br az els vzlatos szekvencit mr 2000-ben
publikltk. Sanger mdszernek tovbbfejlesztsvel (automata fluoreszcens szekvenls), majd a
kzelmltban n. j-genercis szekvenlsi mdszerek megjelensvel, mint pl. a piroszekvenls
(2004) tovbb gyorsult a genom szekvenlsok teme (ld. 5.3. fejezet). A robbansszer fejlds
eredmnyekppen tbb mint 4000 teljes genom szekvenlsa kszlt el 2013-ra, melyek kztt majdnem
200 eukarita genomot is tallunk.
21
1.5.1. A polimerz lncreakci felfedezse
Az in vitro DNS sokszorosts lehetsgt a polimerz lncreakci felfedezse teremtette meg 1983-ban. A
felfedezs elmleti httere mr rgen ismert volt, hiszen Arthur Kornberg 1957-ben felfedezte a DNS
biolgiai szintzisnek mechanizmust. Munkja sorn E. coli baktriumbl izollt DNS-polimerz I
enzimmel dolgozott, amely segtsgvel j DNS szlat tudott szintetizlni. A tanulmny megmutatta, hogy a
folyamathoz kell egy templtknt szolgl DNS lnc, tovbb, hogy a DNS-polimerz I enzim mkdshez
szksg van Mg
2+
ionokra, valamint mind a ngy fajta DNS ptkre, aktivlt monomerekre (dNTP-k).
Mr ma tudjuk, hogy a DNS-polimerz enzim nmagban nem tudja elkezdeni az j lnc szintzist, ehhez
egy oligonukleotid primerre van szksg (amely a sejtekben egy rvid RNS darab lesz, amit a primz nev
RNS-polimerz llt el), s ezt a primert kpes a DNS-polimerz 53 irnyban meghosszabbtani.
Ezen httr informcik ismeretben a PCR eljrst Kary Mullis dolgozta ki. Mullis rdeme abban rejlik,
hogy ciklikuss tette az in vitro DNS polimerizcit s egyszerre kt oligomer primert hasznlt, amelyekrl
egyms fel trtnik az j DNS szlak szintzise. Meg kell emlteni azt is, hogy az tlet mr Kjell Kleppe
fejben is megfordult, azonban azt csak elmletben fogalmazta meg, gy minden szabadalom Mullis, illetve
az t alkalmaz Cetus Corportion biotechnolgiai cgnl kttt ki. Kezdetben Mullisnak mindssze egy 25
bzispr hossz szakaszt sikerlt szintetizlnia. Elszr az E.coli-bl szrmaz DNS-polimerz Klenow-
fragmentumval dolgozott, ksbb azonban mr a htr Thermus aquaticus baktrium DNS-polimerzt
(Taq-polimerz) hasznltk. Ennek kvetkezmnyeknt mr nem kellett a magas hmrsklet miatt minden
ciklus utn j adag polimerz enzimet adni a reakcihoz, s gy 1988-ban mr 2 ezer bzispr hossz DNS
szlakat tudtak szintetizlni.
A mdszer a 90-es vek vgre mr szles krben elterjedt s szmos tudomnyterleten tett lehetv ttr
sikereket (pl.: archeolgia, igazsggyi orvostan; ld. 6.4. fejezet).
1.5.2. Gntechnolgiai eljrsok magasabbrend szervezetekben
Az els transzgenikus llnyt Rudolf Jaenisch (1942-) s Beatrice Mintz (1921-) hozta ltre 1974-ben.
Jaenisch korai egr embrikba (blasztocisztkba) injektlt SV40 vrus DNS-t. (Az SV40 egy majomvrus,
egrben nem kpes szaporodni.) Az embrikat nstny egerek mhbe ltette, ahol azok egszsges
utdokk fejldtek.
Ralph Brinster s Richard Palmiter 1982-ben ttr munkt vgeztek a transzgenikus llnyek
ellltsnak terletn. Megtermkenytett egr petesejtekbe injektltak plazmid DNS-t, mely idegen gnt
hordozott egy induklhat promter (az egr metallotionein gn promtere, amely nehzfmek jelenltben
aktivldik) szablyozsa alatt. Az ilyen mdon kezelt petesejteket nstny egerek mhbe ltettk. Az gy
ltrehozott egerek szveteiben az idegen DNS azonos mennyisgben volt jelen (az egr nem volt mozaikos).
A bevitt DNS konstrukci integrldott a genomba, st az idegen gnrl fehrjeszintzis trtnt. A mdszer
teht lehetsget teremtett arra, hogy brmilyen gnt bejuttassanak az llatok genomjba gy, hogy az
minden szvetben s sejtben jelen legyen. Az gy mdostott organizmusban a gnt szablyoz rgik
megfelel megvlasztsval lehetsges induklt, vagy konstitutv fehrje expresszit ltrehozni, akr szvet-
vagy sejtspecifikus mdon.
A transzgn technolgival prhuzamosan, szintn az 1980 vekben jelent meg az gynevezett knock-out,
azaz gnkits technolgia. A mdszer kifejlesztsben kulcsszerepet jtsz Mario Capecchi (1937-),
Oliver Smithies (1925-) s Martin Evans (1941-) 2007-ben fiziolgiai s orvostudomnyi Nobel-djat
kapott. Evans elsknt izollt embrionlis ssejteket korai egr embrikbl s azokat blasztocisztkba
injektlva sikeresen hozott ltre kimra llatokat (olyan llatok, melyek bizonyos sejtjei, szvetei az
ssejtekbl fejldnek, gy genetikai rtelemben mozaikosak). Capecchi s Smithies egymstl fggetlenl
bizonytottk, hogy az emls sejtekben lejtszd homolg rekombinci felhasznlhat arra, hogy adott
gneket clzottan mdostsanak a genomban. Ksbb az Evans ltal kifejlesztett mdszert hasznlva,
embrionlis ssejtek genomjt sikerlt clzottan mdostaniuk. Capecchi ksbb kidolgozott egy szelekcin
22
alapul mdszert, melynek segtsgvel tesztelhetv vlt a homolg rekombinci sikeressge brmely
megclzott DNS szakasz esetn. A mdosts nem felttlenl jelenti a megclzott gn inaktivlst (knock-
out); lehetsges a megclzott helyre egy teljes, funkcikpes j gn beptse is (knock-in). A technolgia
forradalmastotta a biolgia szmos terlett, hiszen lehetsg nylt brmely gn funkcijt kzvetlenl, a
teljes llnyben vizsglni (ld. 0. fejezet). Taln a legjobb plda erre, hogy ma mr szmos genetikai
eredet emberi betegsg kutatshoz elengedhetetlen modellrendszer a megfelel KO (knock-out) egr.
Egy msik fontos mdszer, mellyel gnek mkdsnek clzott mdostsra van lehetsg, az gynevezett
RNS interferencia. A ms nven glcsendestsnek nevezett mdszer felfedezsrt 2006-ban Andrew Fire
(1959-) s Craig Mello (1960-) kapott Nobel-djat. A kt kutat modellorganizmusknt a Caenorhabditis
elegans nev fonlfrget hasznlta. A kutatk kimutattk, hogy az llat testbe injektlt ktszl RNS az
adott gn funkcivesztses mutcijhoz hasonl fenotpust eredmnyezett. (Az egyszl mintk esetn alig
volt kimutathat hats.) A ktszl RNS teht interferlt a gn mkdsvel. Fire s Mello ms gneket
megclozva is megismtelte a ksrletet, gy kimutattk, hogy a jelensg ltalnos, tovbb specifikus a
megclzott gnre. Mivel az RNS interferencihoz igen kis mennyisg ktszl RNS is elg volt,
feltteleztk, hogy valamilyen katalitikus komponens is szerepet jtszik a jelensg mgtti molekulris
mechanizmusban. Ma mr bizonytott, hogy az RNS interferencia a legtbb eukaritban mkd jelensg,
mely mgtt a sejtekben szintetizld mRNS molekulkat lebont enzimatikus mechanizmus ll. Ez az
enzimrendszer szmos fontos funkcival rendelkezik, gy pldul vdelmet nyjt a vrusokkal, vagy a
transzpozonokkal (mobil genetikai elemek) szemben, de elengedhetetlen szmos gn mkdsnek
szablyozshoz is. Napjainkra az RNS interferencia a gnmkds tanulmnyozsnak fontos eszkzv
vlt, st vrhat, hogy a jvben a humn gygyszatban is szerepet kap (ld. 0. fejezet).
1.6. Tovbbi olvasnival a fejezethez
Avery, OT, MacLeod, CM, and McCarty, M (1944) Studies on the Chemical Nature of the Substance
Inducing Transformation of Pneumococcal Types. Journal of Experimental Medicine 79: 137-158.
Watson JD, Crick FH (1953) Molecular structure of nucleic acids; a structure for deoxyribose nucleic acid.
Nature 171 (4356): 737738.)
Hershey A, Chase M (1952) Independent functions of viral protein and nucleic acid in growth of
bacteriophage. J Gen Physiol 36 (1): 39-56.
Nirenberg MW, Matthaei JH. (1961) The dependence of cell-free protein synthesis in E. coli upon
naturally occurring or synthetic polyribonucleotides.Proc Natl Acad Sci USA. 47:1588-602
Cohen, SN, Chang, ACY, Boyer, HW & Helling, RB (1973) Construction of biologically functional
bacterial plasmids in vitro. Proc. Nat. Acad. Sci. USA 70, 32403244
Sanger F, Nicklen S, Coulson AR (977). DNA sequencing with chain-terminating inhibitors. Proc. Natl.
Acad. Sci. U.S.A. 74: 54637
Palmiter RD, Brinster RL, Hammer RE, Trumbauer ME, Rosenfeld MG, Birnberg NC, Evans RM (1982)
Dramatic growth of mice that develop from eggs microinjected with metallothionein-growth hormone fusion
genes. Nature. 300(5893):611-5.
Saiki, R.; Gelfand, D.; Stoffel, S.; Scharf, S.; Higuchi, R.; Horn, G.; Mullis, K.; Erlich, H. (1988) Primer-
directed enzymatic amplification of DNA with a thermostable DNA polymerase. Science 239 (4839): 487
491
Fire A, Xu SQ, Montgomery MK, Kostas SA, Driver SE, Mello CC (1998) Potent and specific genetic
interference by double-stranded RNA in Caenorhabditis elegans. Nature 391:806-811.
23
2. A gntechnolgia alapja: molekulris klnozs
A rekombinns DNS technolgia (gnsebszet, genetic engineering) eszkztra lehetv teszi az
llnyek egyes tulajdonsgait meghatroz gnek azonostst, jellemzst s szabadon trtn
megvltoztatst. Megismerhetjk akr egy adott llny teljes genetikai llomnynak (genom)
informcitartalmt is, hiszen napjainkra a DNS szekvenlsa rutinszer feladatt vlt. Feltrhatjuk a gnek
mkdst szablyoz rgikat. Clzottan, irnytott mutcikat hozhatunk ltre, st, akr teljes gneket is
eltvolthatunk az adott llnybl, illetve mdostott, mutns gneket vihetnk be ksrleti llnyekbe
(reverz, azaz fordtott irny genetika). Ilyen mdon megrthetjk az egyes gnek, illetve az ltaluk kdolt
fehrjk mkdst. A genetikai kd univerzlis mivoltt kihasznlva lehetsges gneket tltetni ms
organizmusokba, ahol megtrtnhet a bevitt szekvencia transzkripcija s transzlcija. Az ilyen
organizmusokat felhasznlhatjuk arra, hogy a kdolt fehrjt nagy mennyisgben s tisztasgban lltsuk el
(heterolg fehrje expresszi). Ez a lehetsg az alapkutatsok mellett (a termeld fehrje mkdsnek
s szerkezetnek vizsglata) a biotechnolgiai ipar illetve a gygyszeripar szempontjbl is kulcsfontossg.
Az expresszlt fehrjt kdol szekvencit mdostva szmunkra hasznos vltozatokat hozhatunk ltre az
adott fehrjbl. Akr az eredetitl eltr funkcit, vagy aktivitst is hozzrendelhetnk ilyen mdon egy
fehrjhez (fehrjemrnksg vagy protein engineering). Arra is lehetsgnk nylhat, hogy sajt
sejtjeinkbe juttassunk be j genetikai informcit bizonyos betegsgek gygytsa rdekben (gnterpia).
Ahhoz, hogy a gntechnolgit tnylegesen alkalmazni lehessen, rekombinns DNS molekulkat kell
ellltanunk. A rekombinns DNS egy hordoz DNS molekulbl (vektor) s a vizsglni kvnt DNS-
bl (inszert) ll hibrid (kimra) molekula, amelyet a ksrletekhez szksges mennyisgben
molekulris klnozssal lltunk el.
.
A molekulris klnozs nem ms, mint egy specifikus inszertet tartalmaz rekombinns DNS
felszaportsa megfelel gazdasejtben (E. coli). Ezeknek a sejteknek a klnjaibl (bakterilis kolnik)
izollhatjuk a molekulris kln rekombinns DNS-t. Ltezik in vitro DNS szaportsi mdszer is, a
polimerz lncreakci (PCR), azonban ezzel a mdszerrel szigoran vve nem molekulris klnokat lltunk
el (ld. 0. fejezet).
2.1. I n vitro rekombinci
A trtneti sszefoglalbl mr kiderlt, hogy a molekulris klnozshoz egyrszt fel kellett fedezni azokat
az enzimeket, amelyekkel a DNS molekult in vitro szabni-varrni lehet, msrszt tallni kellett olyan DNS
molekulkat, amelyeket vektorr lehet alaktani (a vektorokkal szemben tmasztott kritriumokrl s a
tpusaikrl rszletesen a 7.1. fejezetben lesz sz). Vgl az in vitro ellltott rekombinns DNS-t egy
gazdasejtbe kell juttatnunk (ld. 4.3. fejezet) s valamilyen ton-mdon ki kell szelektlni azokat a sejteket,
amelyekbe az ltalunk megtervezett rekombinns DNS kerlt be.
A DNS manipulci, a molekulris klnozs in vitro szakasznak legfbb eszkzei a restrikcis
endonuklezok s a DNS-ligz enzim (a gntechnolgiban hasznlatos DNS-mdost enzimekkel
rszletesen a 3. fejezet foglalkozik).
A restrikcis endonuklezok (rviden restrikcis enzimek) foszfodiszter ktst hidrolizl enzimek. A
baktriumokat az idegen DNS-ekkel szemben vdelmez molekulris rendszer (ld. 1.2. fejezet), a
restrikci-modifikci DNS bont elemei, amelyek nagy szmban s sokflesgben llnak a gntechnolgus
rendelkezsre. Az enzimek tbbsge kzppontosan szimmetrikus, n. palindrom szekvencikat ismer
fel. Amennyiben a DNS kt szlnak elhastsa egymssal szemkzti foszfodiszter-ktseknl trtnik,
gynevezett tompa vgek (blunt end) keletkeznek (pl. DraI, ld. 2.2. bra). Ha azonban egymshoz kpest
elcssztatva, nhny bzissal tvolabb a felismerhely szimmetriatengelytl, gy ragads vgek (sticky
rekombinns DNS = vektor DNS + inszert DNS
24
end) jnnek ltre (pl. EcoRI, ld. 2.1. bra). A DNS-ligz enzim foszfodiszter kts ltrehozsval kpes
kt DNS molekult, vagy egy molekula kt vgt kovalensen sszekapcsolni. Ha kt klnbz eredet
DNS molekult EcoRI enzimmel hastunk, majd sszekevernk, akkor a DNS-ligz in vitro
rekombincival ltrehozhat hibrid, azaz rekombinns DNS molekulkat, mint azt a 2.1. bra szemllteti.
A restrikcis endonuklezokkal rszletesen a 3.2.1. fejezet foglalkozik.
2.1. bra: I n vitro rekombinci. Kt klnbz eredet DNS hastsa EcoRI restrikcis endonuklezzal. A ltrejv
DNS fragmentumok egymst felismer ragads vgekkel rendelkeznek. sszekapcsolsuk DNS-ligz segtsgvel
trtnik. Amennyiben a kt klnbz eredet DNS-vg kapcsoldik ssze, in vitro rekombinci trtnik.
Megjegyzend, hogy egy DNS molekula kt vgn tallhat ragads vgeket is sszekapcsolhatja a DNS-ligz. Ebben
az esetben nem jn ltre rekombinci, hanem pl. ha egy linearizlt vektor DNS-rl van sz, az cirkularizldik. Az
n. vektor nzrds kikszblhet, ha a hastott DNS 5-vgrl a foszft-csoportokat foszfatz enzimmel
eltvoltjuk (ld. 3.4.2. fejezet)
2.2. Rekombinns DNS ltrehozsa
A molekulris klnozs in vitro szakaszban alaktjuk ki a rekombinns DNS-t. A hordoz DNS
leggyakrabban egy cirkulris plazmid vektor (a plazmidok extrakromoszomlis elemek, a
baktriumsejtekben nllan replikld n. replikonok, ld. 7.2. fejezet)), mg a vizsgland DNS lehet egy
eukarita kromoszma. Pldaknt egy olyan klnozsi stratgit mutatunk be, ahol az inszertet a
kromoszmbl kt klnbz restrikcis enzimmel hastjuk ki. Ha a vektor DNS-t ugyanazon kt
restrikcis endonuklezzal hastjuk s a tiszttott hastsi termkeket sszekeverjk, a DNS-ligz a
kmcsben lezajl reakci sorn gyakorlatilag csak ezt a ktfle eredet DNS-t kpes egymshoz kapcsolni,
ezltal rekombinns DNS jn ltre, mint azt a 2.2. bra mutatja. Ez a direkcionlis vagy irnytott
klnozs, amit rszletesen a 4.2. fejezetben ismertetnk.
25
2.2. bra: Rekombinns DNS ltrehozsa irnytott klnozssal. A plazmid vektort s a kromoszomlis DNS-t is
ugyanazzal a ktfle restrikcis enzimmel hastjuk. Az egyik vgn "ragads" (EcoRI), a msik vgn "tompa" vg
(DraI) DNS molekulkat a DNS-ligz kovalens sszekapcsolja, ezzel ltrejn a rekombinns DNS.
2.3. Molekulris klnok kialaktsa
A DNS klnozs in vivo szakasza a rekombinns DNS gazdasejtbe juttatsa s felszaportsa. A DNS
sejtekbe juttatsra tbbek kztt a bakterilis transzformci jelensgt lehet kihasznlni (tovbbi
gnbeviteli eljrsok lersa a 4.3. fejezetben olvashat). Egy baktrium sejt ltalban csak egyetlen
rekombinns DNS-t vesz fel. Mivel a transzformci hatsfoka alacsony, szksgnk van valamilyen
szelekcis eljrsa. A vektor tartalmaz egy antibiotikum elleni vdelmet biztost gnt (antibiotikum
rezisztencia gn), amely megfelelen vlasztott krlmnyek kztt szelektv tllst tesz lehetv a
rekombinns DNS-t hordoz sejtek szmra. A transzformls utn a sejteket olyan, antibiotikumot
tartalmaz, szelektl tptalajra helyezzk, ahol csak a rekombinns plazmidot (s gy az adott
antibiotikumra rezisztencit biztost gnt) tartalmaz sejtek kpesek szaporodni. Minden sejtbl egy
kolnia keletkezik (amely genetikailag azonos sejtekbl, klnokbl ll). Sok ezer ilyen, a kromoszma
klnbz darabjt tartalmaz kolnia egyttesen egy genomilis knyvtrat reprezentl (ld. 8.2. fejezet).
Egy-egy kolnin bell azonos rekombinns DNS-t tartalmaz sejtek vannak, melyeket tovbb lehet
szaportani, s a klnozott DNS-t izollni lehet. A folyamat smjt a 2.3. bra mutatjuk be.
26
2.3. bra: A molekulris klnozs elvi vzlata. A rekombinns DNS-t transzformcival juttatjuk az E. coli
gazdasejtbe, ahol az a baktriumsejt kromoszmjtl (amit nem brzoltunk) fggetlenl replikldik s tbb
kpiban lesz jelen az utdsejtekben, ezzel is hozzjrulva a DNS kln felszaportshoz (amplifikci). A klnbz
inszerteket tartalmaz baktriumok egyedi klnok. A kromoszma egszt darabokban tartalmaz E.coli klnok
sszessge a genomilis knyvtr (ld. 8.2. fejezet). A rekombinns DNS a sejtekbl tiszta formban egyszeren
kinyerhet (ld. 4.1.1. fejezet).]
2.4. Tovbbi olvasnival a fejezethez
Watson, JD et al. (2007) Recombinant DNA: Genes and Genomes. A Short Course. W. H. Freeman. ISBN-
10: 0716728664
Brown TA (2010): Gene Cloning and DNA Analysis: An Introduction. Wiley-Blackwell, 6th Edition
27
3. DNS mdost enzimek s felhasznlsuk
A manapsg rutinszeren alkalmazott biotechnolgiai s molekulris biolgiai eljrsok jelents rsze a
DNS mdostst clozza. Ezeknek a mdszereknek a kialaktsa az 1970-es vekben kezddtt, amikor a
kutatk elkezdtk a DNS manipullsra szolgl enzimeket tiszttott formban ellltani s vizsglni.
Ksbb ezeket az enzimeket, amelyek a termszetben a rekombinci, replikci s hibajavts
folyamataiban vesznek rszt, sikeresen hasznltk a DNS molekulrl trtn msolatok ksztsre, a
DNS sztvgsra vagy ppen sszeragasztsra. A mdszerek fejlesztse lehetv tette, hogy megszlessen
a rekombinns DNS technolgia, vagyis klnbz DNS szakaszok jrakombinlsra, sszeptsre
nylt lehetsg plazmidok s ms eredet DNS fragmentumok (pl. kromoszmk darabjainak)
felhasznlsval. Mindez megteremtette a DNS klnozsnak lehetsgt is (ld. 2. s 4.2. fejezet). Ehhez
elegend egy gnt vagy ms DNS fragmentumot plazmidba vagy egyb hordozba (vektor) pteni, majd
megfelel gazdaszervezetbe juttatni, s ott a rekombinns DNS replikldni kpes.
A DNS mdostsra szolgl enzimeknek ngy nagy csoportjt klnbztethetjk meg.
- DNS-polimerzok:
Funkcijuk egy, a templt DNS-sel vagy RNS-sel komplementer j polinukleotid szl szintzise.
- Nuklezok:
Kpesek a nukleotidokat sszekt foszfodiszter ktseket elhastani (hidrolizlni), s gy a DNS-t
(le)bontani.
- Ligzok:
Foszfodiszter kts ltrehozsval kpesek kt DNS molekult, vagy egy molekula kt vgt
sszekapcsolni.
- Lncvg mdost enzimek:
A DNS lnc vgeinek mdostsval egyes klnozsi technikkban van szerepk.
3.1. DNS-polimerzok
Szmtalan molekulris biolgiai mdszerhez elengedhetetlen a DNS-polimerzok alkalmazsa, gondoljunk
akr csak a PCR-re (Polymerase Chain Reaction; ld. 0. fejezet) vagy a DNS szekvenlsra (ld. 5. fejezet).
ltalnossgban DNS-polimerznak nevezzk azokat az enzimeket, amelyek kpesek DNS szintzisre
dezoxiribonukleozid-trifoszft (dNTP) ptkvek (aktivlt monomerek) felhasznlsval. Ezen bell
megklnbztethetjk a templt-fgg DNS-polimerzokat, amelyek egy minta, templt DNS vagy
RNS alapjn, annak msolatt ksztik el, valamint lteznek templt-fggetlen DNS-polimerzok is (ilyen
enzim pl. a terminlis dezoxinukleotid-transzferz).
A DNS-polimerzok multifunkcis enzimek, amelyek a szintzis mellett kpesek a DNS lncvgeinek
hidrolzisre is. Mg a szintzis szigoran egy irnyban, az 5-vgtl a 3-vg irnyban zajlik, a lebonts
a lnc mindkt vge fell megvalsulhat, az adott polimerz aktivitstl fggen. Az egyszerbb
trgyalhatsg rdekben rdemes megismerkedni a DNS molekula kapcsn a direkcionalits fogalmval.
A molekulris biolgiban direkcionalitsnak, vagy egyszeren irnynak nevezzk az egyszl
nukleinsavak hosszanti kmiai orientcijt (a DNS, RNS, a fehrjelncok direkcionlis polimerek). A
DNS szl vgeinek elnevezse a nukleotidok cukorgyrjnek konvencionlis szmozsbl ered (ld. 3.1.
bra), ily mdon egyrtelmen meghatrozhat a szl 5- (ejtsd: t-vessz) s 3- (hrom-vessz) vge.
Amennyiben egy hossz DNS szakasz rgiit szeretnnk megklnbztetni, beszlhetnk upstream
(felfel irnyul) szakaszokrl, amelyek az 5-vghez esnek kzelebb, illetve downstream (lefel
28
irnyul) szakaszokrl a 3-vghez kzelebb. A templt-fgg DNS-polimerzok azon tulajdonsga, hogy j
foszfodiszter kts kialaktsra csak a 3-hidroxil csoporttal kpesek, meghatrozza a szintzis 53
irnyt.
3.1. bra: A DNS molekula irnyultsga, 5- s 3-vge. A) A guanin nukleotid a dezoxiribz gyr szmozsval,
aminek alapjn meghatrozhat a DNS lnc 5- s 3-vge. B) A DNS molekula kmiai szerkezete, kln jellve a
DNS felptsben rsztvev dezoxiribonukleotidokat (rszlet).
A lnc bontsa kapcsn ktfle aktivitst klnbztethetnk meg, amelyekkel kln-kln vagy egytt
szintn mindegyik DNS-polimerz rendelkezik.
- 35-exonuklez aktivits: Az irny megjells arra utal, hogy az enzim a DNS szlon visszafel
haladva kpes a mr szintetizlt nukleotidot eltvoltani. A polimerz ezen tulajdonsgt
proofreading vagy hibajavt aktivitsnak is nevezzk, mert ez biztostja, hogy egy esetlegesen
rosszul, nem a bzisprosods szablyainak megfelel nukleotid bepls javtsa megtrtnjen.
- 53-exonuklez aktivits: Kevesebb polimerz rendelkezik ezzel az aktivitssal, aminek sorn az
enzim kpes a lncon elre haladva az esetleg mr ott tallhat, a templttal komplementer DNS szlat
elbontani (ezt a hasads-elmozduls ketts aktivitst nevezi a szakirodalom nick transzlci-nak,
ld. 3.3. bra). A termszetben a DNS replikcija sorn van szksg erre a funkcira.
A templt fgg DNS-polimerzok mkdsnek fontos jellemzje, hogy de novo szintzisre nem kpesek.
j DNS szl szintzishez szksges egy rvid ktszl szakasz, s gy az j szl szintzise egy mr
meglev 3-vgrl indulhat. A termszetben az j szl szintzise mindig egy rvid RNS szakasszal, a
primerrel indul. A biotechnolgiai gyakorlatban primerknt ltalban egy rvid szintetikus oligo-
dezoxiribonukleotid (rviden oligonukleotid) molekult hasznlnak, ami a templt DNS-hez kapcsoldva
biztostja a szksges ktszl szakaszt (ld. 3.2. bra). Ennek nagyon fontos gyakorlati jelentsge, hogy
gy a DNS polimerizci kezdpontja bellthat, vagyis brmilyen, hosszabb DNS szl szintetizlhat a
megfelel helyre tervezett primer segtsgvel. (Mindez termszetesen nem lenne lehetsges, ha a DNS
polimerizci vletlenszer helyrl indulna.)
29
3.2. bra: A primerek jelentsge. A) A templt-fgg DNS-polimerzok mkdshez ktszl DNS-re van
szksg, ami a templttal komplementer rvid oligonukleotid, primer hozzadsval biztosthat. B) A primer a
bzissorrendjnek megfelel komplementer szakaszhoz hibridizldik, ezzel meghatrozva a DNS szintzis
kezdpontjt.
3.1.1. A DNS-polimerz I s a Klenow-fragmentum
A legkorbban felfedezett DNS-polimerz, amelyet eredetileg Escherichia coli baktriumbl izollt Arthur
Kornberg, de minden prokaritban megtallhat. Fontos szerepe van a bakterilis genom replikcijban,
eltvoltja az RNS primert a kvet szlrl s az Okazaki-fragmentumok sszektst vgzi (ld. Bevezets a
biokmiba elmleti e-jegyzet).
Ngyfle enzimatikus aktivitssal rendelkezik:
- 53 DNS-fgg DNS-polimerz aktivits
- 35 exonuklez aktivits (proofreading aktivits)
- 53 exonuklez aktivits (RNS primer eltvoltsa s kivgsos hibajavts)
- 53 RNS-fgg DNS-polimerz aktivits (valsznleg nincs biolgiai jelentsge)
A molekulris biolgiai gyakorlatban a natv enzim hasads-elmozduls, angolul nick-translation
kpessgt hasznljk ki (ld. 3.3. bra). A termszetben az RNS primerek eltvoltsra s DNS-re
cserlsre szolgl a folyamat. A laboratriumban a ktszl DNS-en mestersgesen, DN-z kezelssel
nick-eket, bevgsokat ejtenek, majd a DNS-polimerz I 53 exonuklez s 53 polimerz
aktivitst kihasznlva, a hasadstl indulva a DNS egy szakaszt kicserlik. Ennek sorn lehetsg van
pldul radioaktvan vagy fluoreszcensen jellt nukleotid analgok DNS lncba ptsre.
Mg a fenti pldban az enzim 53 exonuklez aktivitst lehet kihasznlni, azoknl az alkalmazsoknl,
ahol kizrlag a polimerz aktivitsra lenne szksg (mint pldul a szekvenls), nem szerencss, hogy az
enzim kpes az jonnan szintetizlt DNS lncot lebontani. Az enzim tovbbi vizsglatakor kiderlt, hogy
proteolitikus hastsa kt fragmentumot (76 kDa s 36 kDa) eredmnyez, amelyek kzl az egyik, a
felfedezjrl Klenow-fragmentumnak nevezett darab rendelkezik mind a polimerz, mind a proofreading
aktivitssal, de hinyzik belle az 53 exonuklez aktivits. A Klenow-fragmentumot manapsg
rekombinns mdon, E. coli sejtekben termelik. A Klenow-fragmentum felhasznlhat a Sanger-fle
30
didezoxi szekvenlsban (ld. 5. fejezet), valamint restrikcis endonuklezok ragads vgnek feltltsre,
illetve 3-tlnyl vgek lebontsra (tompa vagy blunt-end vg kialaktsra).
3.3. bra: Nick transzlci (hasads-elmozduls). A DNS-polimerz I enzim az 53 irny polimerz aktivits
mellett 53 irny exonuklez aktivitssal is rendelkezik, s ezek kombincija teszi lehetv a hasads-
elmozdulst. A laboratriumi gyakorlatban jellt nukleotidok beptsre hasznlhat a jelensg. Elsknt a
dezoxiribonuklez I (DN-z I) enzimmel kis bevgsokat (nick) ejtenek a DNS szlain. Ezutn a DNS-polimerz I a
bevgstl indulva a sorban kvetkez nukleotidokat kivgja, s a reakcielegyhez adott jellt nukleotidokat pti be.
A reakci eredmnyeknt kapott DNS szlon a nick elmozdul elre fel addig a pontig, ahol a DNS-polimerz I
levlik a DNS lncrl. A lnc folytonossga liglssal llthat helyre.
3.1.2. T4 DNS-polimerz
Ktfle enzimatikus aktivitssal rendelkezik:
- 53 DNS-fgg DNS-polimerz aktivits
- 35 exonuklez aktivits (proofreading aktivits)
A T4 jel E. coli bakteriofg genomjbl szrmazik. Tbb, mint 200-szor ersebb 35 exonuklez
aktivitssal rendelkezik, mint a DNS-polimerz I vagy a Klenow-fragmentum. Tompa vg kialaktsra
alkalmas, valamint a ligz-fggetlen klnozsban is hasznljk a vektor megfelel ragads vgeinek
kialaktsra (ekkor dTTP hozzadsval biztostjk, hogy a kvnt nukleotidig vgja vissza az enzim a
DNS megfelel szlt) (ld. 4.2.5. fejezet).
3.1.3. T7 DNS-polimerz
A T7 DNS-polimerz in vivo a T7 bakteriofg DNS-nek gyors replikcijrt felels. Az enzim kt fehrje,
a T7 bakteriofg 5-s gn fehrjetermknek (80 kDa) s az E. coli tioredoxin fehrjjnek (12 kDa)
komplexe.
Ktfle enzimatikus aktivitssal rendelkezik:
- 53 DNS-fgg DNS-polimerz aktivits
31
- 35 exonuklez aktivits (proofreading aktivits)
A 35 exonuklez aktivitsa jelents, krlbell 1000-szerese a Klenow-fragmentumnak, ami egyben
jelzi, hogy nagyon nagy hsg (high fidelity) enzim, vagyis a DNS szintzis nagy pontossggal zajlik.
Kiemelkeden magas az enzim processzivitsa is, ami annyit jelent, hogy hossz ideig a DNS szlon marad,
s gy kpes akr tbb ezer nukleotid szintzisre. Szekvenlsra ez az enzim, br magas processzivitsa
fontos elny, eredeti formjban nem alkalmas, mert a szekvenls sorn elkerlend brmifajta exonuklez
aktivits, nehogy az enzim kivgja a lnctermincis nukleotidot. Ezrt erre a clra az enzim egy mdostott,
Sequenase nven forgalmazott formjt hasznljk, amelybl teljesen hinyzik az exonuklz aktivits. A T7
DNS-polimerzt ezen kvl alkalmazzk helyspecifikus mutagenezis mdszereknl is (ld. 0. fejezet).
3.1.4. Hstabil DNS-polimerzok
Br mr viszonylag korn, a 1960-as s 1970-es vekben izolltak hstabil DNS-polimerzokat, igazi
jelentsgk a polimerz lncreakci (PCR) elterjedsvel (ld. 6.2.2. fejezet) mutatkozott meg, amihez
magas hmrskleten is aktv enzimre van szksg.
3.1.4.1. Taq-polimerz
Eredetileg a Yellowstone Nemzeti Parkban tallhat hforrsokban l Thermus aquaticus nev termofil
baktriumbl izollta Thomas D. Brock 1965-ben (a baktrium nevbl szrmazik a polimerz neve,
ugyanazt a logikt kvetve, mint a restrikcis endonuklezok elnevezse; ld. 3.2.1.). Kivlan hasznlhat
PCR-hez, mert az enzim flletideje mg 95
o
C-on is 40 perc. Mivel nem rendelkezik 35 exonuklez
aktivitssal, nem tartozik a nagy hsg polimerzok kz. A hibagyakorisga ~10
-4
, de a pontos rtk
ersen fgg az adott ksrleti elrendezstl. 1 kb mret clszekvencit ~30 sec alatt msol le. Ms, 35
exonuklez aktivits nlkli enzimekhez hasonlan templt-fggetlen dezoxinukleotid-transzferz
aktivitssal rendelkezik, aminek kvetkeztben (preferltan) adenin nukleotidokat pt be a DNS 3-
vgre. Ezt a tulajdonsgt hasznljk ki a TA klnozsnl (ld. 4.2.4. fejezet). A gyakorlatban manapsg
leginkbb rutin PCR-hez, fknt kolnia PCR-hez hasznljk, amikor a cl a baktrium kolnik kzl
azokat kivlasztani, amelyek egy adott klnt tartalmaznak. Ilyen esetben nem problma egy-egy mutci a
PCR termkben.
3.1.4.2. Pfu-polimerz
A hipertermofil Pyrococcus furiosus sbaktriumbl szrmaz DNS-polimerz. A Taq-polimerznl
jelentsen nagyobb hstabilitssal rendelkezik. Ezen kvl legfontosabb tulajdonsga, hogy rendelkezik
proofreading aktivitssal, ezrt minden olyan alkalmazsra hasznlhat, ahol fontos a pontos msols
(tlagosan kb. 350-400 ezer bzispronknt pt be hibs nukleotidot). Valamivel lassabb, mint a Taq-
polimerz, 1-2 perc alatt amplifikl 1 kbp mret DNS-t 72
o
C-on. Nagyon sok laboratriumban a Pfu-t
hasznljk elsdleges DNS-polimerzknt, mind PCR-hez, mind pldul helyspecifikus mutagenezishez.
3.1.4.3. Phusion-polimerz
A Phusion-polimerz egy proofreading aktivits Pyrococcus-szer polimerz s egy DNS-kt domn
fzis (innen a nv) termke. Egyesti magban a Taq- s a Pfu-polimerzok elnyeit. Rendkvl nagy
msolsi hsg (fidelity) enzim, tbb, mint 2 milli bzispronknt pt be hibs nukleotidot. Ezen kvl
kifejezetten gyors is, ami jelentsen cskkenti a PCR reakci idejt, valamint a sikeres PCR-hez
gyakorlatilag nem szksges optimalizci sem. Alkalmas mind rutin, mind kompliklt, pldul hossz vagy
32
nehz templtokkal val munkra is. Egyetlen htrnya, hogy az emltett polimerzok kzl ez a
legdrgbb.
Nhny tovbbi, a PCR-hez hasznlt polimerz enzimet az 6.2.2. fejezetben ismertetnk.
3.1.5. Reverz transzkriptz
RNS-fgg DNS-polimerzok, amelyek a retorvrusok replikcis ciklusban jtszanak szerepet. A
retrovrusok genomja RNS-bl ll, amirl DNS msolat kszl a gazdaszervezet fertzse utn. A
laboratriumi gyakorlatban reverz transzkriptzok hasznlhatk mRNS molekulkrl DNS msolat
ksztsre. Az gy szintetizlt, a templt mRNS-el komplementer szlat nevezik cDNS-nek. A cDNS
templtknt szolglhat tovbbi PCR reakcihoz. Az mRNS-bl kiindul, s vgl amplifiklt DNS termket
eredmnyez reakcit RT-PCR-nek, reverz transzkripcis PCR-nek hvjk (ld. 6.4.4. fejezet). (Az RT-PCR
nem sszekeverend a valsidej, real-time PCR-rel, aminek sorn a fluoreszcensen jellt DNS
amplifikcijnak kvantitatv meghatrozsa trtnik.) A reverz transzkriptz fontos felhasznlsi terlete a
cDNS knyvtrak ksztse is (ld. 8.3. fejezet).
3.2. Nuklezok
Szmos nuklezt hasznlnak rutinszeren a mindennapos molekulris biolgiai laboratriumi gyakorlatban.
A legtbb nuklezt kt csoportra lehet osztani:
- Exonuklezok: olyan enzimek, amelyek a DNS vagy RNS kt vgrl kpesek nukleotidok
eltvoltsra.
- Endonuklezok: a nukleinsavak kzbls rszein tallhat foszfodiszter ktseket tudjk elhastani.
3.2.1. Restrikcis endonuklezok
A restrikcis endonuklezok baktriumokban, archekban, s egyes vrusokban megtallhat enzimek, s a
restrikcis-modifikcis rendszer komponensei (ld. 1.2. fejezet).
A restrikcis endonuklezok (vagy rviden restrikcis enzimek) specifikus helyeket ismernek fel a DNS
molekuln, majd a DNS mindkt szlt tvgva kpesek azt elhastani (foszfodiszter ktseket
hidrolizlnak). Elnevezsknek kln nmenklatrja van. A HindIII enzim nevnek magyarzata, hogy a
Haemophilus influenzae baktrium d szerotpusbl harmadikknt izolltk. Hasonlkppen kpezhet az
EcoRI enzim neve is: az Escherichia coli RY13 trzsbl elsknt izolltk.
Egy random bzissorrend DNS-t tekintve a statisztikai hastsi gyakorisg attl fgg, hogy milyen hossz
az enzim felismersi szekvencija. Ha az emsztenzim felismer helye 4 bzisprt tartalmaz, akkor, mivel
minden egyes bzispr helyn ngyfle varici (A, T, G, C) lehetsges, 4
4
= 256 bzispronknt
szmthatunk hasthelyre. Ha a felismer hely 6 nukleotid hosszsg, a hasts valsznsge 1/4096-ra
mdosul (4
6
= 4096). A valsgban a DNS szekvencija nem vletlenszer, ezrt a hasthelyek eloszlsa
sem teljesen kveti a fentieket. Vannak restrikcis endonuklezok, amelyek felismerhelye megegyezik, de
hasthelyk klnbz, ezeket neoskizomereknek nevezik. Azokat az enzimeket, amelyeknl mind a
felismer, mind a hasthely egyforma, izoskizomereknek hvjk.
A restrikcis enzimek leggyakoribb felhasznlsi terlete a molekulris klnozs (ld. 2. s 4.2. fejezetek),
valamint a DNS fizikai trkpezse (ld. 9.1.1. fejezet) s az ahhoz kapcsold terletek (pl. diagnosztika,
bngyi orvosszakrti vizsglatok). A restrikcis endonuklezokat hagyomnyosan ngy csoportba osztjk
a felismert szekvencia, a hasthely, az alegysg kompozci s a kofaktor szksglet szerint.
33
3.2.1.1. I-es tpus restrikcis endonuklezok
Multifunkcis fehrjk restrikcis s metil-transzferz aktivitssal rendelkeznek. Komplex, hrom
alegysgbl felpl szerkezetk van, Mg
2+
szksges a mkdskhz, valamint kofaktoruk mg az ATP
s az S-adenozil-L-metionin (AdoMet) is. Hasthelyk a felismersi helytl tvol (tbb ezer bzisprnyira)
helyezkedik el. Korbban gy gondoltk, hogy az I-es tpus enzimek ritkk, azonban a teljes genomok
vizsglatbl kiderlt, hogy valjban nagy szmban tallhatk meg. Br a szervezet biokmiai
folyamataiban fontos szerepk van, gyakorlati hasznosthatsguk kicsi, mert nem szigoran meghatrozott
a hasts pozcija a felismer helyhez kpest.
3.2.1.2. II-es tpus restrikcis endonuklezok
Vltozatos szerkezet enzimek, csak restrikcis funkcival rendelkeznek (a metiltranszferz komponenst
kln gn kdolja). A mkdskhz Mg
2+
-ot ignyelnek. Hasthelyk a felismer helyben vagy annak
kzvetlen kzelben tallhat. Ebbe a csaldba tartozik a restrikcis endonuklezok tlnyom tbbsge,
eddig krlbell 4000 ilyen tpus enzimet rtak le. A felismerhely ltalban 4-8 bzispr hosszsg, s
jellemzen palindrom szekvencia. A palindrom kifejezs azt jelenti, hogy a DNS bzissorrendje elre s
htrafel olvasva (a kt, komplementer lncra vonatkoztatva) ugyanaz. Pldul a KpnI nev enzim felismer
helye az 5-GGTACC-3 szekvencia. Ennek a komplementer prja 35 irnyban CCATGG, ami
visszafel olvasva ppen GGTACC.
A restrikcis enzimek hasthelye eredmnyezhet ragads vget vagy tompa vget. Elbbinl a hasts
eremnyeknt az egyik szlon rvid tlnyl vg jn ltre, pldul az emltett KpnI az tdik nukleotid utn
hast (GGTAC/C), s gy ragads vget eredmnyez, 3-tlnyl vggel (ld. 3.4. bra).
3.4. bra: Ragads s tompa vgek. A restrikcis enzimek hastsnak termke lehet ragads vg (sticky end) vagy
tompa vg (blunt end) DNS. A) A KpnI enzim ragads vgeket hoz ltre, mert a palindrom hasthelyet
aszimmetrikusan vgja szt. B) A SmaI enzim a hasthely kzepn vg, ezrt nem keletkezik tlnyl vg.
Ezzel szemben a SmaI enzim, amelynek felismer helye a CCCGGG szekvencia, a harmadik nukleotid utn
hastva (CCC/GGG) tompa vget hoz ltre. A restrikcis enzimek egyik legismertebbje, az EcoRI a
GAATTC szekvencit ismeri fel s az els nukleotid utn hastja (G/AATTC), ezltal 5-tlnyl vg jn
ltre (ez a gyakoribb tlnyl vg tpus).
A II-es tpus enzimek meghatrozott helyen hastjk a DNS-t, gy az emszts reproduklhat s a
keletkezett termkek szekvencija pontosan meghatrozott lesz. Ma mr tbb ezer ilyen enzimet
ismernk (>3000 enzim, >250 felismerhellyel 750 baktrium trzsbl) s sok szz kaphat kereskedelmi
34
forgalomban. A II-es tpus endonuklezok legtbbje homodimer szerkezet (ld. 3.5. bra), amely
szerkezeti tulajdonsg egyrszt sszecseng a felismerhely szimmetrikus szerkezetvel, msrszt a kt
azonos DNS-kthely (bivalencia) ersebb DNS ktdst tesz lehetv.
3.5. bra: Az EcoRI restrikcis enzim trszerkezete. A II-es tpus restrikcis endonuklezok egyik tipikus
kpviselje az EcoRI enzim. Homodimer szerkezet, egyenknt 31 kDa mret alegysgekbl ll. Mindkt alegysg
tartalmaz egy hurok rgit, amelyek krbelelik a DNS-t (narancssrga). Az brn lthat, hogy a DNS aszimmetrikus
elhasadsa rvn ragads vgek jnnek ltre. Az enzim kristlyostsa mangn-ionok jelenltben trtnt (lila
gmbk), amelyek a natv enzimben megtallhat magnzium-ionok helyt foglaljk el.
Ksbb tbb alkategrijt lltottk fel ennek az enzimcsaldnak, ahov azok az enzimek tartoznak,
amelyek jellegzetes tulajdonsgaikban klnbznek a tipikus II-es tpus endonuklezoktl. A II.M tpus
enzimek pldul kpesek metillt DNS felismersre s elhastsra is. Ilyen a DpnI nev restrikcis
endonuklez, amelyet helyspecifikus mutagenezisnl hasznlnak a templt DNS elbontsra (ld. 11.2.2.
fejezet). A II.M tpus enzimek meghatrozott helyen hastjk a DNS-t, a DpnI hastlye pldul GA/TC. A
IV-es tpus restrikcis endonuklezoknak is metillt DNS a szubsztrtja, azonban a II.M tpustl eltren
nem specifikus helyen hastanak.
3.2.1.3. III-as tpus restrikcis endonuklezok
Nagymret, kt alegysgbl felpl fehrjk (hidrolizl alegysg s metill alegysg). Szintn Mg
2+
-
fgg enzimek, kofaktoruk az ATP, az S-adenozil-L-metionin segti a metil transzfer reakcit, de nem
felttlen szksges a mkdskhz. Hasthelyk a felismersi hely kzelben (tlalban 25-27
bzisprnyira) tallhat, nem palindrom. Akrcsak az I-es tpus enzimek, itt is kt szekvencia rszbl ll a
felismer hely, s az enzim kpes a DNS szl transzlokcijra. A hasts az egyik felismer hely kzelben
trtnik.
3.2.1.4. IV-es tpus restrikcis endonuklezok:
Mdostott, ltalban metillt DNS-t ismernek fel s hastanak, specifitsuk alacsony. Nem a restrikcis-
modifikcis rendszer rszei.
35
3.2.2. Egyb nuklezok
3.2.2.1. S1-nuklez
Az Aspergillus oryzae gombbl szrmaz S1-nuklez olyan endonuklez, amelyik egyszl DNS-t vagy
RNS-t kpes lebontani. Az enzim tszr aktvabb DNS-en, mint RNS-en. Ktszl polinukleotid is lehet az
S1-nuklez szubsztrtja, ha tartalmaz egyszl szakaszokat, ilyen lehet egy hurok rgi vagy egy gap.
Kofaktora a Zn
2+
, pH optimuma a savas tartomnyban, 4.0-4.3 kztt van. Felhasznlhat tompa vg
kialaktsra, illetve egyszl DNS s RNS szelektv lebontsra.
3.2.2.2. Dezoxiribonuklez (DN-z) I
A dezoxiribonuklez I (DN-z I), ellenttben a fentebb trgyalt S1-nuklezzal, egy- s ktszl DNS
lebontsra egyarnt kpes. A 31 kDa mret enzim ngy izoenzim keverke, s maximlis aktivitst
kalcium-, magnzium- vagy mangn-ion jelenltben mutat. Specifitsa s hatsmechanizmusa a jelen lev
kofaktortl fgg. Mg pldul Mg
2+
jelenltben a kt szlat random helyeken hastja, Mn
2+
jelenltben
nagyjbl egy helyen trtnik a hasts, tompa vagy egy-kt nukleotidnyi tlnyl vget kialaktva. A
molekulris biolgiai gyakorlatban sokrten felhasznlhat, pldul didezoxi- (Sanger-fle) szekvenlskor
vletlenszer DNS fragmentumok kialaktsra, vagy jellt DNS ltrehozsra hasads-elmozduls (nick
translation) technikval (ld. 3.3. bra). Nagyon gyakran alkalmazzk fehrje vagy RNS prepartumok
DNS-tl val megtiszttsra is.
3.3. DNS-ligzok
A restrikcis endonuklzzal kezelt DNS fragmentumok jra sszekthetk kovalensen DNS-ligz
hozzadsval. A ligz tpustl fggen a reakci kofaktora ATP (eukaritk, vrusok s bakteriofgok)
vagy NAD
+
(baktriumok).
Az emlskben a DNS-ligzok ngy tpusa fordul el, szerepk van tbbek kztt az Okazaki-
fragmentumok sszekapcsolsban (DNS-ligz I), illetve klnbz hibajavt mechanizmusokban, mint
pldul a nukleotid-kivgssal jr DNS hibajavts (DNS-ligz III), vagy a ktszl DNS trse s javtsa
(DNS-ligz IV).
A laboratriumi gyakorlatban leggyakrabban a T4 bakteriofggal fertztt E. coli-bl izollt T4-ligzt
hasznljk. Hatsmechanizmusnak lnyege, hogy kpes a DNS egy szln tallhat lyukakat
foszfodiszter kts ltrehozsval betmni (ld. 3.6. bra). Kicsit bonyolultabb eset, ha egy restrikcis
hasts eredmnyeknt kapott kt DNS vget szeretnnk jra sszekapcsolni, vagy egy plazmidba
szeretnnk j inszertet liglni. Ekkor az enzimnek kt foszfodiszter kts szintzist kell elvgeznie.
Aktivitshoz ATP-re van szksge (ellenttben az E. coli DNS-ligzzal, amely rdekes mdon
energiaforrsknt NAD-ot hasznl). Ezen kvl az is felttele a sikeres reakcinak, hogy a ligland kt
DNS vg egymshoz megfelelen kzel kerljn, mert az enzim csak a szintzist vgzi, a DNS kt vgt
nem tartja egyms kzelben. Ragads vgek esetn egyszerbb a helyzet, mert a vletlenszeren
egymshoz kzel kerl vgek gyengn (a bzisprok hidrognktsein keresztl) sszekapcsoldhatnak, s
ha ez a klcsnhats elegend ideig fennll, a ligz hozz tud kapcsoldni a DNS-hez, s ltrehozza a
hinyz foszfodiszter ktseket (kondenzcis reakcival). Tompa vgek esetn nincs lehetsg az emltett
tmeneti klcsnhats kialakulsra, ezrt a liglsi reakci hatkonysga ebben az esetben alacsony (az
enzimkoncentrci nvelsvel javthat). Megjegyzend, hogy ellenttben a T4 DNS-ligzzal, az E. coli
DNS-ligz a tompa vgek sszekapcsolsra nem kpes.
A laboratriumban a liglsi reakci egyik legfontosabb faktora a hmrsklet. Az enzim hmrskleti
optimuma 25
o
C, ezen a hmrskleten azonban cskken a DNS vgek tmeneti klcsnhatsnak eslye.
36
Ezrt a liglst tipikusan alacsonyabb hmrskleten, 16
o
C-on vgzik, de a tlnyl DNS vgektl fggen
akr arra is szksg lehet, hogy 4-8
o
C-on trtnjen a reakci. Ilyenkor a szoksos nhny perc helyett tbb
ra szksges a hatkony liglshoz.
3.6. bra: A DNS ligz mechanizmusa. A DNS ligzok ltal katalizlt reakciknak hrom alapvet lpse van. 1)
Elsknt kovalens enzim-AMP intermedier jn ltre pirofoszft keletkezse mellett (feltve, hogy ATP a kofaktor), az
enzim egy lizin aminosavn keresztl. 2) Kvetkez lpsknt az adenil-csoport (AMP) a DNS szabad 5-foszft
csoportjnak addik t, s 3) aktivlja azt. Vgl a 4.) lpsben a 3-hidroxil csoport nukleofil tmadknt reagl az
aktivlt 5-foszft csoporttal, gy sszektve a foszftgerincet AMP felszabadulsa mellett.
3.4. Vgmdost enzimek
3.4.1. Terminlis transzferz
A biotechnolgiai gyakorlatban borj csecsemmirigybl izollt terminlis transzferz enzim
homopolimer ragads vgek kialaktsra hasznlhat (farkazs). Az enzim gyakorlatilag egy
templt-fggetlen DNS-polimerz. Ahogy fent emltettk, a tompa vg ligls hatsfoka igen alacsony,
amin segteni lehet ragads vg mestersges kialaktsval. A tompa vget eredmnyez hasts utn a
terminlis transzferz aktivitst kihasznlva pldul poli(G) farkat lehet a DNS-re szintetizlni dGTP
hozzadsval, ami egy hasonl reakciban elksztett, de dCTP hozzadsval kialaktott, immr ragads
vg DNS darabhoz liglhat (ld. 3.7. bra).
37
3.7. bra: A terminlis transzferz enzim aktivitsa. A terminlis transzferz aktivitsa hasznlhat tompa vg
DNS molekulk mdostsra, mivel templt nlkl is kpes polinukleotid lnc szintzisre. Az brn bemutatott
pldn dGTP hozzadsval az enzim poli(G) lncot szintetizl a DNS 3-vgre, amely knnyen liglhat a
komplementer szlon poli(C) farkat tartalmaz molekulval.
3.4.2. Alkalikus foszfatz
A vgmdost enzimekhez sorolhat a hidrolzok kz tartoz alkalikus foszfatz is. ltalnossgban az
alkalikus foszfatz funkcija foszftcsoport eltvoltsa klnbz makromolekulkrl (nukleinsavak,
fehrjk, alkaloidok). Az alkalikus foszfatz ltal katalizlt folyamatot defoszforillsnak nevezik (ld. 3.8.
bra).
A molekulris biolgiai gyakorlatban leggyakrabban borjblbl izollt alkalikus foszfatzt hasznlnak
(CIAP: Calf Intestinal Alcaline Phosphatase) a DNS 5-vgn lev foszft-csoport eltvoltsra. A plazmid
vektorba val klnozs sorn az egyik lehetsges hibaforrs, hogy a felnyitott plazmid resen ligldik
ssze (nzrds). A foszftcsoport eltvoltsa ezt akadlyozza meg, nvelve ezzel az inszertet
tartalmaz konstrukcik szmt s cskkentve az gynevezett res vektor htteret.
3.8. bra: Az alkalikus foszfatz ltal katalizlt reakci. Klnozskor az res plazmid nzrdsnak kivdsre
alkalmazhat az alkalikus foszfatzzal val kezels, amely monofoszft szterek (mint pl. az 5-foszforillt DNS)
defoszforillst katalizlja.
38
3.4.3. T4 polinukleotid-kinz
A T4 polinukleotid-kinz (PNK) az ATP -foszft csoportjnak a DNS szabad 5-hidroxil vgre trtn
tvitelt katalizlja. (A DNS-rl hinyozhat az 5 foszft-csoport elzetes defoszforilci miatt, vagy ha
pldul az oligonukleotid primereket kmiai szintzissel lltottk el.) A PNK ezen kvl ADP jelenltben
kpes a foszft csoport cserjre is (ld. 3.9. bra). A reakci felhasznlhat oligonukleotidok, DNS vagy
RNS 5-vgnek jellsre (-
32
P) ATP hasznlatval.
3.9. bra: A T4 polinukleotid-kinz enzim mkdse. A) A T4 polinukleotid kinz (PNK) az n. forward reakci
sorn a polinukleotid szl 5-vgre viszi t az ATP -foszft csoportjt. Radioaktv ATP-t alkalmazva a reakcival
foszft-jellt (P*) nukleotidot lehet ellltani. B) A kicserldsi reakci akkor megy vgbe, ha feleslegben ADP-t
adunk a reakcihoz. Ekkor az enzim els lpsben a nukleinsav 5-foszftjt viszi t az ADP-re, majd a jellt ATP -
foszftjt a nukleinsavra.
3.5. Tovbbi olvasnival a fejezethez
Tindall KR, Kunkel TA (1988) Fidelity of DNA synthesis by the Thermus aquaticus DNA polymerase.
Biochemistry 27, 6008-6013.
Pingoud A, Fuxreiter M, Pingoud V and Wende W (2005) Type II restriction endonucleases: structure and
mechanism. Cell. Mol. Life Sci. 62, 685-707.
Martin IV, MacNeil SA (2002) ATP dependent DNA ligases. Genome biology 3, reviews 3005-
reviews3005.7
Oakeley EJ (1999) DNA methlyation analysis: a review of current methodologies. 1999. Pharm. Ther. 84,
389-400.
39
4. Alapmdszerek s rekombinns DNS konstrukcik
tervezse
A gntechnolgiai mdszerek fejldse lehetv tette, hogy brmilyen organizmusbl izollhassunk
brmilyen tetszleges gnt, az izollt gnt klnozssal felszaportsuk, s szekvenlssal kiolvassuk a
genetikai informcit. Ebben a fejezetben a gntechnolgia alapmdszereit ismertetjk, kezdve a DNS
tiszttstl s a szeparcis technikktl (glelektroforzis, ld. 4.1.2.), a hibridizcis technikkon (ld.
4.1.3.) t a DNS konstrukcik tervezsig (ld. 4.2.) s a DNS gazdasejtbe juttatsnak mdszereiig
(gnbeviteli eljrsok, ld. 4.3.).
4.1. Alapmdszerek
4.1.1. A DNS tiszttsa s analzise
A rekombinns DNS-ek ellltsa a vektor s a majdani inszert DNS tiszttsval kezddik. Ezt kveten
meg kell gyzdnnk a DNS pontos mretrl, mennyisgrl s tisztasgrl. A DNS izollsa az RNS-hez
kpest egyszerbb, mert az RNS esetben nehz megszabadulni a szinte mindenhol jelen lv RN-z
enzimektl. Ez az alfejezet a DNS ellltshoz s izollshoz szksges oldatokat, reagenseket, a
tiszttshoz hasznlt mdszereket (pl. miniprep) s a DNS koncentrcimrs lehetsgeit mutatja be.
4.1.1.1. Oldatok, reagensek
A vektor DNS-t baktrium tenyszetekben lltjuk el, s ugyanezeket a tenysztsi krlmnyeket
hasznljuk a rekombinns DNS felszaportshoz is a molekulris klnozs sorn. A baktriumok
tenysztshez, nvekedshez tptalajra van szksgnk. Leggyakrabban steril LB (Luria-Bertrani;
sszettele: tripton, leszt kivonat, NaCl) vagy 2YT (tbb leszt kivonatot s triptont tartalmaz)
mdiummal dolgozunk. A mikrobiolgiban hasznlatos tptalajok lehetnek folykonyak s szilrdak.
Szilrd tptalajt gy kaphatunk, ha a sterilezst megelzen valamilyen szilrdt anyagot kevernk a
tpleveshez, leggyakrabban agart. Magas hmrskleten az agar felolddik, majd a kihls eltt Petri-
csszkbe ntjk, s hagyjuk megdermedni (agar lemez). A 4.1. bran folyadk s szilrd halmazllapot
tptalajokat mutatunk be. Nagy mennyisg baktriumsejt felnvesztshez folykony tptalajra van
szksg, de abbl az egyedi klnokat nem tudjuk sztvlasztani. Azrt kell a szilrd tptalaj, hogy a
sejtszuszpenzit hgan eloszlatva, az egyedi klnok egymstl sztvlaszthat egyedi telepeket kpezzenek.
4.1. bra: Folyadk s szilrd halmazllapot tptalajok. Az agar lemezen az egyedi baktriumtelepek ltszanak.
40
Nagy mennyisg plazmid DNS ellltshoz elszr a felszaportani kvnt plazmidot (ld. 7.2. fejezet)
kompetens E.coli baktriumokba kell transzformlni (ld. 4.3.1.). Ahhoz, hogy kizrlag a plazmidot felvett
baktriumsejtek nvekedjenek, a tptalajhoz valamilyen antibiotikumot is kell adni, hiszen a plazmidot
felvett sejtek rendelkeznek legalbb egy antibiotikum rezisztencit kdol gnnel (ld. 7.1.2. fejezet), s gy
tovbb tudnak osztdni, mg az resen maradt sejtek elpusztulnak (szelekci).
4.1.1.2. Plazmid DNS preparls
A felszaportand plazmidot tartalmaz baktriumsejtekkel folykony tptalajt inokullunk, s egy jszakn
t, 37C-on nvesztjk, majd a sejteket centrifuglssal sszegyjtjk. A baktriumsejtekbl trtn DNS
izolls klasszikus mdszere az n. alkalikus lzis, amely sorn SDS-t tartalmaz NaOH oldattal tesszk
tnkre a sejtmembrnt s denaturljuk a makromolekulkat. (Birnboim and Doly dolgoztk ki ezt a mdszert
1979-ban). A sejtek feltrst elrhetjk enzimekkel (lizozim, proteinz K) vagy mechanikai hatssal is (pl.
szonikls ultrahanggal, nagy nyoms az n. French-press mdszernl, tbbszrs fagyaszts-felolvaszts).
Az oldatba kerlt DNS molekulkat el kell vlasztani a tbbi sejttrmelktl s fehrjktl. Az risi mret
kromoszomlis DNS-t (3,6 Mbp) knnyen ki lehet csapni (neutrlis pH-n), az RNS-eket s a klnbz
fehrjket enzimekkel lehet degradlni. A fenol-kloroform-izoamilalkoholos extrakci esetn a fenol s a
kloroform, mint szerves oldszerek denaturljk a fehrjket, a plazmid mret (2-10 kbp) nukleinsavak
viszont a vizes fzisba kerlnek. Az izoamilalkohol cskkenti a bifzisos oldat habosodst. Vgl a DNS-
tl etanollal vagy izopropanollal vonjuk el a vizet s ezzel csapjuk ki, majd centrifuglssal kileptjk az
extrakromoszomlis plazmid DNS-t egy manyag Eppendorf-cs falra. Az alkohol eltvoltsa utn vzben
vagy Tris-EDTA (TE) pufferben visszaoldjuk a tiszta DNS-t.
A nyers liztum tiszttsnak egy msik hagyomnyos mdja a CsCl-os srsggradiens centrifugls,
amit manapsg mr ritkbban hasznlnak, mivel fl napos nagy fordulatszm (350.000 g) lepts
szksges hozz. Viszont nagy tisztsg DNS-t lehet vele kinyerni, s psgben maradnak a nagyobb
mret (>10 kbp) DNS molekulk is, amelyek mechanikailag rzkenyek a pipettzsnl is fellp
nyrerkre. A 4.2. bra a CsCl srsggradiens centrifugls smjt mutatja be.
4.2. bra: A srsggradiens centrifugls smja. Ers centrifuglis er hatsra a nehz Cs
+
ionok
srsggradienst kpeznek. Centrifugls hatsra a CsCl oldatban lv makromolekulk klnbz helyzet svokat
alkotnak a gradiensben (pl. a DNS molekulk izopiknikus pontja 1,6-1,8 mg/ml CsCl koncentrcinl van). A DNS
svok elhelyezkedst UV fnyben lehet detektlni a fluoreszcens festknek ksznheten. Az izollt DNS-rl vgl
n-butanollal az etdium-bromid, dializlssal a CsCl vlaszthat el.
41
Az eddig ismertetett mdszerek htrnya, hogy nagy elvigyzatossgot ignyel a mrgez reagensek (pl.
fenol, etdium-bromid) s a veszlyes hulladk miatt, drga eszkzk (pl. ultracentrifuga) szksgesek hozz
s rendkvl idignyesek. A kis mennyisg bakterilis DNS (miniprep) alkalikus lzisen alapul
kivonsra manapsg szmos, kereskedelemi forgalomban kaphat kit ll rendelkezsre, melyekkel nagy
tisztasgban s mennyisgben lehet kinyerni a plazmid DNS-t. Ezek a kitek alapveten a rszletesen
ismertetett alkalikus lzis mdszern alapulnak, de a fenolos extrakcis lps helyett egy szilikt tartalm
oszlopon (vagy membrnon) trtn tiszttst tartalmaznak. A minipreppel ltalban 10-100 g DNS-t
lehet kinyerni. Vannak olyan kitek is, amelyekkel jval nagyobb mennyisg DNS-t is lehet tiszttani. A
midiprep mdszernl kb. 25-50 ml sejtkultrbl indulunk ki, s 100-350 g DNS-t kaphatunk. Ennl
tbb DNS maxi- mega- s gigaprep-pel (100 ml-5l sejtkultra, 500 g-10 mg DNS) llthat el.
Miniprep protokoll-lersokat tbbek kztt itt tallnak az interneten.
4.1.1.3. A DNS koncentrci meghatrozsa
A plazmid DNS koncentrcijt leggyakrabban fotometrival mrjk. A nukleinsavak elnyelsi maximuma
260 nm-nl van az aroms gyrk miatt. Az elnyels alapjn megadhat a DNS koncentrcija. Ha az
abszorbancia A
260
= 1, ez az rtk megfelel 50 g/ml duplaszl DNS-nek (37 g/ml egyszl DNS-nek
vagy 40 g/ml RNS-nek). A fehrjk elnyelsi maximuma 280 nm-nl van, teht klnbzik a DNS-tl,
ezrt knnyedn megllapthat a minta fehrje szennyezettsge is, melyet az A
260
/ A
280
hnyados hatroz
meg pontosan. Ha ez az rtk kevesebb, mint 1,8, akkor a minta fehrjvel szennyezett. Ha viszont 2 felett
van, akkor RNS-t is tartalmazhat. A mrst elvgezhetjk hagyomnyos UV fotomterben, de ehhez sok
anyagra van szksgnk. Ma mr legtbbszr n. nanodrop technikt alkalmazunk (ld. 4.3. bra), melynl
egy csepp (~2 l) DNS koncentrcijt mrjk egy specilis spektrofotomterben.
4.3. bra: DNS koncentrci mrse nanodrop technikval
4.1.2. Glelektroforzis
Mindenfajta glelektroforzis azon az elven alapul, hogy a tltssel rendelkez molekulk az elektromos
trben az ellenttes tlts elektrda fel vndorolnak. A vndorls sebessgt a tltsen kvl a molekula
alakja s mrete hatrozza meg. Ez a hrom tulajdonsg teszi lehetv, hogy klnbz minsg s
prusmret glekben az eltr tulajdonsg biomolekulkat elvlasszuk egymstl.
4.1.2.1. Agarz glelektroforzis
Az agarz a vrsmoszatok agar-agarjnak egyik poliszacharid sszetevje, mely a D-galaktz s 3,6-
anhidro-L-galaktopiranz lineris polimere. Rendkvl jl alkalmazhat nukleinsavak szeparlsra. A
biokmiban az agarz glelektroforzis DNS molekulk, elssorban mret s alak szerinti elvlasztsra
szolgl. Agarz glben nhny 10 bp-tl tbb 10 kbp-ig terjed mret (hosszsg) DNS molekulkat
42
lehet sztvlasztani. A DNS molekula negatv tltse cukorfoszft gerince miatt egyenesen arnyos a
hosszsgval. Ezrt egy vzszintesen elhelyezett agarz glben (horizontlis glelektroforzis) a pozitv
plus fel vndorl DNS molekulk mobilitsa arnyos lesz a hosszukkal. Az agarz 0,5-2%-os oldata
forralssal kszl. Dermedskor az agarz trhls szerkezet lesz. A forralst kveten a glhez
interkall fluoreszcens festket is adunk, amely a DNS-t UV fnyben lthatv teszi. Rgebben a mr
korbban is emltett etdium-bromidot (ld. 4.4. bra) alkalmaztk erre a clra, azonban ez ersen mutagn
hats, ezrt manapsg ms, biztonsgosabb festkeket hasznlunk helyette (pl. SYBR Safe, Gel Green).
4.4. bra: Az etdium-bromid fluoreszcens DNS-festk szerkezeti kplete
A gl ntsekor, az nt formra merlegesen, fellrl egy n. "fst" is elhelyeznk, ami a mintafelvitelhez
szksges zsebeket fogja kialaktani. A fs mrett a minta mennyisgtl fggen vlasztjuk ki. A
dermedt glbl vatosan kivesszk a fst, s a zsebekbe pipettzzuk a mintnkat, majd egy elektrdkkal
elltott kdba helyezzk a glt. Az elektroforzishez szksges egyenramot a tpegysg biztostja. Minden
egyes minthoz "DNS-kezel" oldatot is kevernk, mely glicerint s ltalban ktfle festket is tartalmaz.
A glicerin arra szolgl, hogy nagyobb srsge rvn a mintkat a zseb aljn tartsa, ne diffundljanak ki a
pufferbe. A festkek segtsgvel pedig megllapthat, hogy hol tart az elektroforzis. A brmfenolkk
lthatv teszi felvitelkor a mintt, s kivl mobilitsi kpessgei kvetkeztben (1%-os glben egy 300
bp-os DNS fragmentummal fut egytt) sttkk szne a futsi frontot jelzi. A xiln-cianol nagyon lassan
halad a glben (kb. 4 kbp DNS-sel fut egytt).
Az elektroforzishez hasznlt puffer (TBE: Trisz-bort-EDTA vagy TAE: Trisz-acett-EDTA) ionerssge
fontos tnyez a DNS elektroforetikus mobilitsa szempontjbl. Tl alacsony ionern a DNS csak lassan
kpes haladni, mg ha tl magas az ioner, akkor a vezetkpessg is nvekszik, tl sok h kpzdik, amitl
a gl meg is olvad. Alacsony feszltsgen a lineris DNS vndorlsi sebessge arnyos a feszltsggel. A
megfuttatott glt vgl UV fnnyel vilgtjuk meg, s a glhez adott fluoreszcens festknek ksznheten
vilgtani fognak a DNS-ek svjai a glben. A lthatv vlt DNS svokat ki is vghatjuk a glbl tovbbi
tiszttsra, felhasznlsra.
Az agarz glelektroforzis kivitelezst a 4.5. bra szemllteti.
4.5. bra: agarz glelektroforzis
43
4.1.2.2. Poliakrilamid glelektroforzis (PAGE)
A nukleinsavakat nemcsak agarz, hanem poliakrilamid glelektroforzissel (PAGE) is el tudjuk vlasztani
egymstl. A PAGE-t a horizontlis agarz elektorforzistl eltren vertiklis (fggleges) elrendezs
kszlkben vgezzk (ld. 4.6. bra). A poliakrilamid gl egyik legjelentsebb eltrse az agarz gltl,
hogy sokkal kisebb a prusmrete. Felbontsa 5-2000 nukleotidig terjed, s kpes elvlasztani az akr 1
nukleotid hosszban klnbz oligo- vagy polinukleotid szlakat is egymstl. A Sanger-fle klasszikus
DNS szekvenls sorn PAGE-vel vlasztjk el a klnbz hosszsg lineris, jonnan szintetizlt
egyszl DNS-eket egymstl. Megjegyzend, hogy az automata DNS szekventorokban kapillris
elektroforzist hasznlnak (ld. 5.2.2. fejezet), amihez ms szintetikus polimereket alkalmaznak. Az
akrilamid vizes kzegben, megfelel inicitorok (pl. peroxidiszulft) s kataliztorok (tetrametil-etiln-
diamin, TEMED) jelenltben gyks polimerizcira kpes, s nagy mlsly lineris polimer,
poliakrilamid keletkezik. A trhls szerkezet a keresztkt gens (N,N-metiln-bisz-akrilamid) jelenltben
alakul ki, aminek segtsgvel a hossz poliakrilamid lncok kztt hidak kpzdnek. Megjegyzend, hogy
a fehrjk elvlasztsra is PAGE-t hasznlunk, mivel mg a nagyobb mret fehrjk (>100 kDa) is jval
kisebbek, mint egy kismret plazmid (1 kbp ~ 600 kDa).
4.6. bra: Poliakrilamid glelektroforzis kszlk kamrinak felltse mintkkal.
Mivel a klnbz hosszsg DNS molekulk relatv tltse azonos (a foszft-csoportok negatv tltse
miatt), ezrt a lineris molekulk mindig mret szerint vlnak szt. Ha valamilyen denaturl genst is
kevernk a glhez, pldul uret, akkor a lineris DNS szlak alakja is egyforma lesz, gy tnylegesen csak a
mret alapjn szeparldnak. Fehrjk esetben is hasonl az elvlaszts elve, de fehrjk szeparlsra a
PAGE szmos ms vltozatt is hasznljuk (2D PAGE, SDS-PAGE, izoelektromos fkuszls).
4.1.2.3. A DNS-ek mretnek meghatrozsa
A DNS mrett ismernnk kell, ha azt analizlni vagy preparlni szeretnnk. A lineris DNS molekula
mretnek logaritmusa s az elektroforetikus mobilitsa kztt fordtott arnyossg van (a mobilits s a
mret logaritmusa kztt lineris az sszefggs). gy egy ismeretlen molekula mrete meghatrozhat a
futsi tvolsg ismeretben, ha mell olyan DNS molekulkat is felvisznk a glre, amelyeknek a mrete
pontosan ismert. Ez a DNS ltra vagy molekulasly marker, ami klnbz mret lineris DNS
molekulk keverke. Az agarz glt alapveten nagyobb mret nukleinsavak elvlasztsra hasznljk,
mivel prusmrete jval nagyobb a poliakrilamid glhez kpest. A gl agarz vagy akrilamid
koncentrcijtl fggen, klnbz mret polinukleotidokat lehet elvlasztani. Minl hgabb, annl
nagyobb, minl tmnyebb, annl kisebb DNS szlakat lehet szeparlni. Minden vizsgland minthoz
44
tartozik egy optimlis prusmret, amelyben a molekulk bizonyos ellenllssal vndorolnak, de nem
akadnak fel, hanem kpesek haladni benne.
A hosszabb molekulk a glben nehezebben haladnak, gy ezek lemaradnak a rvidebb, kisebb
molekulkhoz kpest. A polinukleotidok glben val mobilitst nagyban befolysolja az alakjuk is. A
cirkulris/relaxlt plazmid formk szttekeredettsgk miatt lassabban haladnak, mint az ersen kondenzlt,
szuperheliklis DNS-ek. A linearizlt plazmidok pedig az elbb emltett kt forma kztt mozognak (a
molekulk alak-szerinti mobilitst a glben alapveten a hidrodinamikai trfogatuk dnti el. DNS mintk
agarz glelektroforetikus kpt a 4.7. bra mutatjuk be.
4.7. bra: Agarz gl DNS ltrval s klnbz DNS mintkkal. A mintkat valamilyen restrikcis
endonuklezzal (1- vagy 2-fle) kezeltk. A 3. minta kivtelvel a DNS mintk kettvgdtak, ezrt kt klnbz
mret svban futnak. A 3-as plazmid DNS minta cirkulris maradt. A kondenzltabb szuperheliklis formk
gyorsabban, mg a relaxlt, kitekeredett molekulk lassabban vndorolnak a glben. A DNS ltrval a molekula
mreten kvl a DNS mennyisgt is meg lehet becslni.
4.1.2.4. DNS-ek izollsa agarz glbl
A megfelel DNS-t (pl. vektor vagy inszert DNS), melyet pl. restrikcis emszts vagy PCR reakci
eredmnyeknt kaptunk, az agarz glbl izollnunk kell ahhoz, hogy megfelelen elvlasszuk a DNS
mellett maradt enzimektl (endonuklezok, DNS-polimerz) vagy a hastatlan vektortl.
Az agarz glelektroforzist kveten a glt ebben az esetben UV fny helyett kk fnyben vilgtjuk meg,
mert az UV roncsoln az izollni kvnt DNS-t. A glhez adott DNS festk (etdium-bromid helyett pl.
SYBR Safe) ugyanis kk fnyben is fluoreszkl, ami lehetv teszi a megbzhat, krosodsmentes DNS
izollst. A glbl a megfelel cskot egy szikvel vgjuk ki (ld. 4.8. bra), amibl a DNS-t tbbfle mdon
is kinyerhetjk.
Az izolls trtnhet elektroelcival, amikor a kivgott gldarabot egy olyan dializl membrnba
helyezzk, ami impermebilis egy bizonyos DNS molekula mretre, s permebilis a folyadkokra. TE
pufferbe ztatjuk a gldarabot tartalmaz dialzis zacskt, s elektromos teret hozunk ltre a dialzis cs
krl. Ugyangy, ahogy a glelektroforzisnl is, a DNS elkezd vndorolni a pozitv elektrda fel. Ebben
az esetben kivndorol a glbl, de nem juthat t a membrnon. A dialzis zacskbl ezutn csak ki kell
pipettzni a mr tiszta DNS-t tartalmaz folyadkot.
45
4.8. bra: DNS agarz glbl izollsa steril szikvel
A DNS-t tovbb lehet mg tiszttani fenolos extrakcival s etanolos kicsapssal. Egy msik hagyomnyos
mdszer a gldarab 80C-on trtn fagyasztsa. Ezen a hmrskleten az agarz szerkezete mr
roncsoldik, gy egy szrn keresztl, centrifuglssal kinyerhet a DNS. Egy tovbbi kivonsi eljrs az
alacsony hmrskleten megolvad (low melting) agarz hasznlata, mivel az oldatfzisba kerlt DNS-t a
miniprep mdszernl ismertetett szilika membrnhoz trtn adszorbcival knnyen tisztthatjuk. A DNS
(s RNS) glbl trtn extrakcijra sokfle kit kaphat a kereskedelemben.
4.1.2.5. Restrikcis trkpezs
A klnbz restrikcis endonuklezok eltr felismer szekvencikkal rendelkeznek, gy ugyanazon DNS
molekult klnbz enzimekkel emsztve klnbz restrikcis fragmentumok keletkeznek. A restrikcis
enzimeket nmagukban vagy kombinlva alkalmazzuk, s a kapott DNS fragmentumokat
glelektroforzissel vlasztjuk el. A fragmentumok mrete alapjn ssze tudjuk lltani az eredeti DNS
molekula n. restrikcis trkpt (ld. 4.9. bra).
4.9. bra: Rekombinns DNS konstrukci trkpezse restrikcis endonuklezokkal
46
Ez egy kiraks jtk, ami azon alapszik, hogy a hasthelyek egymshoz viszonytott helyzete dnti el,
hogy melyik emsztsnl milyen mret fragmentumok keletkeznek. Akr egy teljes genomot is fel lehet gy
trkpezni (ld. 9.1.1. fejezet). Az ilyen mintzat minden embernl ms s ms ezt DNS ujjlenyomatnak
nevezik s tbb clra is fel tudjk hasznlni (ld. 4.1.3.2. fejezet).
4.1.3. Hibridizcis technikk s nukleinsav prbk
A molekulris biolgiban a hibridizcis technikkkal valamilyen ismeretlen biolgiai mintbl akarunk
kimutatni egy adott DNS, RNS vagy fehrje szakaszt. Meg akarunk bizonyosodni annak jelenltrl,
mennyisgrl, minsgrl. A hibridizcis technikknak ksznheten nincs szksg felttlenl
szekvenlsra, ha a genomban egy mutcit vagy strukturlis vltozst akarunk azonostani. A hibridizcis
technikk molekulris httert az a tny adja, hogy a DNS kt komplementer szla reverzibilis mdon
denaturlhat, s a renaturci nem csak a kt eredeti szl kztt megy vgbe, hanem egy oligonukleotid
prba jelenltben az is anelll (hozztapad) a vele komplementer szlhoz.
Ezekhez az eljrsokhoz teht mindig szksges valamilyen ismert szekvencij DNS vagy RNS prbra.
Prbnak nevezzk a radioaktvan vagy ms mdon (leginkbb fluoreszcencival) jellt (az esetek
tbbsgben oligonukleotid mret) oligo- vagy polinukleotidot, ami komplementer a vizsglni kvnt
nukleinsav egyik lncnak szekvencijval. Az egyszl prba csak egyszl cl nukleinsav lnchoz
kpes kapcsoldni. A hibridizci szigorsga (stringency) attl fgg, hogy milyen s koncentrcit s
hmrskletet alkalmazunk. Magas anellcis hmrskleten s alacsony ioner n. szigor (stringent)
krlmnyeket jelent, ilyen esetben csak a prbval tkletesen egyez nukleotid szlak fognak hibridizlni.
Azonban magas ionern s alacsonyabb hmrskleten a csak rszben hasonl szekvencikhoz is
hozztapadhat a prba.
A fejezet els rszben a prbakszts s jells lehetsgeit vzoljuk fel, a tovbbi alfejezetekben a
Southern- s Northern-lenyomat (blot) mdszerrl, az in situ hibridizcirl s a DNS chipekrl lesz
sz. Nhny tovbbi hibridizcis mdszert (pl. kolnia- vagy plakk-hibridizci) az azt alkalmaz
mdszert ler fejezetben trgyalunk (ld. 8. fejezet). (A hibridizcirl mg ld. 18.1. animci: Hibridizci
4.1.3.1. Nukleinsav prbk ellltsa s jellse
Korbban szinte kizrlag izotpjellst hasznltak. A jellt molekula a prbakszts mdszertl fggen
(ld. albb) lehet -ATP, o-ATP, o-CTP. Az izotpot tekintve hasznlhatunk
32
P-t (felezsi id =14 nap),
33
P-t (t
=25 nap),
35
S-t (t
=87 nap). A hibridizls eredmnyt radioaktv prba esetn autoradiogrfival
tesszk lthatv. Ksbb megjelentek egyb jellsi mdok is, amelyek kztt a radioaktivitssal azonos
rzkenysg fluoreszcens prbk terjedtek el leginkbb. A fluoreszcens prbkrl rszletesebben a
szekvenls (ld. 5. fejezet) s a PCR fejezetben (ld. 6.3.2. fejezet) lesz sz. A nem-radiokatv s nem-
fluoreszcens prbk kztt megemltjk a digoxigenint, egy ersen immunogn (ami azt jelenti, hogy igen
nagy affinitssal hozzktd antitestek llnak rendelkezsnkre), nvnyi eredet szteroid, ami
nukleotidokra konjuglhat, s bepthet nukleinsav prbkba (az elhvs az antitest jellsvel vagy a
hozz konjuglt enzim ltal termkknt ellltott festkkel vagy kemiluminszcencival trtnhet).
Az oligonukleotid prbkat szilrdfzis szintzissel (szintetiztorokban), mg a hosszabb DNS vagy
RNS prbkat enzimatikus ton lltunk el. Az egyik lehetsg a DNS molekula vgjellse. Az 5-
vgjellshez kt enzimre van szksg. Alkalikus foszfatzzal eltvoltjuk a foszft-csoportot, majd
polinukleotid-kinz segtsgvel ATP-bl izotp jellt foszft-csoport (-foszft jellt!) pthet be a DNS
5-vgre. A 3 vgjellshez a DNS-polimerzok 35 exonuklez aktivitst hasznljuk ki. A
visszargott szlhoz a polimerz aktivits rvn dNTP-bl izotp vagy fluoreszcens jel pl be a 3-vg
kzelbe. Ebben az esetben ltalban jellt dCTP-t hasznlnak (ennl a mdszernl az -foszftot kell
jellni!). Kszthetnnk enzimatikusan random DNS prbkat gy is, hogy DNS-polimerz segtsgvel
47
dCTP-bl pl be a jel az jonnan szintetizlt lncba. Ugyanezen az elven RNS-polimerzzal DNS-
templtrl jellt RNS-prbk is elllthatk in vitro transzkripcival.
Megjegyzend, hogy lteznek szintetikus n. peptid-nukleinsav (PNA) prbk is, amelyekben a
cukorfoszft gerinc s a foszfodiszter ktsek helyett poli N-(2-aminoetil)-glicin vz tallhat s a bzisok
ehhez metiln-karbonil csoporton keresztl kapcsoldnak (a bzisok tvolsga megegyezik a
foszftgerinchez kapcsold bzisok tvolsgval, teht a PNA is tud bzisprosodni egy komplementer
lnccal). Egy PNA rszlett a 4.10. bran mutatjuk be
4.10. bra: Egy peptid-nukleinsav rszlete
4.1.3.2. Southern-blot (lenyomat) technika s az RFLP mdszer
A Southern-blot (magyarul lenyomat) technika specilis DNS szakaszok kimutatsra szolgl egy
komplex DNS mintban. Pldul egy adott gn jelenltt tudjuk vizsglni klnbz fajok teljes
genomjban. Ezzel a technikval a gn mret vagy szerkezetbeli megvltozsa is kimutathat. A
lenyomatra azrt van szksgnk, mivel a glbl a DNS diffzival az oldatba kerlne a hibridizls
sorn, msrszt a gl trkeny s nehezen kezelhet.
A Southern-blot kivitelezsekor elszr a nagyobb mret DNS molekult, akr egy teljes genomot,
restrikcis endonuklezokkal kisebb darabokra hastunk, majd agarz glben futtatjuk a mintt. A
hibridizci miatt egyszl DNS molekulkra van szksgnk, ezrt NaOH segtsgvel denaturljuk a
ketts szlat, majd K-acetttal semlegestjk. A glt elektrolit oldatba helyezzk (ami lehet egy szivacs,
vagy a blottol folyadkkal titatott szrpapr), s a tetejre simtjuk a nitrocellulz- vagy
nylonmembrnt. A membrn fl tovbbi nedvszv anyagot (pl. szrpapr) rtegeznk. A kapillrishats
miatt a DNS-molekulk a glbl a membrnba vndorolnak. A membrn csak az egyszl DNS-eket kti
meg ugyanabban a pozciban, ahogyan azok eredetileg a glben elhelyezkedtek (ld. 4.11. bra). A
nitrocellulz membrn esetben szraz hkezelssel (60-100C-os vkuumban), a nylonmembrn esetben
pedig UV-kezelssel kovalensen hozzktjk a DNS-t a membrnhoz. Ezt kveti a hibridizcis prbval
trtn inkubls. Majd a membrnrl lemossuk a nem ktdtt nukleinsav prbkat s rntgenfilmen
autoradiogrfival, fluoromterrel vagy fotomterrel detektljuk a jelet (a prba jellstl fggen).
Radioaktv prba esetn elhvskor a membrnra egyszeren egy rntgenfilmet helyeznk, s ahol a prba
hozzktdtt a minthoz, elfeketedik a film. Ezek a stt svok tkletesen egybeesnek a hibridizlt, azaz
azonostani kvnt DNS svjval. Ma mr elterjedtek az olyan eljrsok is (az n. foszfo-image screen), ahol
a radioaktv jelet kzvetlenl digitlis jell lehet alaktani. A radioaktivits hasznlata a sugrzs
veszlyessge miatt ma mr kevsb hasznlatos. A detektls trtnhet mg kolorimetrival, amikor a
48
prbn valamilyen festkanyag tallhat, amely enzim (pl. alkalikus foszfatz, peroxidz) jelenltben
oldhatatlan sznes csapadkk alakul, s megfesti a membrnt. Ez szabad szemmel is jl lthat. Egy msik
nem izotpos detektlsi md a fluoreszcens kimutats, amikor biotinlt prbt alkalmazunk, s a
membrnt fluoreszcens reagenssel jellt avidinnel vagy sztreptavidinnel kezeljk, majd fluorimetrival
detektljuk. Manapsg jval elterjedtebb s kzkedveltebb a kemilumineszcencin alapul elhvs (ECL:
Enhanced Chemiluminescence: megnvelt kemilumineszcencia). Ennl a mdszernl a prbra kovalensen
valamilyen enzimet, ltalban torma-peroxidzt konjuglnak. Ezutn a membrnt olyan anyaggal kezeljk,
ami a torma-peroxidz szubsztrtjt, leggyakrabban luminolt tartalmaz. Az oxidci sorn, hidrogn-peroxid
jelenltben, a luminol gerjesztett llapotba kerl, s egy fotont bocst ki, amit megfelel detektorral vagy
rntgenfilmen azonosthatunk. Fenol vzzal rendelkez molekulk jelenltben a fnykibocsts akr 1000-
szeresre is nvelhet. Ettl lesz megnvelt kemilumineszcencia az eljrs.
4.11. bra: Southern-blot (lenyomat) technika. A glben lv DNS-t nitrocellulz vagy nylon membrnra
transzferljuk, gy az elvlasztott DNS mintzatnak replikjt kapjuk. A transzfer ltalban egy szivacson keresztl
trtnik, amit egy puffer tartlyba helyeznk. A glt s a membrnt a szivacsra tesszk, fl pedig vastag rtegben
szrpaprt helyeznk, hogy felszvja a puffert a szivacson, glen s membrnon keresztl. Ezltal a DNS a glbl a
membrnba vndorol, s ersen immobilizldik.
Southern-blot technika segtsgvel analizljuk az RFLP (Restriction Fragment Length Polymorphism:
restrikcis fragmentum hossz polimorfizmus) mdszer alkalmazsa sorn kapott DNS fragmentumokat
is. Az RFLP mdszer lnyege, hogy homolg DNS molekulk variciira (SNP: single nucleotide
polymorphism, kiejtve sznip) vilgthat r. Az eljrs sorn teljes genombl indulunk ki, melyet restrikcis
endonuklezokkal kezelnk. Az klnbz endonuklezok (ld. 3.2.1.2. fejezet) eltr DNS szakaszokat
ismernek fel. Az endonuklezos kezels utn kapott DNS fragmentumok szma az enzim ltal felismert
szekvencik szmtl, mrete pedig ezek tvolsgtl fgg. A restrikcis fragmentumokat ezt kveten
glelektroforzissel szeparljuk, s Southern-blot hibridizcival detektljuk. RFLP abban az esetben
jelenik meg, ha a vizsglt DNS szlon tallhat inszerci, delci vagy SNP egy meglv restrikcis helyet
tnkretesz vagy egy jat hoz ltre. Ilyenkor glelektroforzissel eltr hosszsg DNS fragmentumokat
kapunk. Az RFLP analzis volt az els DNS ujjlenyomatot feltrkpez, szles kren elterjedt technika
(DNA profiling, DNS tipizls), amelyet bevezettek az igazsggyi orvostani s a brsgi gyakorlatba is.
Az RFLP technika nagyon fontos eszkz volt a genomok fizikai feltrkpezsben, klnbz mutcik
kimutatsban. Ezzel a mdszerrel klnbz betegsgek, vagy az azokra val hajlam is kimutathat.
A 4.12. bran egy bntny elkvetjnek Southern-blot mdszerrel ellltott RFLP mintzat alapjn
trtn azonostst mutatjuk be. Ezt az alkalmazst Alec Jeffrey vezette be a gyakorlatba az 1980-as vek
kzepn (a szexulis-indttats gyilkossg elkvetjt a brsg a DNS ujjlenyomat alapjn 1992-ben
letfogytiglani brtnbntetsre tlte ez volt a brsgi gyakorlatban az els eset, ahol gntechnolgiai
bizonytk alapjn szletett meg az tlet).
49
4.12. bra: RFLP, mint DNS ujjlenyomat ellltsa. Az eljrs sorn az egynekbl vett DNS mintt restrikcis
endonuklezokkal emsztik, glelektroforzissel elvlasztjk, majd Southern-blot hibridizlssal lltjk el a DNS
ujjlenyomatot, amellyel akr egy bntny elkvetjt is azonostani lehet (ld. a bemutatott brt).
4.1.3.3. Northern-blot
A Southern-blottal rokon technika a Northern-blot, csak ebben az esetben DNS helyett RNS molekulkat
analizlunk. Ez az eljrs jval nagyobb elvigyzatossgot ignyel, mivel az RNS rendkvl bomlkony.
Ezrt minden oldatot s eszkzt RN-z mentesteni kell. Segtsgvel megllapthat egy adott sejt
pillanatnyi gnexpresszis llapota s annak vltozsa pldul differencilds sorn vagy patolgis
esetekben. Az izollt mRNS mintt agarz glen vlasztjuk el, de a gl formaldehidet vagy glioxlt is
tartalmaz, amelyek denaturljk az RNS-t, megszntetik az esetleges msodlagos szerkezeti elemeit. Kisebb
mret RNS molekulk esetn (pl. siRNS, miRNS) uret tartalmaz poliakrilamid glt alkalmaznak a
tkletesebb elvlaszts rdekben. Az gy elvlasztott RNS-t tartalmaz glt nylon membrnra blottoljk a
Southern-blothoz hasonl mdon. A blottols utn az RNS membrnhoz rgztst UV keresztktssel
vgzik. A hibridizci krlmnyeit a kimutatand RNS, a hasznlt prba (vgjellt oligonukleotid, random
jellt DNS vagy RNS prba) s a hasznlt hibridizcis puffer egyttesen hatrozzk meg. A kapott jelet a
Southern blottnl lertakhoz hasonlan hvhatjuk el. A hasznlt radioaktv prba megfelel krlmnyek
kztt (alacsony skoncentrci, magas hmrsklet) a membrnrl lemoshat. Az gy lefztt membrn
RNS-eket detektl j radioaktv prbval jrahibridizlhat.
4.1.3.4. I n situ hibridizci, kariotipizls
Az in situ hibridizcis eljrs sorn, sejten, szveten bell tudunk komplementer nukleotid szakaszokat
hibridizltatni jellt prbkkal. Az in situ DNS hibridizls ltalban a kromoszma struktrk
megfigyelsre hasznlatos mdszer, mg az in situ RNS hibridizlssal az adott szvetben expresszl
mRNS-eket, illetve miRNS-eket tudjuk kimutatni mikroszkopikus metszeteken Az egyik legelterjedtebb
vltozata ennek a techniknak a fluoreszcens in situ hibridizci (FISH), amellyel a genom egy-egy
50
kisebb szakaszt lehet megjelenteni. A FISH technikk fejldsvel, nagy pontossggal s biztonsggal
lehet citogenetikai diagnzisokat fellltani, tumoros sejteket azonostani. A klnbz mret s tpus
DNS szakaszok kimutatshoz tbbfle prba ll rendelkezsre. A prbkat egy haptnnel (pl. biotin,
digoxigenin, sztradiol) jellik, amelyhez klnbz fluorokrmok (pl. FITC, rodamin) kapcsoldnak.
Teljes hosszsg kromoszmk kimutatshoz az n. painting prbk alkalmasak. Ha a prbkat eltr
szn fluorokrmmal jellik, akkor a klnbz kromoszmk ms-ms sznnel fognak vilgtani. Az n.
mulitplex-FISH (M-FISH) technikval egyidejleg jellhet az sszes kromoszma (ld. 4.13. bra), s
ezltal sokfle DNS trendezds kzvetlenl kimutathatv vlik.
4.13. bra: Multiplex-FISH. A humn kromoszmkat klnbz fluoreszcens festkkel jelltk (forrs:
JackeyCheng.com)
A kromoszmk telomer s centromer rgiiban egy adott kromoszmra jellemez ismtld szakaszok
tallhatk, gy ezekre a szekvencikra talltk ki a repetitv prbkat. Ezek a prbk fknt a kromoszmk
szmbeli eltrseinek kimutatsra alkalmasak. A gnspecifikus s trspont-specifikus prbkkal specilis,
rvidebb szakaszok jelenltt, hinyt vagy struktrjt lehet feltrkpezni. A FISH-sel ellltott jel
mikroszkpban is megfigyelhet. Azonban a detektls legrzkenyebb mdja n. CCD kamerkkal
trtnik. Ez a kamera -20C-on olyan fluoreszcens jeleket is rzkel, amelyre az emberi szem mr nem
kpes. A FISH felbontsi kpessge 50 kbp-tl 2 Mbp-ig terjed, a DNS kondenzltsgtl fggen. (A FISH
mdszerrl mg ld. 18.2. animci.)
4.1.3.5. DNS-chip (microarray) technika
A hibridizcis technikk legjabb vltozata a DNS-chip vagy microarray. Egy kis mret (1-2 cm
2
)
szilrd hordoz (pl. szilikon, veg) felletre szablyos elrendezsben tbb 10000, eltr szekvencij
DNS prbt rgztenek kovalensen. Ez trtnhet pl. epoxi- vagy amino szilnnal, de gyakoribb a
fotolitogrfis eljrssal trtn in situ szintzis (oligonukleotid prbk esetn). A chipen 1 pont kb. 1 pml
mennyisg DNS-t tartalmaz. A prbk 20-5000 nukleotid hosszsgak, gnekre vagy cDNS-ekre
specifikus oligonukleotidok vagy in vitro szintetizlt DNS-fragmentumok. Az eljrs lnyege, hogy
mikroszkp segtsgvel detektljuk azokat a prbkat a chipen, amelyekkel komplementer DNS vagy RNS
van jelen a mintban. A klasszikus, az elz alfejezetekben ismertetett hibridizcis mdszerekhez kpest a
chip technolginl megfordult a prba s a minta viszonya: itt a prbt, mg az elz mdszereknl a
mintt immobilizljk (blottolssal).
A chipekhez hasznlatos cDNS mintk ltalban gy kszlnek, hogy a vizsglni kvnt szvetet vagy
sejtkultrt feltrjk, s kivonjk az mRNS-t, amibl reverz transzkriptzzal cDNS-t szintetizlnak. Ez a
mennyisg cDNS azonban nagyon kevs lenne a tovbbi munkkhoz. Ezrt PCR reakcival, fluoreszcens
mdon jellt primerek segtsgvel (pl. Cy5: vrs; Cy3: zld) sokszorostjk a target DNS szlakat, majd
ezt a cDNS-t tartalmaz oldatot inkubljk a chipen. A nem ktdtt DNS darabokat lemossk, s a chipet
ltalban egy specilis fluoreszcens elhv kszlkkel (chip reader) vizsgljk. A chip pontjai ltal
51
kibocstott fny sznt s intenzitst detektljk. A kapott kpet szmtgpes programok segtsgvel
elemezik; sszehasonltjk a klnbz mintk hibridizcis rtkeit, gy egy adott kezelsre trtn
expresszis vltozsokhoz olyan szmok rendelhetek, melyek a relatv expresszit fejezik ki. A kirtkels
rszleteire ebben a jegyzetben nem trnk ki.
A DNS microarray mdszert szleskren alkalmazzk a funkcionlis genomikban; gnexpresszis
vltozsokat, valamint az SNP-ktl kezdve a teljes genomot tfog genetikai klnbsgeket lehet a
mdszerrel analizlni. Tovbbi rdekessgeket a mdszer alkalmazsrl itt olvashatnak. . (A DNS
microarray-rl mg ld. 18.3. animci.)
Egy gn-chipet s egy expresszis sszehasonlt vizsglat smjt a 4.14. bra mutatja be.
4.14. bra: Gn-chip (az Affimetryx biotechnolgiai cg termke). A bemutatott kt chip-en egyidejleg tbb mint
40.000 humn (bal) s egr (jobb) transzkriptumot lehet analizlni. Az mRNS-eket a chip-en in situ fotolitogrfival
szintetizlt specifikus komplementer DNS prbk reprezentljk (bal) (forrs: Wikipedia, GNU Free Documentation
License). sszehasonlt gnexpresszis vizsglat (rkos s egszsges sejt) hibridizcis chipen (jobb)
4.2. Rekombinns konstrukcik tervezse
A rekombinns DNS molekula egy olyan mestersges konstrukci, amely kt (vagy tbb) DNS
molekulbl llthat ssze. Az egyik maga a vizsglni kvnt DNS szekvencia, a msik a hordoz DNS,
amely lehetv teszi a replikcit (s egyes esetekben a gnexpresszit is). Teht ha egy idegen DNS
darabot (inszert) egy replikldni kpes DNS szekvencival (vektor) kapcsolunk ssze kovalensen, s
bejuttatjuk egy, a vektornak megfelel gazdasejtbe, akkor az idegen szekvencia is le fog msoldni. A
52
rekombinns DNS-ek nem csak a vektor replikonjnak megfelel gazdasejtekbe, de akr teljes
organizmusokba is bejuttathatk. Az utbbi esetben genetikailag mdostott llnyt (GMO) hozunk ltre
(ld. 0. fejezet).
Ebben az alfejezetben a molekulris klnozshoz szksges rekombinns DNS elksztsnek f lpseirl,
a konstrukcik tervezsrl lesz sz. Honnan szrmazhat, s hogyan lltjuk el a vizsgland DNS
fragmentumot, az inszertet s a hordoz DNS-t, a vektort. Rszletezzk az inszert s a vektor
endonuklezokkal trtn hastst; az inszert s a vektor liglst, a rekombinns DNS-t tartalmaz
gazdasejtek szelektlsi lehetsgeit s vgl a rekombinns DNS szekvencijnak ellenrzsi mdszereit.
4.2.1. Az inszert ellltsa
A rekombinns DNS tervezsnek els lpse, hogy kivlasztjuk a vizsgland DNS szakaszt. Amennyiben
a vizsgland DNS szekvencija nem ismert, mert pldul egy korbban nem kutatott llny specifikus
funkcijrt felels gnjt keressk, valsznleg genomilis vagy cDNS knyvtrat kell ltrehoznunk (ld.
8. fejezet). Br manapsg technikailag jelentsen kisebb kihvs egy ilyen munka, mint egy vtizeddel
ezeltt, komoly id s pnz rfordtssal kell szmolnunk. Jelentsen egyszerbb a helyzet, ha olyan llny
DNS-rl van sz, amely genomjt mr szekvenltk (ld. 0. fejezet), teht az adott DNS szakaszok
szekvencija ismert. Ekkor a kiindulsi szekvencia informcit DNS adatbzisokban talljuk meg (ld.
10.1.2. fejezet). Hrom lehetsg ll elttnk. Az els, hogy mi elllthatjuk az inszertet, amennyiben
rendelkezsnkre ll genomilis DNS vagy RNS minta a megfelel szervezetbl vagy szvetbl. A msodik
lehetsg, hogy szintetizltatjuk az inszertet, ami mra, br mg mindig elg drga szolgltats, az elnyei
miatt (minimlis munka s idrfordts) egyre elterjedtebb. A harmadik eset a legolcsbb vltozat, amikor
egy kln adatbzisbl szerezzk be a bennnket rdekl inszertet tartalmaz ksz rekombinns DNS-t (ilyen
klnmegoszt szolgltats pldul az Addgene, amelybe brki beteheti az ltala elksztett konstrukcit, s
azt brki megkaphatja, csak a szlltsi kltsget kell kifizetnie). Ebben az esetben a rekombinns DNS-bl
restrikcis enzimekkel kzvetlenl kivghatjuk, vagy PCR segtsgvel (ld. 6.4.1. fejezet)
szubklnozhatjuk az inszertet.
Az inszert ellltsa attl is fgg, hogy egy gnt, gn fragmentumot vagy cDNS-t akarunk klnozni. A
cDNS (complementary, azaz komplementer DNS) az mRNS-rl reverz transzkriptz enzimmel ksztett
msolat. Ez utbbira akkor van szksgnk, ha vagy cDNS knyvtrat akarunk ellltani (ld. 8.3. fejezet)
vagy expresszis konstrukcit akarunk ellltani, azaz a rekombinns fehrje a vizsglatunk trgya (ld. 0.
s 0. fejezet). Fontos emlkeztetnnk r, hogy az eukaritban a gnek ltalban intronokat is tartalmaznak,
azaz a gn ltal kdolt mRNS szekvencia nem egyezik meg a gn DNS szekvencijval, ami tnyt
figyelembe kell vennnk a DNS konstrukcik tervezsekor.
4.2.1.1. Genomilis DNS inszert
Ha a gnnel akarunk dolgozni, akkor vagy az adott faj genomilis knyvtrra van szksgnk vagy
genomilis DNS-t kell izollnunk. A genomilis knyvtrbl kikereshetjk a bennnket rdekl klnt
valamilyen hibridizcis eljrssal (kolnia- vagy plakk-hibridizci; ld. 8.2. fejezet), de ma mr sokkal
egyszerbb kt specifikus primer segtsgvel a specifikus DNS-t gnknyvtrbl vagy az ltalunk izollt
genomilis DNS-bl szrmaz templtrl PCR-rel amplifiklni (ld.0. fejezet). A PCR primerek 5 vgbe
bepthetnk restrikcis endonuklez felismerhelyeket, gy a klnozs a tovbbiakban egy lpsben
megvalsthat lesz (ld. 6.4. bra a 6.4.1. fejezetben)
Ahogy korbban mr bemutattuk, a legclravezetbb klnozsi stratgia a direkcionlis klnozs (ld. 0.
fejezet). A PCR-t kveten agarz glben futtatjuk a mintt, s izolljuk a DNS termket, ha az a DNS
ltrhoz viszonytva a megfelel mret. Az izollst kveten olyan restrikcis endonuklezokkal hastjuk
az inszertet, amelyek felismer helyt a primerekkel beptettk az amplifiklt DNS-be. Az inszertnk a
hastst kveten ragads vg lesz, azaz egy komplementer szekvencij, ragads vg DNS darabbal
53
ssze tud tapadni (lehetsges tompa vget eredmnyez restrikcis enzimet is hasznlni, de a tompa-vg
DNS-ek liglsa, mint az korbban mr emltettk, nehezebb feladat). Vgl jbl megtiszttjuk a DNS- egy
szilika oszlopon, hogy elvlasszuk az enzimektl s apr nukleotid trmelktl, s ezzel elksztettk a
liglsra ksz inszertet.
4.2.1.2. mRNS izolls s cDNS inszert
Amennyiben a gn ltal kdolt fehrje a vizsglataink trgya, akkor az esetek tbbsgben csak cDNS
szintzis vagy esetleg szintetikus DNS jhet szba. Kivtel, ha be tudunk szerezni (vagy mi ksztnk) egy
cDNS knyvtrat, amibl vagy expresszis szkrnelssel keressk meg a szekvencinkat tartalmaz klnt
(ld. 8.3. fejezet) vagy PCR-rel lltjuk el az inszertet.
Ha cDNS-t akarunk ellltani, tudnunk kell, hogy milyen sejtekben, szvetekben expresszldik nagyobb
mennyisgben az adott mRNS. Kivlasztjuk a megfelel szvetet vagy sejtkultrt, amibl elszr totl
RNS-t izollunk. Az RNS izollsra szmtalan mdszer s kit ll rendelkezsre, amelyek kzl itt csak egy
klasszikus mdszert emltnk. Ennl a mdszernl az RNS izolls sorn egy lpsben trtnik a sejtfeltrs
s a szerves-vizes fzis alap extrakci guanidium izotiociant-fenol-kloroform oldattal. A vizes fzis
tartalmazza a totl RNS-t, amit DN-zzal kell kezelni a kromoszomlis DNS szennyezs eltvoltsa
rdekben. Ha cDNS knyvtrkszts a clunk, a totl RNS-bl mRNS-t kell izollni, ami nehz feladatnak
tnik, mivel az mRNS a sejt teljes RNS kszletnek csak nhny szzalka. Azonban, legalbbis az
eukarita mRNS-eknek van egy tulajdonsga, a poli-A farok, amelyet kihasznlhatunk egy egylpses
affinits kromatogrfis tiszttsi eljrshoz. Oligodezoxitimidint (oligo-dT) ktnk kovalensen egy
sznhidrt mtrixhoz (pl. oligo-dT cellulz), s a teljes RNS kszletbl csak az mRNS-ek ktdnek az
oszlophoz. A cDNS-t reverz transzkriptz enzimmel (ld. 3.1.5. fejezet) lltjuk el, oligo-dT primert
alkalmazva.
Amennyiben egy expresszis konstrukci elksztse a cl, kzvetlenl a totl RNS-rl is rhatunk t cDNS-
t amelyet PCR-rel sokszorosthatunk (RT-PCR, ld. 6.4.4. fejezet). A PCR-hez ebben az esetben is olyan
primereket clszer tervezni, amelyek a tapad rgin kvl tartalmaznak egy restrikcis endonuklez
felismerhelyet az 5 tlnyl vgkn.
4.2.2. A vektor elksztse
Nagyon sokfle klnoz s expresszis vektor ll rendelkezsnkre. Fontos tudnunk, hogy csak klnozni
akarunk E. coli sejtekben vagy ms gazdasejttel is dolgozni akarunk, mivel a vektorok replikonjai
specifikusak a gazdasejtekre. Amennyiben a rekombinns DNS konstrukcinkat tbb gazdba is be akarjuk
juttatni, akkor binris (shuttle: ingz) vektort kell hasznlnunk, ami kt gazdban is kpes replikldni.
Figyelembe kell venni a rendelkezsre ll klnozhelyeket, a szelekcis markereket, esetleg tovbbi
szablyoz elemek jelenltt vagy hinyt az alkalmazni kvnt vektorban. A cljainknak legmegfelelbb
vektort kivlasztjuk (ld. 0. fejezet), a vektor DNS-t felszaportjuk s elksztjk az inszert befogadsra.
Az res, vagyis inszertet mg nem tartalmaz vektorbl nagyobb mennyisgre van szksgnk. Ehhez E.coli
baktriumokba transzformlunk egy kis mennyisg DNS-t, majd miniprepet ksztnk (ld. 4.1.1.2.). A
vektor DNS-t ezutn az inszert ksztsekor hasznlt restrikcis endonuklezokkal hastjuk (pl. itt is BamHI
s XhoI), gy az is ragads vg lesz, komplementer az inszert DNS 5- s 3-vgvel. Ezzel a vektor is
kszen ll a mr emltett direkcionlis klnozsra. Ha csak egyfajta restrikcis endonuklezzal hastunk,
fennll a veszlye a vektor nzrdsnak vagy konkatamerek kpzdsnek. Ezrt a hastott vektort
alkalikus foszfatzzal (CIAP) kezeljk, ami eltvoltja a linearizlt vektor DNS 5-vgrl a foszft
csoportot (ezzel megakadlyozhatjuk a vektor-nzrdst). A vektort ezt kveten glbl izolljuk (ld.
4.1.2.4. fejezet).
54
4.2.3. Ligls
A ligls az a folyamat, melynek sorn kt kompatibilis, ragads vagy tompa vg DNS molekult
sszekapcsolunk. Ezzel a lpssel ptjk be a vizsglni kvnt DNS szekvencit, az inszertet a vektorba. A
ligls krlmnyeit gondosan kell megvlasztani, hogy sikeres legyen. Elszr meg kell bizonyosodnunk
arrl, milyen koncentrcij az inszert s vektor DNS oldatunk.
Elvileg megbecslhet, hogy milyen valsznsggel jnnek ltre rekombinns molekulk, ha egyfle
enzimmel nyitottuk fel a cirkulris vektort s ugyanazok a ragads vgek tallhatk az inszertnk kt vgn.
Az n. effektv vgkoncentrci kiszmolhat:
j = 51,1 x [Ms]
(Ms: molekulatmeg; teht pl. egy linearizlt pBR322 fg j rtke 32 g/ml). Ha a vektor koncentrcija
jval kisebb, mint az effektv koncentrci (c<<j), akkor a cirkularizci kerl tlslyba (azaz res vektorok
keletkeznek), ellenben ha magasabb (c>>j), akkor elssorban konkatemerek jnnek ltre. A teoretikusan
legtbb rekombinns DNS kb. 1:2,5 vektor:inszert koncentrciarnynl keletkezik, teht ebben az esetben
kb. 2-3-szoros inszert felesleg jelenltben rdemes liglni. Ha a vektor nzrdst kivdtk a 4.2.2.
fejzetben ismertetett mdon, az inszert felesleget 3-4-szerese emelhetjk.
A reakci elegybe a kt DNS-en kvl a DNS-ligz enzimet s puffert kell adni. Enzimknt leggyakrabban a
T4 bakteriofgbl szrmaz DNS-ligzt hasznljuk, amely a foszfodiszter kts ltrehozshoz szksges
energit ATP-bl nyeri (az ATP-t ltalban az enzimmel egytt vsrolt puffer tartalmazza). Elnye ennek
az enzimnek az E.coli sajt DNS-ligzval szemben, hogy tompa vg DNS-eket is ssze tud liglni (ld. 3.3.
fejezet). Az enzimreakci lezajlsa utn E.coli sejtekbe kell juttatnunk a cirkularizldott rekombinns
DNS-t, transzformlssal. Ezt kveten agar tptalajt tartalmaz Petri-csszkre szlesztjk a transzformlt
baktrium kultrt (kb. 200 l). Mivel a vektorok mindig tartalmaznak valamilyen antibiotikum
rezisztencia gnt, ezrt az agarba antibiotikumot keverve szelektlhatak azok a baktrium sejtek, amelyek
felvettk a plazmidot. Mivel az resen sszezrdott, inszertet nem tartalmaz, de az antibiotikum
rezisztencia gnt hordoz plazmidot tartalmaz baktrium-telepek is megjelenhetnek a lemezen, a
rekombinns DNS-ek kivlasztshoz egy msodlagos szelekcira is szksgnk lesz, amire plda a ksbb
ismertetend n. kk-fehr szelekci (ld. 7.2.3.1. fejezet).
A rekombinns klnokbl nhnyat egy steril pipettahegy vagy fogpiszkl segtsgvel 3-5 ml-es trfogat
tplevesbe oltunk. Ezekbl miniprepet ksztnk. A tiszttott rekombinns DNS-t nagyon fontos jbl
ellenriznnk, hogy valban tartalmazza-e a megfelel inszertet. Ezrt azzal a kt endonuklezzal kezeljk,
amelyekkel a klnozs elejn a vektor felnyitottuk. Ha agarz glben futtatjuk az emsztst kveten a DNS
mintt, akkor sikeres konstrukci esetn kt DNS svot kell ltnunk. Az egyik a linearizlt res vektor, a
msik pedig az inszert DNS a megfelel mretnl. A glen mintt vihetnk fel negatv kontrollknt az res
vektor kt adott (itt BamHI s XhoI) restrikcis enzimmel emsztett elegybl, pozitv kontrolknt pedig az
izollt inszertbl is.
A 4.15. bran pldaknt egy expresszis vektor konstrukci elksztsnek smjt, f lpseit mutatjuk be:
- a fentieknek megfelelen ellltjuk az inszertet (ebben az esetben cDNS-t ksztnk reverz
transzkripci, majd PCR segtsgvel; tovbbi rszletek a 6.4.4. s a 8.3.1. fejezetekben)
- elksztjk a vektort (ebben az esetben egy expresszis vektort hasznlunk)
- in vitro ligljuk a vektort s inszertet
- a rekombinns DNS-t gazdasejtbe juttatjuk transzformlssal (ld. 4.3.1. fejezet)
- a rekombinns DNS-t felvett sejteket felszaportjuk s a rekombinns fehrjt expresszljuk (ld. 12.2.
fejezet).
55
4.15. bra: Egy expresszis konstrukci elksztsnek smja. A plda egy expresszis vektorba liglt cDNS
inszert ellltsnak lpseit mutatja: inszert elksztse, vektor elksztse, ligls, transzformls, sejtnveszts s
fehrje expresszi
4.2.4. TA/Topo-klnozs
A TA- vagy ms nven Topo-klnozs egy olyan klnozsi technolgia, melynek sorn sem DNS-ligzra,
sem restrikcis endonuklezokra nincs szksg. A TA-klnozs alapja, hogy az inszertet olyan DNS-
polimerzzal amplifikljuk, aminek hinyzik az 53 hibajavt nuklez aktivitsa, viszont van templt
fggetlen polimerz aktivitsa (terminlis-transzferz aktivitsa) s meg tudja hosszabbtani egy
nukleotiddal a DNS szlak 3-vgt. Ilyen enzim a Taq-polimerz, amely preferencilisan egy adenin
nukleotidot ad hozz a lncvgekhez. Szksgnk van mg egy specilis vektorra is. A TA-klnoz
vektorok linearizlt, 3-tlnyl timin ragads vgeket tartalmaznak, amelyek bzisprosodnak az inszerten
lv 3-tlnyl adeninnal. A linearizlt vektor 3-vghez a vakcnia vrus DNS-topoizomerz I enzimet
kovalensen hozzkapcsoltk, amely elsegteni a kt DNS szl ligldst (ld. 4.16. bra). A konstrukcikat
a transzformlst kveten itt is a kk-fehr szelekci elvn lehet szelektlni (ld. 7.2.3.1. fejezet).
56
4.16. bra: Az n. TA-klnozs smja. A vakcnia vrus DNS-topoizomerz enzime egyarnt funkcionl restrikcis
enzimknt s ligzknt. Egy specilis szekvencit ismer fel a dupla szl DNS-en: 5-CCCTT-3'. Az enzim a
replikci sorn ennl a szekvencinl hastja a DNS foszfodiszter ktst az egyik szlon egy tlnyl timint
hagyva, majd a szuperheliklis DNS feszltsge lecskken, s az enzim jra liglja a lncot a 3 timin foszft
csoportjnl. Az elvgott szl 3-vgnek foszftja s a topoizomerz tirozinje kztt kovalens kts alakul ki. Ha a
vektort s az inszertet sszekeverjk, akkor a PCR termk 5-vgi OH- csoportja tmadja a foszfotirozil ktst,
elsegtve a ligz reakcit s a topoizomerz levlst. A kereskedelemben kaphat vektorokat linearizlva lehet
megvsrolni, topoizomerzzal ktve. gy a vektort 5 perc alatt liglja a megfelel kompatibilis vg PCR termkkel.
4.2.5. Ligls-fggetlen klnozs
Ennl a mdszernl sincs szksg DNS-ligzra s restrikcis enzimre. A mdszer egyes DNS-polimerzok
(pl. T4, Pfu) 35 exonuklez aktivitsra pl, amelynek ksznheten hossz, ragads vgek
keletkeznek az inszerten s a linearizlt vektoron egyarnt. Az inszertet PCR reakcival amplifikljuk. A
primereket gy kell megtervezni, hogy legalbb 15 nukleotid hosszsg tlnyl vggel rendelkezzenek,
melyek majd kompatibilisek lesznek a vektor tlnyl vgeivel. Az inszertet tartalmaz vektor ligls nlkl
is transzformlhat kompetens sejtekbe, ahol az endogn DNS-ligz hozza ltre a foszfodiszter ktseket.
A primer tlnyl vgeibl hinyzik valamelyik nukleotid, pl. a dCMP. Ebben az esetben egy 35
exonuklez aktivits polimerz dGTP jelenltben a 3-vgtl kezdve eltvoltja a nukleotidokat, amg nem
tallkozik az els citozinnal a templton, ahova beptheti a guanin nukleotidot (ld. 4.17. bra).
4.17. bra: A ligls-fggetlen klnozshoz elksztett inszert
57
A vektort is hasonl mdon kell elkszteni, de elbb hastani kell egy restrikcis endonuklezzal (pl.
tompa vget kialakt enzimmel), amelynek krnyezetben ugyanolyan tvolsgra helyezkedik el az els
gunanin nukleotid, mint az inszert esetben a citozin nukleotid. A vektort is kezeljk a 35 exonuklez
aktivits polimerzzal dCTP jelenltben, gy komplementer ragads vget fogunk kapni.
4.2.6. Restrikcis hasts nlkli ligls rekombincival (attB, attP)
Ez a mdszer a helyspecifikus rekombinci elvn alapszik, ahol a DNS szakasz kivgdst vagy
beplst rvid, specifikus bzissorrend szakaszok teszik lehetv. Ilyen pldul a -fg attB s baktrium
attP (attachment site) rgii. Az inszertbe a primerrel visszk be ezeket a szakaszokat. Ezt a reakcit a
Invitrogene cg BP-klonz enzime katalizlja (a klnoz rendszert Gateway-nek neveztk el). A Cre-Lox
rendszerrel knnyedn ki lehet alaktani delcit, inszercit, inverzit s transzlokcit sejten bell attl
fggen, hogy a Lox helyek hogyan helyezkednek el. A P1 bakteriofg Cre-rekombinz enzime elhastja a
DNS-t, ha LoxP (34 nt) felismersi szekvencit tall, s rekombincit katalizl. Ez a mdszer fleg
transzgenikus llnyek ltrehozshoz hasznlatos (ld. 14.3.2. fejezet). A Gateway klnozsrl tovbbi
rszleteket a 14.3.2. fejezetben olvashatnak.
4.3. Gnbeviteli eljrsok
A plazmid DNS baktrium, leszt vagy egyb eukarita (leszt, nvny, llat) sejtbe val bejuttatsra
szmos lehetsg ll rendelkezsnkre. Ebben a fejezetben a gnbeviteli mdszerek kzl a baktrium sejtek
transzformlst, az eukarita sejtek transzfektlst, az infekcit, az elektroporcit s a gnpuska
hasznlatt mutatjuk be.
4.3.1. Transzformls
A baktrium sejtek kpesek a krnyezetbl DNS molekulk (pl. plazmid DNS) felvtelre. A jelensget
transzformcinak nevezzk, s ez a horizontlis gntranszfer egyik formja (ld. 1.1.2. fejezet). A
gntechnolgiban a transzformci a rekombinns DNS baktrium sejtbe juttatsnak egyik
legltalnosabban hasznlt mdja. A sikeres gnbevitelhez elszr n. kompetens sejteket kell
ltrehoznunk (az a sejt kompetens, amelyik kpes a krnyezetbl DNS-t felvenni). Mivel az E. coli sejtek
viszonylag knnyen kompetenss tehetk, ez a tny is hozzjrult, hogy a gntechnolgiban a legfontosabb
gazdasejt ez a baktrium faj lett.
Kompetens sejteket legegyszerbben gy hozunk ltre, hogy a sejteket CaCl
2
-ot tartalmaz oldatban
inkubljuk (tptalaj sszetevk nlkl). Ez elsegti a plazmid DNS ktdst a baktriumfal
lipopoliszacharidjhoz. A pozitv tlts Ca
2+
-ok vonzzk a negatv tlts DNS-t. Hsokk hatsra pedig a
sejtmembrn fluidabb lesz, s a DNS be tud jutni a citoplazmba (a pontos mechanizmust nem ismerjk).
Ilyenkor a sejteket 4C-rl 42C-ra melegtjk 30-60 sec-ra (hsokk). A sejteket ezutn tpanyagds
kzegben hagyjuk regenerldni, majd szelektv tptalajra szlesztjk ket. A kompetens sejt
transzformcis hatkonysgt szmadattal gy fejezzk ki, hogy kis mennyisg (nhny ng) plazmidot
transzformlunk a gazdasejtbe, megszmoljuk a kolnik szmt az agar lemezen, s azt 1 g plazmid DNS-
re vonatkoztatjuk. 10
7
-10
8
telep/g plazmid DNS esetn magas kompetencirl beszlhetnk. Tapasztalati
alapon kidolgoztak olyan protokollokat is (klnbz fmion keverkkel kezelve az E. coli sejteket),
amelyekkel mg ennl is ersebb kompetencia rhet el (max. 10
10
telep/ g plazmid DNS). A 4.18. bran
baktrium telepek ltszanak agar lemezen.
58
4.18. bra: E.coli telepek agar lemezen
4.3.2. Transzfektls
A transzfekci alapja ugyanaz, mint a transzformls, csak itt a clsejtek emls sejtekbl szrmaznak. Az
elsknt alkalmazott s legelterjedtebb mdszer, a kmiai ton trtn transzfektls, amikor valamilyen
kationos hordozhoz ktdik a negatv tlts DNS, s ezt a komplexet juttatjuk a sejtbe. A kmiai
mdszerek htrnya, hogy sok faktortl fgg a transzfekcis hatkonysg, mint pldul a DNS nukleinsav
sszettele, az oldat pH-ja s a sejtmembrn aktulis llapota. Leggyakrabban olyan kationos lipidet
hasznlunk (pl. lipofektamin), amely liposzmkat kpez, magba foglalva a DNS-t. A liposzma fuzionl
a sejtmembrnnal s ez ltal juttatja be a DNS-t a sejt citoplazmjba.
Igen olcs s egyszer mdja a kmiai transzfektlsnak, amikor kalcium-foszftot alkalmazunk. Foszft
ionokat tartalmaz pufferhez (pl. HEPES) kalcium-klorid oldatot adunk a transzfektlni kvnt DNS-sel. Ez
ltal egy precipittum kpzdik a pozitv tlts kalciumbl s a negatv tlts foszftbl, ami megkti a
felletn a DNS-t. Ezt a szuszpenzit adjuk vgl a sejtekhez, amelyek felveszik a precipittumot a DNS-sel
egytt. Egy msik mdszer a kationos polimerekkel (pl. DEAE-dextrn, polietilnimin) trtn
transzfektls. A negatv tlts DNS a polikationhoz ktdik, majd a sejt endocitzissal veszi fel a
komplexet.
A jval hatkonyabb, s jabban hasznlatos fizikai transzfektls mdszerei kz tartozik mg az optikai
transzfektls s az elektroporci. Az optikai transzfektls esetben lzer segtsgvel kismret (~1 m)
lyukakat kpeznk a sejtek plazmamembrnjn. A mdium s a citoplazma kztti ozmotikus klnbsg
miatt a DNS beramlik a sejtbe.
4.3.3. Elektroporci
Az elektroporci az egyik leghatkonyabb mdszer a cirkulris DNS sejtbe juttatshoz.
Ez a technika a sejt loklis transzmembrn- feszltsgtl fgg. Az elektroporcit egy elektroportor
nev berendezssel vgezzk, amely egy elektromgneses teret hoz ltre a sejteket tartalmaz oldatban.
A sejtszuszpenzit, a bejuttatni kvnt DNS-sel egy olyan kvettba pipettzzuk, aminek a kt oldaln
alumnium elektrdk tallhatak, s nagyfeszltsget hozunk ltre (10,000-100,000 V/cm nhny sec-
msec-ig, a sejt tpustl s mrettl fggen). Nagyon fontos a megfelel skoncentrci. Ha tl magas,
akkor elektromos kisls jhet ltre, ami nagyarny sejtpusztulst okoz. A nagy trer ideiglenesen
lyukakat kpez a foszfolipid ketts rtegen s a sejtfalon. A sejten kvli nagy plazmid koncentrci miatt
hirtelen megindul a lyukakon keresztl a DNS beramlsa a sejt belsejbe. Majd a membrn tltttsge
megsznik, a foszfolipid ketts rteg sszell ismt, gy gyorsan megsznnek a prusok. Ezt kveten az
59
letben maradt sejtek nagy arnyban tartalmazzk a plazmidot, de azonnal mdiumba kell ket helyezni,
hogy regenerldhassanak. Az elektroporci nagy elnye, hogy szinte minden sejttpusra alkalmazhat, s
nagy hatkonysggal lehet vele bejuttatni a DNS-t a sejtbe. Htrnya viszont, hogy ha az elektromos
pulzusok hossza vagy intenzitsa tl nagy, akkor nagy lyukak keletkeznek a sejteken, s elpusztulnak. A
4.19. bran mutatunk be egy elektroportort s a sejteket tartalmaz kvettt.
4.19. bra: Elektroporl kszlk s kvetta
4.3.4. Infekci
Az infekci rekombinns fg illetve rekombinns eukarita, vrus ltal kzvettett gntranszfer baktrium
vagy eukarita (elssorban rovar s emls) sejtekbe. Egy donor baktrium populciban szaportjuk fel a
fgokat s a recipiens baktriumokat fertzzk a rekombinns fg populcival. Az eukaritk esetben is
csak a vrus specifikus gazdasejtjbe lehet rekombinns DNS-t bejuttatni. A mdszer nagy elnye, hogy a
transzformcival ellenttben, ami igen kis hatkonysg gnbeviteli mdszer, az infekci gyakorlatilag
100% hatkonysg (nvnyi gazdasejtek kivtelvel).
4.3.5. Gnpuska
Ez a mdszer egy kzvetlen gntranszfer, melyet eredetileg nvnyi sejtek transzformlsra fejlesztettek ki.
Egy fmbl kszlt (pl. arany) elemi hordozt bevonnak a bejuttatni kvnt DNS-sel. A gnpuska kszlk
segtsgvel szinte akrmilyen sejtbe be lehet lni a gneket. A puska hajtereje nagynyoms hlium
gztartly, ezzel gyorstjuk fel a lvedket. A makrolvedkek egy fkez lemezen fennakadnak, mg a
mikrolvedkek meghatrozott sebessggel sztszrdva becsapdnak a clszvetbe. Az eljrs sikeressgt
a DNS-sel bejuttatott markerek megjelense jelzi. Egy gnpuska vzlatos rajzt a 15.1.2.1. fejezetben, a
15.3. bran mutatjuk be.
4.4. Tovbbi olvasnival a fejezethez
Brown TA (2010): Gene Cloning and DNA Analysis: An Introduction. Wiley-Blackwell, 6th Edition. ISBN-
10: 1405181737.
Sambrook, J and Russel, DW (2001) Molecular Cloning. A Laboratory Manual. CSHL Press, volume 1-3,
Third edition. ISBN: 0879695773.
60
5. DNS szekvenls
A DNS molekula felfedezst kveten intenzven foglalkoztatta a tudomnyt, hogy a klnbz fajok vagy
fajon belli egyedek DNS-e milyen mrtkben mutat egyezst vagy eltrst. Mi az, ami befolysolhatja
klnbz tulajdonsgok megltt vagy hinyt, illetve bizonyos betegsgek kialakulst. Ezrt egyre
fontosabb vlt olyan mdszerek kifejlesztse, melyek segtsgvel meg lehet hatrozni a DNS
szekvencijt. Definci szerint a DNS szekvenls az a folyamat, melynek sorn meghatrozzuk egy
DNS molekula nukleotid sorrendjt. Napjainkban a DNS szekvenls a molekulris biolgia egyik
legmeghatrozbb eszkzv vlt. A modern szekvenl technikkkal mr szmos llny teljes genomjt,
kztk az embert is sikeresen meghatroztk (ld. 0. fejezet).
Az 1970-es vektl kezdve kt mdszert fejlesztettek ki, amelyek kzl a Sanger-fle lnctermincis
(enzimatikus) mdszer szinte egyeduralkodv vlt. A fluoreszcens detektls megjelensvel s
automatizlsval knnyebb s gyorsabb vlt a DNS szekvenls. Vgl az ezredforduln jelentek meg a
teljesen ms mechanizmuson alapul, mg nagyobb hatkonysg s olcsbb n. j-genercis szekvenl
mdszerek (next-generation sequencing), amelyek az informciszerzs mennyisgt tekintve jabb
forradalmi vltozst indtottak el a molekulris biolgiba. Jelenleg ezeket a mdszereket s az automata
lnctermincis szekvenlst prhuzamosan hasznlja a gntechnolgia. A fejezetben ezeket a mdszereket
tekintjk t.
5.1. Kmiai szekvenls: radioaktv vgjellt templt
Az eljrst kidolgozirl Maxam-Gilbert-fle szekvenlsnak is nevezzk. 1977-tl ez volt az els szles
krben elterjedt szekvenl eljrs. Manapsg azonban mr nem igazn hasznljk, mert kiszorult a Sanger-
fle mdszer kidolgozst kveten.
A mdszer a DNS kmiai mdostsn s az azt kvet specifikus bzis mentn trtn hastson alapult. A
DNS szlak 5-vgt radioaktv
32
P-tal jelltk (polinukleotid-kinz enzimmel, ld. 3.4.3. fejezet), majd a kt
komplementer szlat glelektroforzissel izolltk. Ezutn ngy rszre osztottk a mintt s ngyfle kmiai
kezels hatsra, meghatrozott nukleotidok vagy nukleotid prok mentn (A+G, G, C+T, C) trsek
keletkeztek a DNS-ben. A ngyfle reakci: a purinok (A+G) hangyasavval depurinlhatak; a guanin
dimetil-szulfttal metilldik; a pirimidinek (C+T) hidrazinnal metilldnak; a hidrazinhoz adott NaCl
gtolja a timin metilldst, gy csak a citozinok mdosulnak. A reakci lezajlsa utn mindegyik minthoz
forr piperidint adnak, aminek a hatsra a cukor-foszft gerinc elhasad. A reagensek koncentrcijt gy
lltottk be, hogy tlagosan egy DNS molekula csak egyszer mdosult. Vgl denaturl poliakrilamid
glelektroforzis segtsgvel elvlasztottk a klnbz mret, akr egy bzis klnbsg DNS-
fragmentumokat, melyek azonostsa autoradiogrfival trtnt. A glben lv ngy reakcisor mintinak
nukleotid sorrendjre a svok helyzetbl lehetett kvetkeztetni.
5.2. Enzimatikus szekvenls: lnctermincis mdszer
Trtnetileg az els DNS szekvenlsi mdszert Sanger mr 1975-ben kidolgozta (ez volt az n. plusz-
mnusz mdszer, amelyet itt nem ismertetnk), de az igazi ttrst az 1977-ben publiklt lnctermincis
(ms nven didezoxi-) szekvenls jelentette. Egyszersgnek s megbzhatsgnak ksznheten hamar
elterjedt, s nagyon npszerv vlt. Nagy elnye volt a kmiai mdszerrel sszevetve, hogy maga az eljrs
kevesebb mrgez vegyszert s radioaktv vegyletet ignyelt.
A DNS-t ennl a mdszernl klnozni kell, az eredeti mdszer szerint egyszl termket eredmnyez
vektorba. Erre a clra az M13-alap bakteriofg vektorok feleltek meg (ld. 7.3.2. fejezet), ma azonban mr
hasznlhatunk brmilyen ktszl rekombinns DNS-t is a Sanger-fle szekvenls cljra, st PCR
termkeket is kzvetlenl szekvenlhatunk. A templtknt szolgl szlrl DNS-polimerz segtsgvel egy
61
szintetikus primertl kezdden jellt j szlat szintetizlunk, de a ngyfel osztott reakcihoz olyan
didezoxinukleotid analgokat hasznlunk, amelyeket ugyan az enzim elfogad szubsztrtknt, de
lncvgzdst (lnctermincit) okoznak. A didezoxinukleotidokrl hinyzik a 3'-hidroxil csoport, ezrt
nem kpesek foszfodiszter ktst ltrehozni a templtnak megfelel kvetkez aktivlt nukleotiddal, azaz a
DNS-polimerz mkdse egy ilyen nukleotid analg beplse utn lell. A didezoxinukleotidokat a
norml dNTP-hez kpest olyan arnyban kell hozzadni a szekvenl reakcikhoz, hogy a szintzis egy
adott ddNTP jelenltben a templton tallhat komplementer nukleotidnak megfelel sszes pozciban
lelljon. Ily mdon annyifle hosszsg j lnc keletkezik, ahny pozciban a ddNTP-vel komplementer
bzis a templt szlon elfordul. A didezoxiribonukleozid-trifoszftok szerkezett az 5.1. bran, a random
lncterminci smjt pedig az 5.2. bran mutatjuk be.
5.1. bra: A didezoxinukleotid hatsra bekvetkez DNS-polimerz lncterminci. A ddNTP-hez, a 3-hidroxil
csoport hinya miatt, nem kpes tovbbi aktivlt nukleotid kapcsoldni a szintzis sorn, gy a DNS polimerizci
megszakad.
5.2.1. Manulis lnctermincis szekvenls
A manulis szekvenls eredmnynek lthatv ttele autoradiogrfival trtnt. A radioaktv jells
lehetett a primeren, a dNTP-ken (leggyakrabban a dCTP-t jelltk) vagy a ddNTP-ken egyarnt. A mdszer
hskorban kizrlag a viszonylag rvid felezsi idej (13,4 nap), bta-sugrz
32
P izotpot hasznltk.
Htrnya volt, hogy a jellt nukleotid minta hamar lefelezdtt s csak szigor biztonsgi intzkedseket
betartva lehetett a szekvenlst vgezni. Ksbb ezt az izotpot felvltotta az alfa-sugrz, ezltal kevsb
veszlyes
35
S izotp (a foszft-csoport egyik oxign atomjt lehet kicserlni knre), ami radsul sokkal
62
hosszabb felezsi idej (87,5 nap) is. Ennek az izotpnak a htrnya viszont az volt, hogy a gyengbb
sugrzs miatt az autoradiogramok elhvsa hosszabb idt ignyelt. A Sanger-fle lnctermincis
szekvenls smjt az 5.2. bran mutatjuk be.
5.2. bra: A lnctermincis enzimatikus szekvenls smja. Az bra aljn a szekvenl ltrrl olvashat le az
jonnan szintetizlt DNS lnc nukleotid sorrendje (a primertl kezdve, ami nem ltszik) alulrl felfel
Az eljrs azzal kezddik, hogy a DNS mintt (templt) ngyfel osztjk. Az egyes mintkhoz a ngyfle
dNTP-t s sorra az egyik ddNTP-t adjk. Pldul az els csbe a ngyfle dNTP mellett ddATP is tesznek,
gy az j szl szintzise a templton lev timin nukleotidok utn random lellhat. A ngy reakcielegy teht
abban klnbzik, hogy klnbz didezoxi-nukleotidot tartalmaz, de elvileg nem lehet bennk azonos
hosszsg, jonnan szintetizldott szl. A reakci eredmnyeknt kapott, klnbz hosszsg DNS-
fragmentumok vgl egy nagymret, lap alak (slab) denaturl poliakrilamid-urea elektroforzis
glen vlaszthatk el egymstl. Azrt kell a glhez urea denaturlszert adni, hogy a jellt j szlon esetleg
kialakul bzisprosod rgik vagy a jelen lev templt szllal kialakul duplex DNS (trszerkezete lvn)
ne befolysolja a DNS szlak mobilitst az elektroforzis sorn.
63
A reakcielegyeket kln futtatjk a ngy ddNTP stop nukleotidnak megfelelen. Egy adott reakci csak
egyfle ddNTP-t tartalmaz, pldul a ddCTP-t tartalmaz elegy mindig a citozinok, a ddGTP-t tartalmaz
pedig a guaninok elhelyezkedst mutatja meg, gy a ngy mintbl sszell a DNS szekvencija
(lnyegben mindegy, hogy az jonnan szintetizlt vagy a komplementer templt szl szekvencijt
olvassuk le). Az elektroforzist kveten a svokat autoradiogrfival teszik lthatv. A nukleotidok
sorrendjnek leolvassa az egyes mintknak megfelel oszlopoknl alulrl felfel trtnik (ezt nevezzk
szekvenl ltrnak). Ha a legrvidebb (a glen a legnagyobb mobilits) csk a didezoxi-citidines
reakcielegynl tallhat, akkor a DNS szekvencija C-vel folytatdik a primer utn (br a gyakorlatban a
primer utni els nhny nukleotid ltalban nem detektlhat). Ha a kvetkez csk a didezoxi-guaninos
elegynl lthat, akkor a szekvencia guaninnal folytatdik. A leolvass gy megy tovbb, amg mg a cskok
megbzhatan elvlnak egymstl (500-1000 nukleotid hosszsgig).
5.2.2. Automata fluoreszcens szekvenls
Az automata fluoreszcens szekvenls kidolgozsa s az automata szekventorok megjelense (a technika
kidolgozsa Leroy Hood nevhez fzdik) tette lehetv a genom projektek megszletst, mivel
nagymrtkben felgyorstotta a Sanger-fle szekvenl reakcik futtatst (ld. 5.3. bra).
5.3. bra: Egy automata fluoreszcens DNS szekventor (a Biomi Kft.-nek ksznjk a fott)
Tovbbi jts volt, hogy a reakci fokozsa rdekben egy PCR kszlkben zajlik a lncszintzis,
ezltal kevesebb templttal lehet indtani a reakcit, illetve tbb jellt j DNS fragmentum keletkezik, gy a
detektls is knnyebb vlik. Az automata fluoreszcens szekvenls sorn radioaktv jellsek helyett
kizrlag fluoreszcens festket alkalmaznak. A fluorofrt vagy a ddNTP-kre vagy a szekvenl primerekre
lehet bevinni. Ma leggyakrabban a BigDye nev, ngyfle fluoreszcens tulajdonsggal (ez ngyfle
hullmhosszon megjelen emittlt fnyt jelent) rendelkez ddNTP analgokat hasznljk (ld. 5.4. bra).
A mdszer egyszersgt az adja, hogy ngy reakcielegy helyett elegend eggyel dolgozni, ksznheten a
ngyfle eltr fluoreszcens festkkel jellt didezoxi-nukleotidoknak. A jellt DNS fragmentumokat
kapillris glelektroforzissel vlasztjk szt. Az eltr mret fragmentumok kimutatsa fluoreszcencia-
spektroszkpival trtnik. A glt UV-lzerrel vilgtjk meg (bele van ptve a detektorba), s amikor
thalad egy jellt oligonukleotid, akkor az emittlt fny amplitdjt ngyfle hullmhosszon egy detektor
rzkeli. Az adatokat vgl szmtgppel lehet analizlni, amely azonnal megmutatja a nukleotidok
sorrendjt (kromatogram vagy szekvenogram). Ngy szn reprezentlja a klnbz nukleotidokat: piros =
64
T, zld = A, srga = G, kk = C. Egy automata szekvenls eredmnyt (szekvenogram) az 5.5. bra
mutatja be.
5.4. bra: A BigDye fluoreszcens ddNTP analgok szerkezete
5.5. bra: Automata fluoreszcens lnctermincis szekvenls eredmnye (kromatogram vagy szekvenogram)
Szekventortl fggen egyszerre akr 96 mintt is tudnak szekvenlni kapillris gllel, s egy futssal
krlbell 900-1000 nukleotidig lehet leolvasni a szekvencit. Enyhe htrnya a mdszernek, hogy a
lncterminl nukleotidok beplse a DNS fragmentumokba eltr mrtk lehet, gy egyenetlen alak s
magassg cscsokat lehet kapni az elektronikusan kirtkelt kromatogramon. Ezeket a problmkat gy
prbljk meg kikszblni, hogy mdostott DNS-polimerz enzim rendszert s festket alkalmaznak,
amely minimalizlja az egyenltlen bepls okozta hibkat. Tovbbi elvrs minden DNS szekvenl
projekt esetben, fggetlenl a mdszertl, hogy mindkt DNS szlat szekvenlni kell, mivel gy, ha a kt
fggetlen informci a komplementaritsnak megfelel lesz, biztosak lehetnk benne, hogy a templt vals
szekvencijt olvastuk le, vagyis fejtettk meg.
Manapsg tbb biotechnolgiai cgtl is vsrolhatunk lnctermincis szekvenl kitet, amely tartalmazza
a szekvenlshoz szksges reagenseket, gy a reakcit magunk is el tudjuk vgezni, csak a futtatshoz
vesznk ignybe szolgltatst. Alternatv megolds, hogy csak a szekvenland templtot (s esetleg
oligonukleotid primert) kldjk el a szolgltatnak, akitl egy szekvencia kromatogramot kapunk vissza. (A
lnctermincis szekvenlsrl mg ld. 18.4. animci.)
65
5.3. j-genercis szekvenls
Az j genercis szekvenlsok kz tartoznak azok a mdszerek, amelyek prhuzamosan sok mintt
kpesek szekvenlni, azaz nagy teresztkpessg (HTP: high-throughput) mdszerekrl van sz (angolul
ms nven deep sequencing-nek, mly szekvenlnak s massively paralel sequencing-nek is hvjk az j
mdszereket). Az j-genercis mdszerek mind a lncszintzis, mind a detektls tern lnyegileg trnek el
a hagyomnyos Sanger-fle szekvenlstl. Hasznlatukhoz fejlett robottechnika s igen nagy szmtgp-
kapacits szksges. Htrnyuk, hogy valamivel tbb hibt ejtenek s egy reakci sorn viszonylag rvid
(nhny 100 bzis) DNS-darabot szekvenlnak, igaz, hogy prhuzamosan akr 1 millit is. Az j-genercis
mdszerek bevezetsvel robbansszeren megnvekedett a DNS-alap vizsglatok hatkonysga s
cskkent a fajlagos kltsge. Egy j-genercis szekventorral pr ht vagy akr pr ra alatt szekvenlni
lehet akr az emberi genomot is. Elssorban a funkcionlis s a krnyezeti genomika (metagenomika),
valamint a transzkriptomok vizsglata terletn alkalmazzk ket. Fontos megjegyezni, hogy ezek a
mdszerek nem csak DNS szekvenlsra, hanem mRNS (RNAseq), kis RNS-ek (small RNA-Seq), s az
n. CHipseq szekvenlsra (ennl a mdszernl az n. kromatin immunoprecipitcival ellltott
gnexpresszi szablyozsban rsztvev DNS rgikat szekvenljk j-genercis mdszerekkel) is
alkalmasak, melybl kzvetlenl kvetkeztethetnk egy sejt, vagy a vizsgland anyag expresszis
llapotra, s DNS szablyoz rgiira.
5.3.1. Piroszekvenls
A piroszekvenlst 1996-ban dolgoztk ki, s nhny ve mr teljesen automatizltt vlt. A mdszer
alapelve teljes mrtkben eltr a Sanger-fle szekvenlstl. A piroszekvenls a szekvenls szintzissel'
elvn alapul, vagyis egy egyszl DNS templtrl enzimatikusan komplementer szlat szintetizlnak. Vals
idben a DNS- polimerz aktivitst detektljk egy kemilumineszcens enzim segtsgvel. Amikor egy
nukleotid bepl a DNS szlba, pirofoszft (PPi) keletkezik, s ennek a mennyisgt mrjk egy kapcsolt
reakcival, ami vgs soron a luciferz enzim felvillanssal jelez. Egyszerre csak egyfle nukleotidot adnak
a rendszerhez, gy biztos, hogy csak egy nukleotid fog beplni nvekv szlba. Ha tbb nukleotid pl be,
akkor arra a fnyintenzits nvekedsbl lehet kvetkeztetni. Kemilumineszcencia csak a megfelel,
komplementer nukleotid esetben kvetkezik be, hiszen csak akkor szabadulhat fel a pirofoszft. A nem
komplementer, felhasznlatlan nukleotid, mg a kvetkez bzis beplse eltt degradldik. Alapveten
azt kell detektlni, hogy ppen milyen nukleozid-trifoszftot adtak a rendszerhez, s az beplt-e az
egyszl DNS-lncba vagy sem.
Az eljrs egy n. emulzis PCR segtsgvel prhuzamosthat, aminek a segtsgvel mr nincs szksg
arra, hogy a szekvenland DNS darabokat klnozzk. A piroszekvenlsnak kt tpusa van, a szilrdfzis
s a folyadk fzis eljrs. Az els esetben a templtokat szilrdfzis polisztirn gyngykre rgztik, mg
a msodik esetben enzimatikusan, apirz s exonuklez kezelssel ksztik el. Rgztett DNS templt
esetben a vizsgland DNS szlat feldaraboljk s PCR-rel felszaportjk mikzben a primerrel biotinljk.
Majd a szlakat sztreptavidint tartalmaz mgyanta (polisztirn) gyngykhz ktik. Egy gyngyhz
mindig csak 1-1 DNS darabot kapcsolnak. Ezt kveten a gyngyket egy olaj/vz emulzihoz adjk. A
vzcseppek melyek a PCR-hez szksges anyagokat tartalmazzk mrete pontosan akkora, hogy
mindegyikbe 1 db gyngy fr el. A gyngyket olyan szloptikbl ksztett lemezre viszik fel, ami nhny
cm
2
mret, de kb. msfl milli n. nanomlyedst tartalmaz. Egy ilyen mlyeds ~15 pikoliter trfogat,
s csak egy gyngy fr bele. Ezekbe centrifuglssal juttatjk be a DNS-t, majd hozzadjk a reakcihoz a
tbbi szksges sszetevt. A vzcseppekben egymstl elvlasztva, kln-kln zajlanak le a reakcik.
Minden gyngyn 100-500 bzis hosszsg DNS szakasz szaporthat fel. A msfl milli miniatr csben
egyszerre zajlanak le a reakcik, s ez ltal nagyon gyorsan, nagyszm nukleotidot lehet szekvenlni.
Az egyszl DNS templtot elszr egy primerrel hibridizltatjk, majd DNS-polimerz, ATP-szulfurilz,
luciferz, apirz, adenozin-5-foszfoszulft (APS, mint szubsztrt) s luciferin (szintn szubsztrt)
jelenltben inkubljk. A reakci els lpse, hogy valamilyen dNTP-t adnak a rendszerhez. Ha az
komplementer a templttal, akkor bepl a szlba, levlik rla a pirofoszft, melyet a szulfurilz megkt s
66
az APS-bl ATP-t llt el. Az ATP-bl luciferin jelenltben, a luciferz oxiluciferint hoz ltre, amely egy
fnyvillanssal jr folyamat (kemilumineszcencia). Fontos megjegyezni, hogy az ATP-nek egy mdostott
vltozatt, (ATPS) alkalmazzk, melyet a DNS-polimerz igen, de az ATP-szulfurilz nem tud
hasznostani. Ezrt a keletkez ATP biztosan a pirofoszftbl szrmazik, s nem a mestersgesen hozzadott
ATP-t hasznlja fel a szulfurilz. Minden egyes felvillanst a szloptika egy kamerhoz vezet, ami detektlja
s rgzti a kpet. Ismtld bzisok esetben (pl.: TTTTT), t darab dATP fog beplni a szintziskor, s t
luciferint fog felhasznlni a luciferz. A kamera kpes arra, hogy ezt pontosan rzkelje, hiszen a keletkezett
fnymennyisg arnyos a bepl bzisok szmval, teht tszr ersebb lesz.
A be nem plt dNTP-ket s felesleges ATP-t rgztett DNS-templt esetben lemossk, szabad templt
esetben pedig apirz enzimmel lebontjk, mg a kvetkez nukleotid hozzadsa eltt, s kezddhet jra a
ciklus. Egy reakci ~10 mp alatt megy vgbe, gy egy lapocskn ~20 milli nukleotidot lehet meghatrozni.
A mdszerhez megfelel informatikai szoftver(ek) kellett fejleszteni, ami pontosan rtelmezni tudja a kapott
jeleket, melyeket nukleotid sorrendre fordt, majd a rvid szekvencik tfedsei ltal, sszerakja a teljes
DNS molekula pontos szekvencijt. A piroszekvenls smjt az 5.6. bra szemllteti.
Amellett, hogy a piroszekvenls egy rendkvl kltsges mdszer, tovbbi htrnya, hogy mivel nagyon kis
trfogatban zajlanak a reakcik, teljesen egyedi DNS templtokkal, egy reakciban 300-500 nukleotidnl
hosszabb templt DNS-t nem lehet alkalmazni, ami jval rvidebb a Sanger-fle lnctermincis
mdszernl szintetizlt j szlhoz kpest (800-1200 nt). Azonban a legjabb technikkkal 5-10 ra leforgsa
alatt meghatrozhat akr 400 Mbp hosszsg szekvencia is egyetlen kszlkkel (egy ilyen futtats kb. 5-
7 ezer dollrba kerl). Baktriumok esetben 4-5 ra, eukaritk esetben pr ht alatt meg lehet
szekvenlni egy teljes genomot.
5.6. bra: A DNS piroszekvenls smja
67
5.3.2. Illumina/Solexa szekvenls
Ezt a mdszert a Solexa cg fejlesztette ki, melyet az Illumina cg ksbb felvsrolt. Jellegzetessge, hogy
ez volt az els rvid leolvassokat vgz technika. A szekvenlni kvnt DNS-t (akr teljes genomot) apr,
100 bp-os darabokra fragmentljk. A dupla szl DNS kt vgt kijavtjk (ragads vgek eltntetse), s
egy adeninnel toldjk meg az 3 vgeket. Ehhez egy timin tlnyl vggel rendelkez adapter DNS-t
liglnak. A liglt DNS-darabokat ezt kveten szelektljk, s egyszlstjk NaOH-dal. Majd a mintt egy
szekvenl lemezre viszik fel, ahova az adapterrel komplementer oligonukleotidokat (primerek)
horgonyoznak ki. Ezekhez hibridizltatjk a DNS fragmentumokat. Ezutn az n. hd-amplifikcis (bridge
amplification) mdszerrel (ld. 5.7. bra) klasztereket kpeznek az egyes szlak kztt s felszaportjk a
meghatrozni kvnt DNS-szakaszt.
5.7. bra: A Bridge-amplifikcis mdszer. A felsznen trtn amplifikci lland hmrskleten (60C) zajlik
megfelel puffer s denaturlszer jelenltben. Minden reagens egy ciklus erejig van jelen, aztn lemosdik. A PCR
reakci vgn kapott dupla szl DNS templt szlt (amit eredetileg hibridizltattak a horgonyra) formamiddal
levlasztjk s lemossk. Az egyszl DNS elhajlik, s a szabad vgvel egy msik lehorgonyzott primerrel hibridizl.
Ezzel is vgbemegy a PCR, s a vgs denaturci. Ezt kveten az trt szlak egymssal vagy msik primerrel
hibridizlhatnak s duplikldnak, majd tovbbi amplifikci utn kszen llnak a szekvenlsra.
Maga a szekvenls itt is szintzissel trtnik. A templthoz egy primert liglnak, majd a reakcihoz
egyszerre adjk hozz a 4 nukleotidot (reverzibilis termintorok, ld. 5.8. bra), melyeket klnbz
fluoreszcens jellssel ltnak el.
5.8. bra: Egy n. reverzibilis nukleotid analg szerkezet
68
A beplt nukleotid fluoreszcens jelt CCD kamerval detektljk. A nukleotid beplse utn kmiai ton
levgjk rla a fluorofrt s a 3' blokkolt, majd lemossk a be nem plt nukleotidokkal egytt. Ezzel a
mdszerrel a humn genomot 7-10 nap alatt lehet szekvenlni, radsul a kltsgek is alacsonyabbak.
5.3.3. SOLiD (Sequencing by Oligonucleotid Ligation and Detection)
A szekvenls oligonukleotid liglssal s detektlssal (SOLiD: Sequencing by Oligonucleotid Ligation
and Detection) technika 2006-ban szletett meg. Elnye, hogy nagysgrendekkel alacsonyabb kltsgekkel
dolgozik, mint a korbbi mdszerek, viszont htrnya, hogy rvid leolvasott szekvencikat eredmnyez
(ezrt pldul genom projektekhez nem igazn alkalmas). Az eljrs ebben az esetben is azzal kezddik,
hogy feldaraboljk a genomot (35-50 bzis hossz fragmentumokra), s egy fragmentum knyvtrat
hoznak ltre. Elszr a fragmentumok kt vgre klnbz adaptereket (pl. A1 s A2) liglnak. Msodik
lpsknt a szlakat mgneses gyngykhz kapcsoljk gy, hogy az 1m-es gyngykhz kapcsolt P1 s
P2 primerek hibridizlnak a komplementer A1 s A2 templt vgekkel. Minden gyngyhz csak egyfle
DNS darab kapcsoldik. Ezt kveten emulzis PCR-rel felszaportjk a szlakat a gyngyk felsznn,
denaturljk a templtot s a gyngyket kovalensen szekvenl lemezre ktik. A szekvencia
meghatrozs itt liglssal trtnik olyan oligonukleotidok segtsgvel, melyek oktamerek, vagyis 8
nukleotidbl llnak, s ngyfle fluorofrral jellik ket (ld. 5.9. bra).
5.9. bra: A SOLiD szekvenlshoz hasznlt primerek. A prbk 8 nukleotidbl plnek fel. Az 1. s 2. nukleotid
specifikusak (X; komplementerek a szekvenland templttal), a 3.,4.,5. nukleotidok degenerltak (N; kpesek
brmilyen nukleotiddal prosodni a templton) s vgl a 6.,7.,8. nukleotidok (z) univerzlisak. A prbk
rendelkeznek egy 3'-hidroxil csoporttal, az 5'-vgen egy fluoreszcens jellel, valamint az 5. s 6. nukleotid kztti
hasthellyel, ahonnan a fluoreszcens jells, a prba beplst kveten lehasad. A prbknak, a kt darab
specifikus nukleotidot figyelembe vve teht 16-fle (4x4) kombincija lehetsges.)
Egy templt szl liglsshoz 7 ciklus szksges, ilyenkor az 5'-vgtl szmtott 1. s 2., a 6. s 7., valamint
hasonlan a tovbbi pozcik prosodnak. Ahhoz, hogy az sszes bzis elhelyezkedst meg lehessen
ismerni, tszr kell megismtelni a htciklusos reakcit. Minden ismtlsnl j primert adnak a reakcihoz,
ami a 3'-vg fel egy-egy bzissal elcsszva (n-1, n-2, stb) anelll a templthoz, gy vgezetl minden bzist
ktszer olvas le a rendszer.
5.3.4. TSMS (True Single Molecule Sequencing: Valdi egymolekuls
szekvenls)
2007-ben fejlesztettk ki ezt a technikt (Heliscope kszlk), amely amplifikci nlkl is kpes
szekvenlni akr egyetlen molekula DNS-t is. Hasonlan az eddig bemutatott eljrsokhoz, a szekvenlni
kvnt DNS-t elszr 100-200 bp-os darabokra hastjk. Majd 94C-on denaturljk a kettshlixeket. Az
egyszl fragmentumokhoz adapter DNS-molekulkkal fluoreszcensen jellt poli-A farkakat ktnek. Erre
azrt van szksg, mert a DNS-darabokat egy kamra fellethez ktik, amihez hatalmas srsgben (100
milli/cm
2
) oligo-T-ket kapcsoltak, s ehhez hibridizltatva lehet a fragmentumokat a felsznhez rgzteni. A
69
szekvenlshoz elksztett kamrt egy kszlkbe helyezik, ami lzerrel vilgtja meg a felletet. Azok a
pontok fognak vilgtani, ahov sikeresen hibridizltak a DNS-darabok. Ezzel tulajdonkppen a detektor
feltrkpezi, hogy hol vannak a szekvenlsra vagyis szintetizlsra alkalmas pontok. Ezt kveten
lehastjk, s lemossk a fluoreszcens molekulkat a felsznrl, majd megkezdik a szintzist. Ehhez DNS-
polimerz s fluoreszcensen jellt dNTP-k szksgesek, primerknt az oligo-T szolgl. Ahogyan a
piroszekvenlsnl, ennl a techniknl is egyszerre csak egyfle nukleotidot adnak a rendszerhez (pl.
dGTP), ami a poli-A farok utni els citozinnal prosodni fog. Gerjeszts hatsra azok a szlak fognak
vilgtani, ahova az adott nukleotid beplt. Majd lemossk a felsznt, s jhet egy msik jellt nukleotid. A
ngyfle nukleotidot mindig egymst kvetve, meghatrozott sorrendben adjk a felsznhez. Minden lps
vgn csak azok a szlak vilgtanak, ahov beplt az ppen aktulis dNTP. A kszlk minden egyes
lpst kveten egy fnykpet kszt a lemezrl. Ezzel a mdszerrel naponta 1 millird bzist is lehet
szekvenlni. Htrnya, hogy 0,5%-os hibval dolgozik.
5.3.5. SMRT (Single Molecule Real-time: Egymolekuls valsidej)
szekvenls
2011-ben fejlesztette ki egy amerikai cg a SMRT kszlket. Ezzel a mdszerrel a humn genomot akr 15
perc alatt meg lehet szekvenlni kb. 100 dollrbl. Ilyen kszlkbl jelenleg kb. 10 darab zemel a vilgon.
1,5-2,9 kbp hosszsg szakaszokkal dolgoznak, ami ltal pontosabb szekvencia meghatrozs rhet el. A
reakcik apr, 'egymolekuls' kamrkban zajlanak, a DNS szintzis pedig fluoreszcensen jellt
nukleotidokkal trtnik. Ez a jells abban klnbzik az eddig lertaktl, hogy a festket nem a bzisra,
hanem a foszftcsoportra rakjk, amely a nukleotid beplskor lehasad a pirofoszfttal egytt. A levl
fluoreszcens pirofoszftot egy nanofotonikus vizualizl kamra detektlja. Egy-egy kamrban 20 zeptoliter
(20
-21
) mintt lehet rzkelni. Minden kamra aljra egyetlen DNS-polimerz van rgztve, ami a szintzist
vgzi. A mdszer igazi erejt az adja, hogy egy lemezen tbb ezer ilyen kamrcska tallhat, ezrt hossz
DNS-szlakkal, nagyon nagyszm minta szekvenlhat meg prhuzamosan. Mint minden szintzisen
alapul szekvenl techniknl, itt is a homopolimerek pontos meghatrozsakor akadnak nehzsgek,
ugyanis ebben az esetben csak a fluoreszcencia intenzitsbeli klnbsgeire lehet hagyatkozni.
5.4. Tovbbi olvasnival a fejezethez
Schuster SC (2008) Next-generation sequencing transforms todays biology. Nature Methods 5:16-18.
Harbers M, & Kahl G (2012) Tag-based Next Generation Sequencing. Wiley Online Library
70
6. Polimerz lncreakci (PCR)
6.1. A PCR lpsei
A polimerz lncreakci 1983-as felfedezse ta (ld. 1.5.1 fejezet) mra a modern biolgiai kutatsok s
szmos alkalmazott tudomnyterlet nlklzhetetlen mdszerv vlt. A PCR jelentsgt az adja, hogy
DNS-polimerz enzimet hasznlva laboratriumban, teht in vitro, molekulris klnozs nlkl is kpesek
vagyunk specifikus DNS molekulkat sokszorostani. A PCR eljrs sorn egy ciklusban hrom fzist
klnbztetnk meg (ld. 6.1. bra).
1. Denaturls: a ketts szl DNS sztvlasztst biztostja.
2. Anellls: szintetikus, rvid DNS oligonukleotidok tapadsa (bzisprosodssal) a templt szlhoz,
amelyek a DNS-polimerz szmra primerknt szolglnak.
3. Polimerizci (extenzi): a cl DNS szintetizlsa aktivlt monomerek (dNTP-k) beptsvel.
6.1. bra: A PCR els hrom ciklusnak sematikus brzolsa. Sznkd: piros, a tbbszrzni kvnt
clszekvencia; kk, a teljes DNS szekvencia; fekete, primerek; zld, jonnan szintetizlt DNS. A msodik ciklusban a
3 fzist megismtelve j vgtermk keletkezik, amelyeknek egyik vge mr egybeesik a kvnt minta vgvel. Vgl
lthatjuk, hogy a 3. ciklusban vgbemen folyamatok a clszekvencia (az amplikon) megjelenshez vezetnek.
6.1.1. Denaturls
A DNS replikci els fzisban a kettshlixnek szt kell vlnia, hogy az egyes szlak templtknt
tudjanak szolglni a polimerizci sorn. Ez a folyamat a sejten bell enzimatikusan megy vgbe, a
71
kettshlix szttekersben motorfehrjk, DNS-helikzok vesznek rszt. A helikzok ATP felhasznlsval
a kmiai energit mechanikai munkv alaktjk t, azaz a DNS szlon vgighaladva a bzisok kztti H-
ktseket sztbontjk. A PCR sorn a DNS kt szlnak sztvlasztsa nem enzimatikusan, hanem
termodinamikai ton trtnik magas hmrsklet hatsra a bzisokat sszetart hidrognktsek
felszakadnak. A msodlagos ktsek sztesshez szksges hmrsklet fgg az adott DNS hossztl
minl tbb bzisprt tartalmaz a polimer, annl magasabb hfok szksges a teljes felbomlshoz. A PCR
els fzisban, a denaturci sorn 92-98C kztti hmrskletet hasznlunk. Ez a hmrsklet
tartomny elegend ahhoz, hogy a DNS templt hossztl (s komplexitstl) fggetlenl teljes mrtkben
sztvlasszuk a kt szlat. A PCR hskorban ez a magas hmrsklet fzis okozta azt a problmt, hogy
minden egyes ciklust kveten j DNS-polimerz enzimet kellett a reakcihoz adni. Ezt a problmt sikerlt
a Taq-polimerz hasznlatval megoldani. A Thermus aquaticus baktriumot a Yellowstone Nemzeti Park
egyik hforrsban fedeztk fel. A hforrs vize 50-80C kztt ingadozik (a baktriumnak optimlis
hmrsklet pedig 72C-on van), ennek ksznheten a benne tallhat fehrjk ezekhez a szlssges
krlmnyekhez adaptldtak, gy kzel 100C-on sem vesztik el natv szerkezetket (pontosabban ezen a
hmrskleten lassan mr cskken az aktivitsuk, amit a PCR ciklusok elrehaladtval folyamatosan
kompenzlni lehet). A manapsg hasznlatos PCR enzimek kztt tbb htr (termofil) s extrm htr
(extremofil) baktriumbl szrmaz termszetes vagy rekombinns, esetleg tovbbi elnys tulajdonsggal
feljavtott DNS-polimerz tallhat (ld. 3.1.4. s 6.2.2. fejezetek).
6.1.2. Anellls
Az PCR msodik fzisban trtnik a rvid DNS primerek templthoz tapadsa, anelllsa. Mivel a
denaturcihoz hasznlt magas hmrsklet megakadlyozn a DNS primerek megfelel helyre val
tapadst, ebben a fzisban a hmrskletet le kell cskkenteni. A megfelel tapadshoz szksges
hmrsklet fgg az adott primerek hossztl s szekvencijtl, teht a reakci sorn ennek fggvnyben
lltjuk be az anellcis hmrskletet. Ha nem megfelelen lltjuk be, akkor attl fggen, hogy
alacsonyabb vagy magasabb hmrskletet hasznlunk, tbb problmba tkzhetnk. Elszr is, ha az
optimlisnl alacsonyabb hmrskletet lltunk be, akkor a primerek tapadsa aspecifikuss vlhat, s nem
a megfelel szekvencij rszhez vagy tbb helyhez ktdve indul el a DNS polimerizci, gy nem a
megfelel, vagy tbbfle termket kapunk (ez a mispriming-nak nevezett jelensg). Ha magasabb
hmrskletet lltunk be az anellcihoz, akkor a DNS primernk nem lesz kpes ktdni a templt
szlhoz. A gyakorlatban tapasztalt idelis hmrsklet tartomny a DNS primerek ktdsre 55-65C
kztt van (az anelllsi hmrskletet megbecslhetjk az adott oligonukleotid olvadsi hmrskletnek
kiszmtsval, ld.6.2.3 s 10.3.4. fejezet).
6.1.3. Polimerizci/lnchosszabbts (extenzi)
A DNS lnc szintzise, a polimerizci vagy lnchosszabbts (extenzi) a DNS-polimerz elsdleges
feladata. Az lvilgban szmtalan klnbz tulajdonsg DNS-polimerz enzim tallhat (ld. 3.1.
fejezet). A kzs jellemzjk, hogy a templt szlra szintetizlt primerekbl kiindulva, azok 3 OH-
csoportjra kpesek a kvetkez dNTP-t a templtnak megfelelen bepteni. Az egyes polimerz enzimek
rendelkezhetnek 3-5 s 53 exonuklez aktivitssal, amelyek kzl az els tulajdonsg a
hibajavtsrt, mg a msodik elssorban az RNS primerek elbontsrt felels (ld. 3.1. fejezet). A
klnbz polimerzok templtrl trtn msolsi hsge is nagyban klnbzhet egymstl, ezrt fontos
hogy a PCR sorn olyan enzimmel dolgozzunk, aminek megfelel a hatkonysga.
A PCR harmadik fzisban htr baktriumokbl izollt, illetve manapsg mr rekombinns mdszerekkel
ellltott polimerzok vgzik a DNS szintzist. Ezeknek az enzimeknek a megfelel mkdshez
optimlis hmrsklet szksges, ami 70-80C kztt van. A mdszer mindhrom fzisban fontos a
megfelel idintervallum belltsa (elg id kell mind a teljes ketts szl DNS sztnylshoz, mind a
primerek megfelel helyre val letapadshoz), de fknt a polimerizcis fzisban kell odafigyelni, mivel
minl hosszabb DNS szakaszt akarunk felersteni, annl tbb idre van szksge az enzimnek.
72
ltalnossgban szmolhatunk gy, hogy 1 perc alatt a DNS-polimerz ezer nukleotidot pt be, de ma
mr kaphatak ennl gyorsabb enzimek is.
A DNS termk mennyisge nagyban fgg a ciklusok szmtl. A lncnvekeds mrtke elmletileg
exponencilis, amit a kvetkez egyenlettel lehet lerni:
N
t
= N
k
(1+H)
n-2
N
k
kiindulsi clszekvencik szmbl n ciklust kveten szintetizldott N
t
(teljes) clszekvencik szma a
totlis vgtermk (amit amplikonnak is neveznk), H hatkonysg mellett. Idelis esetben H = 1, azonban a
DNS-polimerz tbb ciklust kveten veszt a hatkonysgbl, valamint a reakci sorn fogy reagensek
kvetkeztben a polimerizci hatkonysga az idvel cskken. Vgl figyelembe kell venni azt is, hogy a
PCR molekulris sajtsga miatt a reakci els kt ciklusban mg nem keletkezik a kvnt mret DNS szl
(ld. 6.1. bra).
Lthat, hogy a PCR folyamn egy ciklus alatt a klnbz fzisokhoz eltr hmrsklet szksges, ezrt
az automatizlt PCR kszlk egy programozhat termosztt (ld. 6.2. bra). (A polimerz lncreakcirl
mg ld. 11.1.2., 11.2.3., 16.2.1. fejezetek s a 18.5. animci.)
6.2. bra: PCR kszlk
6.2. A PCR reakci komponensei
Az in vitro DNS sokszorostshoz a fent lertak szerint szmos komponensre van szksg. Ezeket
rszletezzk ebben a fejezetben, elssorban praktikus szempontokat eltrbe helyezve.
73
6.2.1. PCR templt
A kvnt clszekvencia felerstshez szksges templt DNS szmos forrsbl szrmazhat. A molekulris
biolgiai alapkutats sorn szmtalan clbl vgezhetnk PCR reakcit, pldul rekombinns fehrjt
kdol gn felerstsre (expresszis konstrukci ksztshez), vagy taxonmiai azonostshoz (pl.
krnyezeti PCR). Az els esetben templtknt klnbz szvetekbl vagy szervekbl szrmaz RNS-rl
kszlt cDNS-t hasznlhatunk (ld. 6.4.4.). Ha nem ll rendelkezsnkre megfelel minsg cDNS (akr
cDNS knyvtr, akr sajt magunk ltal totl RNS prepartumrl ksztett cDNS), akkor az egyes DNS
konstrukcikhoz hasznlt templtot meg is rendelhetjk valamely biotechnolgiai cgtl vagy a non-profit
rekombinns DNS klnmegoszt szervezettl, az Addgene-tl.
A faj alap azonostsokhoz ma mr elengedhetetlen a PCR hasznlata. A mikrobiolgia ennek a
mdszernek a segtsgvel kpes klnbz forrsbl szrmaz mintkban elfordul baktriumokat nagy
pontossggal azonostani. Az orvosi diagnosztikban pldul a pciensbl szrmaz mintkbl felerstett
PCR termk segtsgvel lehet megmondani, hogy a fertzst milyen krokoz okozhatta (legyen az akr
egysejt eukarita, akr baktrium, akr vrus). Az igazsggyi orvostanban a DNS-t minta alapjn lehet egy
apasgi perben a biolgiai apt, egy bngyben pedig az elkvett (amennyiben DNS-t tartalmaz biolgia
mintt hagy htra a tett sznhelyn) azonostani.
A PCR, mint DNS amplifikcis mdszer risi elnye, hogy a templt DNS-nek nem kell tiszttott
prepartumnak lenni, azaz sejt- vagy szvetminta, DNS-t tartalmaz brmilyen, akr koszos minta PCR
templtknt szolglhat. gyelnnk kell azonban egyes mintkban (pl. vr, talaj) a PCR inhibitorok
jelenltre. Ezeknek a negatv hatst szmos mdon lehet cskkenteni (pl. a vr esetben hozzadott BSA-
val vagy Chelex gyantval).
6.2.2. PCR enzimek
A forgalomba kerlt, magas hmrskletet elvisel, rviden hstabil DNS-polimerz enzimek szma az
utbbi kt vtizedben megtbbszrzdtt. Ezeket leggyakrabban hforrsokban l baktriumokbl,
mlytengeri, vagy cenaljzaton l hipertermofil sbaktriumokbl izolljk.
A htr baktriumokbl izollt enzimeket rendszerint klnozzk, annak rdekben, hogy rekombinns
fehrjeknt nagyobb mennyisgben s nagyobb tisztasggal tudjk ellltani megfelel baktriumokban,
pldul E. coli-ban. Ilyen enzim a Taq-polimerz tulajdonsgaival rendelkez Amplitaq, amelyet szintn a
Cetus szabadalmaztatott, s mg ma is idelis rvid DNS szakaszok tbbszrzsre. Ugyanakkor problma,
hogy az eltr gyrtktl kaphat ugyanolyan fajta enzimek is eltrnek egymstl a felersthet termk
hosszban, mennyisgben s msolsi pontossgban. A Taq-polimerz htrnya az alacsony msolsi
pontossg (1 hiba/10
4
bp), aminek az az oka, hogy az enzim nem rendelkezik 35 hibajavt exonuklez
aktivitssal. Szles krben elterjedt a Vent- s a Pfu-polimerz enzimek, amelyek 35 exonuklez
aktivits DNS-polimerzok. A Vent DNS-polimerzt a Thermococcus litoralis, mg a Pfu DNS-
polimerzt a Pyrococcus furiosus hipertermofil, mlytengeri hidrotermlis krtkben el Archea
baktriumokbl klnoztk. Az utbbi a jelenleg ismert legnagyobb msolsi hsggel mkd polimerz
enzim (~10
-6
hiba/bp). Elnyk mg, hogy magas hmrskleten jval alacsonyabb a felezsi idejk a Taq
enzimhez kpest. A 35 exonuklez aktivits enzimek kiemelked msolsi hsgknek ksznheten
jval hosszabb lnc DNS szekvencik tbbszrzsre is alkalmasak, mint a Taq enzim, ugyanakkor
ltalban lassabb a lnchosszabbt sebessgk.
Helyspecifikus mutcival a polimerz enzimek pontossga, hstabilitsa tovbb fokozhat. Pldul a Pfu
polimerzt gy mdostottk, hogy a polimerz domnjhez egy ketts-szl DNS-kt domnt
fuzionltattak, ezzel megnvelve az enzim pontossgt s hatkonysgt (ez a Phusion DNS-polimerz).
(A hstabil DNS-polimerzokkal a 3.1.4. fejezet is foglalkozott.)
74
Bizonyos DNS-polimerzok, megfelel krlmnyek mellett, RNS reverz transzkripcijra is kpesek; ilyen
enzim a Thermus thermophilus-bl izollt Tth DNS-polimerz. Ennek az enzimnek a hasznlatval nem
szksges kln reverz transzkriptz enzimet adni a reakcihoz, amennyiben RNS mintbl indulunk ki s
RT-PCR (ld. 6.4.4. fejezet) vagy kvantitatv, vals idej PCR-t (ld. 6.3.2. fejezet) vgznk. A vgtermk
tisztasgnak nvelse rdekben egyes DNS-polimerzokat gy mdostottak, hogy csak a denaturcis
hmrskleten aktivldjon. Ezt a mdszert hvjuk Hot Start PCR-nek. Trtnhet az ideiglenes
inaktivls ellenanyaggal is, amely a DNS-polimerzhoz kapcsoldik, majd a denaturcis hmrskleten
elvlik tle, s visszafordthatatlanul denaturldik. A Hot Start PCR-rel mkd enzimek kztt igen
szles a vlasztk, ilyen DNS-polimerz pldul az AmpliTaq Gold nven forgalmazott mdostott Taq-
polimerz.
6.2.3. PCR primerek
A PCR sorn trtn DNS sokszorostshoz szintetikus (dezoxi)oligonukleotid primereket hasznlunk. A
reakcihoz egy n. "forward" (5-) s egy "reverse" (3-) primer szksges. Az els a felersteni kvnt
DNS szakasz 5-vgn a komplementer szlhoz fog anelllni, mg az utbbi az trand DNS szakasz 3-
vgvel komplementer. A mindennapi gntechnolgiai alkalmazs sorn ltalban 18-25 nukleotid
hosszsg primereket rdemes tervezni, ennl hosszabb primerek mr nem nvelik jelentsen a reakci
fajlagossgt. A primerek szekvencijnak a 3-vgtl legalbb 10 nukleotid tvolsgra tkletesen
komplementernek kell lennie a templt szllal, a primer 5-vgen viszont nem felttel a komplementarits
(ezt a lehetsget lehet kihasznlni pldul a PCR termk vektorba trtn beptse sorn, ld. 6.4.1.)
A primerek tervezse sorn tbb szempontot figyelembe kell venni. Elszr is a kt tervezett primer
(forward, reverse) ne legyen egyms komplementere, mg rszlegesen sem. Ekkor ugyanis n. primer
dimerek jnnek ltre, mivel a kt primer kapcsoldst kveten a DNS-polimerz az egyiket templtknt
hasznlva rvid szakaszokat szintetizl. A primer dimerek kialakulsa nagyban cskkenti a helyes PCR
termk keletkezst. gyelni kell arra is, hogy a tervezett primeren bell ne alakuljon ki msodlagos
szerkezet, pldul hajtkanyar, mert az ersen gtolja a templt DNS-re val ktdst. A reakci sorn az
alkalmazott primer koncentrci is dnt fontossg, mivel tl alacsony koncentrci esetn cskken a
letapads eslye az anellls sorn, mg tl magas primer mennyisget alkalmazva nem kvnt, aspecifikus
termkeket is kaphatunk. Az anellls hmrskletnek meghatrozshoz kiemelkeden fontos a primerek
szekvencija. A templthoz ktds jellemz tulajdonsg a T
m
, ms nven olvadsi hmrsklet. Ez a
paramter jelzi azt a hmrskletet, ahol a ketts szl DNS-ek fele sztvlik. Ennek meghatrozshoz
figyelembe kell venni a primerek hosszt s nukleotid tartalmt. Krlbell 20-40 nukleotid hosszsgig a
kvetkez egyszer formulval (n. Wallace-szably, ld. 10.3.4. fejezet) szmolhatjuk ki az olvadsi
hmrskletet:
T
m
(C) = 4(G + C) + 2(A + T)
A kplet szerint a guanin-citozin (G-C) bzisprok 4C-kal, mg az adenin-timin (A-T) bzisprok 2C-kal
jrulnak hozz az olvadsi hmrsklethez. A primerek olvadspont szmtsrl tovbbi rszletek
tallhatk a 10.3.4 fejezetben. A PCR reakci alatt az anellcihoz szksges hmrskletet (T
a
) ltalban a
T
m
-nl 5C-kal alacsonyabban hatrozzuk meg. A tervezs sorn gyelni kell arra, hogy a kt primer
anellcis hmrsklete ne trjen el nagyon egymstl, gy a PCR sorn mindkt primer kapcsoldsi eslye
kzel azonos lesz.
6.2.4. Egyb PCR komponensek
A megfelel PCR-hez a fent lertakon kvl szmos ms reagens is szksges. Az egyes DNS-polimerzok
helyes mkdshez az adott enzimhez optimlis puffert kell hasznlni, amit ltalban a megvsrolt
enzimhez adnak. A DNS-polimerzokhoz kaphat klnbz pufferoldatokban ltalban Tris-HCl s
valamilyen s, pldul NaCl, KCl tallhat. Az oldatok pH-ja ltalban 8,5 krl van, ami majd a reakci
75
sorn (a magasabb hmrskleten) ~7,2-re cskken. A kereskedelmi forgalomban lv pufferoldatok
ltalban tzszer tmnyebbek a vgs koncentrcikhoz kpest, gy hgtani kell ket a reakci
sszemrsekor. A pufferoldatok ezen kvl tartalmazhatnak egyb, a reakci hatkonysgt nvel
anyagokat. Pldul reduklszereket (pl.: ditiotreitolt), detergenseket (pl: Triton X-100) vagy ms n.
erst szereket, pldul: glicerint, zselatint vagy DMSO-t. Ezek az anyagok fleg a DNS-polimerzt
stabilizljk, nvelik a hatsfokt, de magas koncentrciban gtolhatjk is a PCR reakcit.
A reakcihoz szksges mg mind a ngy fajta dezoxiribonukleotid (dNTP), egyenl arnyban, ugyanis az
eltolt dNTP arny negatvan befolysolhatja az amplikon keletkezst. A dNTP-k egyfell a DNS
szintzishez szksges aktivlt monomerek, msrszt energiaforrsknt szolglnak a DNS-polimerz motor
funkcijhoz (a polimerz vgighalad a templton, teht nem csak kmiai, hanem mechanikai munkt is
vgez). Kereskedelmi forgalomban kivl minsg dNTP keverkekhez juthatunk hozz, 2-10 mM
koncentrcij trzsoldatban. A PCR sorn ltalban 50-200 M koncentrci kztt dolgozunk
A DNS-polimerzok helyes mkdshez az enzimnek szksge van valamilyen ktrtk kationra. A
legidelisabb a Mg
2+
, de a fehrje kpes Mn
2+
mellett is mkdni, igaz nem a legjobb hatsfokon. Emellett
ezek az ionok a dNTP-kel komplexet kpezve szolglnak szubsztrtknt az enzim szmra. Megjegyzend,
hogy sokszor a ktrtk kation koncentrcija befolysolja az amplikon mennyisgt s specifitst is,
ezrt nem minden pufferoldatban van benne elre a Mg
2+
,
mi is hozzadhatjuk a reakcihoz, amennyiben azt
optimalizlnunk kell.
6.3. A PCR termk (amplikon) detektlsa s kvantitatv PCR
6.3.1. Agarz s poliakrilamid glelektroforzis
A PCR helyes vgbemenetelnek ellenrzsre tbb mdszer ll rendelkezsnkre. A legegyszerbb s a
legltalnosabban hasznlt mdszer az agarz vagy poliakrilamid glelektroforzis, amelyek segtsgvel
mret alapjn tudunk DNS fragmentumokat elvlasztani. Mindkt mdszer esetn a polimerizlt szilrd
fzis tmnysgvel lehet belltani az elvlasztsi tartomnyt (ld. 4.1.2. fejezet), gy a vrt PCR termk
hossznak megfelelen tudunk detektlni. A DNS szlak lthatv ttelt valamilyen interkall festkkel
(pl.: etdium-bromid, SYBR Green) vgezzk el, amelyek a ketts szlba plve UV-fny hatsra
megjelentik a termket. A PCR reakcik dnt tbbsgt (amennyiben az amplikon hossza >100 bp) agarz
elektroforzissel detektljuk (ennl kisebb PCR termk esetn jn szba a PAGE)
6.3.2. Vals idej (real-time) vagy kvantitatv (q-) PCR
A vals idej, angolul real-timePCR mdszer lnyege, hogy a DNS sokszorostst kvantitatvan tudjuk
nyomon kvetni. Ezzel a technikval nagy pontossggal meg tudjuk hatrozni a DNS templt kiindulsi
mennyisgt, ami sok szempontbl igen hasznos lehet (pl. az orvosi diagnosztika terletn, amikor egy
vrusfertzs mrtkre vagyunk kvncsiak). A real-time PCR-t tbbfle mdon is meg lehet valstani.
A vals idej PCR sorn a DNS mennyisgnek meghatrozs azon a kzs elven alapszik, hogy a
clszekvencihoz olyan primer prbt (szondt) ksztenek (harmadik oligonukleotid), amely nem a
forward vagy reverse primer letapadsi helyre ktdik, hanem attl klnbz helyre, valahol kzttk.
Kezdetben olyan szintetikus oligonukleotidot alkalmaztak, amely 5-vgn radioaktv izotp foszftot
tartalmazott, a 3-vget viszont gy mdostottk, hogy arrl ne tudjon a polimerz szlhosszabbtst
indtani. A polimerizci sorn, mikor az enzim a szondhoz elrt, annak 53 exonuklez aktivitsa
elbontotta azt s ksbb az oldatban megjelen izotpjelet mrni lehetett. Napjainkban mr olyan szondkat
alkalmaznak, amelyek az izotp hasznlatval szemben jval biztonsgosabbak. A Taqman nven ismert
mdszernl a szonda oligonukleotid vgein klnbz fluoreszcens csoportokat tartalmaznak, egy riporter
s kiolt (quencher) fluorofrt, amelyek a fluoreszcens rezonancia-energiatranszfer (FRET) jelensget
76
kihasznlva biztostjk a detektls lehetsgt. A quencher molekula a riporter csoporthoz kzel kioltja
annak emisszijt, ha azonban a DNS-polimerz elbontja a szondt, a kt fluoreszcens molekula az oldatban
tvol kerl egymstl, s gy mr kpesek vagyunk a riporter molekuln keresztl detektlni a mennyisgi
nvekedst (a fluoreszcencia jel nvekedse s az jonnan szintetizld DNS mennyisge egyenes
arnyos). A gyakorlatban a Taqman mdszer sorn hasznlhatunk kt szondt is, amelyek letapadsi helye
egymshoz kzel kell hogy legyen. Ebben az esetben az egyik a kioltt, mg a msik oligonukleotid prba
pedig a riporter fluorofrt tartalmazza s a polimerz 53 exonuklez aktivitsa biztostja a mrt jel
nvekedst.
A Taqman mdszer egy alternatvja a Molecular Beacon mdszer, ahol a szonda egy hajtkanyar
msodlagos szerkezetet tartalmaz, s ennek kvetkeztben kerl egymshoz kzel a kiolt s riporter
fluoreszcens csoport. A DNS polimerizcit kveten a szonda kpes ktdni az jonnan szintetizldott
szlra, gy ez a msodlagos szerkezet kinylik, a kt fluorofr tvol kerl egymstl s a riporter emisszijt
kvetni tudjuk.
A vals idej PCR megvalstsnak hrom lehetsges mdjt a 6.3. bra mutatja be.
6.3. bra: Vals idej PCR mdszerek. A klnbz panelek (A: TaqMan, B s C: Molecular Beacon) az eltr
mdszereket brzoljk sematikusan. Az R-rel jellt molekula a fluoreszcens riporter, a Q az elnyom fluoreszcens
molekula, R1 s R2 eltr fluoreszcens festkek.
77
6.4. A PCR az alapkutatsban
6.4.1. A PCR termk (amplikon) klnozsa s klnozs PCR-rel
A mindennapi gntechnolgiai gyakorlatban a PCR termket, az amplikont sokszor hagyomnyos
klnozssal rekombinns DNS-s alaktjuk. Megjegyzend, hogy az amplikon szigoran vve nem
molekulris kln, mivel nem felttlenl egyfle szekvencit tartalmaz (emlkezznk, hogy a hibajavt
aktivitssal nem rendelkez PCR enzimek tbb hibt vtenek, s a PCR sorn, lvn in vitro mdszer,
hinyoznak a sejtek nagy replikcis hsgt biztost tovbbi hibajavt mechanizmusok is).
Az amplikont taln legtbbszr a rekombinns fehrjegyrtshoz szksges konstrukci elksztshez
hasznljuk fel (azaz a PCR segtsgvel klnozunk, ld. 6.4. bra). Ahhoz, hogy valamely prokarita vagy
eukarita expresszis rendszerben fehrjt tudjunk ellltani, az adott fehrjt kdol DNS szakaszt egy
expresszis vektorban kell bejuttatnunk a gazdasejtbe. PCR segtsgvel az amplifikci utn kt egyszer
lpssel el tudjuk lltani a megfelel konstrukcit. Elszr a kvnt DNS szakasz felerstse sorn a
primerekbe mr a tervezs sorn restrikcis endonuklez helyeket ptnk be, amelyek megfelelnek az
adott vektor klnoz helyeinek. Ezutn hastjuk a megfelel enzimekkel az amplikont, s mris jhet a ligls
a megfelel mdon elksztett expresszis vektorba (ld. 4.2. fejezet).
6.4. bra: PCR termk klnozsnak els lpsei a primerekbe beptett restrikcis helyek (zld s srga) segtsgvel
6.4.2. Szekvenls PCR kszlkben
A Sanger ltal 1977-ben kidolgozott lnctermincis DNS szekvenls (ld. 5.2. fejezet) jval hatkonyabb
s gyorsabb vlt a PCR mdszerrel kombinlva. A Sanger-fle szekvenls sorn a denaturcit kveten
78
az alap PCR reakcival szemben itt csak egy primerrl indul a DNS szintetizls. Ennek megfelelen a
templt mennyisge minden ciklusban szaporodni fog (de termszetesen nem exponencilisan, mint a kt
primeres PCR reakcinl).
6.4.3. Mutagenezis
A PCR segtsgvel a fehrjemrnksg eszkztra is szmotteven bvlt. Mind az in vitro, mind az in
vivo vizsglatokhoz kpesek vagyunk olyan fehrje mutnsokat tervezni, vagy random mdon ellltani,
amelyek segtsgvel jobban megismerhetjk az egyes fehrjk szerkezeti s funkcionlis tulajdonsgait.
Ebben a fejezetben csak rviden emltjk azokat a mutagenezis mdszereket, amelyeket PCR segtsgvel
lehet elvgezni. Az in vitro mutagenezis mdszerekrl tovbbi rszletek a 11.2.3. fejezetben olvashatnak.
6.4.3.1. Random (error prone: hibt ejt) PCR mutagenezis
A random mutagenezis sorn vletlenszeren okozunk mutcit a DNS szlban. Ezt tbb mdon is
elrhetjk. Pldul ha UV-fnnyel vilgtjuk meg, vagy mutagn szert alkalmazzunk a PCR sorn. A
random mutcik gy is bekvetkeznek a DNS sokszorosts sorn, ha a PCR reakcit sszelltva nem
optimlis krlmnyeket biztostunk a Taq-polimerz szmra (error prone PCR). Plda erre, ha
egyenltlen dNTP arnyt hasznlunk, vagy Mg
2+
helyett Mn
2+
-t tesznk a reakcipufferbe. A mdszert
rszletesebben a 11.1.2. fejezetben mutatjuk be.
6.4.3.2. Helyspecifikus mutagenezis PCR-rel
A helyspecifikus vagy ms nven irnytott mutagenezis sorn a DNS szlon bell jl meghatrozott helyre
tudunk tervezni mutcit. Az n. megaprimer PCR s az overlapping PCR mdszerek rszleteit a 11.2.3.
fejezetben ismertetjk.
6.4.4. Reverz transzkripcis (RT-) PCR
A reverz transzkripcis (RT-) PCR mdszer alapja, hogy a reakciban lv reverz transzkriptz enzim kpes
az RNS templtrl DNS-t szintetizlni. Ebbl addan ezzel a mdszerrel tudunk mRNS molekulkat
sokszorozni. Az orvosi diagnosztikban az RT-PCR s a vals-idej PCR kombinlsa idelis pldul az
RNS alap vrusfertzsek vagy rkos sejtmarkerek azonostsra. Az RT-PCR alkalmazsval lehetsg
van arra is, hogy kvantitatv mdon hatrozzunk meg transzkripcis szinteket, valamint a mdszer
segtsgvel kpesek vagyunk sejt- vagy szvetspecifikus cDNS knyvtrakat ltrehozni. Amennyiben egy
adott gn expresszis szintjt akarjuk meghatrozni, az mRNS-re specifikus 3- s a komplementer szlra
specifikus 5-oligonukleotidot kell terveznnk. Ha cDNS knyvtr ksztse a cl, akkor az rett, teht
intronokat nem tartalmaz RNS-ek trst kell biztostani. Ehhez a reakcihoz olyan oligo-dT primert
adunk, ami az rett mRNS 3' vgn tallhat poli-A farkval komplementer s gy biztostja annak egy szl
DNS-s val trst.
Az RT-PCR sorn az els ciklusban a reverz transzkriptz enzim csak az RNS-szlra specifikus primert
tudja meghosszabbtani, de a msodik ciklus sorn mr a komplementer DNS lnc is templtt vlik, s
mindkt primerrel beindulhat a lncreakci (ld. 6.5. bra). A problma az, hogy ennek az enzimnek nincs
knnyen hozzfrhet, termofil llnybl szrmaz vltozata, ezrt a reakcihoz egy hstabil DNS-
polimerzra is szksgnk van, amely a msodik ciklustl kezdheti meg a mkdst. A RT-PCR sorn
figyelembe kell venni azt a molekulris sajtsgot, hogy a reverz transzkriptz enzim dNTP ktse
gyengbb a DNS-polimerzoknl, gy magasabb koncentrciban kell a reakcihoz adni.
79
6.5. bra: A reverz transzkripcis (RT-) PCR smja.
6.4.5. Tovbbi PCR mdszerek (random, fzis, multiplex, fszkes s
inverz)
A PCR alkalmazsainak mg szmos vltozata ismert, amelyekbl itt nhnyat ismertetnk.
Az n. random PCR (ms nven RAPD: random amplification of polymorphic DNA) sorn olyan DNS
fragmentumok amplifiklsa is megoldhat, amelyekre nem tudunk specifikus primert tervezni. Ilyen
esetben klnbz, 8-12 nukleotid hosszsg, tetszleges (arbitrary) szekvencij primereket hasznlnak
(egy PCR-hez egyfle primert), s ezzel vgzik az ltalban genomilis eredet DNS sokszorostst, annak
ellenre, hogy a primerek letapadsi helyt nem ismerjk. Ennek a mdszernek az elnye, hogy kpesek
vagyunk a pontos szekvencia ismerete nlkl is polimorf DNS-ek sszehasonltst elvgezni.
A fzis PCR (angolul jumping, azaz ugrl PCR-nek is nevezik) sorn lehetsgnk nylik kt klnll
DNS fragmentumot az amplifikci sornk sszekapcsolni, vagy rszben degradldott DNS templtrl
specifikus, hosszabb DNS rgikat amplifiklni. A mdszer alkalmazsa sorn, ha a kt klnll
fragmentum tartalmaz tfed szekvencit, akkor a kt DNS szl egy-egy vgre tervezett, egy forward s
egy reverz primerrel elrhetjk, hogy a keletkez DNS szl mr mindkt darabot egyszerre magban
foglalja. Ha a fuzionltatni kvnt fragmentumok nem tartalmaznak tfed szekvencit, akkor els lpsknt
a szlakra egyenknt olyan primereket terveznk, amelyek kzl az egyik szl reverz, mg a msik szl
forward primere tartalmazza ugyanazt a szekvencit. Ezt kveten olyan amplikonokat kapunk, amelyek
mr rendelkeznek azonos, tfed rgikkal s ezek utn mr a fent lertaknak megfelelen tudjuk egyesteni
a kt DNS darabot. Ennek a mdszernek a segtsgvel az smaradvnyokbl szrmaz fragmentlt
genomilis DNS-t kpesek vagyunk (legalbbis egy bizonyos hatrig) jra egy molekulv alaktani,
valamint a fzis PCR alkalmazsval klnbz gnek egyestsvel egy lpsben tudunk kimra
fehrjket kdol konstrukcikat (ld. 12.2.3. fejezet) ellltani (ld. 6.6. bra).
80
6.6. bra: A fzis PCR sematikus brzolsa. Az els esetben (A) a kt fuzionltatni kvnt DNS szl tartalmaz
tfed rgit. A msodik esetben (B) az els krben PCR-rel ltre hozzuk tfed szakaszokat, amit a reakci sorn
egy-egy primer biztost (narancs), majd ezt kveten egy jabb PCR sorn mr a kvnt termket kapjuk.
A multiplex PCR mdszer lnyege, hogy a reakcihoz tbb klnbz primer prt is adunk, gy tbb
amplikont kapunk egy amplifikls sorn. A tbb primer pr alkalmazsa miatt az egyes amplikonok
mennyisge arnyosan kevesebb lesz, mintha kt specifikus primert alkalmaznnk. A multiplex PCR tovbbi
technikai nehzsge, hogy el kell kerlni a klnbz primerek egymssal kialaktott klcsnhatst, mert
azok gtoljk a reakci megfelel vgbemenetelt. Fontos a detektls szempontjbl, hogy az
amplikonokat klnbz mretre tervezzk. A mdszert tbbek kztt patognek azonostsra, DNS-
profil ksztsre (ld. 6.5.2. fejezet) s nagy teljestmny genotipizlsra alkalmazzk.
A nested (fszkes) PCR segtsgvel a nem kvnatos termkek (mispriming) megjelenst kszblhetjk
ki, amely abbl eredhet, hogy az egyik alkalmazott primer aspecifikusan (is) kt a clszekvencihoz. A
mdszer sorn kt, egymst kvet PCR-t alkalmaznak, mely sorn a msodik primer pr az els pron bell
anelll az els termkhez, ezzel nagyban nvelve a vgs termk specificitst. (ld. 6.7. bra)
6.7. bra: A "nested" PCR sematikus brzols. Az els PCR sorn a nem kvnatos termket, valamint a
clszekvencit tartalmaz szakaszt erstjk fel. A msodik krben a kt termk kzl a cl szekvencit tartalmaz
termket hasznljuk a tovbbiakban templtknt.
81
Az inverz PCR olyan esetekben alkalmazhat, amikor egy ismert DNS rgi krnyezetben lv ismeretlen
szekvencit szeretnk feltrkpezni (ld. 6.8. bra).
6.8. bra: Az inverz PCR smja
A mdszer lnyegi lpse, hogy az ismert szekvencitl nagy tvolsgra valamely restrikcis
endonuklezzal hastjuk a DNS szlat, majd a mintt hgtjuk, s DNS-ligzzal a DNS fragmentumokat
cirkulrizljuk. Ezt kveten a cirkulris DNS-t az ismert szekvencia rgin bell hastjuk egy msik
endonuklezzal, gy olyan lineris termket kapunk, amelynek kt vgt pontosan ismerjk. Erre a templtra
mr kpesek vagyunk PCR-t alkalmazni az ismert rginak megfelel primerek segtsgvel. A mdszer
gyakorlati szempontbl fkpp mobilis DNS elemek (retrovrusok, transzpozonok) genomba val
bekeldsnek pontos helynek meghatrozsra alkalmazhat.
6.5. PCR az alkalmazott kutatsban
Napjainkra a PCR-rel szmos alkalmazott tudomnygban rtek el tt sikereket. Az orvosi
diagnosztikban, az igazsggyi orvostanban ma mr alapmdszerr vlt, de rdekes mdon a rgszet, st
az slnytan is alkalmazza (amennyiben a krdses mintban DNS-t vagy legalbbis nukleinsav tredket
lehet detektlni). Ezen kvl hasznljk a mezgazdasgban, az lelmiszeriparban is. A kvetkezkben
rviden ttekintjk a PCR szerept az alkalmazott tudomnyokban.
6.5.1. Orvosi diagnosztika
Az orvosi diagnosztikban egyes betegsgek kimutatsa a diagnosztikhoz hasznlt mdszer
rzkenysgtl fgg. Minl rzkenyebb az eljrs, annl hamarabb meg lehet kezdeni a szksges
beavatkozst, valamint jobban elkerlhetek a hibs negatv eredmnyek (igaz, hogy a fals pozitv esetek
82
szma nvekedhet). Vrusfertzseknl, mint pldul a HIV, a vrusos hepatitisz, klnsen fontos a PCR-
rel trtn rzkeny diagnosztika hasznlata. Tumorok vizsglatra a vals-idej kvantitatv reverz
transzkripcis PCR a megfelel eszkz. A rkos sejtek vagy a vrusfertzsek transzkriptumaik alapjn
kimutathatak.
Az onkolgiai diagnosztikban a gntrendezdsek kvetkeztben megjelen fzis mRNS termkek
kimutatsra is hasznlnak PCR-t. Akut mieloid leukmira utal pldul az AML1ETO fzis
transzkriptum megjelense. A gygyult betegeknl klnsen fontos kimutatni a minimlis rezidulis
betegsget (MRD), a kis mennyisg visszaesshez vezet maradk rosszindulat sejtet. PCR-rel az AML1
ETO fzis transzkriptum mennyisge pontosan megbecslhet. Az MRD megllaptsa alapulhat mg
klonlis tumor markereken, kromoszomlis transzlokcis markereken s egyb, jonnan ltrejtt fzis
transzkriptumokon. A vals-idej PCR technikk hasznlatval a felsorolt markereket vizsglva letbevg
elrejelzsek szlethetnek. A telomerz aktivits a tumorok 85%-ban kimutathat, mg az egszsges
szvetekben ltalban jval alacsonyabb mrtkben vagy egyltaln nem fordul el, gy tbb rkos
megbetegedsnl is gretes diagnosztikai marker lehet a PCR-rel trtn kimutatsuk. Hasnylmirigyrk
vizsglatnl a hasnylmirigy nedvben mrve is sikerlt valsidej idej PCR-rel a telomerz hTERT
alegysg mRNS-nek szintjt mrni. A kutatsban a kimutatott hTERT mRNS szintje korrellt a
hasnylmirigyrk megjelensvel. Sok ms pldt is fel lehetne mg sorolni a PCR tumordiganosztikai
alkalmazsrl.
6.5.2. Igazsggyi orvostan (DNS ujjlenyomat)
Az igazsggyi orvostanban (forensic science) komoly fejldst eredmnyezett a DNS profilok megjelense.
A humn genomban tbb tzezer rvid, tandem ismtld (STR: Short Tandem Repeat)) szekvencia
tallhat, amelyek szemlyenknt eltrek. Napjainkban a DNS ujjlenyomat ksztsre fkpp az STR
szekvencikat vizsgljk PCR segtsgvel. Az eljrs sorn multiplex, azaz egyszerre tbb, lkusz-
specifikus primer prt hasznlva amplifikljk az STR szekvencikat, s az gy kapott, (ltalban kapillris)
elektroforzissel kimutathat, eltr hosszsg fragmentumok kpezik az azonosts trgyt. Az USA-ban
s Eurpban bizonyos eltrsek vannak a vizsglt STR lkuszok hasznlatban. Az azonos DNS
ujjlenyomatok elkerlsnek rdekben a 90-es vekben hasznlt STR lkuszok szmhoz kpest mra
jval tbbet, akr 16 STR lkuszt is amplifiklnak egyszerre. A DNS ujjlenyomat hasznlatval apasgi
tesztet is vgezhetnk, amennyiben a gyerek apjnak szemlye krdses. Rokonsgi viszonyok feltrsa is
lehetsges PCR analzis (DNS profil) segtsgvel. Hogy csak egy pldt emltsnk: nhny vvel ezeltt
ezzel a mdszerrel azonostottk a Jekatyerinburgban 1918-ben lemszrolt Romanov orosz cri csald fldi
maradvnyait.
6.5.3. s-PCR
Az sidk kutatinak is nagy segtsget nyjt a PCR mdszer. Egyrszt a paleontolgiai vizsglatoknl az
smaradvnyokbl kinyert DNS felsokszorostsval s tovbbi mdszerek alkalmazsval pontosabb
informcikat nyerhetnk az adott llny taxonmiai azonostshoz, s ezzel evolcis lptkben is
tisztbb kpet kaphatunk az adott strtneti kor bioszfrjrl. p DNS-t nyilvnvalan nem lehet egy
smaradvnybl remlni, de pl. a fzis PCR segtsgvel kisebb darab DNS-eket is lehet amplifiklni, a
bennk trolt informcit szekvenlssal kinyerni, majd evolcis kvetkeztetseket levonni. A PCR
legnagyobb hrverst kapott slnytani alkalmazsnak a dinoszauruszok korbl szrmaz DNS minta
(borostynkbe zrt rovarbl) PCR sokszorostsa s szekvenlsa tnt, de ksbb kiderlt, hogy a minta
ksbbi korok DNS-vel volt szennyezve. Viszont vals eredmnyeket kaptak tbb ezer ves mintkbl. Az
eddigi legrdekesebb eredmny a legalbb 50 ezer ve kipusztult neandervlgyi sember gyakorlatilag
teljes genomjnak feltrsa volt (ld. 9.4. fejezet), annak ellenre, hogy tredezett DNS-t lehetett csak a
csontmaradvnyokbl kivonni.
83
Az archeolgiai kutatsok esetn a PCR-t tbb szempontbl is hasznlhatjuk. Az egyik f irny az emberi
populcik, npcsoportok csontmaradvnyaibl szrmaz DNS analzise, msrszt a rgszeti lelhelyeken
tallt tovbbi biolgiai eredet mintk (hzillatok, termesztett nvnyek, telmaradvnyok, szerves eredet
trgyak) PCR sokszorostsa, szekvenlsa s azonostsa. Msrszt azt a biolgia sajtsgot hasznlhatjuk
ki, hogy a megtermkenyts utn a fejld embri mindig az anyai mitokondriumot rkli. A
mitokondriumban tallhat DNS alapjn pedig kpesek vagyunk az egyes npcsoportok fldrajzi
elhelyezkedst s ennek vltozsait nyomon kvetni, valamint a npcsoportok kztt tallhat rokonsgi
kapcsolatokat is felderthetjk ezzel a mdszerrel. Pldul archeo-PCR vizsglatsorozattal igyekeznek
genetikusok s archeolgusok egyttmkdsben feltrni a honfoglals kori magyarsg genetikai eredett.
A honfoglals idszakbl szrmaz csontmaradvnyokbl vonnak ki DNS-t s ebben az esetben az apai
rklds Y kromoszmra jellemz marker rgikat amplifiklnak (a tredezettsg miatt a mintkat
elszr random PCR-nek vetik al) multiplex PCR-rel.
6.6. Tovbbi olvasnival a fejezethez
Erlich HA, Arnheim N. (1992) Genetic analysis using the polymerase chain reaction. Annu Rev Genet.
26:479-506
Hofreiter M, Serre D, Poinar HN, Kuch M, Pbo S. (2001) Ancient DNA. Nat Rev Genet. 2(5):353-9.
Valasek MA, Repa JJ. (2005) The power of real-time PCR. Adv Physiol Educ. 29(3):151-9.
Saunders, NA and Lee, MA, editors (2013) Real-Time PCR: Advanced Technologies and Applications.
Caister Academic Press. ISBN: 978-1-908230-22-5
84
7. Vektor-gazda rendszerek
Korbban bemutattuk, hogy rekombinns DNS ellltshoz szksgnk van egy hordoz DNS vzra, a
vektorra, amibe in vitro a molekulris klnozs trgyt, az inszert DNS-t bepthetjk (0. s 4.2. fejezetek).
A klnozs in vivo rszhez a rekombinns DNS-t megfelel gazdaszervezetbe kell juttatnunk (gnbevitel,
ld. 4.3. fejezet). Ebben a fejezetben a vektorok tpusait ismertetjk. A vektor legfbb tulajdonsga, hogy
kpes nll szaporodsra valamilyen gazdaszervezetben, azaz egy replikon. A replikcihoz szksg van
egy replikcis origra s az azt krlvev szablyoz szekvencikra. A replikon milyensge dnti el, hogy
az adott vektor milyen gazdasejtben kpes szaporodni. Vektorokat eredetk szerint plazmidokbl,
bakteriofgokbl, vrusokbl, transzpozonokbl s kromoszmkbl (bakterilis, leszt, st humn
kromoszmk) lehet ellltani, gntechnolgiai ton. A plazmidok s a fgok hasznos tulajdonsgainak
tvzsbl szlettek meg a kevert tpus kozmid s fgmid vektorok.
A gazdasejteket tekintve a mindennapi gntechnolgiai gyakorlatban a Gram-negatv E. coli legelterjedtebb
gazdaszervezet. Klnozni gyakorlatilag csak kli sejtekben szoktunk. Egyes alkalmazsokhoz (pl. fehrjk
tltermeltetsre) kutatsi s ipari clra ms baktrium fajokat is hasznlnak, mint pl. a Gram-pozitv
Bacillus subtilis, de ebben a jegyzetben csak E. coli gazdatrzsekkel foglalkozunk. A bakterilis rendszer
elnye, hogy sokfle vektor tpushoz hasznlhat, egyszer s relatve olcs a laboratriumi fenntartsa,
gyorsan szaporodik (optimlis krlmnyek kztt 20 perc alatt osztdik), s mivel az emberi vastagbl
bioflrjnak tagja, ezrt nem allergn. Ugyan lteznek patogn E. coli trzsek is (pl. az O104:H4), a
gntechnolgiai gyakorlatban elssorban hasznlt K-12-es trzs s tbb szz genetikai varinsa igen
biztonsgosnak tekinthetk, az emberi blcsatornban nem kpesek szaporodni. A gntechnolgiban
hasznlatos legfontosabb E. coli K-12 altrzseket, genotpusukat s jelentsgket, valamint a fontosabb
genetikai markereket a 7.1. tblzatban s 7.2. tblzatban foglaljuk ssze (nem mindegyik fenotpussal
foglalkozunk a jegyzetben, ezekrl mikrobiolgiai kziknyvekben, illetve ezen a weblapon tallhat
tovbbi informci). A K-12 trzs mellett a B trzs nhny varinst is hasznljuk a gntechnolgiban, pl.
a fehrjeexpresszihoz a BL21-et s szrnazkait. Ezekrl rszletesebben a 12.2.2.2. fejezet olvashatnak.
Az eukarita gazdasejtek kzl a laboratriumi tenysztst tekintve az leszt ll legkzelebb az E. coli
sejtekhez. Klnbz gntechnolgiai clokra hasznlunk mg rovarsejteket, nvnyi s llati sejteket is,
amelyekkel a jegyzet ksbbi fejezeteiben foglalkozunk. Fontos megjegyezni, hogy az eukarita gazdasejtek
esetben gyakorlatilag minden esetben n. shuttle (ingz) vektorokat hasznlunk, amelyek ktfle
gazdban is szaporodni tudnak (binris = ketts replikonnal rendelkeznek). Ennek az az oka, hogy mint azt
mr emltettk, a molekulris klnozs, a rekombinns DNS elksztse minden esetben E. coli gazdban
trtnik, s a mr felszaportott konstrukcit juttatjuk be az eukarita gazdba.
7.1. tblzat: E. coli K-12 altrzsek
85
7.2. tblzat: Nhny fontos E. coli genetikai marker
7.1. A vektorok ltalnos jellemzi
A vektorok az egyes gazda szervezetek DNS informcijnak mdostshoz hasznlt ltalnos
gntechnolgiai eszkzk, a klnozand DNS (az inszert) hordozmolekuli.
Milyen tulajdonsgokkal kell rendelkezni egy DNS molekulnak, hogy vektor cljra hasznlhassuk?
nll replikcira kell kpesnek lennie. Kicsi mretnek kell lennie, mivel akkor knny dolgozni vele a
laboratriumban; az idelis mret 2-5 kbp (1,4-3,5 MDa). Egyedi restrikcis helyekkel kell rendelkeznie, s
vgl kell tartalmazni legalbb egy szelekcis marker gnt.
7.1.1. Klnoz s expresszis vektorok
86
A vektorokat felhasznlsuk alapjn kt nagy csoportra oszthatjuk. Az els csoportba a klnoz vektorok
tartoznak, melyeket specifikus DNS informci trolsra, sokszorostsra hasznlhatunk fel. Ezek a
vektorok a gazdaszervezetre jellemz replikonnal kell, hogy rendelkezzenek A j vektorok
alapkvetelmnye, hogy az organizmus DNS llomnynak replikcijtl fggetlenl kpesek
sokszorozdni, ebbl kifolylag tbb kpiban is elfordulhatnak. Minden vektornak, amelybe
mestersgen kvnunk idegen DNS informcit pteni, rendelkeznie kell klnoz hellyel. A legtbbszr
ezek n. multiklnoz (poliklnoz) helyek (MCS: Multiple Cloning Site), amelyek a vektorban csak
egyszer elfordul, egyms mellett elhelyezked klnbz restrikcis endonuklez felismer helyek.
Szelekcis marker gnknt a legtbb vektorban antibiotikum rezisztencia gnt hasznlnak.
A msodik nagy csoportba az expresszis vektorok tartoznak. Ezek a DNS konstrukcik olyan szablyz
elemeket tartalmaznak, amelyek lehetv teszik, hogy a bennk trolt DNS informci (az inszert) kpes
legyen fehrjeknt kifejezdni, expresszldni. Az expresszis vektoroknak tartalmazniuk kell a klnoz
hely eltt egy promter rgit, ami lehetv teszi a transzkripcit s ami leginkbb meghatrozza az
expresszland fehrje mennyisgt. A promter mkdsnek szablyozhatsga kulcsfontossg a
gyakorlatban ennek segtsgvel elkerlhetjk az id eltti fehrje expresszit, illetve azt
kvnalmainknak megfelelen indthatjuk el. Az egyik legismertebb s leginkbb alkalmazott szablyz
mechanizmus az E. coli lac operon elemeire pl, amelynek lnyege rviden, hogy a gnexpresszi csak
allolaktz jelenltben indul be. A gyakorlatban az allolaktzt metabolikusan nem bonthat analg
molekulval, izopropil -D-tiogalaktoziddal (IPTG-vel) helyettestjk.
7.1.2. Antibiotikum rezisztencia gnek
A plazmidok felfedezsekor hamar fny derlt arra, hogy ezek az extrakromoszomlis elemek gyakran
tartalmaznak antibiotikum-rezisztencia gneket, amelyek horizontlis gntranszferrel nem csak a fajon bell,
de klnbz fajok kztt is vndorolhatnak. A gyakorlatban az antibiotikum-rezisztencia gneket
szelekcis marker gnekknt hasznljuk. Ha a vektor rendelkezik valamely antibiotikum-rezisztencia
gnnel, az adott antibiotikumot tartalmaz tptalajon csak azok az egyedek lesznek letkpesek, amelyekbe
bekerlt a vektor DNS (azonban az antibiotikum az res s az inszertet tartalmaz vektor kztt nem
szelektl, arra pldul a kk-fehr szelekci alkalmas (ld. 7.2.3.1).
Az egyik legelterjedtebb antibiotikum az ampicillin, ami az elsknt felfedezett penicillin flszintetikus
vltozata (ld. 7.1. bra). Az ampicillin, eldjhez hasonlan, bta-laktm antibiotikum, amely ktdik s
n. ngyilkos szubsztrtknt gtolja a sejtfal peptidoglikn szintzisben szerepet jtsz transzpeptidz
enzimet, s ezltal gtolja a baktrium nvekedst. Szerkezeti sajtsga, hogy egy aminocsoport
kapcsoldik a penicillin alapstruktrjhoz (aminopenicillin), gy nhny Gram-negatv baktrium
fehrjeburokkal vdett membrnjn is t tud hatolni, ezzel szlesebb baktriuml spektrummal rendelkezik.
Egy msik penicillin vltozat a karbenicillin (karboxipenicillin), ami a fent lert ampicillinhez kpest a
Gram-negatv baktriumok fel szlesebb hatsspektrummal br. Annak ellenre, hogy a karboxipenicillinek
a bta-laktamz enzimekkel szemben kevsb ellenllak, a knnyen degradld ampicillinhez kpest jval
stabilabbak. Mindkt gtlszer elleni rezisztencit a mr fent emltett bta-laktamz enzim biztostja,
amely kpes elhastani a bta-laktm-gyrt, ezltal hatstalantja a molekult.
7.1. bra: Az ampicillin szerkezete
87
A kloramfenikol antibiotikumot 1949-ben lltottk el elszr. Alkalmazsa igen elterjedt, mert gyrtsa
olcs s nagyon hatkony baktrium-nvekedst gtl szer, hatsspektruma szles. Bakteriosztatikus
kpessgnek molekulris httere, hogy a transzlci sorn a riboszma komplex 50S alegysghez kt, gy
gtolja a fehrjeszintzist. A laboratriumi gyakorlatban hasznlt kloramfenikol rezisztencia gn egy
kloramfenikol-acetiltranszferz enzimet kdol, amely gy kpes inaktivlni az antibiotikumot, hogy arra
kt darab acetil-csoportot kt, gy a szer mr nem kpes kifejteni a hatst.
Egy msik fehrjeszintzis gtl antibiotikum a tetraciklin, amelyet a Streptomyces baktriumok termelnek
s egy szles spektrum poliketid tpus termszetes antibiotikum. A kloramfenikollal ellenttben az
aminoacil-tRNS mRNS-riboszma komplexhez val ktdst gtolja a 30S alegysghez ktdve. A
tetraciklin rezisztencit egy 40 kDa-os membrnfehrje biztostja, amely aktv mdon kipumplja az
antibiotikumot a sejtbl.
A kanamicin nev antibiotikumot a Streptomyces kanamyceticus baktrium termeli, s a tetraciklinhez
hasonlan a prokarita riboszma 30S alegysghez kt, s ott transzlcis hibt indukl, amellyel gtolja a
fehrjk trdst. A kanamicinnel kzeli rokon molekula a neomicin. Mindkt antibiotikum
aminoglikozid tpus szer, tovbb mindkett hatkonyan gtolja fkpp a Gram-negatv, kisebb rszben a
Gram-pozitv baktriumok nvekedst. Inaktivlsukat egy acetil-transzferz enzim vgzi, amely egy
vektorban kdolva biztostja a rezisztencit.
A sztreptomicin nev antibakterilis szert, ahogyan nevbl is kiderl, a Streptomyces griseus nev
baktrium bioszintzisnek termszetes termkeknt fedeztk fel 1943-ban. Gygyszati felhasznlsban a
tuberkulzis kezelsben vlt igen npszerv. A kanamicinhez s neomicinhez hasonlan ez az
antibiotikum is az aminoglikozidok kz tartozik, s a fehrjeszintzist gtolja. Hatst a 30S riboszma
alegysg 16S rRNS-hez ktve fejti ki. Ennek kvetkeztben kodon elcsszs alakul ki, ami vgs soron a
baktrium hallhoz vezet. A rezisztencia gnje sztreptomicin-6-foszfotranszferz enzimet kdol, ami az
antibiotikumot foszforillva gtolja annak mkdst.
Az utolsknt bemutatott antibakterilis molekula a zeocin, amely egy glikopeptid, s mikrba l
kpessge abban rejlik, hogy a kettsszl DNS-be interkalldva, kettsszl-trst okoz. Ezen
tulajdonsgnak ksznheten szles spektrum antibiotikum. A sejten kvl a zeocin rz-ionnal komplexet
kpezve inaktv formban van, mg a sejten bell a redukl krnyezetben a rz-ion levlik a glikopeptidrl
s gy aktvv vlik. A zeocin-rezisztencia gn egy Streptoalloteichus hindustanus nev organizmusbl
szrmaz 14 kDa molekulatmeg fehrjt kdol, ami megkti az antibiotikumot, s gy az nem kpes a
DNS-t hastani.
7.2. Plazmid vektorok
7.2.1. A plazmidok ltalnos jellemzi
Az els plazmidot az 1940-es vek elejn azonostottk egy Shigella baktrium fajbl. A plazmidok rvid,
nhny kbp s 200 kbp kztti mret, extrakromoszomlis, ketts szl cirkulris DNS molekulk,
amelyek az organizmus kromoszmjtl fggetlenl kpesek replikldni (azaz replikonok).
Replikcijukat a baktrium kromoszmjnak replikcijhoz szksges enzimek egy rsze vgzi (DNS-
polimerz I, DNS-polimerz III, stb.). A replikci kezdpontjt itt is a replikcis orig jelli ki. Az orig
krnykn tallhat szekvencik szablyozzk a kpiaszmot. A legtbb plazmid a kromoszomlis DNS-ek
ltalnos bidirekcionlis replikcis mechanizmustl eltren unidirekcionlisan msoldik (azaz az
origtl csak egy replikcis villa indul el). A ma hasznlatos plazmid vektorok replikcija fggetlen a
sejtosztdstl, n. relaxlt kontroll alatt ll. Ilyen pldul a pMB1 plazmidban tallhat replikon. (Ezt a
plazmidot elszr egy klinikai mintbl izolltk 1974-ben). Az eredeti szekvencij pMB1 replikont
tartalmaz vektorok kpiaszma sejtenknt 15-20. Az E. coli plazmidok kztt tbb klnbz replikon
szekvencit is talltak (ColE1, p15A, pSC101). Kt klnbz szekvencij, klnbz tpus replikont
88
tartalmaz plazmid egyms mellett stabilan fenntarthat ugyanabban a sejtben. Az azonos replikcis
origt hordoz plazmidok azonban egymssal inkompatibilisek, ezekbl csak egyfle fordulhat el egy
sejtben (kivve, ha kt klnbz antibiotikummal ketts szelekcit alkalmazunk a kt azonos replikonnal
rendelkez plazmid esetn).
Minthogy a plazmidok replikcija nem fgg fehrjk expresszijtl (a szksges enzimek hossz
letidejek a sejtben), a gazdasejt fehrjeszintzisnek kloramfenikollal val gtlsval el lehet azt rni,
hogy a sejt nem lesz kpes a kromoszomlis DNS-t repliklni, de a plazmid szintzise tovbb folyik. Ezzel
az eljrssal, melyet amplifiklsnak neveznk, tovbb nvelhet egy plazmid kpiaszma.
A plazmidokat funkcionlis szempontbl tbb csoportba oszthatjuk. Az elsbe az n. konjugatv plazmidok
tartoznak, mint pl. az E. coli F-faktora (fertilitsi-faktor), amelyek a baktriumok kztti ivaros
szaporodst, a konjugcit biztost episzmk (kromoszmn kvli genetikai elemek). A konjugci sorn
a kt baktrium az F-faktor-kdolta pilin oligomer fehrjbl ll piluson keresztl kapcsoldik ssze. A
plazmidok nagy msik csoportjba tartoznak a mr emltett rezisztencia gneket hordoz plazmidok,
amelyek szintn kpesek horizontlis gntranszferrel ms egyedekbe tjutni s biztostani az adott
antibiotikummal szemben ellenllsgot. A harmadik plazmid csoport az E. coli baktriumra jellemz,
ltaluk termelt s ms E. coli vonalakra (s ms baktriumokra) hat toxinokat kdol.
Ebben a fejezetben nhny klasszikus plazmid-alap vektort s vektorcsaldot fogunk bemutatni, tovbbi
plazmid vektorokrl a ksbbi fejezetekben lesz sz.
7.2.2. A pBR322 vektor
Az els szles krben ismertt vlt E. coli kompatibilis klnoz vektort 1977-ben lltottk el a Kaliforniai
Egyetemen, amelyet pBR322 nvre kereszteltek el (BR a feltall Bolivar Rodriguez monogramja). Ez a
vektor 4361 bzisprbl ll, megtallhat benne egy ampicillin s egy tetraciklin rezisztencia gn, valamint
egy termszetes E. coli plazmidbl, a pMB1-bl szrmaz replikcis orig. A plazmidon bell 40 egyedi
restrikcis hasthely tallhat, amelyekbe inszertet lehet bepteni. 11 klnoz hely a tetraciklin
rezisztencit, mg 6 darab az ampicillin rezisztencit kdol rgiban tallhat, gy az inszert beplsre az
adott rezisztencia gn funkcivesztse mellett lehet szelektlni. (Ebben a vektorban mg nem volt
multiklnoz hely) (ld. 7.2. bra).
7.2. bra: A pBR322 vektor trkpe. A replikcis orign kvl (ori) lthat a kt antibiotikum rezisztencia gn
(AmpR s TcR), valamint a bennk tallhat 6, illetve 11 restrikcis endonuklez felismer hely.
89
7.2.3. A pUC vektorcsald
A pUC klnoz vektorcsald is a Kaliforniai Egyetemen ltott napvilgot (az UC rvidts a University of
California nvbl ered). Sikert egy igen tletes tulajdonsgnak ksznheti, ami jcskn leegyszerstette a
klnozs sikert bizonyt msodlagos szelekcit (az elsdleges szelekci az antibiotikum rezisztencia,
viszont annak eldntsre, hogy res vektor vagy rekombinns DNS kerlt a gazdasejtbe, szksgnk lehet
egy msodlagos szelekcira is).
7.3. bra: A pUC18 vektor trkpe. A replikcis orig (ori) mellett ampicillin rezisztencia gnt (AmpR), a kk-
fehr szelekcit biztost -galaktozidz (LacZ) -fragmentumt kdol gnt s az utbbin bell egy multiklnoz
helyet (MCS) tartalmaz.
7.4. bra: A pUC vektor csald kt tagjnak (pUC18 s pUC19) multiklnoz helyei, amelyek egymshoz kpest
reverz irnyban helyezkednek el
A pUC vektor egy 2686 bp mret plazmid, ami a pMB1 replikcis orign kvl tartalmaz mg egy
ampicillin rezisztencia gnt, valamint a -galaktozidz (lacZ) enzimet kdol gn egy darabjt (lacZ).
Ennek a gnnek ksznhet a msodlagos, n. kk-fehr szelekci (ld. lentebb). Tovbbi elnye, hogy a
pMB1 replikon szekvencijnak mdostsval a kpiaszm 500-700-ra nvekedett. A vektorcsaldon bell
a pUC18 s a pUC19 abban klnbznek, hogy a multiklnoz helyk (MCS) egymshoz kpest reverz
mdon helyezkedik el (ld. 7.3. bra s 7.4. bra).
90
7.2.3.1. A kk-fehr szelekci
A kk-fehr szelekci segtsget nyjthat annak eldntsben, hogy a ltrehozni kvnt rekombinns
plazmid tartalamazza-e az inszertet. Azok a baktrium telepek, amelyekben sikeresen klnozott, inszertet
tartalmaz plazmid van, fehrek lesznek, az res vektort tartalmaz telepek viszont kkek. A
ltvnyos teszt molekulris alapja a -galaktozidz enzim mkdsben rejlik s az n. o-
komplementcin alapszik. A -galaktozidz ngy azonos alegysgbl ll fehrje, s csak ebben a
formban aktv. Az egyes alegysgek kt peptidre bonthatk szt (egy rvidebb N-terminlis LacZ o-
fragmentumra s egy nagymret LacZ e-fragmentumra), aminek kvetkeztben felbomlik a
homotetramer szerkezet, s az enzim inaktv lesz. Ha a kt peptidet jra sszekeverjk (vagyis az e-
fragmentumot kiegsztjk az o-fragmentummal, amit genetikai kifejezssel o-komplementcinak
hvunk), spontn kialakul az aktv enzimszerkezet.
A szelekci sorn az enzimnek ezt a spontn sszeszereldsi kpessgt hasznljuk ki oly mdon, hogy
az o-fragmentumot a plazmid kdolja, mg az e-fragmentumot a gazdasejt genomja. Mivel a cl az inszert
beplsnek a vizsglata, a vektorban a multiklnoz hely (MCS) az o-fragmentumot kdol
szakaszba van beptve. Vagyis sikeres klnozs esetn az o-fragmentumot kdol szakasz elromlik,
s az o-fragmentum nem tud kifejezdni. Ebben az esetben teht az IPTG-vel val indukci
eredmnyeknt az inszert ltal kdolt fehrje fog expresszldni, s a telepek fehrek lesznek. Az res
vektort tartalmaz baktriumok IPTG indukci hatsra az enzim mindkt fragmentumt szintetizljk,
ami azt eredmnyezi, hogy egy kromogn szubsztrt, az 5-brm-4-klr-3-indolil--D-galaktozid (X-gal)
jelenltben kk szn baktrium telepek keletkeznek. (ld. 7.5. bra).
7.5. bra: A kk-fehr szelekci molekulris httere. A csonkolt -galaktozidz enzim (srga) IPTG jelenltben
a gazdasejtben termeldik, de inaktv marad, mg a vektorban kdolt enzim o-fragmentum (piros) aktvv nem teszi.
Ez az o-komplementci jelensge. Az aktv enzim az X-gal szubsztrtot bontja, kk csapadk s kk sznv telepek
keletkeznek. Ha az inszerci sikeres, akkor az -fragmentum nem termeldik, a kolnia fehr szn marad.
91
7.2.4. Fgmidok
A fgmidok, mint kpzett sz fonalas (bakterio)fg s plazmid kombincijra utalt. Ebbl addan
jellemzi az elbbi kett tulajdonsgainak keverke. A fgmidok a gyakorlatban klnoz vektorknt
hasznlhatk. Egyrszrl tartalmaznak egy plazmid replikcis origt, msrszrl megtallhat bennk az
f1 fgbl szrmaz f1 orig is. Ez utbbi a fonalas (fibrzus) fgokra jellemz s biztostja azt, hogy a
fgmidrl egyszl DNS is trdjon, majd az virionba pakoldva, a ksbbi gazda organizmusba tvihet
legyen. A fg rszecskbe csomagolshoz szksg van n. segt (helper) plazmidokra is, amelyek az
egyszl DNS replikcijt biztostjk s a virionba val pakolshoz szksges gneket kdoljk. A
fgmidok, a fibrzus fgokhoz hasonlan nem ltikusak, teht kiszabadulsukkor nem esik szt a gazdasejt,
hanem a sejtet folyamatosan j vrusrszecskk kivlasztsra kszteti. A fonalas fgok, s ebbl addan a
fgmidok fertz kpessghez az is szksges, hogy a gazdasejt rendelkezzen pilussal. A fgmidok teht
kizrlag olyan gazdasejttel alkalmazhatak, amelyben megtallhat vagy F-faktor, vagy annak valamilyen
vltozata. A fgmidokat korbban szekvenlsra, valamint irnytott mutagenezishez alkalmazott
konstrukcikhoz hasznltk, mivel egyszl templtot lehet rla egyszeren ellltani (maga a rekombinns
fgmid a fg rszecskben egyszl).
Az egyik legismertebb klnoz fgmid a pBlueScript (pBS) vektor, amely a pUC vektorcsaldra nagyon
hasonlt (ld. 7.6. bra). Egyrszt tartalmaz egy plazmid s egy f1 replikcis origt. Ezen kvl ampicillin
rezisztencia gnt kdol, valamint 21 restrikcis endonuklez kompatibilis MCS-t, amely a pUC vektor
csaldra jellemz -galaktozidz -peptidet kdol rgijn bell tallhat. Utbbinak ksznheten az
inszert beplse nyomon kvethet a kk-fehr szelekci segtsgvel. Megemltend mg, hogy a
poliklnoz hely kt vgn egy-egy T7 illetve T3 fg-specifikus promter tallhat, amelyekrl az adott
promterre specifikus RNS-polimerzzal in vitro transzkripcit lehet vgezni az inszert mindkt szlrl.
7.6. bra: A pBlueScript fgmid vektor trkpe. A vektor tartalmazza, mind a plazmid (ori), mint a fonalas fgokra
jellemz f1 replikcis origt. Ezen kvl tallhat benne egy ampicillin (AmpR) rezisztencia gn, valamint a "kk-
fehr" szelekcit biztost -galaktozidz (LacZ) fragmentum kdol rgija, s ez utbbin bell egy MCS. A
klnozott gn kifejezdst T7, illetve T3 promterrel is el lehet indtani
92
7.3. Bakteriofg vektorok
A bakteriofg-alap vektorok elnye a plazmidokkal szemben, hogy fertz tulajdonsguk rvn sokkal
hatkonyabban kpesek az idegen DNS-t a gazdasejtbe bejuttatni (a gnbeviteli mdszereket rszletesen a
4.3. fejezetben trgyaljuk). A tipikus bakteriofg egy kls, fehrjbl ll kapszidbl s a benne lv
rktanyagbl ll. A genomjukat alkothatja RNS s DNS is, egy- vagy ktszl formban is. Vektor
ellltsra elssorban az ikozaderes -fgot s a filamentzus M13 fgot hasznljk.
7.3.1. -fg vektorok
A gntechnolgia alkalmazsban az egyik legelterjedtebb bakteriofg az E. coli specifikus -fg (ms nven
enterobakteriofg-). Szerkezetben tipikus fg struktrt mutat, rendelkezik fej, ms nven egy kapszid
rgival, amelyben lineris ketts szl DNS rktanyag tallhat, valamint farok rgival, amin
keresztl a DNS bejuthat a gazdasejtbe. A vrus genomja ~48500 bp-bl ll s kzel 60 gnt kdol, amelyek
biztostjk a fg szaporodshoz s becsomagolshoz szksges enzimeket, azok szablyz fehrjit,
valamint burokfehrjket. A vrus lineris genomja kpes cirkularizldni a gazdasejten bell, ezt a DNS
szlak vgn tallhat kt ragad cos rgi biztostja. Az -fg ktfle letciklust mutat. A ltikus
letciklus sorn a vrus rktanyaga miutn bejutott a gazdasejtbe, ott tbbszr replikldik, majd a fej s
farok struktrt kpz fehrjk expresszijt kveten j vrusrszecskk kpzdnek, amik a gazdasejt
elpusztulsa utn tovbbi sejteket fertznek. Ezzel ellenttben a lizogn letciklusba akkor lp a fg, amikor
az rktanyaga bepl az E. coli kromoszmjba, azzal egytt replikldik. A sejt osztdsval tovbb
rkld, ltens fgot profgnak nevezzk (ld. 7.7. bra).
7.7. bra: A -fg ltikus s lizogn letciklusa
A -fg-alap vektorokon bell megklnbztetnk inszercis s szubsztitcis (helyettest) vektorokat.
Elbbi esetn a lineris DNS-ben tallhat egy restrikcis endonuklez hely, ahova maximum 7 kbp mret
DNS inszertet pthetnk be. Ezt a tpust fknt cDNS knyvrak ellltshoz hasznljk (ld. 8.3.
fejezet). A helyettest vektorok esetn a lineris DNS-en bell tallhat egy "kitlt" szekvencia (amely
rgi eredetileg a vrus ltikus letciklushoz nem esszencilis gneket tartalmaz), amelyet elsknt ki kell
vgni a vektorbl s annak helyre tudjuk bepteni az idegen gnszakaszt). Szubsztitcis vektorok
alkalmazsnl a maximlis bepthet inszert mret 20 kbp, s fleg genomilis knyvtrakat lltanak
el bellk (ld. 8.2. fejezet). Egy helyettest -fg vektor konstrukcit brzol a 7.8. bra.
Az -fg alap vektorok alkalmazsakor gyelni kell a bepteni kvnt inszert mretre, ugyanis ha az
inszert tl kicsi, akkor nem alakul ki a fg fejben a fertzshez nlklzhetetlen nyoms, mg ha tl nagy,
93
akkor nem fr el a DNS a virion feji rszben. A rekombinns konstrukcik elksztsnl nehzsget jelent,
hogy a vektor bal s jobb karjt kell az inszerttel liglni, azaz hrmas ligls trtnik. A -fg vektorok
hasznlatnak viszont nagy elnye, hogy a rekombinns DNS in vitro becsomagolhat a
vrusrszecskkbe (ehhez olyan csomagol kit-eket hasznlunk, ami a virionok kialakulshoz szksges
sszes komponenst tartalmazza), s ezltal infekcival a megfelel gazdasejtbe juttats hatsfoka kivl.
7.8. bra: Rekombinns DNS helyettest -fg vektorban. A -fg genomjnak kzps szakasza (piros) a fg
mkdshez nem esszencilis, ezrt az inszerttel helyettesthet. Mivel a DNS fgba pakolshoz a DNS mretnek
egy szk tartomnyba kell esnie, gy az idegen DNS nlkl a visszazrd forma tl kicsi ahhoz, hogy a specifikus
fehrjk fgba ptsk. Az in vitro pakolrendszer a fg genom kt vgn ismer fel egy rvid DNS szekvencit.
7.3.2. M13-alap vektorok
Az M13 fonalas bakteriofg egy 6,4 kbp-bl ll, egyszl DNS rktanyaggal rendelkez, a -fghoz
hasonlan E. coli-t fertz vrus. A viriont kb. 2700 kpiaszm kapszidburok fehrje (P8) alkotja, melynek
egyik vgt a P9 (5 kpiban) s P7, mg msik vgt a P6 (5 db) s P3 fehrjk zrjk le (ld. 7.9. bra).
7.9. bra: Az M13 fg sematikus brzolsa. Az egyszl cirkulris DNS-t krlvevl kapszidot a P8 (kk) fehrje
alkotja. A viriont az egyik oldalrl a P6 (piros) s P3 (zld), a msikrl a P9 (srga), s a P7 (lila) fehrjk zrjk le.
A P3 fehrje szerepe igen fontos a gazdasejt pilusn t trtn fertzsben. Az M13 fg nem ltikus a
gazdasejtre nzve. A fg egyszl DNS-e a replikci sorn ktszl replikatv formv alakul, amely a
94
piluson t trtn transzfer sorn jra egyszlv vlik s gy fertz tovbb. A laboratriumi gyakorlatban a
ktszl replikatv formt hasznljk klnoz vektorknt. A vrus restrikcis endonuklez hast helyeket
tartalmaz (pl.: az M13mp18 fg-vektor a pUC18 plazmid vektor tulajdonsgait rklte), ahova knnyen be
lehet pteni az inszertet. A vrusrszecske mrete nem limitlt, mivel a P8 fehrjbl rendkvl sok darab
is kpes kapszidburkot kpezni, ezrt a bepteni kvnt DNS mrete igen nagy lehet. Legfontosabb
felhasznlsa az M13 fg-alap vektoroknak, hogy egyszl templtot szolgltat a Sanger-fle DNS-
szekvenlshoz s az irnytott mutagenezis egyes mdszereihez. Ezek mellett az M13 fg kivlan
alkalmazhat irnytott evolcis mdszerekhez, mint pldul a fg-bemutats (ld. 0. fejezet).
7.4. Kozmidok
A kozmid vektorok tvzik a plazmidok s a -fg vektorok elnyeit. A plazmid vektorok megfelel
gazdasejtekben val fenntartshoz nincs szksg msra, csak replikcis origra, antibiotikum-rezisztencia
gnre s egy poliklnoz helyre. Mr emltettk, hogy a -fg nagy elnye, hogy rendkvl hatkonyan
kpes a fg rszecskbe pakolt DNS sejtekbe juttatsra. Ezen kvl a fg rszecskben hossz inszerteket
tartalmaz klnok is biztonsgosan fenntarthatak annak veszlye nlkl, hogy az inszert egy rsze
rekombincis folyamatok kvetkeztben elveszik. A kozmid vektorokat gy alaktottk ki, hogy a
sejtekben plazmidknt fenntarthatak legyenek, ugyanakkor lehetsg legyen a vektorok fertzkpes -
fg rszecskkbe trtn becsomagolsra, s ez ltal a rossz hatkonysg transzformci fg fertzssel
trtn kivltsra. Ezekhez a funkcikhoz nincs szksg 5-6 kbp DNS-nl tbbre. Ennek ksznheten a
kozmid vektorokba akr 45 kbp-os inszert is bepthet gy, hogy a keletkez vektor mg fg rszecskbe
pakolhat mret maradjon. A kozmid vektorok tulajdonkppen -fg cos szekvencit tartalmaz
plazmidok. Fontos kiemelni, hogy a kozmid vektorok a cos szekvencin kvl nem tartalmaznak a -fg
genomjbl szrmaz szekvencit.
A kozmidok rendelkezhetnek akr tbbfle replikcis origval is. Ezek meglte hatrozza meg, hogy az
adott kozmid vektor milyen sejtekben s milyen mdon szaporthat. A kozmid vektor rendelkezhet pldul
az emls sejtekben mkd SV40 origval s ColE1 origval, ami a ktszl replikcihoz szksges
prokarita rendszerben. Bizonyos kozmid vektorok az F-plazmid replikcis origjt tartalmazzk. Ez az
orig a plazmid kpiaszmt 1-2 pldnyban hatrozza meg. Ezeket a vektorokat fozmidoknak is nevezik.
Egyes vektorok tartalmazzk az f1 origt is, ami a vektor egyik (adott) szlnak szaportst teszi lehetv
baktrium sejtekben fonalas fgok (pl. M13 fg) fehrjinek jelenltben. A megfelel pakol szignllal
elltva ezek a vektorok fonalas fg virionba is becsomagolhatak.
7.5. Mestersges kromoszmk (PAC, BAC, YAC, HAC)
A gntechnolgia fejldsvel megjelent az igny egy olyan vektor tpusra, amelybe genom-szint
analzisekhez szksges, mrett tekintve igen nagy inszerteket (>100 kbp) lehet bepteni s klnozni. Ezt a
clt elrend terveztk meg az n. mestersges kromoszmkat.
Az els ilyen mestersges kromoszmhoz a P1 E. coli fg genomja adta az alapot. A P1 fg a -fggal
ellenttben lizogn letciklusa alatt a sajt DNS-t nem integrlja a gazdaszervezet genomjba, hanem
extrakromoszomlisan, episzmaknt szaporodik a gazdasejttel egytt. A vrus genomja 93 kbp mret
ketts szl lineris DNS, az E. coli-ba bejutva azonban cirkularizldik. A vrus genomjt felhasznlva kb.
100-300 kbp mrettartomnyban lehet idegen DNS-t bepteni a P1 fg-alap mestersges kromoszmba
(PAC: P1-derived Artificial Chromosome). A gyakorlatban a PAC konstrukciba restrikcis endonuklez
hasthelyek segtsgvel beptik az inszerteket, majd elektroporcival a sejtbe juttatjk.
A bakterilis mestersges kromoszma (BAC) csald az E. coli baktrium F-faktor episzmjnak
mdostott vltozata. A BAC-t szintn nagymret inszertek befogadsra fejlesztettk ki, s mg a PAC-nl
is nagyobb, akr 350 kbp mret DNS darabokat is bele lehet pteni. A BAC s PAC kzs vonsa, hogy
95
mindkt vektor tartalmaz a replikcihoz szksges bakterilis gneket, valamint szelekcis markereket (pl.:
antibiotikum-rezisztencia gneket), amelyek lehetv teszik a mestersges kromoszmt tartalmaz sejtek
kivlasztst. A replikcijuk a bakterilis kromoszmhoz kttt, azaz egy sejtben ltalban csak egy
kpiban fordulnak el (szigor, azaz stringens replikci). Ez a tulajdonsg nagymret rekombinns
DNS-ek esetben hasznosabb, mint a nagy kpiaszm, ugyanis gy kisebb valsznsggel trtnik homolg
rekombinci, a konstrukci stabilabb marad a felszaports sorn.
A harmadik mestersges kromoszma tpus eukarita eredet, ugyanis a srleszt gomba, a Saccharomyces
cerevisiae genom tulajdonsgait rklte meg. leszt mestersges kromoszmkat (YAC: Yeast Artificial
Chromosome) hasznltak eleinte a Humn Genom Program sorn is, mivel az elbb emltett PAC s BAC
vektorokkal szemben akr Mbp nagysg DNS inszerteket is kpes trolni, gy az emberi genom teljes
lefedshez elegend kb. 10000 lesztkln. (Ksbb azonban a YAC klnok instabilitsa miatt teljesen
elhagytk ezek hasznlatt.) Az elbbi kett mestersges kromoszmval szemben a YAC nem cirkulris,
hanem lineris felpts. Rendelkezik az eukaritkra jellemz centromer s telomer rgikkal is,
amelyek megakadlyozzk a vektor letrst s ms DNS darabbal val kapcsoldst. A YAC tartalmaz
minden olyan szakaszt, amely a kromoszma replikcijhoz s az utdsejtbe kerlshez (partci)
szksges. Ezeken a szakaszokon kvl a YAC vektor rendelkezik mg egy, a gazdasejtben mkdkpes
replikcis origval is. A YAC vektor htrnya a msik kt mestersges kromoszmval szemben, hogy
mivel eukarita gazdasejtben tartjk fenn, gy a rekombincis folyamatoknak jobban ki van tve, ezen kvl
a konstrukci ltrehozsakor gyakrabban alakulnak ki konkatamer inszertek.
Vgl meg kell emlkeznnk a humn mestersges kromoszmkrl (HAC: Human Artificial
Chromosome) is, mint a legkomplexebb vektor tpusrl, amely gretes eszkz a gnterpia szmra is, mint
gnszllt molekula. Megjegyzend, hogy az els emls-alap mestersges kromoszmt a Szegedi
Biolgiai Kzpontban Hadlaczky Gyula (1948-2013) lltotta el, akinek tbb vtizedes munkja lehetv
tette, hogy ezt a gntechnolgiai eszkzt ma mr emls sejtvonalakban gygyszermolekulk termelsre,
nvnyekben a biozemanyag-ellltsra is fel lehet hasznlni (ld. 0. fejezet). Mitotikusan stabil HAC-ot
ltre lehet hozni meglv kromoszmkbl s de novo is (telomer s centromer szekvencik kellenek hozz,
az utbbiakon funkcionlis kinetokrral). Mretk 1-10 Mbp kztt lehet, s a HAC-ba bepthet
inszertnek potencilisan nincs mrethatra.
7.6. leszt s egyb eukarita vektorok s gazdasejtek
Az eukarita rendszerek bevonsa a gntechnolgiba hamar megkezddtt, hiszen vilgos volt, hogy
amennyiben a rekombinns DNS-t be lehet juttatni egy eukarita sejtbe, a baktriumoknl megismert elvek
alapjn brmilyen sejtben fenn lehet tartani s akr ki is lehet fejezni idegen gneket. Az els nem prokarita
vektor tpus a Saccharomyces cerevisiaesrlesztben tallt, n. 2-mikronos gyr nev plazmid, amely
egy autonm mdon replikld DNS molekula. Van replikcis origja (ARS: Autonomously Replicating
Sequence), s n. REP gnjei, amelyek kis extrakromoszomlis kpiaszmot biztostanak gy, hogy csak
akkor vlasztjk szt a plazmid replikcit az leszt genomjnak megduplzstl, amikor a plazmid
kpiaszma lecskkent a sejtben. Ekkor beindul a plazmid fggetlen replikcija, amely addig tart, amg a
kpiaszm el nem ri a sejtenknti 30-50 darabot. A 2-mikronos gyrt YEp-nek is nevezik, azaz leszt
episzomlis plazmidnak (yeast episomal plasmid), amelyeken bell kt tpust klnbztetnk meg. Az els
az leszt replikld plazmid, YRp (yeast replicating plasmid), amelyek tartalmazzk a 2-mikronos
gyrre jellemz n. ARS szekvencit, ami biztostja az autonm replikcit. Ennek a tpusnak a htrnya,
hogy a sejt osztdsakor nem biztostott a nagy kpiaszm, s a vektor utdsejtbe trtn tkerlse. A
msik csoport az leszt integrld plazmid, YIp (yeast integrating plasmid), amely a YRp-vel
ellenttben a hordozott informcit bepti az leszt genomjba s azzal egytt replikldik, valamint
osztdskor az utdsejtbe is tkerl. Az leszt vektorokkal az expresszis rendszerek kapcsn a 13.1.6.
fejezetben foglalkozunk rszletesebben.
A plazmid tpus vektorokon kvl az eukarita gazdaszervezeteket is transzformlhatjuk vrus alap
vektorokkal. A legtbb vrus alap rendszer esetn szksges egy kztes prokarita tmeneti rendszer
96
hasznlata is, mivel a klnozs mindig E. coli-ban trtnik. Ezeket a ketts replikon tpus vektorokat
shuttlebinris vektornak hvjk.
Az eukarita vektor-gazda rendszerek kztt emltsre rdemes a rovarsejtek hasznlata bakulovrus, azaz
rovar-specifikus vrus-alap vektorok alkalmazsval. Mivel a f felhasznlsi terletk a heterolg
gnexpresszi, rszletesebben ott lesz rluk sz (ld. 13.2. fejezet).
Nvnyi sejtek transzformlsra (transzgenikus nvnyek ellltsra) egy nvnyi parazita, az
Agrobacterium tumefaciens tumor indukl (Ti) plazmidjt alaktjk binris vektorr. A Ti plazmid
vektorknt val alkalmazst rszletesen a 14.4.4. fejezetben trgyaljuk.
Az emls gazdaszervezethez hasznlt vektorok az esetek tbbsgben vrus eredetek. A leggyakrabban
hasznlt vektorok SV40-, adeno-, retro-, vagy vakcina vrusokon alapulnak. Az SV40 a legkorbban lert s
legltalnosabban hasznlt emls vrus vektor. Mrete kicsi, a gmb alak kapszidfejben egy 5,2 kbp mret
cirkulris DNS tallhat. A kis mret elnys, ha in vitro beavatkozst vgznk, de htrnyos olyan
szempontbl, hogy a genomon nincsenek felesleges rszek, melyeket helyettesteni lehetne a klnozand
DNS-sel. Ennek megoldsa az volt, hogy a vrus ksi gnjeit a klnozand DNS-re cserltk. A ksi
szakasz hinya a vrusok termelsnek hinyhoz vezet. Ennek elkerlshez a vrustermelst egy
segdvektor (helper vrus) alkalmazsval oldottk meg, amely tartalmazza a rekombinns vrusbl
hinyz gneket. Ezt kveten a vrus ltikus letciklusbl add sejtpusztt tulajdonsgt kellett
kikszblni, amelyet gy oldottak meg, hogy kifejlesztettk a nem ltikus SV40 vrustrzset s mell egy
specilis gazdasejt vonalat, amelyben fenntarthat a vektor.
Emls vektorokknt adenovrusokat is hasznlhatunk. Az adenovrusok az emls szervezetekben normlis
krlmnyek kztt enyhe lefolys megbetegedseket okoznak. A laboratriumi gyakorlatban az
adenovrusokat ltalban expresszis vektorknt hasznljk fel. Alkalmazsuk sorn a klnozand fehrje
gnjt beptik a vrusgenomba, majd az in vitro becsomagolt vrussal fertzik a gazda organizmust. Az
adenovrusok ms vrusokhoz hasonlan gnjeiket kpesek gy bekapcsolni, hogy nagy kpiaszmban
replikldjanak, ebbl addan a gnek ltal kdolt fehrje is nagy mennyisgben fog termeldni. A
vakcnia vrus a brnyhiml vrus rokona, azonban rtalmatlan s biztonsgos, amelyet a gyakorlatban
tbb terleten is alkalmaznak. Szmos sejtvonalat kpes fertzni s nagy elnye, hogy nagymret idegen
DNS fragmentumokat lehet belepteni. A retrovrusok RNS genommal rendelkeznek. A klnbz RNS
vrusok felptse igen hasonl, az RNS genom egy kzps magban helyezkedik el, ahol a reverz
transzkriptz enzim s klnbz szerkezeti fehrjk is megtallhatk. Ezt a magot lipidburok veszi krl. A
retrovrusok vektorknt val alkalmazsa igen sokrt, mivel szinte minden llatfajnl alkalmazhatk
clgnek sejtmagba juttatsra, ahol az a gazdasejt genomjba integrldva kifejezdik. Az emls
gazdasejtekben hasznlhat vrus-alap vektorokrl tovbbi rszleteket a 13.3. fejezetben olvashatnak.
7.7. Tovbbi olvasnival a fejezethez
Brown TA (2010): Gene Cloning and DNA Analysis: An Introduction. Wiley-Blackwell, 6th Edition. ISBN-
10: 1405181737.
Sambrook, J and Russel, DW (2001) Molecular Cloning. A Laboratory Manual. CSHL Press, volume 1-3,
Third edition. ISBN: 0879695773.
Shizuya H, Birren B, Kim U-J, Mancino V, Slepak T, Tachiiri Y, Simon M (1992) Cloning and stable
maintenance of 300-kilobase-pair fragments of human DNA in Escherichia coli using an F-factor-based
vector. Proc Natl Acad Sci USA 89: 87948797.
Kim JH, Kononenko A, et al (2011) Human artificial chromosome (HAC) vector with a conditional
centromere for correction of genetic deficiencies in human cells. Proc Natl Acad Sci U S A. 108:20048-53
97
8. Rekombinns DNS knyvtrak
A gnek s az azokrl termeld fehrjk vizsglata tjban az 1970-es vekig komoly akadlyt jelentett az,
hogy a kutatk nem tudtk a gneket megfelel tisztasgban s mennyisgben izollni. A rekombinns DNS
technolgik fejldse az 1970-es vek vgre lehetv tette az egyes gnek klnbz vektorokba trtn
klnozst (ld. 2. s 4. fejezet). A vizsglni kvnt gnt tartalmaz vektort a megfelel gazdasejtbe juttatva a
gn illetve az arrl termeld fehrje nagy mennyisgben, tisztn elllthat. Ez lehetv tette akr egsz
genomok DNS szekvencijnak meghatrozst, a gnek mkdsnek, szablyozsnak megismerst s a
gnekrl termeld fehrjk biokmiai mdszerekkel trtn vizsglatt.
A rekombinns DNS technolgik nemcsak egyedi gnek s fehrjk vizsglatra alkalmas rendszerek
ltrehozsra hasznlhatak. Ugyanezek a technikk alkalmasak rekombinns DNS knyvtrak
ltrehozsra is. Ezek a knyvtrak hatalmas mennyisg DNS-ben kdolt informcit tartalmazhatnak. A
knyvtr ltrehozsa sorn elszr a klnozni kvnt DNS megfelel mret fragmentumait lltjk
el, majd ezeket a fragmentumokat klnozzk a vlasztott vektorba. Az gy ltrejv knyvtr teht a
DNS klnbz rszleteit tartalmaz klnok sszessge. Az egyes klnok, amelyek a klnozott DNS ms-
ms rszlett tartalmazzk, megfeleltethetek egy hatalmas knyvtrban elhelyezett klnbz knyveknek,
innen ered a rekombinns DNS knyvtr elnevezs. A rekombinns DNS knyvtrbl a vizsglni kvnt
gnt tartalmaz klnt vagy klnokat klnbz, ksbb rszletezett technikk segtsgvel ki lehet
vlasztani, s a tbbi klntl el lehet klnteni. Ez az eljrs a knyvtrak szrse, angol eredet
kifejezssel szkrnels. Ezltal a vizsglatokat tiszta klnokon lehet elvgezni. Az egsz DNS knyvtr
vagy az egyes kivlasztott klnok a megfelel gazda rendszerben szaporthatak, azaz a DNS knyvtr
bizonyos rtelemben lland forrsa a specifikus klnoknak is.
8.1. A knyvtrak tpusai
Ahogy a hagyomnyos knyvtraknak, gy a DNS knyvtraknak is klnbz tpusai vannak. A
knyvtrak csoportostsnak legfontosabb szempontjai a knyvtr ksztse sorn felhasznlt DNS forrsa,
s a felhasznlt vektor. Az gynevezett genomilis knyvtrak klnjainak sszessge egy adott llny
teljes genomjt, vagy annak egy nagyobb rszt, pldul egy kromoszmt tartalmaz. Az gynevezett cDNS
(complementary DNS) knyvtrak egy adott sejttpusban egy adott pillanatban kifejezd fehrjket
kdol rett mRNS-ek szekvenciit tartalmazzk. Egy llny klnbz tpus sejtjeiben klnbz
fehrjk fejezdnek ki, gy az ezekbl ksztett cDNS knyvtrak is klnbzek lesznek. Egy adott DNS
knyvtr tulajdonsgait s felhasznlhatsgt meghatroz msik fontos tnyez az, hogy az adott knyvtr
milyen vektor hasznlatval kszlt. Az egyes vektorok ms-ms mret inszertek befogadsra alkalmasak.
Ez alapveten meghatrozza azt, hogy egy knyvtr milyen jelleg ksrletek sorn hasznlhat. Ebben a
fejezetben a klnbz tpus knyvtrak ltrehozsnak lpsei, az alkalmazott vektorok, valamint a
knyvtrak felhasznlsnak mdjai kerlnek tertkre.
8.2. Genomilis DNS knyvtrak
8.2.1. A genomilis knyvtrak ltrehozsrl ltalban
Genomilis knyvtr ltrehozsa sorn az elzleg izollt genomilis DNS-t megfelel mret
fragmentumokra kell darabolni. A DNS fragmentlsa kivitelezhet restrikcis endonuklezokkal, vagy
fizikai mdszerekkel, pldul ultrahang alkalmazsval (szonikls). A felhasznlhat fragmentumok
mrett a knyvtr kszts sorn alkalmazott vektor hatrozza meg, ezrt elnys, ha a folyamat sorn
keletkez tlagos fragmentum mretet a kutat meg tudja hatrozni.
98
Meg lehet-e becslni, hogy adott inszert mretnl s ismert genom mretnl hny rekombinns klnbl kell
llnia a knyvtrunknak? Igen, st azt is megadhatjuk elre, hogy milyen valsznsggel fogja tartalmazni
a knyvtr a teljes genom szekvencit. Az idelis cl 100%, m ez nem rhet el, csak megkzelthet.
Legyen a kvnt valsznsg 99%, ez gyakorlatilag teljes lefedettsget fog eredmnyezni. Vlasszuk a
humn genomot (3x10
9
bp), valamint egy olyan vektort, amelybe 10
5
bp mret inszerteket lehet bepteni.
Az albbi kplettel szmolunk:
N = ln(1p)/ln[1(I/G)]
ahol N a rekombinns klnok szma, p a teljes lefedettsg valsznsge, I az inszert mret s G a genom
mrete. A fenti plda esetn:
N = ln(10,99)/ln[1(2x10
5
/3x10
9
)] = 70.000
azaz 70 ezer egyedi klnbl kell llnia a knyvtrnak, hogy nagy valsznsggel lefedje a 23
kromoszmnkon trolt teljes genetikai informcit.
A restrikcis endonuklezokkal trtn fragmentls esetn a megfelel enzim kivlasztsval elrhet,
hogy a legtbb fragmentum a kvnt mrettartomnyban keletkezzen. Az enzim kivlasztshoz tudni kell,
hogy az egyes enzimek hasthelyei eltr gyakorisggal fordulnak el a fragmentlni kvnt clpont DNS-
en.
Amennyiben a bzisok vletlenszer eloszlsban fordulnnak el a DNS szekvenciban, gy egy tetszleges
4 nukleotidbl ll restrikcis hasthely 256 bzisonknt ismtldne, egy 6 karakteres megkzeltleg 4
kilobzisonknt, mg egy 8 karakteres nagyjbl 66 kilobzisonknt fordulna el. A valsgban a helyzet az,
hogy a bzisok eloszlsa nem vletlenszer. Pldul egy GC gazdag genomban egy AT gazdag szekvencia
motvumot felismer restrikcis enzim hasthelyei vletlen eloszls esetn a vrtnl tvolabb lehetnek
egymstl. Az emberi genomban pldul a 8 karakteres szekvencit felismer enzimek kzl az SwaI
hasthelye a vletlenszer eloszls esetn vrtnl gyakrabban fordul el, mg az FseI, AscI s NotI enzimek
hasthelye jelentsen ritkbb. A helyzetet tovbb bonyoltja, hogy a restrikcis endonuklezok nem
egyforma valsznsggel hastjk a DNS-t az sszes hasthelynl. Ezt pldul a szubsztrt DNS komplex
szerkezete hatrozza meg. Ezrt az alkalmazott enzim a knnyen hozzfrhet hasthelyeket hamar, mg a
nehezen hozzfrhet hasthelyeket csak hosszabb inkubls alatt kpes elhastani.
A fent lertak illusztrljk, hogy szmos szempontot figyelembe kell venni a kvnt eredmny elrshez.
Ilyen szempontok a megfelel restrikcis enzim kivlasztsa, valamint a DNS fragmentls
krlmnyeinek, nevezetesen a reakci idtartamnak vagy az alkalmazott enzim koncentrcijnak
megvlasztsa. Mindazonltal a restrikcis endonuklezok felhasznlsval lehetsg van a kvnt mret s
knnyen vektorba pthet DNS fragmentumok ellltsra. A genomilis DNS knyvtrak ellltsa
sorn ltalban arra trekednek, hogy a hasthelyeknek csak egy rszn kvetkezzen be hasts (rszleges
fragmentls). gy egymssal tfed DNS szakaszok jnnek ltre, azaz a keletkez knyvtr tagjai
egymssal tfed inszerteket hordoznak. Az egyes klnok ltal hordozott inszertek kzti tfeds a
genomilis knyvtrak fontos tulajdonsga.
A megfelel mret fragmentumokat ezutn a tbbitl elvlasztjk. Ez ltalban agarz glelektroforzissel
trtnik. A DNS-t a glbl izolljk, majd a vlasztott vektorba klnozzk. Ezzel ltrejn a rekombinns
DNS knyvtr, azaz a klnozott DNS klnbz szakaszait tartalmaz vektor klnok (illetve a
rekombinns DNS-ek) sszessge. A knyvtrat ezutn a vektornak megfelel gazdaszervezetbe, ltalban
E. coli, vagy ritkbban S. cerevisiaesejtekbe juttatjk (ld. 4.3. fejezet) a knyvtrat alkot vektorok
szaportsa cljbl (az utbbira plda az leszt kt-hibrid rendszer hasznlata, ld. 17.1. fejezet). A
genomilis knyvtrak ltrehozsnak ltalnos smjt a 8.1. bran mutatjuk be.
99
8.1. bra: Genomilis knyvtrak ltrehozsnak ltalnos smja
8.2.2. Knyvtr vektorok
A knyvtr legfontosabb paramtereit a vlasztott vektor hatrozza meg. A befogadhat inszert mreten
kvl a vektortl fgg tbbek kztt az is, hogy milyen gazda rendszerben tarthat fenn s szaporthat a
knyvtr. Ezrt mindenkppen szt kell ejteni az egyes vektorcsaldok knyvtrkszts szempontjbl
relevns tulajdonsgairl.
A korbban rszletesen bemutatott plazmid vektorok (ld. 7.2. fejezet) elvileg alkalmasak brmilyen tpus
knyvtr befogadsra, azonban van nhny olyan alkalmazhatsgi korltjuk, ami miatt mgsem
hasznljuk ket genomilis knyvtrak ksztsre. Az egyik ilyen problma az, hogy a plazmidokkal val
transzformls hatkonysga nagyon alacsony, s a plazmid mretnek nvekedsvel ez a hatkonysg
tovbb romlik. Ezen kvl a nagy inszertet tartalmaz plazmidok nem tarthatk fenn stabilan, ugyanis tbb
pldnyban vannak jelen a sejten bell, s egyms kzti rekombincis folyamatok rvn hajlamosak
elveszteni az inszert egy rszt, illetve trendezni azt. A plazmidok egybknt alkalmasak nagyobb, akr 10-
15 kbp mret inszertek befogadsra, azonban a transzformci rossz hatkonysga s a nagy inszertek
instabilitsa miatt kielgten mkd, azaz vltozatlan informcitartalommal fenntarthat plazmid
knyvtrat csak sokkal kisebb, 3-5 kbp mret inszertek alkalmazsval lehet ltrehozni. A plazmidoknak
ezek a htrnyos tulajdonsgai sztnztk a kutatkat a hatkonyabban transzforml, s nagyobb
inszertek befogadsra kpes vektorok fejlesztsre (ld. 0. fejezet).
8.2.3. -fg knyvtrak
A fgot az 1950-es vek ta intenzven tanulmnyozzk. letciklusa, gnjeinek szablyozsa rszleteiben
is jl ismert. Ez tette lehetv, hogy mdostsval szmos, a mikrobilis genetikai, molekulris genetikai s
molekulris biolgiai kutatsokban hasznlhat eszkzt fejlesszenek ki (ld. 7.3.1. fejezet). A -fg
helyspecifikus (int) s homolg (Red) rekombinz rendszereit elterjedten alkalmazzk rekombinns DNS
konstrukcik s genetikailag mdostott llnyek ellltsra (ld. 0. s 0. fejezetek). Ezen kvl a -fg
genom egyszer mdostsokkal klnoz vektorr alakthat t. A -fg alap klnoz rendszerek nagy
100
elnye a plazmidokkal szemben az, hogy segtsgkkel a rekombinns DNS konstrukcit a -fg fertzs
folyamatnak hatkonysgt kihasznlva lehet a gazdasejtekbe juttatni. A fg fertzs hatkonysga a
plazmiddal val transzformlsnl kb. hrom nagysgrenddel nagyobb.
8.2.3.1. -fg knyvtrak ltrehozsa
A -fg alap helyettest vagy szubsztitcis klnoz vektorok 25 kbp mret inszertek befogadsra
kpesek annak fggvnyben, hogy a fg genomjnak mekkora, a ltikus ciklusban val szaporodshoz nem
nlklzhetetlen rszt tvoltottk el az adott rendszerben. Genomilis knyvtrak ltrehozsra alkalmas
vektorok pl. a EMBL3/4, a DASH II s a FIX II.
A -fg knyvtr ltrehozsa sorn a genomilis DNS-t ragads vget eredmnyez restrikcis
endonuklezokkal hastjk, majd a megfelel mret DNS fragmentumokat izolljk. A -fg vektort olyan
restrikcis enzimmel kezelik, ami a genomilis DNS fragmentumain kialaktott ragads vgekkel
komplementer vgeket eredmnyez. A karokat ezutn megtiszttjk a kztes, gynevezett kitlt (stuffer)
szekvencitl. A kitlt szekvencira azrt van szksg, hogy az res, eredeti llapot vektor mrete
megfelel legyen ahhoz, hogy az azt tartalmaz fgrszecskk fertzkpesek legyenek.
A nagyobb inszertek befogadsra kpes gynevezett helyettest -fg vektorok olyan tulajdonsgokkal
vannak felruhzva, amelyek lehetv teszik a kitlt szekvencit tartalmaz, eredeti llapot klnok elleni
szelekcit. Az egyik lehetsg, hogy a kitlt szekvencirl annak vektoron belli orinetcijtl
fggetlenl termeldnek azok a fehrjk, amelyek jelenlte gtolja a fgok ltikus ciklust gynevezett P2
profgot tartalmaz baktrium trzsekben. Ezeket a vektorokat P2 profgot tartalmaz trzsben hasznlva az
E. coli pzsiton nem kpeznek plakkot azok a klnok, amelyek a kitlt szekvencit tartalmazzk. Ilyen
vektort eredeti llapotban ellltani nyilvnvalan csak P2 profgot nem tartalmaz trzsben lehetsges.
Egy msik lehetsg a kitlt szekvencia jra beplse elleni szelekcinak az, ha a kitlt szekvencia kt
oldaln egymssal megegyez poliklnoz helyek vannak egymshoz kpest fordtott orientciban. Egy
ilyen vektort kt, a poliklnoz helyen bell hast enzimmel kezelve a keletkez karok az egyik, mg a
kitlt szekvencia a msik enzim ltal generlt, egymssal nem kompatibilis tapads vgekkel fognak
rendelkezni. Az gy kezelt vektor karok kz a kitlt szekvencia nem tud jra beplni. A -fg EMBL3
vektor lehetsget ad a kitlt szekvencia jra beplse elleni szelekci mindkt mdjra (ld. 8.2. bra).
8.2. bra: Rekombinns -fg konstrukcira trtn szelekci
101
A genomilis DNS-t restrikcis enzimekkel daraboljk, majd a fragmentumok DNS szlainak 5-vgrl a
foszftcsoportot eltvoltjk, hogy a ligls sorn eredetileg nem szomszdos szakaszok ne
kapcsoldhassanak ssze. A vektor karokat s a genomilis DNS-t a kezelst kveten sszekeverik, s
DNS-ligz segtsgvel kovalensen sszekapcsoljk. A reakci sorn hossz konkatamer DNS molekulk
keletkeznek, amelyek a fg ltikus ciklusban val szaporodshoz szksges sszes gnbl, a virionba
pakoldshoz szksges cos szekvencikbl, valamint a vizsglt genom egy-egy rszletbl felpl
ismtld egysgekbl llnak.
A DNS knyvtrat ezutn in vitro fg burokba csomagoljk (in vitro pakols; ld. 8.3. bra). Ez gy
trtnik, hogy a knyvtrat sszekeverik E. coli sejtek kivonatval, ami tartalmazza a preformlt fg burok
fej s farok egysgeket, valamint a DNS fejekbe pakolst elvgz fehrjket (in vitro pakol extraktum).
Ezt a kivonatot olyan fggal (A
) fertztt sejtekbl lehet kszteni, amelyek genomjban mutcival
elrontottk a DNS virionba csomagolshoz nlklzhetetlen A fehrje gnje, azaz a burok ltrejn a
fertztt sejtben, de a fg DNS nem tud pakoldni. Ezt a sejtkivonatot kiegsztik tiszttott A fehrjvel,
majd a rekombinns DNS-sel. A DNS a cos szekvenciknl elhasad s a ltrejv molekulk burokba
csomagoldnak. Ezzel ltrejn a genomilis -fg knyvtr.
8.3. bra: Rekombinns -fg in vitro pakolsa
A rekombinns DNS-t tartalmaz fgok knyvtrbl hgtsi sort ksztenek, majd ennek egyes tagjaival E.
coli sejteket fertznek s a sejteket 37C-on inkubljk. A fertzst kveten 10-15 perccel a sejteket 45-
48C hmrsklet, 0,6-0,8% agart tartalmaz tpoldatban, n. top agarban felveszik, majd elmelegtett
agarlemez felsznre tertik szt. gy a sejtek pzsitot alkotnak, amin tarfoltnak (ms nven plakk) nevezett
vilgosabb vagy ttetsz foltok figyelhetek meg ott, ahov a sztterts sorn fggal fertztt sejt kerlt. A
fertztt sejtbl ugyanis a sejt pusztulsakor a krnyezetbe jutnak az j fgok, amik a szomszdos sejteket
fertzik s elpuszttjk azokat, mikzben jabb fg rszecskk termeldnek. Ezrt a fertztt sejtek
kzelben nem tudnak osztdni a sejtek, ez figyelhet meg plakkok formjban. A plakkokbl izollhat
fgok egy rekombinns DNS klnt kpviselnek. A fertzshez hasznlt fg hgts s a fertzs utn
keletkezett plakkok szma alapjn meghatrozhat a knyvtr fg koncentrcija, azaz titere is, aminek
ismeretben kiszmthat, hogy a knyvtrat milyen mrtkben kell hgtani, s hny agar lemezt kell
102
kszteni, hogy az sszes kln megjelenjen a lemezeken plakkok formjban. gy elllthat a knyvtr az
E. coli pzsiton plakkok formjban.
8.2.3.2. -fg knyvtrak szaportsa, a knyvtr fenntartsa
A DNS knyvtr sszes tagjnak nagy mennyisgben val ellltshoz a knyvtrral E. coli sejteket kell
fertzni. A fertztt sejtek az ket fertz klnt 100-200 pldnyban lltjk el, s a frissen termelt fgok
jabb sejteket kpesek fertzni. gy a knyvtr tagok knnyen szaporthatak. Az viszont korntsem biztos,
hogy minden kln ugyanolyan mrtkben szaporodik a knyvtr nvesztse sorn. A knyvtrban minden
kln egyedi, a baktrium sejteknek klnbz nehzsg feladatot jelent ezek szaportsa. A felnvesztett
knyvtrban ltalban vannak az tlagosnl jobban s rosszabbul termeld, azaz alul- s fellreprezentlt
klnok egyarnt. Egyes klnok akr ki is halhatnak, ha a knyvtr tbbszr is felnvesztsre kerl, ami
rtkes informci elvesztst jelenti.
A -fg knyvtrak esetben az a legjobb megolds, hogy a knyvtrat csak egyszer nvesztik fel nagy
mennyisgben, majd a fgokat izolljk s tbb adagban lefagyasztjk. gy sok ksrletre elegend
mennyisgben s azonos minsgben ll rendelkezsre a knyvtr hossz idn t. Az egyttmkd
kutatcsoportok akr meg is tudjk osztani egymssal a knyvtraikat, ehhez elg egy lefagyasztott adag
fgot elkldeni. Az sszes knyvtrra igaz, hogy megfelel, glicerinnel kiegsztett oldatban lefagyasztva
hossz ideig trolhatak.
8.2.3.3. A -fg knyvtrak szrse (szkrnelse) plakk hibridizcival
A korai knyvtrakat, s a modern knyvtrak nagy rszt is azrt lltjk, lltottk el, hogy adott gneket
s azok szablyoz rgiit izolljk tovbbi vizsglatok cljbl. A keresett gn szerencss esetben akr
tbb kln inszertjben is jelen lehet teljes hosszsgban, azonban gyakran elfordul, hogy a keresett
informcit tbb, egymssal tfed inszertet tartalmaz kln egyttese tartalmazza. Ez az egyik oka annak,
hogy ltalban arra trekednek a knyvtrkszts sorn, hogy az inszertek egymssal tfedjenek.
A knyvtrat szrni (szkrnelni) kell, hogy a rengeteg kln kzl azonostsuk azokat, amelyek a keresett
informci egszt vagy rszleteit tartalmazzk. A szkrnels gyakran alkalmazott mdja specifikus
egyszl DNS vagy RNS prbk hasznlatn alapul s plakk (tarfolt) hibridizcinak hvjuk (ld. 8.4.
bra). A szrs els lpseknt a fg knyvtrat E. coli sejtekbe kell juttatni, s olyan sejtpzsitot
tartalmaz lemezeket kell kszteni, amelyeken 150-200-fg plakk keletkezik. Ezt kveten a lemezekre
nitrocellulz membrnt fektetnek. Minden plakkbl kerlnek fgok a membrnra, gy azon ltrejn az
eredeti lemez lenyomata. Ezutn a membrnokat ntrium-hidroxiddal kezelik, hogy a fgok fehrje burkt s
a DNS-t denaturljk. A DNS-t ezt kveten hevtssel fixljk a membrnokon. Az elksztett
membrnokat radioaktvan vagy fluoreszcensen jellt DNS vagy RNS prba oldatba ztatjk. A prba
szekvencija komplementer a keresett szekvencia egy rszletvel, teht a megfelel klnok DNS-hez
hibridizl. Radioaktv prba esetn a membrnt rntgenfilm segtsgvel hvjk el, mg fluoreszcens prba
esetn a megfelel hullmhosszon trtnt gerjesztst kvet emisszit detektljk az egyes pontokon. A
rntgenfilmen megjelen, vagy fluoreszcens jelet ad pontok pozcija a membrnon megegyezik az eredeti
plakk pozcijval az agar lemezen, azaz a keresett szekvencit, vagy annak egy rszt tartalmaz kln vagy
klnok ezzel a mdszerrel azonosthatk. A mdszerhez szksg van a keresett gn szekvencijnak vagy a
keresett gnhez a genomban kzel elhelyezked marker ismeretre.
A kivlasztott fgokkal baktrium sejteket fertznek s friss fgokat termeltetnek, hogy az ltaluk hordozott
genomilis DNS szakasz megfelel mennyisgben s minsgben lljon rendelkezsre a tovbbi
vizsglatokhoz.
103
8.4. bra: Plakk hibridizci
Ha nincs jelen olyan kln a kivlasztottak kztt, amelyik a teljes keresett szekvencit tartalmazza, akkor a
kromoszma sta (chromosome walking) mdszervel azonostanak s sorba rendeznek tbb olyan
tfed inszertet tartalmaz klnt, amelyek egyttesen tartalmazzk az sszes keresett informcit (ld. 8.5.
bra).
A kromoszma sta sorn szksg van kt ismert markerre, amelyek a keresett szekvencia kt vgn
tallhatak. Az egyik prbval szkrnelik a knyvtrat, s olyan klnokat azonostanak, amelyek a keresett
informcinak ezt a rszt tartalmazzk. Ezutn restrikcis trkpezssel feltrkpezik az adott
fragmentumot, s az els prbtl legtvolabbi vgvel komplementer prbt ksztenek, amivel jra szrik
a knyvtrat. gy jabb klnokat tallnak, amelyek az j prba szekvencijt tartalmazzk. A folyamat sorn
kivlasztott, egymssal tfed s sorba rendezett klnok sszessgt kontignak nevezzk.
104
8.5. bra: Kromoszma sta
8.2.4. Kozmid knyvtrak
A -fg vektorok s a felhasznlsukkal ksztett knyvtrak lehetv tettk, hogy 20-25 kbp tlagos inszert
mret knyvtrakat hasznljanak a genetikai s genomikai kutatsok sorn. Azonban szmos gn hossza
ennl jelentsen nagyobb lehet, ezrt tovbbra is fennllt az igny nagyobb inszertet befogadni kpes
vektorok fejlesztsre, s knyvtrak ksztsre val felhasznlsra. Erre a clra elszr a kozmid
vektorokat hoztk ltre (ld. 7.4. fejezet).
8.2.4.1. Kozmid knyvtrak ltrehozsa
Az res, eredeti llapot kozmid vektor E. coli sejtekben plazmidknt szaporthat, s a plazmidokkal
azonos mdszerekkel izollhat. A knyvtrksztsi folyamat sorn a vektort restrikcis endonuklezokkal
felnyitjk, majd a keletkez 5-vgekrl a foszft-csoportot eltvoltjk. A vektort ezutn egy msik
enzimmel is megemsztik. A reakci sorn vektor karok jnnek ltre, amelyek vgeiken cos szekvencikat
tartalmaznak. A vektor molekulkat mret szerint elvlasztjk a nem megfelelen hasadt DNS molekulktl.
Ezutn az emsztett vektort sszekeverik a klnozsra elksztett, azaz a megfelel enzimmel kezelt s
defoszforillt genomilis DNS-sel, s ligljk a komplementer DNS vgeket. . A ligls sorn a -fg
vektorokhoz hasonlan konkatamer DNS molekulk jnnek ltre. Ezekhez a hossz DNS molekulkhoz
preformlt -fg fej s farok egysgeket s a becsomagolshoz szksges fg fehrjket tartalmaz sejt
kivonatot adnak. Ekkor a hossz DNS molekulk a cos helyeknl elhasadnak s egyesvel fg burokba
pakoldnak. A megfelel mret inszertet tartalmaz vektorok becsomagoldsa fertzkpes fg
rszecskt eredmnyez.
A rekombinns kozmid vektorokat tartalmaz fgokat, azaz a kozmid knyvtrat izolljk, majd azokkal
baktrium sejteket fertznek. A sejtben a vektor kralak molekulv zrdik, s plazmidknt replikldik.
Sajnos a kozmid vektorok esetben is fennll annak a veszlye, hogy a nagy inszertek egy rsze elveszik,
105
amikor a knyvtr tagjai sejtekben vannak fenntartva. A rendszernek megvan viszont az az elnye, hogy ez
a veszly a fg burokba csomagolt knyvtr esetben nem ll fenn.
8.2.4.2. Kozmid knyvtrak szaportsa, a knyvtr fenntartsa
A kozmid knyvtr klnjainak sokszorostsnak els lpseknt a klnokat tartalmaz vrusokkal E. coli
sejteket fertznek, majd rvid nveszts utn a sejteket a vektornak megfelel antibiotikumot is tartalmaz
agar lemezekre szlesztik. A lemezeket 37C-on inkubljk. Az antibiotikum szelekcinak ksznheten
csak a kozmid vektor klnnal transzformlt sejtek tudnak osztdni a lemezeken. Msnap a lemezekrl a
sejteket lemossk a megfelel tpoldattal s a kozmid vektorokat hordoz sejteket tartalmaz tplevest egy
csben sszegyjtik s alaposan sszekeverik. Ezt kveten glicerinnel kiegsztik a mintt, sztosztjk tbb
adagra, lefagyasztjk s -80C-on troljk.
A kozmid knyvtrakat baktrium sejtekben, agar lemezek felsznn fenntartani, de a fent lert mdon,
mlesztve amplifiklni nem knny feladat. Egyrszt a nagy inszerteket hordoz klnok instabilak,
msrszt a knyvtrban maradt nem rekombinns, eredeti llapot kozmiddal, vagy kisebb inszertet
tartalmaz vektorral transzformlt sejtek kisebb terhet viselnek, ezltal gyorsabban osztdnak a nagy
rekombinns vektort hordoz trsaiknl. Vizsglatok kimutattk, hogy egy 2-3% eredeti vektort tartalmaz
kozmid knyvtrban egy amplifikcit kveten a sejteknek akr 40%-a eredeti vektort hordozhat. Ezt
kikszblni rendkvl sok munkt ignyl mdon lehet. Egy lehetsges mdszer az sszes kln
megrzsre az, hogy az elksztett knyvtrat sejtekbe juttatjk, s a sejteket szlesztik agar lemezeken
gy, hogy a lemezeken egyedi, klonlis telepek njenek. A telepeket ezutn egyesvel leoltjk 96 lyuk
sejttenyszt lemezek tplevessel tlttt mintahelyeire. Egy nagy knyvtr esetben tbb tzezer klnt kell
kzzel leoltani, de gy biztosthat, hogy minden kln fennmaradjon. A lemezek sszes mintahelyrl
idnknt a sejtek egy rsze j lemezekre tvihet, s gy a knyvtr bizonyos ideig fenntarthat. Ez utbbi
mvelet robotok segtsgvel automatizlhat. sszessgben elmondhat, hogy a kozmid knyvtrak
esetben megfontoland lehet a knyvtr ismtelt elksztse bizonyos idkznknt, vagy akr minden
jabb szkrnelst megelzen.
8.2.4.3. A kozmid knyvtrak szrse kolnia hibridizcival
A kozmid knyvtrak szkrnelse sorn az agar lemezek felsznn nveked baktrium telepek egy rszt
nitrocellulz membrnra viszik t, majd a membrnt nhny pldnyban sokszorostjk. A telepek
lenyomatt tartalmaz egyik membrnt NaOH oldattal kezelik, hogy a sejtek feltrdjanak, majd a DNS-t
kmiai mdszerrel, vagy hevtssel fixljk a membrnon. A fixlt membrnokhoz radioaktvan vagy
fluoreszcensen jellt DNS prbkat hibridizltatnak, gy azonostjk a keresett informcit tartalmaz
klnokat. Az eljrst kolnia hibridizcinak nevezzk. A folyamat tulajdonkppen a legtbb lpsben
nagyon hasonlt a -fg knyvtrak plakk hibridizcijhoz.
A szkrnels sorn pozitvnak bizonyult klnok felszaportsa ltalban nem magtl rtetd feladat a
kiindulsi lemezeken tapasztalt nagy kolnia srsg miatt. Ilyen esetekben az eredeti membrnon az
autoradiogram vagy az elhvott membrnrl kszlt fluoreszcens fot alapjn azonostjk azt a rgit, ahol
a pozitv kln megtallhat. Ezutn a kivlasztott rgiban tallhat sejtekkel tptalajt oltanak be s a
sejteket szaportjk. A sejteket ezutn hgtjk s agar lemezen szlesztik gy, hogy kis klnsrsg
lemezek keletkezzenek, azaz a msnapra megjelen telepeket alkot sejtek egyetlen kozmid klnt
hordozzanak. A kis klnsrsg lemezeket ezutn ismt szkrnelik. A msodik szrs sorn azonostott
pozitv klnok mr izollhatak tiszta formban.
A fent lert kt ciklusban trtn szkrnelsre azrt van szksg, mert ha a knyvtr sszes klnjt akarnk
szleszteni gy, hogy klonlis telepek njenek fel a szrend lemezeken, akkor a lemezek szma
csillagszati lenne. sszessgben sokkal kevesebb munkt jelent az sszes klnt szrni nagy klnsrsg
106
lemezeken, majd a pozitv klnokat a fent lert mdon megkeresni a szrs sorn kivlasztott rgikban
jelen lev klnok kzl.
A -fg s a kozmid knyvtrak sszehasonltsa sorn a legfontosabb szempontok szerint arra a
megllaptsra juthatunk, hogy a kozmid knyvtrak a nagyobb befogadhat inszert mretnek
ksznheten feleannyi klnnal lefedhetnek egy adott genetikai informcit.
8.2.5. Mestersges kromoszma knyvtrak (BAC s YAC)
Az eddig bemutatott rendszerek ltal befogadhat inszert mret mg mindig nem elegenden nagy ahhoz,
hogy belthat s knnyen kezelhet mennyisg kln ltrehozsval a vizsglt genomot, vagy annak
kivlasztott rszt reprezentl knyvtrakat lehessen kszteni, valamint hogy a leghosszabb gneket,
egytt szablyozott gncsoportokat egszben hordoz klnokat lehessen ellltani. Ezt az ignyt a
mestersges kromoszma vektorok kifejlesztse s genomilis knyvtrak ksztsre trtn alkalmazsa
elgtette ki. A mestersges kromoszma vektorok sokkal nagyobb, nhny szz kbp (BAC), vagy akr
kt-hrom Mbp (YAC) mret inszertek befogadsra alkalmasak. Ez tbbszrse a korbban
bemutatott rendszerek ltal befogadhat inszertek mretnek
8.2.5.1. Mestersges bakterilis kromoszma (BAC) knyvtrak ltrehozsa
A BAC vektorok az E. coli F-plazmidjnak replikcis origjt tartalmazzk (ld. 7.5. fejezet). Ennek
ksznhet, hogy a BAC vektor pldnyszma szigoran szablyozott (stringens), s egy sejtben az
osztdst megelz replikcit leszmtva csak egyetlen pldnyban fordul el. A BAC knyvtrakat
elterjedten alkalmazzk a genom projektek sorn a genom nagyobb rszleteinek amplifiklsa, fenntartsa, a
genom fizikai trkpezse s szekvenlsa sorn (ld. 9.1.2. fejezet).
A BAC knyvtrak ltrehozsa sorn alapveten a korbban mr ismertetett technikkat hasznljk. A nagy
inszert mret miatt ugyanakkor bizonyos dolgokra nagyobb figyelmet kell fordtani. A genomilis DNS
izollsa sorn kerlni kell, hogy a DNS-re hat nyrerk kvetkeztben, vagy brmi ms okbl a DNS
krosodjon. A DNS szlon bekvetkez nem clzott trsek rontjk a klnozs hatkonysgt s
cskkenthetik az elrhet maximlis inszert mretet is. A restrikcis endonuklezzal kezelt DNS
fragmentumok mret szerinti elvlasztsa is ms mdszerrel trtnik a szz kbp-os mrettartomnyban. A
kvnt 100-300 kbp tartomnyban a DNS molekulkat nem lehet mret szerint elvlasztani hagyomnyos
glelektroforzis technikk segtsgvel. A megolds a pulzl-ter glelektroforzis (PFGE: pulsed field
gel electrophoresis) technika alkalmazsa (ld. 8.6. bra).
A PFGE sorn az alkalmazott feszltsg irnya adott idkznknt vltozik. Az egyik legegyszerbb
elrendezsben a gl hossztengelyre merleges irnyon kvl a tengelytl mindkt irnyban 60-os szget
bezr feszltsget alkalmaznak mg. A mdszer alapja, hogy a feszltsg irnynak megvltozsakor a
kisebb molekulk gyorsabban reaglnak, s kezdenek el a megvltozott irnynak megfelelen mozogni,
ezltal gyorsabban haladnak. Mivel a klnbz irnyokban egyforma ideig alkalmazzk a feszltsget,
ezrt a halads irnya sszessgben a gl tengelyvel prhuzamos marad.
A megfelel mrettartomnyba es DNS molekulk izollsra is tbb lehetsg van. Az egyik, a DNS
molekulkat tartalmaz agarz gldarab kezelse a polimerizlt agarzt lebont agarz enzimmel. A DNS-re
hat nyrerk ezzel a mdszerrel kizrhatak. Egy msik mdszer az gynevezett elektroelci. A DNS-t
az izollst kveten koncentrlni is kell. Ez ltalban dialzissel trtnik a nyr erk fellpsnek
elkerlse miatt.
107
8.6. bra: Pulzl-ter glelektroforzis
A BAC vektorokat a klnozst megelzen restrikcis endonuklezzal felnyitjk, majd a DNS vgekrl a
foszft csoportot alkalikus foszfatz enzimmel eltvoltjk, hogy megelzzk a vektor nzrdst (ld. 3.4.2.
fejezet). A kezelt vektort s a genomilis DNS fragmentumokat ezutn sszekeverik s ligljk. A knyvtr
sejtekbe juttatsa vagy kmiai transzformlssal, vagy a ltrejv vektorok nagy mrete miatt
elektroporlssal trtnik.
8.2.5.2. BAC knyvtrak szrse s fenntartsa
A BAC knyvtrakat a kozmid knyvtrakhoz hasonlan lehet szkrnelni. A klnbz eljrsok sorn jellt
DNS prbkat hibridizltatnak a klnok membrnon fixlt DNS-hez, majd a kivlasztott klnokat izolljk,
s tiszta formban szaportjk. A BAC knyvtrak fenntartsra szintn alkalmazhatak a kozmid
knyvtrak esetben ismertetett mdszerek. Az eredeti agar lemezek lenyomatait tartalmaz membrnok,
vagy a klonlisan, sejttenyszt lemezeken nvesztett klnok formjban a knyvtr hosszabb idn
keresztl, megfelel minsgben fenntarthat.
8.2.5.3. leszt mestersges kromoszma (YAC) knyvtrak s ltrehozsuk
A YAC vektorok a BAC vektorokhoz hasonlan eredeti llapotukban E. coli sejtekben fenntarthat, plazmid
szer cirkulris DNS molekulk (ld. 7.5. fejezet). Tartalmaznak bakterilis s leszt replikcis origt,
szelekcis markereket a YAC-ot hordoz baktrium illetve leszt sejtek szelekcijhoz, valamint
multiklnoz helyet is. A YAC vektoroknak rendelkeznik kell a telomer s centromer rgikbl
szrmaz szekvencikkal is, ezek ugyanis nlklzhetetlenek a genomilis DNS szakaszt tartalmaz YAC
vektor lesztsejtekben val stabil fenntartshoz s az osztdskor trtn pontos sztvlshoz. A YAC
vektorok ltal befogadhat 2-3 Mbp mret inszertek idelis eszkzkk tehetnk ket a genom projektek,
genomok trkpezse s szekvenlsa sorn, azonban szmos olyan htrnyos tulajdonsggal rendelkeznek,
ami megnehezti a YAC knyvtrakkal val munkt.
A YAC knyvtrakban trolt informci jval kevsb stabil, mint a BAC knyvtrakban trolt. A
YAC knyvtrakban gyakran elfordul, hogy az egyes klnok ltal hordozott inszert nem a genom egyetlen,
folytonos rgijnak felel meg, azaz kimra. Ennek oka lehet az, hogy egyetlen YAC vektorba tbb inszert
is bepl a ligls sorn, vagy az, hogy a knyvtrral val transzformls sorn egyetlen lesztsejtbe tbb
YAC vektor is bejut, s a vektorok kztt rekombincis folyamatok jtszdnak le. Ezen kvl az inszert
egy rsznek delcija vagy inverzija is gyakran megfigyelhet. Egyes vizsglatok szerint a YAC
knyvtrakban a klnok akr felre igaz lehet, hogy a hordozott inszert nem felel meg egy folytonos
genomilis rginak. Ez a jelensg ksrletes mtermkeket eredmnyez, s tves kvetkeztetseket
okozhat. A fent felsorolt htrnyok ellenre bizonyos esetekben a YAC vektorba trtn klnozs az
egyetlen megolds. Az lesztben pldul szlssgesen magas A-T tartalm DNS szakaszok stabilabbak,
mint bakterilis rendszerekben.
108
8.2.5.4. YAC knyvtrak fenntartsa s szrse
A YAC knyvtrakat 96 vagy 384 mintahelyes sejttenyszt lemezeken lehet fenntartani. Ehhez a
knyvtrral transzformlt s tplemez felsznn nvesztett leszt klnokat egyesvel le kell oltani s a
sejttenyszt lemez mintahelyeire kiosztott tptalajba kell oltani. Adott idkznknt a sejttenyszt
lemezen ntt sejtek egy rszt j sejttenyszt lemezekre kimrt friss tplevesbe viszik t. A knyvtr ilyen
formban 4C-on nhny htig tarthat el, vagy a mintahelyeket glicerinnel kiegsztve a lemezek le is
fagyaszthatak, gy a knyvtr hosszabb ideig is eltarthat.
A YAC knyvtrak szkrnelsnek leghatkonyabb mdja szintn DNS prbk hibridizlsn alapul. A
hibridizls sorn hasznlt membrnt agar lemezek felsznre fektetik, majd a sejttenyszt lemezeken
fenntartott knyvtr klnokat automatizltan, robotok segtsgvel felviszik a membrnra meghatrozott
elrendezsben. A klnokat az agar lemezen nvesztik, majd a membrnt eltvoltjk. A membrnon az
sszes kln jelen van szablyos elrendezsben. A membrnon lev sejteket ezutn a korbban lertakhoz
hasonlan feltrjk, majd a DNS-t denaturljk s fixljk a membrnon. A prba hibridizlsa s elhvsa
utn azonosthatak a membrnon s a sejttenyszt lemezen azok a klnok, amelyek a prba szekvencijt
hordozzk.
8.2.5.5. A BAC s YAC rendszerek sszehasonltsa
A mestersges kromoszma rendszerek sszehasonltsa alapjn megllapthat, hogy a knyvtrkszts
sorn kritikus transzformlsi hatkonysg a BAC knyvtrak esetben jelentsen, mintegy kt
nagysgrenddel jobb, mint a YAC knyvtraknl. A cirkulris BAC vektorok kompakt, szuperheliklis
szerkezetknek ksznheten egyszeren izollhatak, mg a lineris s nagyobb mret YAC vektorok
gyakran krosodnak a tiszttsi folyamat sorn. A YAC vektorok elnye viszont, hogy mg a BAC
vektorokhoz kpest is hatalmas a befogadhat inszertek mrete, valamint bizonyos esetekben a DNS YAC
vektorba ptve s leszt sejtekben fenntartva stabilabb, mint bakterilis rendszerben.
8.2.6. Genomilis knyvtrak felhasznlsi terletei
A genomilis knyvtrakat szles krben hasznljk genetikai s genomikai kutatsokban, kiemelten a
genom projektekben. A felhasznls clja lehet egy gn, gn klaszter vagy akr a teljes genom fizikai
trkpnek elksztse, j markerek azonostsa s elhelyezse a trkpen, vagy akr a teljes genom
szekvencijnak meghatrozsa. Brmilyen alkalmazs sorn az els feladat, hogy az ppen keresett
informcit tartalmaz klnt vagy klnokat a korbban bemutatott szrsi technikk segtsgvel
megkeresik s izolljk. A szkrnels sorn kivlasztott klnok ltal hordozott inszertek vizsglatnak els
lpse gyakran a restrikcis trkpezs. Ez a mdszer hasznos informcikat szolgltat az inszertrl a
genom szekvenlsa sorn, s akkor is, ha a cl a genom egy adott rgijnak azonostsa, amplifiklsa s
tovbbi vizsglata. A restrikcis trkpezs folyamn informci gyjthet arrl, hogy az adott inszertben
bizonyos restrikcis endonuklezoknak hny hasthelye van, ezek milyen sorrendben, s egymstl milyen
tvolsgban helyezkednek el. Ez az informci azrt hasznos, mert a hasthelyek helyzetnek ismerete egy
korbban nem trkpezett DNS szakasz fizikai trkpnek els ismert pontjait adhatja. Ezek a pontok
hatalmas segtsget nyjthatnak az inszert tbb rszletben trtn szekvenlst kveten az egymssal
tfed szekvencik sorba rendezsben, ha a ltrehozott restrikcis trkp felbontsa megfelel. (ld. 9.1.2.
fejezet)
8.3. cDNS knyvtrak
A cDNS knyvtrak ksztsnek clja alapveten ms, mint a genomilis knyvtrak esetben. A cDNS
knyvtrak a knyvtrkszts sorn hasznlt sejttpusban kifejezd fehrjk rett mRNS szekvenciirl
109
kszlt komplementer szlakat tartalmazzk. Ilyen knyvtrakat leginkbb adott fehrjk kdol
szekvencijnak ellltsra hoznak ltre. A cDNS knyvtrbl klnozott eukarita gn intronokat nem
tartalmaz. Ennek ksznheten lehetsges a fehrje bakterilis expresszis rendszerben trtn ellltsa. A
cDNS knyvtrak nem alkalmasak az egyes gnek kifejezdsnek, az expresszi szablyozsnak
vizsglatra, mert a gnekhez tartoz szablyoz elemek nincsenek jelen. A cDNS knyvtr elksztse eltt
krltekinten, elzetes ismeretek alapjn kell megvlasztani azt a sejttpust, amelyben a vizsglni kvnt
fehrjk nagy mennyisgben jelen vannak. A sejttpus megfelel kivlasztsa nveli annak az eslyt, hogy
a keresett gnek jelen lesznek a knyvtrban.
8.3.1. cDNS knyvtrak ltrehozsa
A cDNS knyvtrak ltrehozsnak els fontos lpse a megfelel sejttpus vagy szvet, illetve az
alkalmazott vektor kivlasztsa. A cDNS knyvtrak ltrehozsa sorn gyakran hasznlt vektorok kz
tartoznak az inszercis s szubsztitcis -fg vektorok, valamint a plazmidok s kozmidok. A cDNS
knyvtrak tlagos inszert mrete nem indokolja a mestersges kromoszma vektorok hasznlatt.
A kivlasztott sejtekbl izolljk az RNS-t, majd az rett mRNS-ek 3 poli-A farkhoz hibridizl oligo-dT
primer s reverz transzkriptz enzim felhasznlsval elksztik az mRNS-ekkel komplementer DNS
(cDNS) szlakat. A cDNS molekulk vektorba klnozshoz szksg van a ltrejv RNS/DNS hibrid
molekulk ktszl DNS megfelelinek ellltsra. Erre is tbb mdszer ll rendelkezsre. Az egyik
leggyakrabban alkalmazott eljrs sorn a reverz transzkripci termkhez RN-z H s DNS-polimerz
enzimet adnak. Az RN-z H nick-eket (bevgsokat) hoz ltre az RNS szlon. A DNS-polimerz a nick-
eknl megjelen szabad 3-OH csoportoktl indulva emszti az RNS szlat s ltrehozza a DNS msik
szlt.
A ltrejv ktszl DNS-t a vektorba liglst megelzen mg tovbbi kezelsnek kell alvetni. A
molekulk vgein az egyik szl esetleges tlnylst egyszl-specifikus DNS-exonuklez enzimmel
emsztik, vagy DNS-polimerz enzimmel feltltik. A DNS vektorba liglshoz a termket restrikcis
endonuklezzal kell hastani. Ehhez el kell ltni a DNS molekulk vgeit a megfelel enzim hasthelyvel,
valamint biztostani kell, hogy az enzim csak a vgeken hastson. Ennek rdekben elszr metil-transzferz
enzimmel kezelik a DNS-t, ami az alkalmazand restrikcis endonuklez hasthelyeit metillja, ezltal
megvja azokat a ksbbi haststl. Ezt kveten a DNS molekulk vgeire tompa vg liglssal linkereket
illesztenek, amelyek tartalmazzk a restrikcis endonuklez metillatlan hasthelyet. A vlasztott vektort s
a cDNS-t restrikcis enzimmel kezelik, majd az inszerteket a vektorba ligljk. A vektor nmagval val
zrdsnak megakadlyozsra alkalmazhat a vektor foszfatz enzimmel val kezelse. A cDNS
knyvtrkszts smjt a 8.7. bran mutatjuk be.
8.7. bra: cDNS knyvtr ksztse
110
8.3.2. cDNS knyvtrak szrse s fenntartsa
A cDNS knyvtrak fenntartsnak mdjt az alkalmazott vektor tpusa hatrozza meg. A klnbz
vektorok felhasznlsval kszlt knyvtrak fenntartsval kapcsolatos tudnivalk a genomilis
knyvtrakkal foglalkoz fejezetben tallhatak.
A cDNS knyvtrak szkrnelsre is alkalmasak a korbban lert, jellt DNS vagy RNS prbk
hibridizlsn alapul eljrsok. Bizonyos vektorok lehetsget adnak a knyvtr szrsnek ms mdjaira
is. Az egyik lehetsg az, hogy a vektorba liglt inszert egy promter mgtt helyezkedik el,
transzkripcival trdik mRNS molekulkba s vgl fehrje formban megjelenik a sejtben. Ilyen
esetekben lehetsg van specifikus, jellt ellenanyaggal azonostani azokat a knyvtr kolnikat,
amelyekben termeldik a klnozni kvnt fehrje, vagy annak az ellenanyag ltal felismert rszlete.
A cDNS knyvtrban elfordul szekvencik nagy rsze nem tartalmazza a fehrjt kdol mRNS teljes
szekvencijt, csak annak egy rszt. A teljes hosszsg cDNS ellltshoz vagy megkeresshez a
knyvtrat jra kell szkrnelni. Ennek sorn ltalban a korbban mr azonostott, de nem teljes hosszsg
kln szekvencijbl ksztett prbt hasznljk. Szmos lehetsg van annak megllaptsra, hogy az
azonostott kln vagy klnok szekvencija tartalmazza-e a teljes mRNS szekvencit. A legegyszerbb az 5
s 3 nem-trd rgik megltnek vizsglata. Ha valamelyik hinyzik, akkor biztos, hogy a megtallt
informci mg nem tartalmazza a teljes mRNS szekvencit. Ugyanakkor fontos szmolni azzal is, hogy egy
adott gnrl alternatv splicing folyamatoknak ksznheten tbbfle mRNS is keletkezhet. Az azonostott
s nem-trd rgikkal is rendelkez szekvencikrl meg lehet llaptani, hogy a keresett fehrje gnjnek
felelnek-e meg, vagy esetleg alternatv splicing termkek. Ha ismert a fehrje molekulatmege, akkor
ellenrizhet, hogy az azonostott szekvencirl termeld fehrje tmege megegyezne-e ezzel.
8.3.3. cDNS knyvtrak felhasznlsi terletei
A cDNS knyvtrak nagymrtkben megknnytik a vizsglni kvnt gnek fehrje kdol szekvencijnak
izollst. Az izollt cDNS szekvencik ksbb vltozatos kutatsokban, sokfle cllal felhasznlhatk. A
cDNS knyvtrakat szles krben hasznljk arra, hogy a vizsglni kvnt fehrjk gnjeit olyan formban
izolljk, ami alkalmas a fehrje expresszis rendszerben val ellltsra.
Az izollt cDNS szekvencikbl jellt prbk kszthetek. A prbk segtsgvel vizsglhat az adott gn
expresszijnak szintje klnbz szvetekben, vagy az expresszi megvltozsa klnbz kezelsek,
beavatkozsok hatsra. Ilyen prbkat szles krben alkalmaznak genomilis DNS knyvtrak szkrnelse
sorn is. gy lehetsg nylik olyan klnok azonostsra, amelyek a vizsglt fehrje gnjt szablyoz
rgikkal s intronokkal egytt tartalmazzk. gy a gn elhelyezhet az llny genomjnak fizikai trkpn,
valamint lehetsg addik bizonyos fenotpusok, pldul rkld betegsgeket markereivel val
kapcsoltsg vizsglatra. A gnszablyoz rgikkal egytt trtn izollsa lehetv teszi a gnkifejezds
szablyozsnak vizsglatt is.
8.4. Tovbbi olvasnival a fejezethez
Deaven L. L. (1992) Recombinant clones for mapping and sequencing. Los Alamos Science 20:218-249.
She K. (2003) So you want to Work with Giants: The BAC Vector. BioTeach Journal 1:69-74.
Seidman J. G. (editor) (2003) Construction of Recombinant DNA Libraries. Current Protocols in Molecular
Biology, Ch 5.
111
9. Genom projektek
A genom egy adott organizmusban megtallhat rkletes informci sszessge ami ltalban a DNS-ben,
de pl. egyes vrusok esetn az RNS-ben kdolt informci. A genom projektek olyan tudomnyos
vllalkozsok, amelyek clja, hogy egy adott organizmus teljes genomjt meghatrozzk, vagyis az
organizmus teljes DNS-t szekvenljk. A genom meghatrozsnak kvetkez rsze, hogy a genomhoz
biolgiai informcit rendelnek hozz, a genomot annotljk. Ennek sorn meghatrozzk, hogy a genom
mely szakaszai tartalmaznak fehrjk kdolsrt felels gneket, vagy egyb fontos szakaszokat (pl.
promterek, enhanszerek stb). Ebben a fejezetben bemutatjuk a teljes genomok vizsglatra irnyul
kutatsok trtnett, a legfontosabb technolgiai jtsokat, s genom projektek nhny eredmnyt.
9.1. A genomszekvenls alapjai
A genom szekvenlsa, vagyis nagyon hossz, sszefgg DNS szakaszok szekvencijnak meghatrozsa
jval komplexebb feladat, mint egy rvid DNS darab bzissorendjnek meghatrozsa. Ennek oka, hogy a
szekvenls eredmnyeknt kapott nhny szz bzispr hosszsg DNS szakaszokbl ssze kell lltani a
nagysgrendekkel nagyobb genom (az egy-egy kromoszmnak megfelel DNS molekulk) teljes
szekvencijt. Az sszelltsra alapveten kt technikt klnbztethetnk meg. Az egyik, korbban
kifejlesztett s nagyon munkaignyes technika a trkp-alap mdszer. A msik az gynevezett teljes
genom shotgun (srtes puska) mdszer, amely egyszerbb, de nagyon komoly szmtstechnikai
kapacitst ignyel. A trkp-alap mdszert szoktk fellrl-lefel (top-down) mdszernek is hvni, mivel
ebben az esetben a nagyobb egysgbl (genom vagy kromoszmk trkpezse) indulnak ki. A shotgun
mdszert ellenben alulrl-felfel (bottom-up) mdszernek is nevezik, mert a genom meghatrozsa
gyakorlatilag vakon trtnik, nhny szz bp hosszsg szekvencia rszletek (read-ek) sszeraksbl ll
ssze a genom. Nagymret genomok esetn a kt technika kombincija a leghatkonyabb.
9.1.1. Trkpezs
A trkp-alap (vagy ms szval kln-kontig) mdszer esetn a szekvenls eltt elksztik a genom
fizikai s/vagy genetikai trkpt, vagy mr meglev trkpet hasznlnak. A genom szekvenls sorn a
trkp segt a szekvenlt DNS darabok genomban trtn elhelyezsben. A fizikai trkpezs egyik
mdszere, hogy a genomot, vagy nagymret genomok esetn a genom feldarabolsval ltrehozott risi
DNS szakaszokat restrikcis enzimmel (pl. HindIII) hastjk, s a kapott darabokat glelektroforzissel
elvlasztjk. Az eredmnyknt kapott hastsi mintzat (ujjlenyomat: DNA fingerprint) elrulja, hogy
mely DNS szakaszok tartalmaznak egymssal tfed rszeket (hiszen ezeken a helyeken az ujjlenyomat
megegyezik), s ez alapjn meg lehet mondani, hogy az adott DNS szakasz hol helyezkedik el a genomban.
A fizikai trkpezs gy abszolt mdon meghatrozza, hogy egyes DNS szakaszok egymshoz kpest
hogyan helyezkednek el, s hol tallhatk (ld. 9.1. bra).
A genetikai trkpezs ezzel szemben az egyes DNS szakaszok egymshoz viszonytott relatv helyzetrl
ad informcit. Az egymshoz kzel elhelyezked gnek illetve rgik nagyobb valsznsggel rkldnek
egytt, mint az egymstl tvolabbiak. Vagyis az egymshoz kzeli DNS szakaszok rekombincis
frekvencija alacsony, mg a tvolabbiak magasabb. Tbb generci vizsglatval s megfelel DNS
markerek hasznlatval feltrkpezhet klnbz gnek egymshoz viszonytott tvolsga. Ilyen markerek
lehetnek fenotpusosan megjelen tulajdonsgok is (ld. 9.1. bra). Tipikus DNS markerek a restrikcis
fragment hosszsg polimorfizmusok (RFLP: Restriction Fragment Length Polymorphism), a szekvencia
hosszsg polimorfizmusok (SSLP: Simple Sequence Length Polymorphism), vagy az egyedi nukleotid
polimorfizmusok (SNP: Single Nucleotide Polymorphism). Az RFLP-k esetn egy restrikcis endonuklez
hastsi mintzatt vizsgljk a kt alllon. Ha ezek eltrnek, vagyis az egyik alllon hinyzik a hasthely
egy mutci miatt, az adott helyet markerknt lehet hasznlni. Az SSLP-k valamilyen ismtld
112
szekvenciarszletet tartalmaznak eltr szmban az alllokon, mg az SNP-k egy bzispr klnbsget
jeleznek (pl. az egyik alllon C, a msikon T tallhat).
9.1. bra: A genom szekvencia sszelltst jelentsen megknnyti, ha rendelkezsre ll genetikai s/vagy
fizikai trkp. A) Fizikai trkpezsre hasznlhatk restrikcis endonuklez hasthelyek. A nagymret klnok
hastsi mintzata alapjn sszellthat egy kln kontig, s az egyes szakaszok helye a genomban kijellhet. B) A
gnek s DNS markerek rekombincis gyakorisga alapjn megllapthat az egymshoz viszonytott helyzetk.
A genetikai s a fizikai trkpezs sorn kapott trkp, a kt mdszer kztti elvi klnbsg miatt, a legtbb
esetben jelentsen klnbzik (ld. 9.2. bra).
9.2. bra: A genetikai s fizikai trkp viszonya. A genetikai s fizikai trkpek nem teljesen egyformk, mert a
genetikai trkp csak a markerek egymshoz viszonytott helyzetrl ad informcit.
113
9.1.2. Genomszekvenls trkp-alap mdszerrel
A trkp-alap szekvenlskor a genomot nagymret, 40-200 kbp mret darabokra hastjk. Az gy kapott
DNS fragmentumokat ezutn olyan vektorokba klnozzk, amelyek kpesek ilyen mret szakaszokat is
befogadni. Tipikusan ilyen vektorok a BAC vektorok, de kozmidok vagy YAC vektorok is hasznlhatk
(ld. 8.2.5. fejezet). Mivel a genom hastsa vletlenszeren trtnt, a kapott DNS fragmentumok is
vletlenszeren tallhatk meg a BAC-knyvtrban, s a fragmentumok egymssal tfed szakaszokat
tartalmaznak. A kvetkez lps teht az, hogy megllaptsk, mely DNS darabok fednek t egymssal.
Ennek sorn a knyvtrban tallhat klnok ujjlenyomatt ksztik el (ld. 9.1.1.). Ha ez rendelkezsre ll,
mr meg lehet hatrozni, hogy a sok DNS fragmentumbl melyek azok, amelyeket felhasznlva fel lehet
pteni a teljes genomot. Ezt angol kifejezssel minimum tiling path-nak hvjk (magyarul a legrvidebb
kirakhat t). Miutn a fizikai trkp elkszlt, a hatalmas, mr trkpezett inszerteket tartalmaz BAC
klnokat shotgun mdszerrel szekvenljk. Ehhez a klnokat vletlenszeren tovbb daraboljk
maximum 1500 bp nagysg szakaszokra, szubklnozzk (pl. M13 fg vagy plazmid vektorba), majd
szekvenljk. A kapott szekvencikat az tfed rgik alapjn egymshoz illesztve meg lehet hatrozni az
eredeti inszertek szekvencijt, majd a trkp alapjn a teljes genomszekvencit (ld. 9.3. bra).
Az sszeilleszts termszetesen nem mindig egyszer. Ha az egyes DNS szakaszokat a rendelkezsre ll
informcik alapjn nem lehet sszeilleszteni, itt a szekvencia egy lyukat, gap-et tartalmaz. Azokat a
nagymret, trkpezett DNS szakaszokat, amelyeket az tfed klnok alapjn, gap-mentesen ssze lehet
illeszteni, kln-kontignak nevezik (a contig elnevezs a contigous, magyarul sszefgg szbl ered). A
kln-kontigok nmileg klnbznek a szekvencia kontigoktl, amikrl a kvetkez fejezetben lesz sz. Ezt
a mdszert hasznltk a srleszt (Saccharomyces cerevisiae) s a Caenorhabditis elegans nev fonlfreg
genomjnak meghatrozshoz, illetve a Humn Genom Program sorn is ezt a technikt hasznlta az egyik
kutatcsoport.
9.3. bra: A genomszekvenls mdszerei. A kln-kontig stratgia esetn a kiindul nagymret inszert helyzete
ismert a genomon bell. Ezt shotgun mdszerrel szekvenljk, majd a genomban elhelyezik. A kontigok genombeli
pozcijt a rajtuk tallhat markerek segtsgvel prbljk meghatrozni. A markerek nagyobb szma mindkt
esetben jelentsen segtheti a vgs szekvencia sszelltst.
114
9.1.3. A shotgun mdszer
A shotgun mdszer esetn elzetes, trkpezsbl szrmaz informci nlkl trtnik a szekvenls,
ezrt sokkal gyorsabb. A DNS-t itt is feldaraboljk, de jval kisebb szakaszokra. Ksztenek egy kb. 2 kbp
s egy kb. 10 kbp darabokbl ll knyvtrat. Mivel a rvidebb inszertek miatt nincs szksg specilis
vektorokra, plazmid vektorokat hasznlnak, s a vgeredmny egy sok szzezer vagy akr milli tagbl
ll plazmid knyvtr. Az gy kapott klnokat szekvenljk, s az tfed szekvenciarszletek alapjn
szekvencia-kontigokat lltanak ssze, majd a teljes genom mester szekvencijt. Fontos megemlteni,
hogy nagymret, komplex genomok esetn a vgs szekvencia sszeillesztsnl trkpek felhasznlsa
nagymrtkben segti a munkt (ld. 9.3. bra).
9.2. Egy plda: a Haemophilus influenzae baktrium
szekvencijnak meghatrozsa
Eleinte a kutatk ktelkedtek abban, hogy egyltaln lehetsges a nagyszm egyedi szekvencibl egy
teljes genomot sikeresen sszelltani. 1995-ben azonban Craig Venter s munkatrsai publikltk a
Haemophilus influenzae baktrium 1830 kb hosszsg genomjt, amelyet shotgun mdszerrel hatroztak
meg (ld. 9.4. bra).
9.4. bra: A shotgun mdszer a H. influenzaepldjn bemutatva. A baktriumbl izollt genomilis DNS-t
szoniklssal daraboljk, majd agarz glelektroforzissel elvlasztjk, hogy 1,6-2 kb nagysg darabokat tudjanak
izollni. Ezekbl kszl a kln knyvtr, amelybl nagyszm, vletlenszeren kivlasztott klnt szekvenlnak. A
szekvencia kontigok sszeillesztsvel kszl el a genom teljes szekvencija.]
A genom szekvenlsnak els lpseknt a baktrium DNS-t szoniklssal (magas frekvencij
hanghullmok segtsgvel) kis darabokra trtk. Az gy kapott DNS szakaszokat elektroforetizltk, s 1,6-
2 kb nagysg darabokat izolltak, majd klnoztak, ltrehozva a plazmid knyvtrat. Ezutn sszesen
19.687 klnt vletlenszeren kivlasztva 28.643 szekvenlst vgeztek, melynek sorn nhny szz bzispr
115
hosszan tudtk leolvasni az egyes klnok szekvencijt (vagyis nem az egsz kln bzissorrendjt
hatroztk meg, csak a klnok vgt) . Tbbnyire egyetlen irnybl trtnt a szekvenls, azonban a
szekvenlsok krlbell egyharmadt a klnok msik vgrl is elvgeztk (lsd 19.687 kln s kb. 30%-
kal tbb szekvenlsi reakci). Ez a megolds komoly segtsget jelentett a teljes szekvencia
sszelltsban. Az sszes szekvenlsi reakci 16%-t sikertelennek tltk, mert a kapott szekvencia
kevesebb, mint 400 bzisprt tartalmazott. A maradk 24.304 szekvenls vgl 12.631.485 leolvasott
bzisprt jelent, ami mintegy hatszorosa a H. influenzaegenomjban tallhat sszes bzisprnak.
Ekkora rhagys (~6x) szksges is ahhoz, hogy teljes lefedettsget lehessen elrni a genom
meghatrozsakor. Ezek utn kvetkezett a kapott szekvencik sszeillesztse, vagyis a rvid szekvenlt
DNS szakaszok tfed rszeit felhasznlva a szekvencia-kontigok sszelltsa, ami a szmtstechnika
akkori fejlettsgt figyelembe vve, komoly feladat volt. A konkrt ksrletben 30 rn keresztl dolgozott a
szmtgp, s vgl 140 szekvencia-kontigot sikerlt meghatrozni.
Termszetesen ezek utn a feladat a kontigok kztti lyukak betmse. A hinyz DNS szakaszok egy
rszt viszonylag egyszeren meg lehetett hatrozni. Ehhez jra vgignztk (szkrneltk) a knyvtr sszes
klnjt, s olyan klnokat keresetek, amelyekben egyszerre tallhat meg kt klnbz kontig
vgszekvencija. Ekkor ugyanis elegend volt vgigszekvenlni az egsz klnt, s meg lehetett hatrozni a
hinyz rszletet a kt kontig kztt. Ezzel a mdszerrel a 140 lyukbl 99-et sikerlt is betmni. Mg
mindig maradt 42 lyuk, amelyet meg kellett szntetni. Mivel valsznleg a lyukakat tartalmaz DNS
szakaszok nem voltak jelen a knyvtrban (mert instabil klnokat eredmnyeztek), j knyvtrat hoztak
ltre, -fg vektort hasznlva. A 42 gap szlein tallhat szekvencikat felhasznlva 84 oligonukleotidot
szintetizltak, amelyekkel vgigprbltk az j knyvtrat. Ha egy klnhoz kt oligonukleotid hibridizlt,
akkor azt vgigszekvenltk, mivel az adott klnnak tartalmaznia kellett kt kontig kztti szekvencit.
Ilyen mdon tovbbi 23 lyukat sikerlt betmni (ld. 9.5. bra).
9.5. bra: A genom szekvenls befejez lpse a szekvencia javtsa s a lyukak eltntetse. A) A szekvencia
lyukak javtsra a knyvtrban megtallhat klnok kzl azokat lehet hasznlni, amelyek kt kontig
vgszekvencijt tartalmazzk. B) Fizikai lyukak esetn a mg nem sszelltott kontigok vgszekvencijrl
szintetizlnak primereket, s ezeket egy teljesen j knyvtr klnjaihoz hibridizltatjk. Az ugyanazon klnhoz
hibridizl primerek jelzik, hogy az adott kln tartalmazza a hinyz szekvenciarszletet (bal oldali panel). A msik
lehetsg, hogy az oligonukleotidokat prba lltva sok PCR-t vgeznek, s a keletkez termket szekvenljk.
116
A hinyz szakaszok meghatrozshoz ugyanezt a 84 oligonukleotidot hasznltk. Egyrszt
vletlenszeren sszeprostottk az oligonukleotidokat, majd PCR elvgzsvel megnztk, hogy kapnak-e
termket a H. influenzae genomjt templtknt hasznlva. Ha igen, akkor a PCR termk szekvenlsval
meg lehetett hatrozni egy-egy hinyz DNS szakaszt. Mivel a lehetsges oligonukleotid prok szma tl
magas lett volna ahhoz, hogy mindegyiket mindegyikkel kiprbljk, egy msik mdszert is alkalmaztak. A
primereket olyan H. influenzae DNS szakaszokhoz hibridizltattk, amelyeket a genom restrikcis
endonuklezzal trtn emsztsvel lltottak el. Azon oligonukleotidok, amelyek azonos restrikcis
fragmentumhoz ktdnek, nagy valsznsggel egymshoz kzeli DNS szakaszokhoz tartoznak. Az gy
kapott primerprokkal PCR-t vgeztek, majd a termket szekvenltk. Vgl az sszes hinyz DNS
szakaszt sikerlt meghatrozni, s ezzel megszletett a H. influenzae teljes genomja (ld. 9.6. bra).
A fenti pldval sikerlt bebizonytani, hogy a shotgun stratgia mkdkpes s nincsen szksg elzetes
informcira a genomrl ahhoz, hogy a szekvencijt meg lehessen hatrozni. Az azta eltelt vek sorn
ezres nagysgrend prokarita szervezet genomjt szekvenltk, kztk olyan fontos patognekt, mint pl. a
TBC-t okoz Mycobacterium tubercolosis, vagy a kolera, a tdgyullads, az anthrax (lpfene)
krokozjt. A kapott genomszekvencik alapjn meghatrozhatk a krokozk gnjei ltal kdolt
fehrjk, s j terpis megoldsok kidolgozsra nylik lehetsg.
9.6. bra: A H. influenzae genomtrkpe.
9.2.1. A lefedettsg (coverage) jelentsge
A H. influenzae ltal bemutatott pldn mr emltettk, hogy az sszes megszekvenlt bzispr krlbell
hatszorosa volt a baktrium teljes genetikai llomnynak. ltalnossgban elmondhat, hogy a szubkln
knyvtrak ltrehozsnak fontos szempontja, hogy a klnok szma optimlis lefedettsget (coverage)
vagy ms szval tbbletet (redundancy) biztostson. A kt kifejezs arra utal, hogy a szekvenls sorn az
eredeti genom mretnl jval nagyobb szm bzispr meghatrozsra van szksg ahhoz, hogy a teljes
genom reprezentlva legyen. A lefedettsg jellemzsre egy szmot szoktak megadni. Az 1x lefedettsg nem
jelenti azt, hogy a teljes genom minden rgija szekvenlsra kerlt. Mivel a kln knyvtrakbl
vletlenszeren kerlnek kivlasztsra a szekvenland klnok, elfordul, hogy ugyanazt a szakaszt
tbbszr is megszekvenljk, mg ms rgik teljesen kimaradhatnak. A kutatk jellemzen 6x-10x
lefedettsget alkalmaznak, ezzel biztosthat, hogy a genom 99,8-99,99%-a legyen szekvenlva. Tovbbi
elnye a nagy feleslegnek, hogy gy megnvekszik az tfed szekvencik szma, ami a kontigok
sszelltsban jelent komoly segtsget.
117
9.2.2. Paired-end szekvenls
Ugyancsak a H. influenzae pldjn lttuk, hogy a szekvenlsi reakcik szma nagyobb volt, mint az sszes
kivlasztott kln szma, mert a szekvenlsok krlbell egyharmadt a msik irnybl is elvgeztk. A
szekvencia read-ek egymshoz rendelse, egymssal val sszekapcsolsa komoly feladatot jelent, s
rengeteg hibalehetsget is rejt magban, elg csak pldul az ismtld szekvenciarszletek okozta
problmkra gondolni. A knyvtrakat gy hozzk ltre, hogy az ezekben tallhat DNS szakaszok
krlbell egyforma hosszsgak legyenek. A paired-end szekvenls sorn a klnoz vektor mindkt
vge fell kszl egy szekvencia. Ennek hatalmas elnye, hogy mivel az adott DNS szakasz hossza ismert,
azt is tudni lehet, hogy a kt read milyen tvolsgra van egymstl. A teljes szekvencia sszelltsa sorn
figyelembe tudjk venni ezt a tvolsg informcit, gy ha egy paired-end szekvenlsi reakci kt termkt
a szmtgp egymstl szzezer bzisprra helyezi, akkor egyrtelmen kiderl, hogy hiba trtnt az
egymshoz rendels kzben (ld. 9.7. bra).
9.7. bra: Paired-end szekvenls. A 2-3 kb hosszsg klnok vgeirl nhny szz bp hosszsg read-ek
kszlnek. Ha mindkt oldalrl szekvenljk a klnokat, akkor az ellenttes oldali szekvencik kztti tvolsg
krlbell megegyezik, feltve, hogy nagyjbl egyforma hosszsg inszerteket szekvenlnak. Ez az informci
felhasznlhat a szekvenciarszletek sszeillesztsekor.
9.3. A Humn Genom Projekt (HGP)
A molekulris biolgia rendkvl gyors fejldsnek egyik legjobb pldja a Humn Genom Projekt, amely
nem kisebb clt tztt ki maga el, mint meghatrozni a teljes emberi genomot. 1953 prilisban jelent meg
a DNS szerkezett ler publikci James Watson s Francis Crick szerzsgvel a Nature-ben, s a
hetvenes vek kzepn fedeztk fel a DNS szekvenls technikjt. Alig harminc vvel ksbb pedig
meghatroztk a teljes emberi genomot. rdekessg, hogy Watson 1990-ben a Humn Genom Projekt
vezetje lett s 1992 prilisig dolgozott ebben a pozciban. (Azrt mondott le ilyen gyorsan, mert
sszeklnbztt a fnkvel a gnek szabadalmaztatsnak gyben. Watson llspontja az volt, hogy a
projekt sszes eredmnyt szabadon elrhetve kell tenni.) A gyors technikai fejlds azt is lehetv tette,
hogy a projekt az eredetileg tervezettnl kt vvel korbban befejezdhessen. A mikrobilis genomok
tlagosan 3 milli bp-bl llnak, mg az emberi genom ennl hrom nagysgrenddel tbb, mintegy 3
millird bp-t talrtalmaz. A Humn Genom Projekt tizenhrom ven keresztl zajlott, s 2003-ban zrtk le.
A projekt cljt az albbiakban hatroztk meg:
1. A humn DNS sszes gnjnek (a korbbi becsls ~100.000 volt, a mai ismert szm <23.000)
azonostsa.
2. A humn DNS nagyjbl 3 millird bzisprjnak meghatrozsa.
3. A kinyert informcimennyisg adatbzisban trtnt trolsa.
4. Az adatfeldolgozsi eljrsok korszerstse.
5. A projekt sorn ltrehozott illetve korszerstett technolgik tadsa a magnszektornak.
6. A felmerl etikai, jogi s trsadalmi krdsek tisztzsa.
118
9.3.1. Nehzsgek a humn genom vizsglatban
Mr a projekt legelejtl vilgos volt, hogy a biolgiai tudomnyok eddigi legnagyobb volumen s
rengeteg technikai nehzsggel jr munkjba vgnak bele. Az els nehzsg mindjrt a vizsglni kvnt
genom mrete volt, amely tbb nagysgrenddel meghaladta a korbban vizsglt genomok mrett. Msik
komoly nehzsg volt az ismtld szekvencik jelenlte.
Egyrszt a DNS-polimerz nem olvassa le a teljes szekvencit, megakad vagy tugrik szakaszokat, ha tl
sok A s T vagy G s C kveti egymst akr tbb szz nukleotidon keresztl. Mg komolyabb problmt
jelentenek a hosszabb (a szoksos 500 bp-os leolvasott szekvencia szakaszoknl hosszabb) ismtld rgik,
hiszen ezek egymstl megklnbztethetetlenek. Duplikcik esetn az is elfordulhat, hogy az
sszeilleszts csak egyszer veszi figyelembe az adott szekvenciarszletet, s gy a vgs szekvencia
sszeomlik, rvidebbnek addik, mint a valsgban (ld. 9.8. bra). Mindezen problmk miatt a kutatk
fontosnak tartottk, hogy j minsg genetikai s fizikai trkpek kszljenek a humn genomrl.
9.8. bra: A kontigok sszeillesztsnek problmi. Ha a genom hossz ismtld szekvencikat tartalmaz, mint
pldul egy 7 kb hosszsg LINE szegmens (long interspersed element), az ismtld rszletek egymstl nehezen
megklnbztethetk a szekvencia kontigok sszeillesztse sorn. A rossz egymshoz rendels eredmnye a
szekvencia sszellts sszeomlsa lehet, amikor az egymshoz tartoz, de kt LINE rgit tartalmaz szakasz
helyett kt klnbz kontigot llt ssze a szoftver, s a duplikci eltnik.
9.3.2. Elindul a HGP
A teljes humn genom vizsglatnak tlete a 80-as vekben merlt fel komolyabban, mikor lehetv vlt a
DNS automata szekvenlsa. 1987-ben az Egyeslt llamok Energia Hivatala (U.S. Department of Energy)
rszvtelvel indult el egy korai genom projekt, amelynek clja a radioaktv sugrzs hatsnak vizsglata
volt, klns tekintettel arra, hogyan lehet megvdeni a genomot a mutagn hatsoktl. Tovbbi
megbeszlsek kvetkeztek, melyben mr az NIH (National Institute of Health) is rszt vett, s a kt
kutatkzpont kzs erfesztsnek eredmnyeknt 1990 oktberben hivatalosan is elindult a HGP.
Szinte azonnal nemzetkzi egyttmkds alakult ki, amiben Anglia, Nmetorszg, Franciaorszg, Kna s
Japn is rszt vett, kialaktva a Humn Genom Konzorciumot. Br a projekt indulsakor mg sok kutat
komoly ellenrzssel szemllte a munkt, megkrdjelezve az egsz projekt hasznossgt, mr a 90-es vek
kzepre jelents mennyisg adatot sikerlt gyjteni. A humn genom egyes rszeinek fizikai trkpe
mellett humn s egr genetikai trkpek szlettek, nagyszm cDNS szekvencia, s teljes bakterilis
genom szekvencik vltak elrhetv. Kialakult a genomika tudomnya. rdekessg, hogy James Watson
119
mr a projekt legelejn felhvta a figyelmet arra, hogy a megszlet eredmnyeknek jelents bioetikai,
szocilis hatsi lehetnek. Ezrt a projekt sszkltsgvetsnek elszr hrom, majd ksbb t szzalkt az
ezzel kapcsolatos kutatsokra fordtottk.
9.3.3. Megjelenik egy versenytrs
1998-ban Craig Venter (aki a H. influenzae genom projektet is vezette) bejelentette, hogy Celera Genomics
nven ltrehoz egy vllalatot, ami 2-3 ven bell vgez a teljes humn genom szekvenlsval. Tervk
szerint shotgun mdszert alkalmaznak, s gy el tudjk kerlni az id s pnzignyes trkpezst. Nem csak
gyorsabban, de olcsbban is dolgoznak: a 3 millird dollros llamilag finanszrozott projekttel szemben 300
milli dollros kltsgvetst tartott relisnak. sszessgben a kialakult verseny jt tett a teljes HGP-nek.
Mindkt kutati csapat nagy erfesztseket tett, hogy minl hamarabb elkszljn az els draft, vzlatos
szekvencia. Ebben a legnagyobb nehzsget a fentebb mr emltett szekvencia sszeilleszts okozta.
Mindkt csoportnak sikerlt olyan algoritmusokat kidolgozni, amik a korbbinl jval nagyobb
hatkonysggal tudtk az egybefgg szekvenciarszleteket sszelltani. A Celera kutati hamarosan
publikltk a Drosophila melanogaster vzlatos szekvencijt, megmutatva, hogy a shoutgun mdszernek a
bakterilis genomoknl jval nagyobb mret genomok esetn is van ltjogosultsga.
9.3.4. A humn genom vzlatos (draft) szekvencija
A HGP egyik legfontosabb mrfldkve egy 2000 jniusban tartott sajtkonferencia volt, ahol a Humn
Genom Konzorcium s a Celera egytt mutatta be a humn genom els vzlatos szekvencijt A humn
genom projekt ekkor mg messze volt attl, hogy ksznek lehessen tekinteni. Az eukromatinnak, vagyis a
kromatin gnekben gazdag rsznek krlbell 90%-a volt megtalhat a bejelentett szekvenciban, de sok
hibval s nagyon sok gap-pel. A kt szekvencit 2001 februrjban publikltk. A Humn Genom
Konzorcium a Nature-ben, a Celera Genomics pedig a Science-ben, mivel utbbi nem volt hajland a teljes
szekvencit teljesen elrhetv tenni, amibe pedig a Nature szerkeszti nem egyeztek bele. Br mindkt
szekvencia ersen hinyos volt, mgis rengeteg j informcit tartalmazott. Sok jdonsg derlt ki az
ismtld szekvencik s a gnek genomon belli elhelyezkedsrl, illetve fny derlt arra is, hogy a
korbban elrejelzett 100 000 helyett csak alig 23000 gn tallhat meg a humn genomban, krlbell
annyi, mint az ecetmuslica genomjban.
9.3.5. 2003-ra elkszl a szekvencia
A draft szekvencik elkszlte utn a feladat a hibk kijavtsnak s a lyukak betmsnek sziszifuszi
munkja volt. A hibajavtsban nagy segtsget jelentettek a klnbz megoldsokkal kszlt trkpek.
Egyedi DNS markereket kerestek, amiket a trkpekbl szrmaz informcikkal sszeprostva meg
lehetett llaptani, hogy egyes kontigok mely ms kontigokkal kapcsoldnak ssze. A H. infulenzae
lersnl emltett mdszereket is alkalmaztk a lyukak betmsre. Voltak olyan gap-ek is, amelyek ppen
egy paired-end mdszerrel szekvenlt 3kb-os kln kzepre estek. Ebben az esetben primer walking
mdszert alkalmaztak, vagyis a kln kt vgn tallhat, nagyjbl 500bp-os mr megismert szekvencira
terveztek egyedi oligonukleotidokat. Megszekvenltak mg 500 bp-t, majd jabb olgonukleotidokat
terveztek, s gy vgigstlva az adott klnon annak szekvencija ismertt vlt. Az egyes javtsok utn
jabb s jabb szakaszok vltak teljess, amit megint jabb javtsok kvethettek a kapott j szekvencia
informcik alapjn. Ezzel az iteratv, az elz eredmnyekre pl mdszerrel vgl sikerlt megalkotni
egy majdnem teljes, j minsg genom szekvencit.
A projekt 2003-as befejezsre az eukromatin 99,3%-rl llt rendelkezsre szekvencia informci, s a
2001-es, teht a draft szekvencia bejelentsekor mg meglev 145 514 lyukat mindssze 281-re sikerlt
120
leszortani. A ksz szekvencia bejelentse 2003. rilis 25-n trtnt meg, ppen 50 vvel a hres Watson s
Crick publikci megjelense utn.
9.3.6. A szekvenls technikjnak fejldse
A Humn Genom Projekt sikerhez nagyban hozzjrult, hogy az vek sorn a DNS szekvenls technikja
is jelents fejldsen ment t. A fluoreszcens technika s az automata szekventorok megjelense
komoly elrelpsnek szmtott a korbbi manulis technikhoz kpest, hiszen nem kellett radoaktvan jellt
nukleotidokat s az elhvshoz rntgenfilmet hasznlni. Mindez azonban nem lett volna elegend egy ilyen
nagyszabs projekthez, mert a teljes humn genom szekvenlshoz krlbell 1 milli glelektroforzist
kellett volna vgezni, mindegyik glen 48 szekvenlsi reakcival. Az ttrst a kapillris elektroforzisen
alapul technika hozta meg, amely jval hatkonyabbnak bizonyult, mert gy nem volt szksg akrilamid
glekre a szekvenlshoz. A 2001-ben bemutatott msodik genercis szekvenl kszlkek tovbb
nveltk a hatkonysgot, napjainkra pedig a harmadik vagy kvetkez genercis kszlkek s az j-
genercis szekvenlsi eljrsok (ld. 5.3. fejezet) bizonytjk, hogy egszen olcs s gyors is lehet a teljes
genom szekvenlsa.
9.3.7. Etikai krdsek avagy kinek a DNS-t hasznltk a szekvenlshoz?
Ahogy korbban emltettk, mr a projekt legelejn felmerlt, hogy a HGP komoly etikai, jogi s szocilis
vonatkozsokkal is rendelkezik. Az egyik legels fontos etikai krds az volt, hogy kinek a DNS-t
hasznljk a szekvenlshoz, illetve hogyan kezeljk a szekvenls sorn keletkez bizalmas adatokat. A
Humn Genom Konzorcium munkatrsai klnsen nagy hangslyt fektettek arra, hogy teljesen anonim
legyen a szekvencia, s mg utlag se lehessen visszakvetni, hogy kinek a DNS-t hasznltk a munkhoz.
Ehhez pldul a mr eredetileg is anoniman kezelt DNS mintk kzl 10-bl egyet vlasztottak ki,
amelyekrl eltvoltottak mindenfajta jelzst. Mra annyit lehet tudni, hogy a HGP sorn meghatrozott
genomszekvencia 70%-a egy donortl, mg a maradk 30% tbb klnbz donortl szrmazik. A
Celera Genomics is anonim mdon tervezte kezelni a mintkat. Huszonegy, klnbz etnikai csoporthoz
tartoz donortl szrmaz mintbl vletlenszeren vlasztottk ki a tnylegesen felhasznlt DNS-t. A
Celera akkori vezetje, Craig Venter a vllalattl trtnt tvozsa utn bevallotta, hogy varilt a mintkkal,
s az DNS-e volt az egyik, amit a munkhoz hasznltak. Bejelentette, hogy a szekvencia alapjn
szvbetegsgre s Alzheimer-krra van hajlama. A tudomnyos kzvlemny rendkvl etiktlannak tartotta
az eljrst, mert ugyan Venter-nek joga van ahhoz, hogy a vilg el trja a sajt DNS-szekvencijt, ezzel a
rokonairl is bizalmas informcikat tesz kzz, amihez azok nem jrultak hozz. Br Venter szerint az
pldja megmutatja, milyen fantasztikus eszkz a sajt genetikai informcink ismerete (aminek hatsra
egybknt azta tbb testmozgst vgez s ditzik), egyben arra is rvilgt, milyen komoly etikai, s az
egynek letre kzvetlenl kihat problmkat vet fel a genom szekvenls. Klns tekintettel arra,
hogy a szekvenls technolgijnak fejldse hamarosan elhozza az 1000 dollros genom idszakt,
amikor gyorsan s olcsn lehet meghatrozni az egyes emberek teljes genetikai llomnyt. (Valjban azt
is mondhatjuk, hogy ez a korszak el is rkezett. Van mr olyan amerikai cg, amely pontosan 1000 dollr
ellenrtkeknt brki teljes exom-jt, azaz a teljes fehrjekdol DNS szekvencit elkszti; a teljes
eukromatint tartalmaz genom pedig 1500 dollrba kerl).
9.4. Tovbbi genom projektek
A szekvenlsi technikk fejldsvel, ami a genom meghatrozs idejt s kltsgt egyarnt jelentsen
cskkentette, tovbbi genom projektek megvalstsra nylt lehetsg. Ezek kzl rdemes megemlteni a
Csimpnz genom projektet, aminek clja, hogy ssze lehessen hasonltani a femlsk s az ember
genomjt, s ezltal tbbet tudjunk meg arrl, mi klnbzteti meg az embert ms fajoktl. Klnsen
rdekes vllalkozs volt a Neandevlgyi ember genom projekt, aminek clja fosszlikbl meghatrozni a
121
neandervlgyi ember genomjt. A draft szekvencit 2010-ben kzltk a Science-ben, s ez alapjn a genom
99,7%-a megegyezik a Homo sapiens-vel (mg a csimpnz esetn ez 98,8% volt). A neandervlgyi
projektben a legnagyobb nehzsget a mintk kezelse jelentette, hiszen a fosszlik egyrszt nagyszm
mikrobval szennyezettek, msrszt a fosszlikkal kapcsolatba kerl kutatk DNS-e is beszennyezhette
ket. A kutatk szerint azonban ezek a problmk jl kezelhetk, s pl. az emberi szennyez DNS mrtke
nem tbb, mint 1%. A genom projektek jvje az egyes fajokon bell minl tbb egyed genetikai
llomnynak meghatrozsa, amellyel kzelebb juthatunk az egyedek kztti genetikai diverzits jobb
megrtshez. (Az egyni humn genomok kztt az elsk kztt szekvenltk James Watson-t).
9.5. Tovbbi olvasnival a fejezethez
Fleischmann RD, Adams MD, White O, Kirkness EF, et al. (1995) Whole-genom random sequencing and
assembly of Haemophilus infulenzae Rd. Science 269: 496-512.
Bentley DR (1996) Genomic sequence information should be released immediately and freely in the public
domain. Science 274: 533-534.
International Human Genome Sequencing Consortium (2001) Initial sequencing and analysis of the human
genome. Nature 409 (6822): 860921.
Venter, JC et al. (2001) The sequence of the human genome. Science 291 (5507): 13041351
Wolfsberg TG, Wetterstrand KA, Guyer MS, Collins FS and Baxevanis AD (2003) A users guide to the
human genome. Nat. Genet. 35: 4.
Green RE, Krause J, Briggs AW et al (2010) A draft sequence of the Neandertal genome. Science 328
(5979): 71022.
122
10. Bevezets a bioinformatikba
A biolgia, klnsen a molekulris biolgia 20. szzad vgi s 21. szzadi fejldse elkpzelhetetlen lett
volna megfelel informatikai httr nlkl. Egyedl a szmtgpek kpesek ugyanis ttekintheten trolni
azt a hatalmas mennyisg adatot, ami a biolgiai polimerek szerkezetnek s mkdsnek megrtshez
szksges. Ugyanezek a szmtgpek teszik lehetv a genomok automatikus sszelltst, gnek
azonostst, a nukleinsavak s fehrjk tulajdonsgainak jslst vrl-vre egyre nagyobb pontossggal.
A szmtgpeket sszekapcsol vilghl segtsgvel a publikcik, ksrletes eredmnyek, a genomok,
gnek, nukleinsavak s fehrjk adatai ma mr brhonnan elrhetek. Ezen fell szmos, szabadon
hozzfrhet program ll rendelkezsre az interneten, amelyekkel nagyon knny molekulris biolgiai
elemzseket vgezni. A kzvetett informcikon alapul jslat termszetesen nem helyettesti a pontos
mrsi eredmnyeket. Ennek ellenre, a molekulris szint ksrletek tervezshez s rtkelshez a
megfelel teljestmny s trol kapacits szmtgpek ma mr nlklzhetetlenek.
10.1. Bioinformatikai adatbzisok
10.1.1. Bibliogrfiai gyjtemnyek
Az olvasban els krdsknt bizonyra felmerl, hogy mi lehet az internetes oldalak haszna a biolgiai
kutats szmra. A vlasz igen sokrt. A legnagyobb elny a ksrletes adatokhoz val szabad hozzfrs
akr teljes cikkek alakjban, akr elemi adathalmazok formjban. Mieltt hozzkezdnk brmilyen
ksrletsorozathoz, azt ltalban jelents tervezi munka kell, hogy megelzze. Ebben az els s
legfontosabb forrsunk az irodalomban mr publiklt eredmnyek lesznek. A vilg legnagyobb ilyen
irodalmi adatbzisa az amerikai NCBI (National Center for Biotechnology Information) PubMed nev
gyjtemnye. A keresprogramja nem tl ltvnyos, de nagyon intelligens: kereshetnk kulcsszavakra,
szerzk, vagy folyiratok szerint is. Az egymsra hivatkoz, rokon cikkeket ssze is fzi a keresprogram (a
"related" oszlopban tekinthetk meg). Mindemellett egyb keresk, kztk a Google Scholar keresfellet
hasznossgt sem szabad lebecslni, ha irodalmat kutatunk. A mr lert eredmnyek ismerete mr csak azrt
is fontos, hogy ne ismteljk meg feleslegesen a mr jl ismert tnyeket bizonyt ksrleteket, illetve hogy
ne lltsunk fel elvben is megvalsthatatlan ksrleti terveket.
10.1.2. DNS szekvencia-adatbzisok: GenBank s Ensembl
Egy molekulris biolgiai laboratrium mindennapi munkja szmra az egyik legfontosabb forrsknt a
gnek s fehrjk pontos kpletei, azaz szekvencii szolglnak. Az ezeket trol s interneten
hozzfrhet gyjtemnyeket nevezik elsdleges szekvencia-adatbzisoknak. Az ismert fajokbl nyert
elsdleges genetikai informci hrom nagy nemzetkzi oldalon frhet hozz: Ilyen az NIH intzmnye, az
NCBI ltal fenntartott GenBank adatbzis (USA), az EMBL (European Molecular Biology Laboratory)
gyjtemnye, az ENA (European Nucleotide Archive) illetve a DDBJ (DNA Data Bank of Japan)
adatbankja. A gyakorlatban leginkbb a GenBank adatbzist szoktuk hasznlni. Itt a genomikus adatokon
tl cDNS informcikat is trolnak. A cDNS szekvencikat knnyen lefordthatjuk aminosav
szekvencikra, de a klnozsi feladatokhoz is elengedhetetlen az ismeretk. A primerek tervezshez is
ismerni kell a cDNS pontos szekvencijt, akr a nem kdol szakaszokat is belertve. A GenBank
adatbzisa lehetv teszi a gnek ltvnyos megjelentst is: ez a Map GeneViewer, amely a Google
trkpek szoftveres felletn alapszik (ld. 10.1. bra).
123
10.1. bra: Az NCBI grafikus nzeget fellete, a GeneViewer. A humn MEF2A gn rszlete
A kijellt gnszakaszt felnagytva (zoom) lthatv vlik az egyedi nukleotid sorrend. A program kln
jelli az mRNS-re trd szakaszokat (az sszes ismert varinst), s nemcsak az exonokat, de azok pontos
aminosav-fordtst is megadja. St, mg a fiziolgis varinsokat (polimorfizmusokat) s a patolgis
mutcikat is jelli. Ez azonban nem az egyetlen genom-vizualizcis program.
Az eurpai Ensembl genom-adatbzis (amely fleg gerincesek s nhny modell gerinctelen llny teljes
genom szekvenciit tartalmazza) internetes fellete szintn knnyen kezelhet. Az utbbi elnye, hogy
tartalmazza pldul a gnekben az eddig lert potencilis mRNS szekvencikat (azokat is, amelyekrl nem
trtnik fehrjeszintzis), az ismert epigenetikai mdostsokat, tovbb rengeteg bioinformatikai jslssal
(predikci) kapott informcit is.
10.1.3. Fehrje-szekvencia adatbzisok: UniProt
A nukleotidokkal ellenttben, a jelenleg ltez legjobb fehrje adatbzis nem az USA-ban tallhat, hanem
Eurpban. Ez nem ms, mint a svjci UniProt gyjtemnye. Ezen adatbank nemcsak a sokfle elrejelz
programnak ksznheti kivlsgt, hanem az adatok manulis feldolgozsnak is. Az adatbzisban mdunk
van a fehrjk neve (akr szinonimk) vagy azonostja alapjn kutatni. A UniProt adott fehrji szekvencia
hasonlsg alapjn, a BLAST programmal is megkereshetek (ld. 10.2.3. fejezet). A bennnket rdekl
tallatokat a kijellsk utn ktegelve ("batch") is letlthetjk, tovbbi analzis cljbl. A szekvencik
FASTA formtumban fognak megjelenni: ktelez ">" jel utn a fejlc-sor tartalmazza a szekvencia
azonostjt, a fehrje nevt, s az organizmus nevnek betkdjt. A msodik sortl kvetkezik csak a
tnyleges aminosav sorrend, egybets kdban.
A UniProt azonban nem csak a fehrjk szekvencijt adja meg: az egy gnhez rendelhet klnfle
(alternatv splicing s alternatv inicici kvetkeztben keletkez) izoformk is kzs oldalon tallhatak (a
klnbsgekre az oldal kln felhvja a figyelmnket). Ezenkvl informcit kapunk a ksrletesen
azonostott ktpartnerekrl, az egyes szerkezeti elemekrl, s msodlagos (poszttranszlcis)
124
mdostsokrl is. A weboldalak rengeteg hasznos, direkt hivatkozst is tartalmaznak, ms adatbzisokra,
pldul a gn, mRNS s a trszerkezet kapcsn (ld. 10.2. bra).
10.2. bra: Az UniProt adatbzis egy oldala. A human ciklin C (CCNC) fehrje adatai
10.1.4. Az "omikk" vilga. Fajonknti adatbankok.
Az eddig emltett nhny adatbzis csupn plda a molekulris biolgiai kutatsi terletek egyedi
adatgyjtemnyeire. Az ilyen terletek neveit divatos szval "-omika" vgzdssel szoks elltni (s a mra a
biolgiai kutatsok egyik f irnyv vlt rendszerbiolgia rszt kpezi), magt az adathalmazt pedig
(etimolgiailag nem teljesen helyes mdon) "-om" vgzdssel. A genomika a genomok vizsglatnak
tudomnya, a transzkriptomika az trt nukleotidok (mRNS), a proteomika a fehrjk. Ezenkvl
beszlhetnk tbbek kztt epigenomikrl (DNS-mdostsok), metabolomikrl (anyagcsere
kztestermkek), lipidomikrl. Ezen rsztudomnyok szmra kln adatbzisok is rendelkezsre llnak.
Pldul a kinom (ami az sszes protein-kinz enzimet jelli) rszletes lersra ott vannak a KinBase vagy a
PhopsphoSitePlus adatbzisok. Hasonlan, a glikom az sszes biolgiailag rdekes sznhidrtot jelli
(amivel a glikomika tudomnyterlete foglalkozik), kln adatbzisokkal (ilyen pldul a cukorlnc
szerkezete alapjn kereshet GlycomeDB). A lipideket kutat szakemberek szintn sajt adatbankokat
hasznlhatnak (pl. Lipidmaps), amire elssorban a poliketidek nagy variabilitsa miatt van szksg. Az
anyagcsere-utak nyomon kvetsre pedig ott a jl ismert KEGG (Kyoto Encyclopedia of Genes and
Genomes), amely enzimenknt s lpsenknt tekinti t az egsz intermedier anyagcsert, interaktv
trkpekkel. Szak-adatbzisokat azonban nem csak az egsz lvilgot ttekint, integratv jelleggel hoztak
ltre. Lteznek egy-egy modell-organizmusra fkuszl genetikai, proteomikai, s egyb ksrletes adatokat
sszest adatbankok is. Ilyen pldul a Caenorhabditis elegansra fkuszl WormBase, a Drosophila
melanogaster (ecetmuslica) molekulris biolgijt taglal FlyBase, vagy a Saccharomyces cerevisiae
(srleszt) genetikjval foglalkoz SGD adatbzis. Ezek az oldalak sszehasonltsokkal is szolglnak: az
Interactive Fly pldul a rovaroktl emberig konzervlt fehrje-rendszerek mkdsnek az egyik ltez
legjobb lerst adja.
125
10.1.5. Szerkezeti s funkcionlis adatbzisok
Az elz alfejezetben lttuk, hogy adatbzisokat nem csak az elsdleges DNS vagy fehrjeszekvencikbl
lehet ltrehozni. Rengeteg gnrl (illetve annak fehrjetermkrl) llnak rendelkezsre a szekvencin
messze tlmutat szerkezeti s mkdsi adatok. Sok fehrje harmadlagos szerkezett is mr meghatroztk.
Ezeket (de a nukleinsavakt is) a Protein Data Bank (PDB) adatbzis sszesti. A PDB valjban hrom
nagy szerkezeti genomikai kezdemnyezs (USA, EU, Japn) koopercijval jtt ltre; clja, hogy a
makromolekulk trszerkezetei minden kutat szmra szabadon elrhetek legyenek. Ennl persze sokkal
feldolgozottabb (msodlagos) adatbzisok is lteznek. A fehrjk szerkezettel br domnjeit a legtbb
esetben elegend egy egyszer doboz-modellel brzolni. Ilyeneket tallunk a SMART (Simple Modular
Architecture Research Tool) msodlagos adatbzisban, amely nevnek megfelelen nagyon intelligens
keresvel rendelkezik: a megkeresett fehrjben automatikusan bejelli az ismert domneket, az intron-exon
hatrokat, st mg listzza a nagy vonalakban hasonl domn felpts, rokon fehrjket is (ld. 10.3. bra).
10.3. bra: A SMART adatbzis rszlete. A human PSD-95 idegi szinapszis-szervez fehrje domn felptse.
Ha csak a fehrje-fehrje klcsnhatsokra vagyunk kvncsiak, erre is szmos, kivl weboldal ll
rendelkezsnkre. Ilyenek az IntAct vagy a BioGRID; de az egyik legltvnyosabb (mind adatok, mind
grafika tekintetben) a STRING adatbzis (ld. 10.4. bra). Ez a klcsnhatsokat, a SMART elemzseit,
st, a hromdimenzis szerkezeteket is egyetlen hatalmas grf-modellbe integrlja. Minden esetben md van
szrk belltsra: ha pldul csak a ksrletekkel megerstett klcsnhatsok utn rdekeldnk, a nagy
teresztkpessg (hight-throughput) mrsek s az adatbnyszattal (data mining) nyert automatikus
kvetkeztetsekre vagy jslatokra nem, erre is megvan a md. Az interakcis grfot pedig tetszs szerint
vgigjrhatjuk, gy az azonos funkcihoz tartoz fehrjk biokmiai hlzata is megfigyelhet lesz. A
fehrjk mkdsnek legrszletesebb osztlyozst egy msik adatbzis, a GO (Gene Ontology) ill. annak
keresje (AMIGO) tartalmazza. A GO minden egyes fehrjhez egy hierarchikusan felptett mkdsi
lerst ad. Pldul az emls izomzat fejldst szablyoz MEF2A transzkripcis faktorra egy alapszint
lers a "transcription, DNA dependent" lehet, egy ennl jval specifikusabb pedig a "heart development".
Ha a sejten belli szablyozsi mechanizmusok finom rszletei rdekelnek bennnket, felkereshetjk a
Reactome vagy a SignaLink oldalt is. Itt minden egyes biokmiai tvonalra kln grf-modellt tallunk. A
sznes folyamatbrk nagyban segthetik a komplex biokmiai folyamatok megrtst, de a ksrletek
tervezst is.
126
10.4. bra: A STRING adatbzis rszlete. A human PSD-95 fehrje fontosabb ismert ktpartnerei.
10.2. Szekvencia-illesztsek s egyb fontos algoritmusok
10.2.1. Pronknti szekvencia-illesztsek (pairwise alignments)
A pronknti szekvencia-illeszts a molekulris biolgia egyik leggyakrabban hasznlt algoritmusa. A
feladat az, hogy kt, hasonl kdsort a lehet legpontosabban megfeleltessnk egymsnak ha szksges,
akr rsek (delcik) s beillesztsek (inszercik) segtsgvel. A kdsor egyedi beti lehetnek nukleotidok
(nukleinsavak esetn) vagy aminosavak (fehrjk esetn): az algoritmus mindkt esetben nagyon hasonl
lesz. A kt kdsor megfeleltetsnek problmja visszavezethet egy hres feladatra, a manhattani turista
problmja".
10.5. bra: A manhattani turista problmja
127
A krds: hogyan tudunk eljutni egy teljesen ngyzethls trkpen az utck (lek) mentn az utcasarkokon
(cscsokon) keresztl a bal fels sarokbl a jobb alsba, gy hogy kzben a lehet legtbb nevezetessget
rintjk? (ld. 10.5. bra). A problmt nagyon knny szmtgppel megoldani, amely pontozssal
megtallja az optimlis utat. Ugyangy lehet DNS vagy fehrjeszekvencikat pontos prokba lltani, itt a
bejrt t az elfogadott vagy elvetett prokat mutatja meg (ld. 10.6. bra). Erre a feladatra szmos program
ll rendelkezsre:pl. a CLUSTAL programcsomag (ld. 10.2.5. fejezet).
10.6. bra: A pronknti szekvencia-illesztsek problmja
10.2.2. A szekvencia-illeszts paramterei
Az illeszts jsga a pontozsi rendszertl fgg. Egyrszt slyozni kell az egyes betk hasonlsgt: egy
leucin aminosav pldul jobban hasonlt egy izoleucinra, mint egy argininre. Ezt klnfle hasonlsgi
mtrixok segtsgvel lehet megtenni (a rszletekre itt most nem trnk ki). A gyakorlatban a fehrjk
szmra a BLOSUM, GONNET vagy PAM mtrixokat hasznljuk, a nukleinsavaknak egyszerbb
mtrixok is megfelelnek (ID). A hosszsgbeli eltrseket, inszercikat/delcikat szintn pontozni kell,
mghozz negatv (bntet) pontokkal. A jobb illesztprogramok ltalban megengedik ezen paramterek
vltoztatst, erre pedig a kvetkez ok miatt lehet szksg: alacsonyabb fok hasonlsg vagy nagyon
eltr hosszsg prok esetn a mdszer sokszor nem tallja meg az sszetartoz szakaszokat. Ilyen
problmk gyakoriak pldul rendezetlen fehrjeszekaszok evolcis vizsglata esetn (ahol nagyon
alacsony a konzervltsg). Teht ha felmerl a gyan, hogy a mdszer tvedett, ne sajnljunk "jtszani" a
paramterekkel, egy jobb minsg illeszts rdekben!
10.2.3. A BLAST algoritmus
A pronknti illesztst nem csak egyenknt lehet vgrehajtani. A legtbb adatbzis lehetsget knl arra,
hogy az sszes ott trolt szekvencia ellenben automatikusan lefuttassuk a pronknti illesztst, s a
tallatokat jsg alapjn rangsorolva visszakapjuk: ez a BLAST algoritmus (Basic Local Alignment Search
Tool). A BLAST-nak szmos vltozata ltezik: fehrjkre s nukleinsavakra egyarnt hasznlhat. A
program a megadott szekvenciban elbb (heurisztikus mdon) kellen egyedi, kicsi darabokat azonost,
ezzel keres, majd az elsdleges tallatokon vgzi el a teljes illesztseket. Az NCBI s a UniProt oldalai
automatikusan felknljk a BLAST programot minden egyes oldalon, az ppen aktulisan kijellt
szekvencira. A visszaadott tallatokon ltalban jellik a megfeleltetett szakaszt, az azonossg/hasonlsg
mrtkvel egytt (sznkddal is). A vletlen egyezs (vagyis a tveds) valsznsgnek rtkt is
megadjk (ez a p-rtk), a rangsor ennek alapjn kszl (ld. 10.7. bra).
128
10.7. bra: Protein BLAST keress a UniProt szerveren (humn ciklin E1 fehrje)
10.2.4. Szekvenls ellenrzse illesztsekkel. Plazmid szerkesztk
A gyakorlatban a pronknti illesztseket leggyakrabban a molekulris klnok ellenrzsre hasznljuk. A
szekvenlssal meghatrozott bzissorrendet ugyanis ssze kell hasonltani az eredetivel. Knyelmes
megolds lehet egy-egy BLAST futtats akr DNS szinten, akr a lefordts utn fehrje szinten. Ennek
azonban vannak bizonyos htulti: a BLAST elssorban kisebb darabonknti egyezseket keres, gy a
mutcik, inszercik s delcik esetleg elkerlhetik a figyelmnket. Tovbb a BLAST nem tud mit
kezdeni a szintetikus, nem termszetes gnekkel (pl. emberi vagy egr eredet gndarab egy bakterilis
plazmidban), gy az eredmny nha meglehetsen rossz illeszts lehet. A legmegbzhatbb megolds, ha
elbb "megptjk" a klnunk elmletben vrt szekvencijt, majd ezt az elmleti szekvencit hasonltjuk
ssze a szekvenls ltal megadottal. A bzissorrendet akr szvegszerkesztkben is sszellthatjuk
(megkeresve a restrikcis helyeket, s kicserlve a szksges oligonukleotidokat), de nagy segtsg lehet
egy-egy plazmid szerkeszt program is. Ilyen pldul az ApE vagy a BioEdit, amelyek ingyenesen
hozzfrhetek s telepthetk az internetrl. Ezek a szerkesztprogramok megknnytik az automatikus
restrikcis enzim hasthely keresst, emellett megtalljk a plazmidok replikcis origit, a gyakoribb
promtereket s egyb fontos rgikat, valamint lehetv teszik a transzlci tesztelst is.
129
10.2.5. Tbbszrs illesztsek (multiple alignments). A Clustal
programcsomag
Az egyszerbb feladatok megoldsra a pronknti illeszts ltalban megfelel. Ha azonban evolcis
sszehasonltsokat szeretnnk kapni, akkor gyakran nagyszm rokon szekvencit kell egymshoz
illeszteni. Hogyan lehet ezt vgrehajtani? A tbbszrs illeszts problmja szerencsre visszavezethet a
pronknti illesztsekre. A legtbb modern illesztprogram elbb vgrehajtja az sszes lehetsges
pronknti illesztst, majd a kt legjobban illeszked szekvencit kivlasztva, konszenzust kpez. Ezek utn
hierarchikusan haladva pti fel a vgleges illesztst. A mdszer lnyegbl fakadan automatikusan
generlt "trzsft" is kapunk, amely az egyes szekvencik "rokonsgi" (hasonlsgi) viszonyait mutatja.
Ahogy pronknti illesztsekre, itt is szmos klnfle szoftver ll rendelkezsre. Taln a legnpszerbb a
Clustal programcsomag: ennek mind a helyileg telepthet vltozata (ClustalX), mind az interneten fut
vltozatai (ClustalW2 s ClustalO) ingyenesek, s knnyen hasznlhatak. A bemeneti szekvencikat
FASTA formtumban kell megadni (a nukleotidok vagy aminosavak egy bets kdsora fl kell egy fejlc-
sor, amelynek ">" jellel kell kezddnie, s egy egyedi nvvel kell folytatdnia). A program automatikusan
detektlja, hogy DNS-rl, RNS-rl, vagy fehrjrl van-e sz, valamint hogy egyszeres vagy tbbszrs
illesztst hajtunk-e vgre. A ksz illeszts alatt a csillag (*) karakter jelli a teljes egyezst, a pontok (: s .)
a klnfle fok rszleges egyezseket (kmiailag rokon aminosavak). Az inszercikat illetve delcikat
ktjelek (-) mutatjk. A Clustal program tbbszrs illeszts esetn a trzsft is megadja, akr kladogram
(azonos ghosszak), akr dendrogram (hasonlsg-slyozott ghosszak) formjban (ld. 10.8. bra).
10.8. bra: Tbbszrs szekvencia illesztsek (plda: human PEA15 fehrje). Az bra jobb oldaln az illeszts
alapjn sszelltott kladogram lthat.
10.2.6. Evolcisan konzervlt elemek azonostsa
A rendelkezsnkre ll nagyszm teljes genom lehetv tesz egy teljesen j megkzeltst a molekulris
biolgiban. Ma mr viszonylag nagy megbzhatsg konzervltsgi analzist tudunk vgezni a legtbb gn
vagy fehrje esetben. A tbbszrs szekvencia-illesztsek rendkvl rtkes adatokkal szolglnak. Az a
tny, hogy egy gn vagy fehrje mkdshez nlklzhetetlen elemek az evolci sorn hosszan
megmaradnak, magtl rtetd. Ezen llts megfordtsa, hogy a konzervlt elemek egyben fontosak is a
makromolekula mkdshez, ltalban nem igaz. Ha azonban elegenden tvoli organizmusokat
vizsglunk (pl. ember, bka s hal vagy csiga, fonlfreg s ecetmuslica), ahol a vletlen mutcik mr
szinte minden olyan pozcit kicserltek, amely nem volt abszolt nlklzhetetlen, akkor a megfordts is
igazz vlik. Ilyen esetekben a tbbszrs szekvencia-illesztsek rendkvl rtkes adatokkal szolglnak.
Ezekhez az elemzsekhez nincs szksg semmifle szerkezeti ismeretre; gy egy hasznos kiegszt technika
130
lehet a ksrletes eredmnyek rtelmezsre vagy akr ellenrzsre. Pldul a DNS-ben tallt hossz
konzervlt szakaszok legtbbszr az exonoknak felelnek meg, mg a kztes, alig-alig konzervlt szakaszok
lesznek az intronok. Hasonlan, a fehrjkben lthat, hosszan konzervlt blokkok ltalban a szerkezettel
rendelkez domneket mutatjk meg, mg a megrztt aminosavakat nem mutat szakaszok legtbbszr
rendezetlenek. Az egybknt teljesen vltozatos fehrjeszekvencia kzepn itt-ott tallhat, rvid
konzervlt szakaszok a molekulk sszekapcsoldst segt felismer elemeknek (lineris
motvumoknak) felelhetnek meg. Ugyangy, a gnek promterben tallhat konzervlt "szigetek" igen
gyakran a transzkripcis faktor kthelyeket jelzik. A mdszer hasznlathoz mindssze arra van szksg,
hogy megtalljuk azt az optimlis evolcis tvolsgot, ahol a krdses gn vagy fehrje mkdse mg
kzel azonos, viszont a szekvencia mr elgg klnbz. Feltve, hogy a szekvencik megbzhatak, az
adatbzisbl BLAST segtsgvel nyert tallatok vatos illesztse ilyenkor nagyon sok informcit nyjthat.
(ld. 10.9. bra)
10.9. bra: Evolcis analzis tbbszrs szekvencia-illeszts alapjn (szerkezeti s szekvencilis predikcik)
10.2.7. Automatizlt mdszerek a szekvencik elemzsre
A bioinformatika egyik legnagyobb kihvsa, hogy ismeretlen makromolekulk tulajdonsgait kell
biztonsggal meg lehessen jsolni. Ezekre az elrejelzsekre (predikcikra) szmos mdszer ll
rendelkezsre, itt csak a leggyakrabban hasznlt nhny algoritmus alapjait fogjuk ttekinteni.
10.2.7.1. Pontozmtrixok (PSSM: Position Specific Scoring Matrices). Logk
Abban az esetben, ha csak egy-egy rvid, jl definilt szakasz felels a DNS, RNS vagy a fehrje adott
biolgiai funkcijrt, viszonylag egyszer feladat jslatokat adni. Ezeket az elemeket szoktk lineris
motvumoknak nevezni. Pldul az llatvilgban megtallhat gynevezett SH3 domn egy konzervlt
szerkezeti elem, s olyan partnerfehrjkhez ktdik, ahol (a fehrje rendezetlen rszn) kt prolin
egymstl hrom aminosav tvolsgra van, ket pedig megfelel pozciban egy arginin kveti. Ilyesfajta
szekvencik azonban risi szmban vannak a fehrjkben: nagy rszk nem tud SH3 domnekhez ktdni.
Hogyan tudjuk mgis j esllyel megmondani, hogy melyek a valdi motvumok? Minden ilyen interakci a
polipeptidlnc specilis szerkezetvel fgg ssze, amely sszefr a partner domn felsznvel. A
szerkezetnek azonban pontosan tkrzdnie kell az aminosav-sszettelben s sorrendben. Ha az ismert
pldk szekvenciit megfelel mdon illesztjk, ltni fogjuk, hogy nemcsak a Pro vagy Arg aminosavak a
rgztettek, hanem a kztes pozcikban is hatrozott preferencik lthatak. Ezeket pozci szerinti (20
tag) vektorokkal lehet kifejezni, az sszes vizsglt pozci vektorai pedig egy pozci specifikus mtrixot
fognak kiadni, amelyet PSSM-nek rvidtnk (Position Specific Scoring Matrix). A szekvencia-
preferencikat legltvnyosabban n. szekvencia log formjban lehet brzolni: Itt minden egyes bet
131
(szimblum) magassga arnyos a mtrix neki megfelel slyval (ezt a gyakorisg rtket az y tengelyen az
adott szimblum informci tartalmval, bit-ekben fejezik ki). (ld. 10.10. bra) Magt a mtrixot pedig fel
lehet hasznlni a tbbi, potencilis motvum jsgnak vizsglatra is: azok a tallatok lesznek a
legeslyesebbek arra, hogy valban mkdkpesek legyenek, amelyek szekvencia-eloszlsa leginkbb
hasonlt a mr ismert pldkra. Sajnos a mdszer alkalmazsa felttelezi azt, hogy nagyszm, ksrletesen
azonostott motvumot ismernk, amelyek mind egyforma mdon ktdnek a partner molekulk felsznhez:
a gyakorlatban ezrt gyakran pontatlan eredmnyeket kapunk.
10.10. bra: A humn Crk fehrjhez ktd peptidek szekvencia logja
10.2.7.2. Rejtett Markov-modellek (HMM: Hidden Markov Models)
A legtbb biolgiai funkci nemcsak egy-egy rvid motvum jelenlttl vagy hinytl fgg, hanem
nagyobb szerkezeti blokkok jelenltt felttelezi. Ezek a blokkok azonban minden esetben lebonthatak
elemi motvumokra: a motvumok sorrendje pedig ltalban rgztett, a hossza viszont vltozatos lehet.
Pldul egy eukarita gn esetben a promter rgi utn exonok kvetkeznek, kzttk intronok, azok utn
pedig egy poliadenilcis hely, mindegyik jellemz szekvencia-sszettellel. Ezen ismereteket fel lehet
hasznlni pldul a gnek automatizlt jslsra. A rejtett Markov-modellek (Hidden Markov Models) a
bioinformatika "nagygyi", amelyeket pontosan ilyen problmk megoldsra dolgoztak ki (ld. 10.11.
bra).
Maga a modell nem ms, mint egy grf, amely llapotokbl (cscsokbl) s llapot-tmenetekbl (lekbl)
ll. Az egyes llapotok kztti tmenet mindig megadott valsznsggel lehetsges. Az egyes
llapottmenetek pedig fggetlenek a megelzektl (a fenti pldban: az exonban haladva minden
nukleotid utn egyforma valsznsggel folytatdhat az exon vagy kvetkezhet egy intron, s ez nem fgg
attl, hogy mennyi nukleotid volt mr eltte). A statisztikban az ilyen rendszereket hvjk Markov-
lncnak.
132
10.11. bra: Plda a rejtett Markov-modellek alkalmazsra
Ez a lnc pedig azrt rejtett, mert nem figyelhetjk meg kzvetlenl a bels llapotokat (pl. intron/exon),
csak egy attl fgg kls vltozt (pldul a nukleinsav-sszettelt). Vegyk a kvetkez, egyszer
modellt: egy kpzeletbeli organizmus gnjeiben a nem kdol rgik A/T gazdagok, a promter rgi
nagyon G/C gazdag, mg a kdol rgi nukleotid eloszlsa egyenletes. Az erre az ismeretekre felptett
rejtett Markov-modell alapjn pontosan ki lehet szmolni hogy a genomban legvalsznbben hol vannak a
fehrje-kdol gnek. A trkk az, hogy minden egyes llapot tmenetkor sszeszorzdnak a valsznsgek,
s a vgn vissza lehet szmolni (szmtgppel) az egyes llapot-utakhoz tartoz egyedi valsznsgeket.
Az effle modelleket nagyon szles krben hasznljk: de ezek felptshez komoly mennyisg ksrletes
adatra van szksg.
10.2.7.3. Neurlis hl mdszerek (Neural net)
A biolgiai gyakorlat tele van olyan problmkkal, ahol viszonylag kevs s nehezen rendszerezhet
ksrleti adat ll rendelkezsre, s ezek alapjn kell komplex jslatokat adni egy msik rendszer
viselkedsre. Az ilyen esetekre nehz egzakt statisztikai modelleket alkotni. Viszont e nlkl is lehetsges
jslatokat adni, mghozz olyan mdszerekkel, mint a neurlis hl algoritmusok. Maga a neurlis hl nem
ms, mint az agykregrl "lemsolt" szmtgpes modell. Az egyes csompontok ("neuronok") egyms
feletti rtegekben tallhatak: a legfels rteg kapja a direkt bemenetet (a nyers informcit hordoz
vltozk formjban), az ez alatti rtegek pedig mindig a megelz rteg csompontjaiban lev (szmszer)
vltozk klnfle logiai kombincit kapjk (pl. "s" opertor, "vagy" opertor, stb.). A vgn, a legals
rteg kimenete fogja megadni a kvnt jslatot. A rendszer mkdshez elbb "tantsra" van szksg:
ismert tulajdonsg pldk feldolgozsval a neurlis hlban elbb rgztjk a rtegek kztti logikai
kombincikat. Csak ez utn kvetkezhet az ismeretlen mintk elemzse. A neurlis hl mkdsnek
hatkonysga a tant pldktl fgg: elegend szm pldval megfelel minsg modellt s viszonylag
megbzhat jslatokat kaphatunk. Megjegyzend azonban, hogy a neurlis hl nem csodaszer: abban az
esetben, ha egzakt modell fellltsra megvan a md, az gyakran jobb eredmnyeket nyjt, mint a neurlis
hl mdszer.
133
10.2.7.4. A Bayes-statisztika s a dntselmlet alapjai (Bayesian inference)
A legutoljra emltett, fontos matematikai mdszer a Bayes-statisztika. Ezt nemcsak a bioinformatikai
jslsokra, hanem a ksrleti eredmnyek kirtkelsre is fel lehet hasznlni (vagyis az elmleti modellek
ellenrzsre). Az egsz Bayes-statisztika egyetlen fontos fogalommal kapcsolatos: ez a feltteles
valsznsg. Amikor a ksrleti rendszernkben egynl tbb vletlen vltozt figyelnk meg egyidejleg,
akkor nemcsak az egybeessek kzs valsznsgt lehet kiszmtani (P(A=x, B=y): Mi a valsznsge
hogy A s B egyszerre x illetve y rtk?), hanem a feltteles valsznsgeket is, mint pldul P(A=x|B=y)
(Mi a valsznsge hogy A=x, ha azt talljuk hogy B=y?). A felttelessget a kpletbe tett fggleges vonal
jelli, s mindig az els vltozrl van sz, a msodiktl fggen. A ktfle, "fordtott" P(A=x|B=y) s
P(B=y|A=x) feltteles valsznsgek ltalban klnbzek: itt a kt ellenkez irny logikai
kvetkeztetsrl van sz. Vagyis: ha A-bl kvetkezik B, ez mg nyilvnvalan nem jelenti azt, hogy B-bl
is kvetkezik A. Tegyk fel, hogy a ksrletnkben az A vltoz rejtett, nem mrhet (de ezt akarjuk tudni),
viszont van egy tle P(B|A)-szerint fgg B vltoz, amit meg tudunk mrni. Az ltalunk tanulmnyozott B
vltoz mrseibl szeretnnk az A-ra kvetkeztetni. Ha csak a B vltozt tudjuk megfigyelni, akkor a
ksrleti rendszerbl add P(B|A) feltteles valsznsg nmagban mg nem mondja meg hogy mi lehet
az A vltoz legvalsznbb llapota. Ehhez a fordtottjt, P(A|B)-t kellene tudnunk! Szerencsre van egy
kplet, amely segtsgvel a ktfle feltteles valsznsg: P(A|B) s P(B|A) tszmolhatak egymsba.
Bayes ttele szerint:
Az egsz dntselmlet lnyegben ezen az egyetlenegy kpleten alapszik. Mindig az A vltoz azon
rtkre kell szavaznunk, amelyre a P(A|B) valsznsg (a mrt B-vel) maximlis. Ekkor lesz a dntsnk
hibja a legkisebb. A fordtott, P(B|A) rtkek a ksrleti rendszer alapjn hatrozhatak meg, a P(A)
valsznsgek pedig elzetes mrsekbl, vagy akr az irodalombl becslhetek. gy dnthetnk kt
vagy tbb rivlis hipotzis, vagy akr tudomnyos elmlet kztt is.
10.3. Nukleinsavak tulajdonsgainak jslsa
10.3.1. Leolvassi keretek s gnek jslsa
A modern vilgban, ahol az eddig ismeretlen organizmusok teljes genomjnak szekvenlsa ma mr
rutinszer eljrsnak szmt, get szksg van olyan mdszerekre, amelyekkel a nyers szekvencikban
teljesen automatizlt mdon meg lehet keresni a fehrjekdol gneket. Az els s legfontosabb feladat
minden ilyen esetben a helyes nyitott leolvassi keret (ORF: open reading frame) megtallsa. Mindez egy
nagyon egyszer elven alapszik: egy START kodon jelenltn s a STOP kodonok hinyn. Mivel a nem-
kdol rgik nincsenek semmifle nyomsnak kitve a kodon-sszettelket tekintve, a STOP-ok
vletlenszeren gyakran fordulnak bennk el. Ezt egyszer mdon mi is kiszmthatjuk. Tegyk fel, hogy a
vizsglt genom nukleotid-eloszlsa (j kzeltssel) egyenletes. Ebben az esetben minden hrom
nukleotidonknt 3/64 valsznsggel tallunk stopot, teht p=0.047 valsznsggel r vget a leolvass s
1p=0.953 valsznsggel folytatdik. Legalbb kt kodont (1p)^2 valsznsggel olvashatunk le,
legalbb hrmat (1p)^3-nal, stb. A ltszlagos ORF-ek hosszsga gy exponencilis eloszlst fog
kvetni:P(x)~(1p)^x, vagyis pontosabban:
P(x) = ln(1p))*exp(x*ln(1p)).
Ennek vrhat rtke:
1/ln(1p) = 20,8 kodon
(azaz 62,5 nukleotid). Ez lesz az tlagosan leolvashat szekvencia hossz, amennyiben vletlenszer
szekvencit prblunk lefordtani. Ugyanez a helyzet, ha egy kdol rgit nem a megfelel keretben
prblunk leolvasni. Ha a gyakorlatban azt talljuk, hogy tbb szz, esetleg tbb ezer nukleotid hosszan
134
rtelmes leolvasst kapunk, annak a valsznsge, hogy ez vletlen lesz, igen kicsiny (a fenti eloszls
birtokban ezt pontosan ki is szmolhatjuk). A mdszer gy nagyon alkalmas arra, hogy akr kzzel
meghatrozzuk a DNS szekvencink helyes leolvassi kerett, pldul a klnunk szekvenlsa utn. Ha
nincs delcink vagy inszercink, ltalban az a keret lesz a helyes, amelyben a leghosszabban rtelmes
szekvencit kapjuk. gy mkdnek az ORF-keres prediktorok (pl: ORF Finder), s ezt hasznljk ki az
automatikus gn-annotl szoftverek is (a prokarita gnekben nagyon ritkk az intronok). Radsul a
legtbb bakterilis gn igen jellemz promter szekvencikkal kezddik (35 rgi s a 10 "Pribnow box"
motvumok, Shine-Dalgarno szekvencia a transzlcis start hely eltt). A rejtett Markov-modell alap
modern gnjsol programok, mint pl. a GLIMMER gy kpesek a bakterilis genomok csaknem teljes
gnllomnyt elre jelezni.
10.3.2. Gn meghatrozs cDNS alapjn. Eukarita gnek analzise
A fehrjt kdol gneket termszetesen ksrletes ton is meghatrozhatjuk. A reverz transzkripcival
cDNS-re trt, rett mRNS-ek szekvenciit sszevetve a genomikus DNS-sel, pontosan meghatrozhat az
trdott rgi kiterjedse. Amennyiben a cDNS knyvtr nem tartalmazza a teljes hosszsg mRNS-t,
csak rvid darabokat, gynevezett EST-ket (Expressed Sequence Tag), a helyzet valamivel nehezebb.
Ilyenkor elbb szmtgpes analzissel ssze kell rakni az sszetartoz EST-kbl a teljes mRNS vrhat
szekvencijt (ahogy a genomi szekvencit is a rvidebb kontigokbl lehet sszelltani). A teljes cDNS
ismeretre azrt van szksg, mert gy knnyen megadhatak az intron-exon hatrok is. Noha az intronok
kivgdsi helyei (splice sites) jellemz szekvencikkal rendelkeznek, az intronok s exonok csak a
genomi DNS-sen alapul jslsa ma is nagyon nehz feladat. Ennek az egyik f oka, hogy a szerkezetileg
"unalmas" DNS-sel ellenttben az egyszl RNS-eknek nagyon komplex trbeli szerkezete lehet, radsul
rengeteg, ma mg kevss ismert RNS-kt fehrje befolysolja az intronok felismerst. Tovbbi nehzsg,
hogy az eukarita promterekben nincsenek ktelez elemek (a Pribnow-box homolgja, a TATA-box az
egyik leggyakoribb elem, de ez is csak a gnek 10%-ban tallhat meg). Ezen okok miatt az eukarita
gnek automatikus analzise sokkal nagyobb kihvs, mint a prokaritk. A kivgsi (splice) helyek
predikcii ma is meglehetsen pontatlanok: az adatbzisokban szerepl, genomikus DNS-bl jsolt
fehrjkben bizony gyakoriak a hibsan megadott exonok. A transzlcis start hely jslsa is bizonytalan
lehet. A legtbb eukarita mRNS-en a metilguanozin-sapka utni els AUG kodont tekintik a transzlcis
start helynek, de ez a sejtben nem mindig van gy. Az eukarita gnek transzlcis kezdpontjt az els
kodont krbevev szekvencia krnyezet (az gynevezett Kozak-szekvencia) hatrozza meg. Nagyon ers
kontextus esetn elfordulhat, hogy nem AUG, hanem ms (pl. CUG) kodonnal indul el a fehrjeszintzis.
Gyenge kontextus esetn pedig a riboszma "tugorhatja" az els AUG kodont. Sajnos ezeket a
klnlegessgeket a mai prediktorok egyltaln nem veszik figyelembe, ahogy az IRES-eket (Internal
Ribosome Entry Site) sem. A szokatlan helyen kezdd fehrjeszintzis ksrleti bizonytsa sem egyszer
(N-terminlis fehrje szekvenlsra van szksg). Eukarita gnek elemzsre ezrt jabban egyre nagyobb
mrtkben hasznlnak evolcis mdszereket is: gy az trt szekvencia, az exonok pozcija s a
transzlcis start helyek jval nagyobb megbzhatsggal jsolhatak.
10.3.3. DNS s RNS szerkezetek jslsa. Oligonukleotid tervezs
A dezoxiribonukleinsav volt az els a biolgiai makromolekulk kzl, amelynek a szerkezett sikerlt
exakt mdon, rntgenkrisztallogrfival meghatrozni. Ebben az is szerepet jtszott, hogy a DNS szerkezete
meglehetsen szigoran rgztett: a dimer kt szla kztti kapcsoldst az egymssal szemben lv bzisok
prosodsa s az egyms alatti bzisok kztti msodlagos kterk (delokalizlt elektronplya
klcsnhatsok: pi-pi stacking) adjk. Ez a szerkezet annyira stabil, hogy csak nagy ritkn pldul az
eukarita telomereken kpesek az egymssal szembeni monomerek "kihurkoldni". Mivel a sejtben
megtallhat RNS-ek oroszlnrsznek nincs komplementer prja, az esetkben a stabilits alapja teljesen
ms lesz. A f klcsnhatsokat itt is a bzisprosodsok s a bzisok tlapoldsa fogja adni, de ezek az
egyszl molekuln bell, nmagukba hurkoldva fognak kialakulni. Az eredmny minden esetben egy
135
komplex trszerkezet. A rvid, egymssal kettshlixben prosod, hajtkanyar szakaszok (stems) kztti
rszek kihurkoldhatnak (loops), nha pedig ahol tbbfle szakasz prosodik egyms utn komplex
csomk (knots) is ltrejhetnek. A bels szerkezetnek komoly szerepe van az RNS-ek biolgiai
funkcijban: elg csak a riboszmkra vagy a tRNS-ekre gondolni. A korbban emltett Kozak szekvencia
is egy "nyeles hurkot" (stem-loop structure) kpez az inicitor kodon krl: a szerepe nem kzvetlenl a
riboszma ktse.
Mivel a nukleinsavak msodlagos (s harmadlagos) szerkezetnek kialakulst lnyegben csak a bzis-
komplementarits vezrli, kisebb molekulk esetn az alapvzat sokszor knny in silico megjsolni.
Ilyenkor md van az egyes lehetsges alternatv konformcik energiinak becslsre, s a legstabilabbak
kivlasztsra. Szmos szoftver ll rendelkezsre a nukleotidszlak szerkezetnek kiszmtsra (RNA123,
KineFold). Taln az egyik legknyelmesebb mdszer az mFold szerver hasznlata (ld. 10.12. bra). A
termszetes RNS-hez hasonlan, a szintetikus, rvid DNS-oligonukleotidoknak szintn lehet bels
szerkezete (Primer Premier, DNASTAR) Ha egy primernek sznt DNS oligonukleotid nmagba
hurkoldik, az ronthatja vagy esetleg lehetetlenn is teheti a PCR reakci kivitelezst. Ezrt jabban tbb
erre szakosodott cg is javasolja, hogy in silico mdszerekkel ellenrizzk az oligonukleotidunk lehetsges
bels szerkezeteit, az ahhoz tartoz elmleti energikat s "olvadspontokat", mieltt megrendelnnk a PCR
primereinket. J esetben ezeknek a szerkezeteknek illik megsznnie a PCR-hez hasznlt anelllsi
hmrskleten
10.12. bra: A humn JNK mRNS jsolt szerkezete az mFold programmal
10.3.4. Nukleinsavak "olvadspontja"
A nukleotidok szerkezetjslsban szerepet jtsz energiatnyezket egyszerbb, s sokkal gyakorlatiasabb
clokra is fel lehet hasznlni. Ki lehet szmolni pldul a nukleotidok s nukleotid-prok denaturcis
136
hmrsklett: ezt a gyakorlatban legtbbszr csak "olvadspontnak" (T
m
: melting temperature) nevezik. Ez
termszetesen rzkenyen fgg a DNS (vagy RNS) monomer-sszetteltl: a C-G prok hrom, mg az A-T
prok csak kt hidrognktsre kpesek, ami alacsonyabb ktsi energikat fog okozni az A/T gazdag
molekulaprokban. A legrgebben ismert kzelts az oligonukleotid-prok olvadspontjra az n. Wallace-
szably:
T
m
(C) = 2*N(A+T) + 4*N(G+C).
Itt az olvadspontot kzvetlenl az egyes prok tpusbl becslhetjk (N(G+C) = G/C prok szma, GC%=
G/C prok arnya). Ez a szably csak 20-40 nukleotid hosszsg tartomnyban igaz, de ott is elg gyenge
kzeltsnek szmt. Ennl sokkal jobb becslst ad klnsen az 50 nukleotidnl hosszabb prokra az
albbi, szintn kzismert kplet:
T
m
(C) = 81.5 + 16.6*log([Na
+
]) + 41*GC% 600/L.
Itt figyelembe vettk nemcsak az oligonukleotid hosszt (L), de az oldat ionerssgt (pl. [Na
+
]) is. Az eddig
emltett kpletek azonban mind csak empirikus kzeltsek s meglehetsen korltozott pontossggal igazak
csak. Bels szerkezetek jslsra egyik sem alkalmas. A mai korszer T
m
becslsek a ktsi energia
kzvetlen szmtsn alapulnak. Tudjuk, hogy egy-egy komplementer nukleotid pr nmagban mg nem
kpes stabil ktdsre (mert nem tud pi-pi klcsnhatsra lpni a szomszdjval). gy nem az egyedi
nukleotid prokat, hanem a prok prjait vesszk figyelembe. A kzelts neve ezrt "a legkzelebbi
szomszd mdszere" (Nearest-neighbour method). A ktsi energikat mr minden szomszd-prra
megmrtk, gy knnyen rendelkezsre llnak (az sszegk is). A szmts pedig a kvetkez, ismert
termodinamikai sszefggsen alapszik:
G = R*T*ln([A]*[B]/[AB]).
Mivel T
m
az a hmrsklet, ahol a prok pontosan fele disszocilt, ezrt ha csak a dimer DNS-bl indultunk
ki, akkor
[A] = [AB] = [AB]
kiindulsi
/2
gy a
T
m
= G / (R*ln([AB]
kiindulsi
/2)).
A megfelel, egyedi S s H rtkek ismeretben ez szmtgppel knnyen kiszmthat. A s
koncentrcival valamint a terminlis nukleotidok gyengbb ktsvel (A) korriglva j egyezst kapunk a
ksrletes adatokkal. Maga a teljes kplet a kvetkez :
T
m
(C) = H*1000 / (A + S + R*ln([DNS
dimer
]/2)) 273.15 + 16.6*log[Na
+
].
Ezt a kpletet hasznljk az internetes "olig kalkultorok", s a nukleotid szintzisre szakosodott cgek
oldalai is. Sajnos 50-nl hosszabb nukleotidok esetben a szomszdossgi mdszer hatkonysga cskken:
gy ez a kplet nem jsolja meg egsz plazmidok vagy kromoszmk denaturcis hmrsklett
10.4. Fehrjk tulajdonsgainak jslsa
10.4.1. A fehrjk egyszer fizikai tulajdonsgainak becslse. Reverz
transzlci
Hasonlan a nukleinsavakhoz, a fehrjk szmos elemi tulajdonsgt is knnyen kiszmolhatjuk a
szekvencia ismeretben. A molekulatmeg szmtsa akr papron is elvgezhet, ugyangy a molris
abszorbancia (extinkcis koefficiens) kiszmtsa. Utbbihoz csak az egyes, az UV tartomnyban elnyel
aminosavak elemi extinkcis egytthatira van szksg. Mindezeket azonban knnyebb szmtgpes
programmal elvgezni. Vannak azonban olyan paramterek, amelyeket "kzzel" kiszmolni meglehetsen
fradsgos lenne: ilyen pldul az izoelektromos pont szmtsa. Egyedi, semleges aminosavak esetn, ahol
az egyes savi (pK
a
) s bzis (pK
b
) llandk messze esnek egymstl, az llandk szmtani kzepvel a pI
knnyen megbecslhet. Ez azonban nem gy van a nagyobb peptideknl, vagy fehrjknl. Mivel az egzakt
137
szmts mg elhanyagolsokkal egytt is hosszadalmas, szmtgpes programok hasznlata szksges.
Ezek az algoritmusok is ltalban kzeltsekkel talljk meg a pI rtkt: nevezetesen, felveszik a becslt
titrlsi grbt, s megkeresik annak metszspontjt az x-tengellyel. Ehhez a szmtshoz persze bizonyos
elhanyagolsokat kell tenni. Ilyenkor is ltalban azt szoktuk felttelezni, hogy a pK
a
s pK
b
rtkeket nem
befolysolja a molekulris krnyezet, valamint azt hogy minden aminosav rintkezik az oldszerrel. Ezrt a
becslt pI is inkbb csak a peptidekre rvnyes, nagyobb fehrjkre nem, legalbbis natv llapotban nem.
Bizonyos programok megjelentik a teljes titrlsi grbt: ez sokkal jobban alkalmas a tiszttsi folyamat (pl.
ioncsere) tervezshez, mint a pI egymagban, hiszen megadja az elmletileg vrt, tlagos tltsszmot az
illet pH tartomnyban. Ezek s sok ms fizikai paramter kiszmtsra alkalmas internetes
programcsomagot tartalmaz az ExPaSy oldala. Nukleinsavak s fehrjk tulajdonsgait egyarnt jsolhatjuk
a Sequence Manipulation Suite (SMS2) javascript alap programjaival. Itt mg komplexebb feladatokat is
elvgezhetnk. Pldaknt emltjk a reverz transzlcit: meg kell keresni egy ismert fehrje-szekvencihoz
tartoz legvalsznbb DNS szekvencit. Mivel a DNS-kdban gyakran tbbfle kodon kdol egy-egy
aminosavat, ez a megfeleltets nem egyrtelm. Ha azonban az a feladatunk, hogy tervezznk egy olyan
mestersges gnt, ami adott (esetleg szintn mestersges) fehrjeszekvencit kdol, akkor statisztikai
megkzeltst rdemes hasznlni. Az egyes llnyek kodon-eloszlsa ugyanis nem egyenletes: mindig
vannak ritka kodonok, amelyhez tartoz tRNS is csak kis mennyisgben van jelen az illet organizmus
sejtjeiben. gy teht, a megfelel mrtk fehrjeszintzishez rdemes a leggyakrabban hasznlt kodont
vlasztani. Ez a megfelel program s kodon-hasznlati adatbzis segtsgvel knnyen kivitelezhet.
10.4.2. Lineris motvumok keresse fehrjkben (s nukleinsavakban)
Ahogy azt korbban emltettk, a fehrjk tulajdonsgainak j rszt a bennk tallhat aminosavak adott
kombincii (szekvencia-motvumok) hatrozzk meg. Amennyiben ezek egyms mellett, rgztett
tvolsgra tallhatak, lineris motvumokrl beszlnk. Ezek az esetek tbbsgben a fehrjk
rendezetlen rszein tallhatak s ms molekulkhoz val kapcsoldsra szolglnak. Az ilyen motvumok
azonban alapveten befolysoljk a polipeptidlnc sorst s lehetsges mdostsait. Pldul ha egy
eukarita fehrje N-terminlis vge megfelelen elrendezett Arg/Lys s hidrofb aminosavakkal kezddik
(szignl peptid), azt a transzlokonok felismerik, gy az extracellulris vagy transzmembrn helyzet lesz. A
szignl peptid elrejelzsre ma mr nagyon j algoritmusaink vannak (pl. a neurlis hl alap SignalP).
Ha a fehrje ezenkvl tbb rvid (~15-30 aminosav), tisztn hidrofb szakaszt is tartalmaz, akkor
valsznstheten tbbszrsen transzmembrn szerkezet lesz a sejtekben. Meglep mdon, a
membrnfehrjk topolgijt (intracellulris / extracellulris szakaszokat) is relatve magas
megbzhatsggal tudjuk jsolni, olyan programokkal, mint a Phobius (amely rejtett Markov-modell alap).
Van md a sejten belli lokalizci megjsolsra ismert pldk alapjn, neurlis hl algoritmussal is: ilyen
a WolfPSort program. Az exportra sznt fehrjn glikozilcis helyek lehetnek, amelyek szintn elre
jelezhetek (NetNGlyc). Az endoplazms retikulum fehrjire pedig a visszatart motvum (idealizlva:
KDEL, Lys-Asp-Glu-Leu) jellemz, ez pldul pontozmtrixokkal tallhat meg knnyszerrel. Egyelre
azonban nincs egyszer mdszer a Golgi-appartus fehrjinek megtallsra. A mitokondrilis, kloroplaszt
s peroxiszomlis fehrjk viszont mind-mind jellemz N-terminlis vagy C-terminlis tranzit- vagy import-
szignlokkal rendelkeznek, amelyek segtsgvel in silico is nagy valsznsggel azonosthatk (pl.
TargetP-vel).
A citoplazmban marad fehrjken is klnfle lineris motvumok irnytjk a legtbb poszt-transzlcis
mdostst. A foszforilci vagy ubiquitinilci ltalban szigoran szablyozottan trtnik, de az enzimet
felismer (kinz-kt vagy ubiquitin-ligz kt) motvumok gyakran tvol esnek a tnylegesen mdostott
helytl. Ms motvumok, pldul a protezok felismer helyei, leggyakrabban az aktulis mdosts helyn
tallhatak. Ezeket a rendkvl sokrt mdostsokat lehet akr egyszerre is jsolni. Az ELM (Eukaryotic
Linear Motifs) szervere erre a feladatra specializldott. A megadott fehrjeszekvenciban megkeresi az
ismert motvumokkal sszefr szakaszokat, st mg pontozst is vgez, mgpedig szerkezeti
(rendezetlensgi) s evolcis konzervltsgi alapon. Az ismert ktelemeket s mdostsi helyeket a
program kln kiemeli. Az eddig azonostott tbb szz klnfle lineris motvum tbbsge nem a
mdostsok irnytsra szolgl, hanem egyszeren csak adott fehrje komplexek sszeszereldsre. Ilyen
138
motvumokat keresni a DNS-en is lehet, st rdemes is: A transzkripcis faktorok kthelyei pldul DNS-
alap lineris motvumok, amelyeket pontozmtrix mdszerrel lehet azonostani a genom klnfle
helyein. Ugyangy jsolhatak a msodlagos (pldul DNS metilcis) mdostsi helyek is (pl. az
gynevezett CpG szigetek)
10.4.3. Fehrjeszerkezetek jslsa. Rendezett s rendezetlen rgik
A 21. szzad egyik legnagyobb informatikai kihvsa a fehrjk szerkezetnek szekvencia alap jslsa.
Ellenttben a nukleinsavakkal, a fehrjk szerkezett a legvltozatosabb oldallnc-oldallnc klcsnhatsok
tartjk ssze, gy a lnc helyi sszettele nem jsolja meg mg a msodlagos szerkezetet sem: a
hromdimenzis knyszerfelttelek ismeretre van szksg. Amennyiben mindenfle elzetes ismeret nlkl
szeretnnk trszerkezetet jsolni (ab initio folding), egy nagyon ersen szmtgp ignyes feladat el
nznk. Ilyen szimulcikat pldul a ROSETTA programmal lehet vgeztetni, de a futsidk ma mg
ltalban elgtelenek a nagyobb, stabil szerkezetek meghatrozsra.
10.13. bra: A ciklin E1 fehrje Jpred programmal jsolt msodlagos szerkezete s a vals msodlagos szerkezet
sszehasonltsa
Valamivel knnyebb dolgunk van, ha csak azt tzzk ki clul, hogy szeretnnk a msodlagos szerkezeti
elemeket megjsolni. Az olyan prediktorok, mint a JPred knnyen megtalljk a msodlagos szerkezeti
elemeket, de a valdi tpusukat (o-hlix, -red, kanyar) sokszor elvtik (ld. 10.13. bra).
Pldul a -redket gyakran hlixnek jsoljk, vagy fordtva. ltalban elmondhat, hogy a stabil szerkezet
jelenltnek tnye sokkal knnyebben jelezhet elre, mint maga a konkrt szerkezet. Ha csak az a clunk,
hogy elklntsk a rendezett domneket a szerkezet nlkli, flexibilis rgiktl, mr ma is szmos
megbzhat program ll rendelkezsre. Ezeket elssorban a rendezetlensg - aminosav-sszettel alap -
jelzsre dolgoztk ki (pl. DisoPred, PondR), de a mdszer megfordtsval kpesek a domn jelleg,
rendezett rgikat is megadni (pl. IUPred). Az eljrs elnye, hogy a teljesen ismeretlen domneket is elre
lehet vele jelezni (de a szerkezetket termszetesen nem) (ld. 10.14. bra).
Az ismert szerkezet domnek azonostsa leghatkonyabban a homolgia-alap kereskkel vgezhet el.
Az egyik legszlesebb krben hasznlt ilyen keres szerver a PFAM (Protein Families). A PFAM az sszes
fontosabb ismert domn egyedi motvum-lenyomatt tartalmazza, amelyeket (rejtett Markov-modellek
segtsgvel) vgigfuttat az ltalunk megadott szekvencin. A statisztikailag ersen szignifikns tallatokat
visszaadva, megkaphatjuk a fehrjnk homolgia alap szerkezeti modelljt. Ilyen keresseket ms
szervereken is lehet vgeztetni. A ProSite (ExPaSy) programcsomag pldul nem csak a lineris motvumok
keressre alkalmas: a keresje szmra megadhatunk akr teljesen egyedi domn defincikat is, ha jszer
domneket szeretnnk azonostani. Persze az a tny, hogy kt domn belseje hasonlt egymsra, mg nem
adja meg automatikusan a vlaszt, ha a rendezettsg pontos kls hatrait szeretnnk tudni: ehhez
konzervltsgi analzisekre is szksg lehet. A domnek illetve azok hatrainak ismerete nagyon fontos a
139
gntechnolgiai alkalmazsok szmra: A fehrje fragmentumok klnozst mindig gy kell tervezni, hogy
ne vgjunk bele a rendezett domnek belsejbe. Ilyenkor ugyanis (j esllyel) egy nagyon instabil, nehezen
oldhat s mindenhez aspecifikusan, vletlenszeren ktd fehrjt kapnnk. E miatt korbban sajnos
nagyon sok fehrje-fehrje klcsnhats-trkpezsi ksrlet bukott meg.
10.14. bra: Rendezett domnek s rendezetlen rgik jslsa az IUPred programmal
10.5. I n silico szerkezeti analzisek
10.5.1. Makromolekulk grafikai megjelentse
Br a makromolekulk trszerkezetnek ksrletes meghatrozsa atomi felbontsban nehz feladat, ennek
ellenre egyre nvekszik az ismert fehrje, fehrje-fehrje s fehrje-nukleinsav komplex szerkezetek
szma. A legfontosabb szerkezeti adatbzis a PDB. Az itt elhelyezett szerkezeteket ltalban ksrletes ton,
rntgenkrisztallogrfival (X-ray diffraction), vagy magi mgneses rezonancia-spektroszkpival (NMR)
hatroztk meg. Az adatbzisbl letlthet file *.pdb kiterjesztssel rendelkezik: ez tartalmazza az atomok
elemi koordintit. Ezen fell szmos egyb fontos adatot szoktak mellkelni (annotci): ilyenek pldul a
szerkezet jsgt jelz statisztikai adatok, a szerkezeti szimmetrik, s a mrshez felhasznlt fehrje
fragmentumok pontos szekvencija. Az atomi koordintkat erre a clra alkotott molekulris rajzol
programokkal jelenthetjk meg lvezhet formban. Rengeteg ilyen vizualizcis program ltezik:
SwissPDBviewer, Chimera, RasMol, JMol, stb. A legtbbjk ingyenesen letlthet s hasznlhat.
A gyakorlatban taln a legelterjedtebbnek szmt a PyMol program hasznlata (ennek hasznlathoz elbb a
Python programnyelvet is telepteni kell). A megjelentsnek szmos fajtja lehetsges (ld. 10.15. bra).
A legegyszerbb mdban csak az atomokat sszekt kmiai ktseket brzoljuk, sznes vonalak
formjban (lines). A szneket a vonalak egyes atomok alapjn kapjk, de md van az tsznezsre az egyedi
lncok alapjn is: a komplexek gy knnyebben megfigyelhetek. Pusztn az a tny, hogy egy szerkezetben
egynl tbb fehrjelnc ltszik, nmagban mg nem igazolja a komplexek ltt: a molekulk a
kristlyosods sorn is sszellhatnak (mestersges dimerekk, oligomerekk). A szmunkra kevss
rdekes lncokat, aminosavakat vagy atomokat a kijellsk utn egy kattintssal tltszv tve akr el is
tntethetjk.
140
10.15. bra: Fehrjeszerkezetek megjelentse PyMol programmal. Drtmodell (A), plcika modell (B), cartoon
(rajzos) modell (C) s a molekulafelszn brzolsa (D)
A vonalas modelleknl persze vannak sokkal szebbek is: ilyen pldul az "iskolai kmiai ptkszlet" goly
s plcika (stick) modellje: ez fleg kis molekulk esetn nagyon ltvnyos (ld. 10.16. bra). A vonalas
vagy plcika-modellek nem ignyelnek nagy szmtsi kapacitst, de az oldallncok mr a nhny tucat
monomerbl ll makromolekulk esetn is ttekinthetetlen "dzsungelt" eredmnyeznek. Nagy molekulk
esetn ezrt gyakrabban hasznljuk a f lncot szalaggal brzol (ribbon) vagy a rajzos (cartoon) mdot.
10.16. bra: Kismolekuls ligandumok (A) s fehrje-fehrje klcsnhatsok (B) ltvnyos megjelentse klnfle
modellek kombincijval, PyMol programmal
Rajzos modellben a nukleinsavak cukor-foszft gerince vastag csnek, mg a nukleinsav bzisok
lapocskknak fognak ltszani. A fehrjk bta-reds rgiit lapos nyilakkal, az alfa-hlixeket
"hajcsavarokkal", mg a tbbi fehrjeszakaszt vkony csvel jellik a programok. A publikcikban is
leggyakrabban ezzel a megjelentsi mddal tallkozhatunk. Fontos megjegyezni, hogy az eddig emltett
modellek egyike sem veszi figyelembe az atomok valdi trkitltst. De ennek brzolsra is van md:
akr hlval (mesh), akr teljes felsznnel (surface). Fehrjk s kisebb molekulk klcsnhatsa klnsen
ltvnyoss tehet, ha a kis molekult plcikkkal, a fehrjt pedig a felsznt mutat mdban brzoljuk. A
felszn brzolsakor sznezhetnk is: nem csak az egyes atomok tpusai, hanem a felszn karaktere szerint
is: pldul brzolhatjuk a hidrofobicitst vagy a tltssrsget. Ha pedig kt rokon molekult szeretnnk
sszehasonltani, arra is van md: a legtbb ilyen megjelent program tartalmaz "trbeli illesztst" lehetv
tev algoritmusokat. A PyMol "align" s "super" parancsa az elsknt megadott molekult addig tolja s
forgatja a trben, amg az a msiktl minimlis tvolsgra s orientciba nem kerl (az atomi koordintk
"euklideszi" klnbsgeit tekintve).
141
10.5.2. Homolgia-modellezs s in silico dokkols
A makromolekulk trbeli szerkezetnek elemzse nem csak "kzzel" lehetsges. Az egyes atomi
koordintk ismerete lehetsget teremt arra, hogy klnbz szerkezeteket automatizlt mdon
sszehasonltsunk, st, akr ismeretlen szerkezeteket is elre jsoljunk, mghozz a homolgia-modellezs
mdszervel. Erre elssorban akkor van md, ha az ltalunk vizsglt fehrje domn szerkezete ugyan nem
ismert, de egy vagy tbb kzeli rokon igen. A homolgia-modell fellltsra jl hasznlhat pldul a
SwissModel szerver: Bemeneti informcinak egy minl pontosabb pronknti illesztst kell megadnunk, s
az ismert partner szerkezett mutat fjlt (vagy pdb kdot). Az eljrs sorn a program nagyrszt
vltozatlanul hagyja a fehrje f lncnak lefutst, de az oldallncokat az j domn szekvencija alapjn
fogja jjpteni. Termszetesen kezelnie kell az inszercik/delcik esett is, mghozz a polipeptidlnc
lefutsnak sszer korrekcijval. De a szerkezetek ismerete nemcsak homolgia-modellezsre
hasznlhat, hanem ismeretlen partnerek ktdsnek modellezsre is. Ennek mindenekeltt a
gygyszermolekulk tervezsben van risi jelentsge. A legtbb, kis szerves molekula esetn a bels
konformcis tmenetek szerepe elhanyagolhat, gy a kis molekula teljesen rigid darabknt kezelhet. A
mdszer neve ezrt "merev-test dokkols" (Rigid body docking). A szmtgp a gygyszermolekult a
"vgtelenbl" kzeltve a clzott felsznhez, megkeresi a lehetsges helyi energiaminimumokat, beillesztve a
kis molekult a fehrje megfelel ktzsebbe (AutoDock). Ilyen szimulcikat peptidek esetre is
vgezhetnk: itt azonban a lehetsges konformcik nagy szma nehezteni fogja a szmtst. Ha
rendelkeznk egy megbzhat (homolgia-) modellel a vrhat vgllapotrl, a ktsi energia akr a f lnc
konformcijnak megvltoztatsa nlkl is megbecslhet: gy mkdik a FoldX nev szimultor
program. Ez fleg olyankor hasznlhat, ha egy szerkezetileg jl ismert fehrje-fehrje klcsnhatsrl van
sz. Termszetesen arra is van md, hogy a peptidlnc konformcija vletlenszeren vltoztathat legyen.
Ilyet knl fel a (Rosetta alap) FlexPepDock szerver. Noha helyesebb modellnek tnik, ezen
megkzeltsnek van egy komoly htrnya: a peptidlnc modellje hajlamos beragadni a loklis energia-
minimumokba, gy a mdszer ltalban albecsli a valsgban mrhet ktsi energit.
10.6. A predikcis mdszerek pontossga
10.6.1. Egy predikci "jsgt" ler paramterek. Optimlis dntsek.
Az elrejelz mdszerek rszletes trgyalsa utn nem kerlhetjk el, hogy magrl az elrejelzs
minsgrl ne beszljnk, ezt kell ugyanis mrlegelni akkor, amikor arrl dntnk, hogy elfogadjuk-e egy
mdszer jslatt vagy sem. A predikcik jsgnak trgyalshoz elbb nhny statisztikai fogalmat kell
bevezetnnk. Egy kt-kimenetel (+/-) mrs, elemzs vagy dnts esetn szenzitivitsnak nevezzk a
sikeresen felismert elemek arnyt (az sszes pozitv elem kzl), specificitsnak pedig a sikeresen elvetett
elemek arnyt (az sszes negatv elem kzl). A legtbb eddig lert algoritmus rendelkezik egy vagy tbb
vltoztathat paramterrel, ami befolysolja a mdszer jsgt. Pldul az illesztsek magas p-rtk mellett
nagyon magas szenzitivitssal (megtalljk az sszes egyezst), de alacsony specificitssal (rengeteg
vletlen egyezst is tallnak) fognak rendelkezni. Alacsony p-rtk (mint hatrrtk) esetn megfordul a
helyzet: az sszes egyezs j lesz (magas specificits), de a valdi egyezsek csak kis hnyadt talljuk meg
(alacsony szenzitivits). A dntsre hasznlt hatrrtket szoktuk levgsi rtknek (cutoff) nevezni. Egy-
egy levgsi rtk jsgt pedig a mrnki tudomnyokbl klcsnvett mdszerrel az gynevezett ROC
grbvel fejezhetjk ki. Az ROC (Receiver Operating Characteristics) grafikon pontosan mutatja, hogy
egy adott paramter-rtk, mint levgsi rtk esetn a valdi pozitvoknak mely rszt talltuk meg, illetve
hogy az sszes lehetsges elem hnyad rszt fogadtuk el (ld. 10.17. bra). Az optimlis dntseket a valdi
pozitvok arnynak becslsvel (Bayes-analzis alkalmazsval) ilyen grbk alapjn mr viszonylag
knny megadni (fleg a tveds "kltsgnek" ismeretben). E szerint minden mdszer rendelkezik egy r
jellemz, fix hibavalsznsggel, mg az optimlis dnts esetn is: ezek lte a mdszer lnyegbl fakad.
142
10.17. bra: ROC grbk hasznlata bioinformatikai jsl mdszerek jsgnak elemzsre
10.6.2. Adatbzisok minsge: elsdleges s msodlagos hibk
A jslataink helyessgt nemcsak az eredend hiba befolysolja. Az adatbzisokban trolt szekvencik
minsge is lehet hibaforrs. Knny beltni, hogy ilyen mennyisg adat mrsnl s elemzsnl hiba
nlkl dolgozni szinte lehetetlen. Az adatbzisokban elfordulhatnak elsdleges hibk: ezek mrsi hibkbl
fakadnak, pldul egy-egy ktes minsg szekvenlsbl. rdekes tny pldul (s knny megfigyelni)
hogy a legkorbban szekvenlt modell organizmusok (pl. Mus musculus, D. melanogaster, S. cerevisiae)
genomi s cDNS szekvencija sokkal tbb hibval rendelkezik, mint az jabban szekvenltak. gy ha azt
talljuk, hogy az egr egy adott gnjnek adott aminosava eltr az sszes tbbi emlsben megfigyelhet,
mindig konzervlt aminosavtl, az eltrs eredete vlheten szekvenlsi hibban keresend: nem arrl van
sz ugyanis, hogy az egr "feltallt" volna szmos, amgy teljesen szokatlan biolgiai megoldst. Mivel a
legtbb llny cDNS-szekvencii nem, vagy csak darabokban hozzfrhetek, nagyon sok, az
adatbzisokban tallhat fehrjeszekvencia valjban csak jslat (ez a tny fog remlhetleg megvltozni az
RNAseq j-genercis szekvenls elterjedsvel; ld. 5.3. fejezet). Az ilyen, prediktlt szekvencikban
pedig viszonylag gyakoriak a msodlagos hibk: tvesen jsolt transzlcis kezdhelyek, eltvesztett
exonok (valjban intron-szekvencik, exonknt trva) s hinyz szakaszok. Ezek az annotl-program
tvedsbl fakadnak. Az ilyen hibkat leginkbb a biolgiai korrelcik segtsgvel, tbbszrs
szekvencia-illesztsekkel szrhetjk ki. Ha pldul a l egy adott, genomi szekvencibl jsolt fehrjjnek
kzepn tallhat egy szokatlan, hossz darab, ami az sszes emlstl klnbzik (de mshol mindig
konzervlt), akkor ebben az esetben egy hibsan jsolt exonrl lehet sz (ld. 10.18. bra).
10.18. bra: Fehrje-szekvencia adatbzisokban elfordul gyakoribb hibk tbbszrs illesztssel kimutatva.
143
10.6.3. Ellenrztt adatbzisok. Ellentmond ksrleti eredmnyek kezelse
Az elsdleges adatbzisok minsge javthat, ha nem csak automatizlt mdszerekkel ellltott adatokat
tartalmaznak. Az ilyen, szakemberek ltal ellenrztt rendszerek (manually curated databases) kz tartozik
pldul a UniProt fehrje adatbzis (ld. 10.1.3.). Itt a gpi analzist ksrleti adatokkal vltjk fel, amikor
azok a szakirodalomban elrhetv vlnak. Ezek a kzi annotcik jelents emberi munkaert ktnek le,
cserben viszont a legmegbzhatbb adathalmazt nyjtjk. Persze a szakirodalomban lert ksrletek sem
mindig mentesek a hibktl: mrsi hibk ppgy elfordulhatnak, mint hibs rtelmezsek. Ebbl fakadan
tallkozhatunk egymsnak tkletesen ellentmond publikcikkal is: hol az egyik, hol a msik, esetleg
mindkt kutatcsoport tvedett.. Mindezek rontjk a "kzi" annotcik pontossgt is. Ezrt a szakemberek
ltal ellenrztt adatokat sem szabad felttlenl hibtlanknt kezelni.
10.6.4. Mikor hasznljunk jslsokat?
Mindezek utn bizonyra felmerl az olvasban a krds: rdemes-e egyltaln elrejelz programokat
hasznlnunk? s ha igen, akkor mikor? ltalnos aranyszablynak annyit mondhatunk, hogy a ksrletes
adatok ltalban pontosabbak, mint a jslatok. A prediktl mdszereket is mindig a rendelkezsre ll
informci alapjn vlasszuk meg. Teht amennyiben md van pl. egy fehrje domnjnek homolgia alap
elemzsre, ne kezdjnk ab initio folding szimulcikba. Fontos megjegyezni, hogy a kutats maga
ktirny: a mr ksrletesen igazolt eredmnyeket is rdemes jra szmtgpes analziseknek alvetni, s
j modelleket pteni rjuk. Rengeteg j felismers, s tudomnyos eredmny szrmazhat gy
10.7. Tovbbi olvasnival a fejezethez
Edwards, D, Stajich, J, & Hansen D (2009) Bioinformatics: Tools and Applications. Springer Science.
ISBN: 978-0-387-92737-4.
Eddy, SR (2004) What is a hidden Markov model? Nature Biotechnology 22:1315-6.
De Fonzo, V, Aluffi-Pentini, F, Parisi, V (2007) Hidden Markov Models in Bioinformatics. Current
Bioinformatics. 2: 49-61.
Neural Networks: http://www.doc.ic.ac.uk/~nd/surprise_96/journal/vol4/cs11/report.html (by
Christos Stergious and Dimitrios Sigianos)
Dickter Wickmann (1999) Bayes-statisztika. ELTE Etvs Kiad. ISBN: 978-963-463-311-2
Bujnicki, JM (2009) Prediction of Protein Structures, Functions and Interactions. John Wiley & Sons Ltd.,
ISBN: 978-0470517673
144
11. I n vitro mutagenezis
Az 1980-as vekben kialakul s napjainkig tretlenl fejld gntechnolgiai mdszerekkel a rekombinns
fehrjket kdol DNS-ben gy a humn fehrjket kdol DNS-ben is mra egyszeren, olcsn s
gyorsan hozhatk ltre mutcik, akr irnytottan is. A DNS-en trtn vltoztats lehet delci, amikor
tetszleges szm nukleotid eltvoltsa trtnik; inszerci, amikor tetszleges szm nukleotid beillesztse
trtnik; vagy szubsztitci, ami egy nukleotid msik nukleotidra val kicserlst jelenti. Az in vitro
mutagenezis kidolgozsval beindult a reverz genetika korszaka.
Mirt lehet szksg a fehrjket kdol DNS vagy a vizsgland gnek szablyz elemeinek clzott vagy
vletlenszer megvltoztatsra? Egyrszt azrt, mert az egyes biolgiai folyamatok vizsglata s
megrtse gyakran a folyamatok rszlpseinek defektusain keresztl trtnik. A klasszikus genetikai
vizsglatokban az egyes gnek vagy szablyz elemeinek funkcijra, az adott folyamatok mkdsre csak
azok termszetes mutciinak s vltozsainak fenotpus vizsglatval volt lehetsg. Az rktanyagban
bekvetkez vltozsok a termszetben azonban nem clzottak s nem rintik az sszes rgit, ezrt szmos
esetben a fehrjk, fehrjerszletek vagy gnjk szablyoz elemeinek funkcija nem vizsglhat. A kutatk
rdekldsnek kzpontjban gyakran az ember ll. A gntechnolgiai mdszerek kifejlesztse eltt a
humn fehrjk funkcijnak vizsglata is csak a termszetben elfordul mutcik s rendellenessgek
vizsglatval volt lehetsges. Az irnytott mutagenezis mdszerekkel rekombinns fehrjkben akr
humn fehrjkben is gyorsan s hatkonyan tudunk vletlenszer vagy akr clzott vltozsokat
ltrehozni. Az egyes aminosavak ms kmiai karakterrel rendelkez aminosavakra cserlsvel vagy akr
nagyobb fehrjerszek mutcijval a fehrjk tulajdonsgait megvltoztathatjuk. A megvltozott
tulajdonsgbl kvetkeztetni tudunk az adott aminosavnak vagy a fehrjersznek a fehrje
enzimaktivitsban, szerkezetben vagy funkcijban betlttt szerepre.
Az in vitro mutagenezis msik felhasznlsi terlete a racionlis fehrjemrnksg, vagy az irnytott
fehrje evolci, melyek sorn irnytott vagy nem-irnytott mutcis mdszerek segtsgvel fehrje
varins sereget hozhatunk ltre (ld. 0. fejezet). Ebbl a varins seregbl ltalunk meghatrozott szelekcis
krlmnyek kztt vgeredmnyben megvltoztatott, valamilyen szempontbl szmunkra elnysebb,
vagy akr jfajta tulajdonsggal rendelkez fehrjk, enzimek, fehrje inhibitorok szelektlhatk (pl.:
protez inhibitorok; stabilabb s gyorsabb enzimek).
A rekombinns fehrjk in vitro mutcis mdszerekkel trtn vizsglata nagymrtkben hozzjrult a
modern biolgia mai sikeressghez. A DNS in vitro mutagenezisre mra szmos mdszert kifejlesztettek.
Ebben a fejezetben a teljesg ignye nlkl ismertetsre kerlnek a leggyakrabban hasznlt, a legismertebb
s a leghatkonyabb nem-irnytott s irnytott mutagenezis mdszerek. A mutagenezis mdszerek
kihagyhatatlan lpse s szerves rsze a mutns DNS szekvencia ellenrzse, aminek a legbiztosabb
mdszere a DNS szekvenlsa. A klnbz szekvenlsi s ellenrzsi mdszerekrl rszletes informci
a 5. fejezetben tallhat.
11.1. Nem-irnytott in vitro mutagenezis mdszerek
Nem-irnytott mutagenezis mdszerek gyakran hasznlatosak irnytott fehrje evolcis mdszerek
esetben, mint pldul az in vitro kompartmentci, a fg bemutats vagy a baktrium bemutats (ld. 0
fejezet). Az irnytott fehrje evolcis mdszerek sorn a termszetben trtn evolcis trtnseket
utnozva (diverzifikci, szelekci s replikci) egy varins seregbl ltalunk meghatrozott krlmnyek
kztt szelektldnak a szmunkra megfelel tulajdonsggal rendelkez knyvtrtagok. A mdszer els
lpse a megfelel varins sereg ltrehozsa. A nem-irnytott in vitro mutagenezis mdszerekkel
ltrehozott varinsok tulajdonsgai a mutci fajtjtl fggen akr nagymrtkben is eltrhetnek a kezdeti
templtknt (vzknt) hasznlt fehrje tulajdonsgaitl. Vgeredmnyben szolubilisabb, szerkezetileg
stabilabb vagy akr teljesen jfajta tulajdonsggal, jfajta enzimaktivitssal rendelkez fehrjk, enzimek is
ltrehozhatk.
145
11.1.1. Muttor baktrium sejtvonalak
Klnfle muttor baktrium sejtvonalak hasznlatval gyorsan s egyszeren lehet nem-irnytott mutcit
ltrehozni a vizsgland rekombinns fehrje DNS szekvencijban. A mdszer alapja, hogy a rekombinns
fehrjt kdol DNS-t tartalmaz plazmid sokszorostshoz hasznlt baktrium sejtvonalakban nem
mkdnek megfelelen a DNS hibajavt rendszerek. Pldul plazmid vektorok sokszorostshoz
ltalnosan hasznlt Escherichia coli baktrium egyik sejtvonalban, az XL1-Red-ben (endA1 gyrA96 thi-1
hsdR17 supE44 relA1 lac mutD5 mutS mutT Tn10 (Tet
r
)) hinyzik a DNS hibajavt tvonalban szerepet
jtsz hrom kulcs fehrje; a mutS, a mutD s a mutT. A mutS fehrje az error prone mismatch hibk
javtsban, a mutD fehrje a DNS-polimerz III 35 exonuklez aktivitsban, a mutT fehrje az oxidatv
folyamatok sorn trtn DNS krosods javtsban vesz rszt. A nem megfelel DNS hibajavts 5000-
szer nagyobb mutcis gyakorisgot eredmnyez ennl a sejtvonalnl a vad tpus Escherichia coli
sejtvonalakhoz kpest. A mdszer elnye, hogy kt egyszer lpssel, a plazmidnak a muttor sejtekbe
transzformlsval, majd a sejtek felnvesztse utn a mr mutns plazmid DNS-nek kinyersvel gyorsan,
sokfajta mutci (delci, szubsztitci, inszerci) ltrehozsa lehetsges. Egyb gntechnolgiai
mdszerek, mint restrikcis emszts, PCR vagy ligls nem szksges. A mdszer htrnya, hogy a
mutcis rta a muttor sejtvonalak hasznlata mellett is igen alacsony (0,5 mutci/kbp). Nagyobb
mutcis rtt a sejtkultra fenntartsi idejnek megnvelsvel lehet elrni. A muttor sejtvonalak a DNS
hibajavt rendszer hinya miatt azonban igen gyorsan halmoznak fel mutcikat sajt genomjukban s a
plazmidnak nem a vizsgland fehrjt kdol DNS rszben is. Megfelel mret varins sereg ltrehozsa
ezrt gyakran ismtelt transzformlsi s plazmid tiszttsi lpseket ignyel.
11.1.2. Hibt ejt (error prone) PCR mutagenezis
Az egyik leggyakrabban hasznlt nem-irnytott mutagenezis mdszer az gynevezett hibt ejt (error
prone) PCR. Alapja, hogy a vizsgland fehrjt kdol DNS szakasz PCR ltali sokszorostsa sorn a
DNS-polimerz szmra nem optimlis krlmnyeket hasznlnak. Nem megfelel krlmnyek kztt a
DNS-polimerz mutcis frekvencija megn. A felszaportott DNS-ben a mutcik vletlenszeren
keletkeznek, szmuk a ciklusszmmal n. Error prone PCR sorn ltalban a Thermus aquaticus
baktriumbl izollt, alacsony hsg (low fidelity) Taq DNS- polimerzt hasznlnak. A Taq-
polimerznak hinyzik a 35 exonuklez aktivitsa, ezrt ha a polimerz a lnchosszabts sorn nem a
DNS bzisprosods szablyainak megfelel bzist pt be, akkor nincs lehetsge a hiba javtsra. A Taq-
polimerz optimlis reakcikrlmnyek kztti mkdse sorn tlagosan egy szubsztitcis mutci
trtnik 10
4
bzispronknt. A Mn
2+
, a Mg
2+
, a DNS-polimerz s a dNTP koncentrcijnak
megnvelsvel stabilizlni lehet a nem komplementer bzisprosodst, cskkenthet a bzisprosods
specificitsa, gy tovbb nvelhet a rosszul anellldott primer oligonukleotidrl trtn lnchosszabts
valsznsge. sszessgben a Taq-polimerz mutcis gyakorisga elrheti ciklusszmonknt a 0,066%-
ot (30 ciklus sorn). A mutcik feldsulst tovbb nvelhetjk a PCR sorn alkalmazott ismtelt hgtsos
lpsekkel s a ciklusszm nvelsvel (60 ciklus; ld. 11.1. bra). Ezzel a mdszerrel sszessgben a
felsokszorozand DNS szekvencijnak akr a 3,5%-a is megvltozhat.
Az error prone PCR sorn delcik s inszercik is elfordulhatnak, jellemzen azonban szubsztitcik
trtnnek. A legtbb polimerz esetben nagyobb valsznsggel trtnik AG vagy TC tranzci
(purinpurin, piridinpiridin), mint transzverzi (purinpiridin, purinpiridin). A ngy
dezoxiribonukleozid-trifoszft arnynak eltolsval s mdostott Taq-polimerz enzim (Mutazyme)
hasznlatval ez a mutcis arnytalansg (mutational bias) javthat. Az error prone PCR haszlatval
ltrehozott DNS inszert ezutn megfelel restrikcis enzimmel val emszts utn a kvnt plazmidba
liglhat. A mdszer htrnya, hogy a ltrehozhat varins sereg mrett korltozza a szubklnozsi lps
sorn alkalmazott ligls hatkonysga.
146
11.1. bra: A hibt ejt (error prone) PCR sorn alkalmazott hgtsos mdszer. A hibt ejt (error prone) PCR
mutagenezis sorn nem optimlis krlmnyek kztt mkd DNS-polimerznak megn a mutcis frekvencija
(ciklusszmonknt a DNS 0,066%-a vltozhat meg). A ciklusszm nvelsvel nvelhet a DNS-ben keletkez
vletlenszer mutcik szma. A hgtsos mdszer minden 4. ciklusa utn a minta krlbell 10%-t toltjk egy
kvetkez reakcielegybe. Az toltssal frisstik a reakcit, gy nvelhet a ciklusszm egszen 60-ig. sszessgben
60 ciklus utn a DNS szekvencijnak akr 3,5%-a is megvltozhat.
11.2. Helyspecifikus in vitro mutagenezis mdszerek
Clyde Hutchison s Marshall Edgell mr 1971-ben felvetette a kis DNS fragmentekre pl irnytott
mutagenezis tlett (DNS kazetta mutagenezis, ld. 11.2. bra). Hutchison s Michael Smith 1978-ban
kifejlesztett egy ltalnosan hasznlhat, szintetikus oligonukleotidokra pl mdszert, mellyel mind
inszerci, delci s szubsztitci is ltrehozhat. Az eredeti protokoll szerint a mutland DNS
fragmentumot elszr uX174 fg DNS-be klnoztk. A mutcit tartalmaz szintetikus oligonukleotidot
ezutn az egyszl uX174 fg DNS-re anellltk, majd DNS polimerz s ligz hasznlatval szintetizltk
s cirkularizltk a mutcit tartalmaz j szlat. Az azta kifejlesztett helyspecifikus in vitro mutagenezis
mdszerek mindegyike szintetikus oligonukleotidot hasznl a rekombinns fehrjk tetszleges
mdostsra.
A szintetikus oligonukleotidok tervezsnl ajnlott, hogy az oligonukleotid a mutcitl mind 5-, mind 3-
irnyban is legalbb 15 bzisprnyi szakaszon komplementer legyen a templt szllal s a 3 vgn lehetleg
G/C bzisokat tartalmazzon. A mutcitl 5- s 3-irnyban tallhat 15 bp ltalban elegend a mutci
specifikus kijellsre. A mutci jelentheti egy bzispr megvltoztatst vagy az oligonukleotid
kihurkoldsval rinthet akr egy nagyobb rgit is. Ezekkel a mdszerekkel ltalunk szablyozott
mdon brmely pozciban megvltoztathat a fehrjket kdol DNS szekvencija. Az irnytott
mutagenezis sorn brmilyen szabs-varrs kivitelezhet; inszerci, delci vagy szubsztitci. Lehetsg
van fehrjk vagy fehrjerszek fzijra, kimrk ltrehozsra. is Az albbiakban a legelterjedtebb s a
leghatsosabb mdszerek kerlnek bemutatsra.
11.2.1. DNS kazetta mutagenezis
Hutchison s Edgell ltal lert DNS kazetta mutagenezis a legegyszerbb s leghatkonyabb irnytott
helyspecifikus mutagenezis mdszer (ld. 11.2. bra). A mutland DNS fragmentumot egy dupla szl
plazmid tartalmazza. Kt restrikcis endonuklez emsztsvel hastjuk ki a mutland DNS szakasz
krnyezett, majd a megfelel ragads vggel rendelkez, mutcit tartalmaz szintetikus
oligonukleotidokkal elksztett DNS kazettt T4 ligz segtsgvel a plazmidba ligljuk s E. coli
147
baktriumba transzformljuk. A DNS kazetta mutagenezis egy gyors, hatkony s knnyen kivitelezhet
mdszer. Fontos szempont, hogy a restrikcis enzim felismerhelyek a mutland DNS szekvencihoz kzel
helyezkedjenek el, gy csak 60-80 bp hossz DNS kazetta szintzise szksges. Ilyen mret oligonukleotid
szintzise olcs s gyors. Ha nagyobb mret DNS kazetta szksges (100-1000 bp), a szintzis kltsgei
jelentsen megnvekednek. Ezekben az esetekben az albbiakban is emltett, rvid oligonukleotidokat
ignyl mdszerek kltsghatkonyabbak.
11.2. bra: DNS kazetta mutagenezis mdszer. A dupla szl DNS plazmidot a mutland DNS szekvencia
kzvetlen krnyezetben restrikcis endonuklezzal emsztjk. A kies DNS fragmentum helyre ligljuk a mutcit
tartalmaz szintetikus DNS kazettt.
11.2.2. Szelektv templt lebontson alap mutagenezis mdszerek
A Smith s Hutchinson ltal kifejleszett irnytott mutagenezis mdszer (ld. 11.2.) hatkonysga igen kicsi.
Elmletben a mutcis rta maximum 50%-os lehet, de a gyakorlatban a nem megfelel oligonukleotid
letapads, a polimerizci s a ligls hinyos mkdse miatt a legjobb esetben is csak pr szzalkot r el.
A mdszer hatkonysgnak nvelse rdekben az jonnan ltrejv mutcit tartalmaz plazmid DNS-
t szelektlni kell a vad tpus plazmid DNS-tl.
11.2.2.1. Kunkel mutagenezis
A rekombinns fehrjk irnytott mutagenezisnek egyik legrgebbi, de nhny terleten mg a mai napig
is hasznlatos mdszert Thomas Kunkel 1985-ben kzlte (ld. 11.3. bra). A mdszer nagy
hatkonysggal kpes ltalunk meghatrozott pozciban inszercik, delcik s pontmutcik
ltrehozsra. A mdszer alapja, hogy a mutland DNS inszertet egy M13 bakteriofg alap egyszl
DNS fgmid tartalmazza. Erre, mint templtra, a mutcit tartalmaz oligonukleotidot anelllnak, majd
T7 DNS-polimerz hasznlatval szintetizljk a mr mutcit tartalmaz j szlat. A mutcit tartalmaz
plazmid vgl megfelel baktrium trzsekben szelektlhat.
Az els lps a mutland DNS inszert M13-alap fgmidba klnozsa. Az inszertet tartalmaz fgmidbl
ezutn egyszl DNS-t hoznak ltre, ami a mutagenezis sorn templtknt fog szolglni. A M13 fgmid
148
vektor tvzi a ktszl DNS plazmidok s az egyszl DNS fg tulajdonsgait, amirl nevt is kapta (ld.
bvebben a 7.3.2. fejezetben). E. coli sejtekben kpes ktszl DNS plazmidknt szaporodni (ez az n.
replikatv forma). M13 helper fg hatsra azonban egyszl DNS msolatok jnnek ltre, amelyek a helper
fg ltal termelt M13 bakteriofg burokfehrjibe csomagoldva M13 virionokat alaktanak ki. Az M13
bakteriofg egy nem-litikus bakteriofg, a kialakul virionok a baktrium kultra fellszjba
szekretldnak, feldsulnak, ahonnan knnyen tisztthatk s bellk egyszl DNS izollhat.
11.3. bra: Kunkel mutagenezis mdszer sematikus brja. A mutland DNS fragmentumot hordoz fgmidbl
egyszl, uracil tartalm DNS templtot lltunk el dut-, ung- E. coli baktriumtrzsben. A mutcit tartalmaz,
szintetikusan ellltott oligonukleotidot a templt DNS-re anellljuk, majd T7 DNS polimerzzal krberjuk azt,
vgl az jonnan szintetizlt szlat T4 ligzzal cirkularizljuk. A duplex DNS-t dut+, ung+ E. coli baktriumtrzsbe
transzformljuk, melyekben a mutns szl szelektldik s a vad tpus szl lebomlik. A mutns fgmid tovbb
szaporthat, belle ktszl vagy egyszl DNS hozhat ltre.
Msodik lpsben az egyszl templt DNS-hez a mutcit tartalmaz oligonukleotidot anelllnak. Egy
mutcis lpsben akr tbb oligonukleotid is hasznlhat, gy egymstl tvolabb tallhat DNS szakaszok
egyszerre is megvltoztathatk. A kvetkez lpsben T7 DNS-polimerz hasznlatval trtnik meg az
egyszl templt fgmid krbersa, a ktszl heteroduplex DNS ltrehozsa (az egyik szl az eredeti
vad tpus templt, a msik szl a mutns). A T7 DNS polimerz egy processzv polimerz, azaz kpes
hossz, akr msodlagos szerkezettel rendelkez templt trsra is anlkl, hogy a templt szlrl
disszocildna. rdemes az oligonukleotidok 5- s a 3-vgre lehetleg G/C bzisokat tervezni, hogy
elkerljk a rossz helyre anelllst (mispriming) s ezltal a nem-megfelel termkek keletkezst. A 3-
vgen tallhat G/C bzisprok biztostjk a T7 DNS- polimerz pontos mkdshez szksges kezd
149
pozcit. Az oligonukleotid 5- vgn tallhat G/C bzisprok pedig megakadlyozzk a T7 DNS
polimerz tlmkdst, az oligonukleotid 5 vgnek a templt DNS szlrl val letrst. Az jonnan
szintetizlt, mr a mutcit tartalmaz DNS szlat T4 DNS-ligz segtsgvel cirkularizljk. A T4 DNS-
ligz mkdshez szksges a szintetikusan ellltott oligonukleotid 5 vgnek foszforillsa, amit az
oligonukleotidnak a templt szlhoz val hozzadsa eltt polinukleotid-kinz enzimmel lehet elvgezni.
A kialakul ktszl heteroduplex DNS fgmidot E. coli sejtekbe transzformljk s gy a tovbbiakban
plazmidknt szaporthat. Smith mdszerhez hasonlan az ilyen mdon ltrehozott fgmidoknak a legjobb
esetben is csak az 50%-a fogja tartalmazni a mutcit. A Kunkel-mdszer sorn ez az 50%-os mutcis rta
a templt DNS szl szelektv lebontsval csaknem 100%-ig eltolhat. Ennek alapja, hogy a templtknt
szolgl egyszl fgmid timin helyett nagyrszt uracilt tartalmaz. Ezt gy rik el, hogy az egyszl DNS
templtot olyan E. coli trzsben szaportjk, ami dUTP-z s uracil N-glikozidz deficiens (E. coli CJ236
K12 dut-, ung-, F pilus+). A dUTP-z hinya miatt a fgmid DNS szintzise sorn a sejtekben a dUTP
koncentrcija megnvekszik s timin helyett gyakran uracil is bepl a DNS-be. Az uracil N-glikozidz
felels a DNS-be mr beplt uracil eltvoltsrt, ezrt az uracil N-glikozilz deficiens trzs nem tudja
kijavtani a DNS-be mr beplt uracilt. A mutcit tartalmaz msodik szl T7 DNS-polimerzzal trtn
in vitro elksztshez dUTP-t nem hasznlnak fel, ezrt az jonnan szintetizlt szl uracilt nem tartalmaz. A
kvetkez lpsben a vad tpus, uracilt tartalmaz, s a mutns, uracilt nem tartalmaz heteroduplex
DNS-t vad tpus E. coli trzsbe (dut+, ung+) transzformljk (E. coli XL1-Blue vagy DH5-alpha). Az
uracilt tartalmaz vad tpus DNS a dut+, ung+ E.coli sejtekben az uracil-N-glikozilz enzim hatsra
preferencilisan lebomlik, mg a mutns vltozat jval nagyobb arnyban fennmarad, gy nvelve meg a
mutcis rtt. A sejtekbl a mutns ktszl fgmid plazmid tisztthat, illetve M13 helper fg
hasznlatval fg s egyszl fgmid is termelhet.
A mdszer elnye, hogy ha a mutland inszertet a tovbbiakban is fgmid vektorban szeretnnk
fenntartani, akkor ez nem ignyel tovbbi klnozsi lpseket, mint pldul restrikcis endonuklezzal val
emsztst vagy liglst. Htrnya, hogy a fgmid vektoroknak korltozott az alkalmazhatsga, gy pldul
ha a vizsgland rekombinns fehrjnket heterolg expresszival E. coli baktriumban szeretnnk
tltermeltetni, akkor a mutcit tartalmaz inszertet szubklnoznunk kell megfelel expresszis vektorba
(pl. pET). A heterolg expresszirl a 0. fejezetben tallhatk tovbbi rszletek.
11.2.2.2. QuickChange mutagenezis
A Stratagene cg ltal kifejlesztett QuickChange mutagenezis az irnytott mutagenezis mdszerek kzl,
mint neve is mutatja, taln a leghatkonyabb s leggyorsabb mdszer (ld. 11.4. bra). Delci, inszerci s
szubsztitci is ltrehozhat vele. Elnye, hogy nem ignyel specilis vektorrendszert, mint a Kunkel
mutagenezisnl alkalmazott M13 fgmid, valamint sszehasonltva a PCR-alap megaprimer, vagy az
overlapping mutagenezis mdszerekkel (ld. 11.2.3.1. s 11.2.3.2.), nincs szksg tovbbi klnoz
lpsekre (restrikcis emszts, ligls) sem.
A mdszer sorn a mutland DNS fragmentumot brmilyen ktszl plazmid tartalmazhatja. A
kivitelezsnek elfelttele, hogy a hasznlni kvnt plazmid vektor guanin bzisai metilltak legyenek. E
felttel teljestse brmely gntechnolgiban ltalnosan hasznlt (dam+) E. coli trzs esetben teljesl,
mint pldul az XL1-Blue vagy a DH5-alpha trzsek esetben (ld. 0. fejezet). A plazmidot vagy lgos
oldattal (NaOH kezelssel), vagy hkezelssel denaturljk. A mutagenezishez olyan oligonukleotid
primer prt hasznlnak, melyek ugyanazon DNS-szakasz kt szlhoz hibridizlnak s tartalmazzk a
kvnt mutcit. A primerek teht egyms komplementerei. rdemes nagyon magas (T
m
> 78C) olvadsi
hmrsklet oligonukleotidot tervezni. Az olvadsi hmrskletet megbecslhetjk a kvetkez egyszer
kplet hasznlatval:
T
m
= 81.5 + 0,41(GC%) 675/N mismatch%
ahol az N az oligonukleotid hossza, a GC% s a mismatch% egsz szmok. Egyszerre tbb primerpr
hasznlatval tbb, akr egymstl tvolabbi DNS szakaszon is ltrehozhatunk vltozst. A kvetkez
150
lpsben egy PCR sorn DNS-polimerz (Pfu, KODI, Fusion/Phusion) hasznlatval trtnik meg a
mutcit tartalmaz j szlak szintzise.
A reakci vgl vad tpus s mutcit tartalmaz plazmidokat s ezek heteroduplexeit eredmnyezi. A
kvetkez lpsben a reakcitermket DpnI restrikcis endonuklezzal kezelik, ami kpes magas
skoncentrci mellett (150-200 mM NaCl) specifikusan a metillt DNS lebontsra, gy a vad tpus
templt plazmidok eliminlsra (clszekvencija: 5-Gm6ATC-3). A kezels utn a mutcit tartalmaz
plazmidok intaktak maradnak. A DpnI enzimmel kezelt mintt, amely elvileg mr csak a metillatlan,
mutns plazmidokat tartalmazza, E. coli baktriumba transzformljk, ahol megtrtnik a plazmid kt
vgnek ligldsa. A DpnI endonuklez s a DNS-polimerz minsgtl fggen ltalban maximum
50%-ban sikeres a reakci. A mutci hatkonysga 80-100%-ra nvelhet, ha uracilt tartalmaz templtot
hasznlunk s a mutagenezis utn a DNS termknket dut+, ung+ E. coli baktrium sejtekbe
transzformljuk. Az uracil tartalm templtot dUTP-z s uracil N-glikozilz deficiens E. coli baktrium
sejtekben llthatjuk el (E. coli CJ236 K12 dut, ung, F pilus+).
11.4. bra: QuickChange mutagenezis sematikus brja. A mdszer sorn brmilyen, dam+ E. coli sejtben termelt
ktszl, metillt plazmid hasznlhat. A plazmidok h- vagy lgos denaturcija utn mindkt szlra komplementer,
a mutcit hordoz oligonukleotidot anelllnak. T7 polimerz s T4 ligz szintetizlja s cirkularizlja az jonnan
kpzd, a mutcit mr hordoz szlat. A metillt, vad tpus DNS-t DpnI endonuklezzal magas skoncentrci
mellett specifikusan lebontjk. A reakcitermket mutS- E.coli sejtekbe transzformljk, melyekben a mutns szl
szelektldik s szaporodik. Az brn a piros csillag a mutcit jelli.
A QuickChange mutagenezis elnye a Kunkel-mdszerrel szemben, hogy nem ignyel specilis
sejtvonalakat s vektorrendszereket. A PCR alap mdszerekkel szembeni elnye pedig, hogy nincs szksg
tovbbi klnozsi lpsekre. Htrnya, hogy az egsz plazmid trsra kerl, ezrt nagyon j minsg, nagy
151
hsg DNS-polimerzt ignyel. Nagymret plazmidok esetn (> 8 kbp) ezrt specilis krlmnyeket s
enzimeket kell hasznlni (rszletesebb lerst a gyrt cg honlapjn itt olvashatnak).
11.2.2.3. GeneEditor mutagenezis
A Promega cg ltal kifejlesztett szelekcis oligonukleotidra pl GeneEditor mdszere a
QuickChange mutagenezis egyik alternatvjaknt szolgl. Minden ltalnosan hasznlt ampicillin
rezisztencit (TME1 |-laktamz) hordoz egyszl s ktszl plazmidban kdolt DNS fragmentum
irnytott megvltoztatsra alkalmas (ld. 11.5. bra). A mutci sorn egyszerre kt oligonukleotidot
hasznlnak fel. Az egyik magt a kvnt mutcit tartalmazza. Egyszerre egymstl tvolabb tallhat
tbb mutci is ltrehozhat tbb mutcis oligonukleotid egyttes hasznlatval. A msik tpus, az
gynevezett antibakterilis szelekcis oligonukleotid, a plazmidon kdolt ampicillin rezisztencia gnt
(TME1 |-laktamz) mdostja. A mdostott rezisztens plazmidot tartalmaz sejtek gy nemcsak ampicillint
tartalmaz tptalajon, hanem GeneEditor Antibiotic Selection Mix-et tartalmaz tptalajon is
fenntarthatk. Els lpsben a plazmidot denaturljk, majd az oligonukleotidok anelllsa utn T4 DNS-
polimerz enzimmel s T4 DNS-ligz enzimmel szintetizljk s cirkularizljk a mutcikat tartalmaz j
szlat (mutci a |-laktamzban s a vizsgland DNS inszertben). A liglshoz itt is szksges az
oligonukleotidok 5 vgnek elzeteses foszforillsa. A mutagenezis termket kompetens E. coli sejtekbe
transzformljk, melyeket ampicillin s GeneEditor Antibiotic Selection Mix-et tartalmaz tptalajon
nvesztenek. Ezen a tptalajon csak azok a sejtek nnek fel, melyek a kvnt, mutns plazmidot
tartalmazzk. A mutagenezis hatsfoka nvelhet, ha a reakcitermket E. coli BMH 71-18 mutS
baktriumtrzsbe transzformljk. Az gy elrhet mutcis rta gyakran nagyobb, mint 90%.
11.5. bra: A GeneEditor mutagenezis sematikus brja. A mdszerrel TME1 |-laktamz alap ampicillin
rezisztencit hordoz plazmid ltal kdolt DNS inszert szekvencijt lehet tetszlegesen vltoztatni. A vektor h-
vagy lgos denaturlsa utn oligonukleotidok hasznlatval kt parallel mutcit trtnik. Az egyik a vizsgland
DNS inszerten, a msik a |-laktamzt kdol gnen. A szintzis (T4 DNS-polimerz) s a cirkularizci utn (T4-
ligz) vad tpus s ktszeresen mutns szlakat kapunk. A termket E. coli mutS- baktriumtrzsbe transzformljuk,
majd GeneEditorTM Antibiotic Selection Mix-et tartalmaz tptalajon nvesztjk, gy csak a megvltoztatott |-
laktamz szekvencit kdol plazmidot tartalmaz sejtek szelektldnak.
152
11.2.3. PCR alap irnytott mutagenezis mdszerek
A polimerz lncreakci egy tetszleges DNS szekvencia hatkony s egyszer felszaportst teszi
lehetv (ld. 0. fejezet). A PCR-re alapozva az utbbi vtizedekben szmos irnytott mutagenezis mdszert
fejlesztettek ki, melyek mindegyike tbb lpses PCR-t s tovbbi klnozsi lpseket ignyel. Mint minden
klnozsi lps sorn, gy a PCR alap irnytott mutagenezis mdszerek esetben is ltalnosan ajnlott a
nagy hsg, azaz hibajavt aktivitssal (high fidelity, proofreading) rendelkez DNS-polimerzok
hasznlata. Ilyen DNS-polimerzok pldul a Pfu-, KODI- vagy a Phusion-polimerz (ld. 3.1.4 fejezet)
11.2.3.1. Megaprimer PCR mutagenezis
A PCR alap in vitro mutagenezis mdszerek kzl az 1990-es vek elejn Sarkar s munkatrsai ltal lert
megaprimer PCR mdszer taln a leggyorsabb, legegyszerbb s legsokoldalbb (ld. 11.6. bra).
11.6. bra: Megaprimer PCR mutagenezis sematikus brja. A mdszer sorn kt egymst kvet PCR
segtsgvel irnytottan, brhol ltrehozhat vltozs az vizsglt DNS szekvencijban. Az 1. PCR lpsben a
mutcit hordoz P2 s P3 oligonukleotidok hasznlatval ltrejv termk az n. megaprimer. A 2. PCR sorn a
P1 primer s maga a megaprimer felhasznlsval amplifikldik a mutcit tartalmaz DNS szakaszunk, melyet a
P1 s a P3 oligonukleotidok ltal kdolt restrikcis enzim felismerhelyeken val emszts utn szubklnozhatunk.
A megaprimer mdszer sorn hrom primer oligonukleotid s a vad tpus DNS templt felhasznlsval
kt PCR trtnik. A hrom oligonukleotidbl kett, a hatrol vagy flanking oligonukleotidok jellik ki
a felszaportand DNS szekvencit s tartalmazzk a ksbbi klnozshoz szksges restrikcis enzim
felismerhelyeket. A harmadik oligonukleotid tartalmazza magt a mutcit, ami lehet inszerci, delci,
szubsztitci vagy ezek brmilyen keverke. A mutci a target gnen bell brhol ltrehozhat. Az els
PCR sorn a mutcit hordoz oligonukleotid s az egyik hatrol primer segtsgvel, valamint a vad
tpus templt DNS felhasznlsval ellltjuk a mutcit tartalmaz megaprimert. Az elkszlt
megaprimer mrete elrheti a tbb szz, vagy akr ezer bp hosszsgot is. A megaprimert agarz
glelektroforzissel elvlasztjuk az aspecifikus termkektl s a PCR sorn fel nem hasznlt primerektl,
153
majd glbl izolljuk. A tiszttott megaprimert, mint egy ltalnos primert hasznljuk fel a msik
hatrol primerrel a msodik PCR sorn a mr mutcit tartalmaz DNS szekvencink sokszorostsra.
A msodik PCR sorn belltott anelllsi hmrskletnl figyelemmel kell lenni a megaprimer extrm
mretre s a msodlagos szerkezet kialaktsra val hajlamra. rdemes a primer prjt gy tervezni, hogy
annak olvadsi hmrsklete 55-60C krnykn legyen. A msodik PCR sorn elkszl mutns DNS
szekvencinak a mennyisgt a reakcielegybe bemrt megaprimer mennyisge fogja meghatrozni, ezrt
ajnlott nagy mennyisg megaprimer ellltsa s a msodik PCR reakciba a lehet legnagyobb
mennyisgben val hozzadsa. A 2. PCR hozamt nagy mennyisg templt hasznlatval is nvelni lehet.
Az elkszlt mutns DNS termk agarz glelektroforzissel vlaszthat el az esetleg megmarad
megaprimertl s a templt DNS-t tartalmaz plazmidtl. A tiszttott mutns DNS inszertet a hatrol
oligonukleotidok ltal kialaktott restrikcis enzim felismerhelyeken emsztik s a megfelelen
elksztett, restrikcis enzimekkel emsztett plazmidba ligljk. A ligtumot kompetens sejtekbe
transzformljk, a mutns DNS inszertet tartalmaz plazmidot szaportjk, majd a szekvencijt
szekvenlssal ellenrzik (a mutcit hordoz inszert plazmidba klnozsnak folyamatrl tovbbi
rszletesebb lers megtallhat a 4. fejezetben).
11.2.3.2. Overlapping PCR mutagenezis
A PCR alap irnytott mutagenezis mdszerek kzl az overlapping PCR mutagenezis hasznlatval a
vizsgland fehrje DNS-n bell brhol ltrehozhat mutci. A mdszer a megaprimer PCR mutagenezis
alternatvjaknt hasznlhat. Hosszabb idignye, az egymst kvet hrom PCR s a ngy primer miatt
szemben a megaprimer PCR sorn hasznlt 3 primerrel kevsb terjedt el (ld. 11.7. bra).
11.7. bra: Az Overlapping PCR mutagenezis sematikus brja. A mdszer sorn kt egymst kvet PCR
segtsgvel irnytottan, brhol ltrehozhat vltozs a vizsglt DNS szekvencijban. Az 1. PCR lpsben a
mutcit kdol, egymssal tfed kztes termkeket lltunk el. A 2. PCR lpsben az tfed DNS szlak
kiegsztse trtnik. Vgl egy mutcit tartalmaz, 5 s 3 vgen restrikcis enzimfelismer helyet kdol inszertet
kapunk, amelyet megfelel plazmidba szubklnozhatunk.
154
Az els kt PCR sorn kt tfed fragmentum jn ltre, melyek tartalmazzk a mutcit s a klnozshoz
szksges restrikcis enzim felismerhelyeket. A kvetkez PCR sorn ezen tiszttott termkek
anelllsbl s lnchosszabbtsbl kialakul, mutcit tartalmaz termk szolgl templtknt a
restrikcis enzim felismerhelyt tartalmaz, a primer oligonukleotidok szmra. A mutcit tartalmaz
inszert megfelel plazmidba klnozsa a korbbiakban lertak alapjn trtnik (ld. 6.4.1 fejezet).
11.3. Tovbbi olvasnival a fejezethez
Hutchison III, C. A. , Phillips, S., Edgell, M. H., Gillam, S., Jahnke, P. and Smith, M. (1978) Mutagenesis at
a specific position in a DNA sequence. J Biol Chem. 253(18), 6551-60.
Cadwell, R. C. and Joyce, G. F. (1992) Randomization of genes by PCR mutagenesis. PCR Methods Appl
2:2833
Kunkel, T. A , Roberts, J. D., and Zakour, R. A. (1987) Rapid and efficient sitespecific mutagenesis without
phenotypic selection. Methods Enzymol. 154, 367-382
Sarkar, G. and SomMer, S. S. (1990) The megaprimermethod of site-directed mutagenesis. BioTechniques
8, 404407.
155
12. I n vitro s prokarita expresszis rendszerek
A rekombinns DNS technolgia egyik legfontosabb vvmnya, hogy a vizsglataink trgyt kpez
fehrjket nagy mennyisgben, tisztn s viszonylag egyszeren el tudjuk lltani. A tisztn kifejezs itt
nemcsak azt jelenti, hogy a prepartum kb. 90-95%-ban a bennnket rdekl fehrjnket tartalmazza, hanem
azt is, hogy pldul nem kell 1 mg neuronlis fehrje ellltshoz 25-30 db patknyt meglni, mint a
gntechnolgit megelz korszakban. Az expresszis rendszerek felhasznlsval a vizsgland fehrjt
nemcsak egyszerbben s nagyobb mennyisgben, hanem a cljainknak megfelelen mdostva irnytott
mutcikkal, nll domnknt, csonkolt formban, klnbz cmkkkel (tag-ekkel) elltva is tudjuk
termeltetni.
Nem mindegy, hogy milyen expresszis rendszert hasznlunk. Ennek kivlasztsban jelents szempont a
szksges fehrje mennyisge, tisztasga, poszttranszlcis mdostsa, aktivitsa, a rfordtott id s pnz,
illetve milyen infrastruktra (s mennyi kutatsi forrs) ll mgttnk. Ebben a fejezetben a sejtmentes (in
vitro expresszis rendszer) s a prokarita expresszis rendszereket ismertetjk. Megbeszljk az
alapjaikat, milyen vektorokat, gazdasejteket hasznlhatunk, mik az elnyeik s htrnyaik, milyen clra
melyik rendszert clszer hasznlni, valamint milyen alkalmazsi lehetsgeik vannak. Az eukarita
expresszis rendszereket a kvetkez fejezetben trgyaljuk (ld. 0. fejezet)
Kezdjk az alapfelttelekkel, azaz mi az expresszis rendszerek kt pillre? A gazdasejt, ami termeli a
rekombinns fehrjt, illetve az expresszis konstrukci, azaz a rekombinns DNS, ami meghatrozza a
termelend polipeptidlnc(ok) aminosav sorrendjt. A rekombinns fehrje kifejezs annyit jelent, hogy
rekombinns DNS segtsgvel expresszltatunk egy fehrjt, ami az esetek tbbsgben megegyezik a
natv fehrjvel (azaz nem kt polipeptidlnc rekombinlsval lltjuk el). A fenti smtl eltr a
sejtmentes, azaz in vitro expresszis rendszer, mivel ebben az esetben nincs szksgnk gazdasejtre, csak a
pro- vagy eukarita sejtbl szrmaz riboszmkra, valamint az in vitro transzkripcihoz s transzlcihoz
szksges egyb komponensekre.
A gazdasejt lehet baktrium (Escherichia coli, Bacilus subtilis), leszt (Saccharomyces cerevisiae, Pichia
pastoris) vagy ms eukarita sejtvonal vagy akr transzgenikus llat s nvny is. Ezek a gazdasejtek
heterolg expresszira kpesek, vagyis arra, hogy nem a sajt, hanem ms fajbl szrmaz fehrjket
termeljenek. Mindegyik rendszernek vannak elnyei, s htrnyai, s megvannak a sajt expresszis
vektorai. Ezek az expresszis vektorok tartalmazzk azokat a szekvencikat, amelyeket a gazdasejt
felismer, s elindtja a kifejezend gn transzkripcijt, majd transzlcijt. A fejezetben tmaszkodunk az 0.
fejezet ismeretanyagra.
12.1. I n vitro expresszis rendszerek
Az in vitro vagy sejtmentes expresszi azon alapszik, hogy in vitro krlmnyek kztt a sejtbl kivont
transzlcis rendszer segtsgvel szintetizltatjuk a kvnt fehrjt. (A sejtmembrnt, illetve eukarita
sejteknl az organellumokat is eltvoltva, a citoplazma s a benne tallhat komponensek alkotjk a
sejtmentes rendszert). A rendszer mkdshez szksg van a genetikai informcira, azaz a kvnt
fehrjt kdol mRNS-re, illetve ltalban egy expresszis vektorban lv rekombinns DNS-re, valamint a
reakci oldatra, mely tartalmazza a szksges transzkripcis s transzlcis aktivitst. A legels sejtmentes
transzlcis rendszer prokarita kivonat volt, ezt kvettk az eukarita sejtmentes transzlcis
rendszerek, rovarsejt (Sf9, Sf21-sejt), nyl retikulocita (RRL), bzacsra, s ma mr humn sejtvonalbl
szrmaz transzlcis rendszer is elrhet. Tovbbi informci a kereskedelmi forgalomban elrhet
rendszerekrl itt olvashat.
12.1.1. Az in vitro transzlcis rendszer komponensei
156
Mi szksges a sikeres in vitro transzlcihoz?
- RNS-polimerz s NTP-k az mRNS transzkripcijhoz
- riboszmk a polipeptidlnc transzlcijhoz
- tRNS-ek s aminosavak
- transzlcis kofaktorok
- ATP, GTP s energiaregenerl rendszer
- dajkafehrjk s ms faktorok a polipeptidlnc feltekeredshez
- templt nukleinsav
A fehrje-komplexeket s faktorokat a kereskedelmi forgalomban kaphat sejtmentes kivonatok
tartalmazzk, csak energiaforrst (ATP, GTP, energiaregenerl rendszert) s aminosavakat kell
hozzadni, valamint rtelemszeren a templt nukleinsavat.
A templt nukleinsav mRNS vagy DNS lehet. Amennyiben a templt DNS, azt elszr t kell rni mRNS-
s, s majd az azt kvet transzlcis reakci sorn lesz belle fehrje. Ezrt ezt a rendszert kapcsolt (linked
vagy coupled) rendszernek hvjk (ld. 12.1. bra).
A kapcsolt rendszer esetn ugyanabban a csben jtszdik le egyms utn a transzkripci s transzlci.
DNS templt esetn a bemen DNS lehet lineris, cirkulris, vagy PCR termk. A DNS-nek tartalmaznia
kell a transzkripci s transzlci elindtsrt felels elemeket, teht a promter szekvencit, s prokarita
rendszernl a riboszma kthelyet (RBS), azaz a Shine-Dalgarno szekvencit. Eukarita rendszernl
ennl bonyolultabb a helyzet, mert a splicing folyamatt (DNS templt esetn), tovbb az mRNS rst s
transzlcijnak inicilst is neknk kell megoldani. Ezrt a megfelel gnexpresszis elemeket (pl.
Kozak-szekvencia, IRES) is tartalmaznia kell a templtnak, illetve intron mentes DNS-t kell bejuttatni a
rendszerbe. Ennek megfelelen specilis prokarita vagy eukarita expresszis vektorokba kell a target
gn cDNS-t bevinni. Ezek az expresszis vektorok expresszis kazettjukban mr eleve tartalmazzk a
gnexpresszihoz szksges elemeket (ld. 12.2. bra).
szekvencija, T7T: T7 transzkripci termincis szekvencia
Ilyen vektorok, illetve in vitro transzlcis kit-ek megvsrolhatk, pl. a NEB (New England Biolabs),
Invitrogen vagy a ThermoScientific biotechnolgiai cgektl. Mivel lineris DNS-t is hasznlhatunk
templtknt, ezrt PCR reakcival mi magunk is elkszthetjk a templtunkat. Ilyenkor olyan primerekkel
kell felszaportani a cDNS-t, amely tartalmazza a megfelel szablyoz elemeket. A 12.2. bra alapjn
lthat, hogy az 5' primernek tartalmaznia kell a promtert az RBS-sel egytt, a 3'-primernek pedig a
termincis szekvencit. Azaz a hasznland primerek sematikus felptse:
- 5'-primer: T7P szekvencia-RBS szekvencia-cDNS-re illeszked szekvencia.
- 3'-primer: cDNS-re illeszked szekvencia-T7T szekvencia (termszetesen ennek a reverz
komplementere kell).
A Roche cg fejlesztse, a Rapid Translation System(RTS 500), E. coli extraktumot hasznl, amely akr
egy napig is kpes folyamatos szintzisre, gy nagyobb mennyisg fehrjt tud ellltani. Ezt gy tudtk
megoldani, hogy gondoskodtak az energia hossz tv regenerlsrl, illetve a kofaktorok, alapanyagok
(nukleotidok, aminosavak) folyamatos betpllsrl s a gtlanyagok elvezetsrl. Ezt gy oldottk meg,
hogy fligtereszt hrtyval elvlasztjk a reakcitrtl a keletkez gtl anyagokat, ami a konvencionlis
mdszer egyik legnagyobb problmja. A rendszerrl tovbbi informci itt olvashat.
157
12.1. bra: A kapcsolt (linked vagy coupled) in vitro transzlcis rendszer smja
12.2. bra: Prokarita expresszis kazetta sematikus brja. T7P: T7-promter szekvencija, RBS: riboszma
kthely szekvencija, ATG: az els metionin aminosav kodonja, Tag: fzis cmke (a pldban C-terminlis)
12.1.2. Elnyk s htrnyok
Elnyk:
- A leggyorsabb expresszis rendszer, nhny rt vesz csak ignybe.
- Egyszer, nem ignyel sejttenysztst, transzformlst, intenzv fehrjetiszttst.
- Fggetlen a gazdasejttl (nincs gazdasejt).
- Toxikus fehrjkre is hasznlhat (nincs sejt, ami elpusztulna).
- Proteolzisre nagyon rzkeny fehrjk expresszija is megoldhat (br a sejtmentes kivonathoz is
szksge lehet protez enzim gtlszerek hozzadsra).
Htrnyok:
- Kevs fehrje llthat el, ltalban egy reakcival 0,1 g/ml fehrjt nyerhetnk ki. Gyakran ki sem
tiszttjuk a fehrjt, hanem a fehrjt tartalmaz reakcioldattal dolgozunk tovbb.
158
- Nem megfelel a poszttranszlcis mdosts (glikozilci, foszforilci), br ez a problma
megfelel in vitro transzlcis rendszer megvlasztsval megoldhat: pl. humn fehrjt humn
sejtvonalbl nyert sejt extraktummal szintetizltathatunk.
- A sejtkivonat endogn mRNS-tl meg kell szabadulni (kezels micrococcus nuklezokkal).
12.1.3. Alkalmazsok
- Gyors s nagyszm mutns vagy csonkolt fehrjk ellltsra funkcionlis analzis cljbl (nagy
teresztkpessg, n. high throughput, HTP mdszer)
- Megfelel poszttranszlcis modifikcival rendelkez humn fehrjk ellltsra.
- Fehrjk stabil izotpos jellsre, nem-termszetes aminosavak bevitelre, mivel a reakcihoz
szabadon hozzadhatk a jellt vagy nem termszetes aminosavak.
- Funkcionlis virionok (vrusfehrjk s nukleinsavak, amelyek spontn virionn llnak szervezdnek),
illetve toxikus polipeptidek ellltsra.
- Adott fehrje feltekeredsnek (folding), stabilitsnak s degradcijnak tanulmnyozsra s
optimalizlsra.
12.2. Prokarita expresszis rendszerek
Nzzk meg a prokarita expresszis vektorok ltalnos felptst, amelynek alapelemei a riboszma
kthely kivtelvel az eukarita expresszis vektorokban is megtallhatak (ld. 12.3. bra).
12.3. bra: Egy tipikus prokarita expresszis vektor felptse
- Replikon, azaz a replikcis orig s szablyoz szekvencik, amelyek a plazmid baktrium sejtben
trtn fenntartshoz, replikcijhoz szksgesek.
159
- Antibiotikum rezisztencia gn a szelekcihoz.
- Promter s szablyoz elemei a kvnt cDNS transzkripcijhoz.
- Riboszma kthely (Shine-Dalgarno szekvencia) a kvnt cDNS-rl trt mRNS transzlcijnak
inicilshoz.
- MCS: poli- vagy multiklnoz hely a kvnt cDNS bevitelhez.
-
Korbbi fejezetekben mr ismertettk a vektorok s ezen bell plazmidok ltalnos felptst (ld. 0.
fejezet), ezrt ebben a fejezetben csak a gnexpresszi szempontjbl legrdekesebb elemekrl, a
promterekrl, s a riboszma kthelyrl (RBS) lesz sz.
12.2.1. Bakterilis promterek s a riboszma kthely
12.2.1.1. Promterek
A bakterilis expresszis vektorok ltalban plazmid-alapak, amelyek legtbbszr induklhat promtert
tartalmaznak. Mr korbban megtanultuk, hogy a prokarita promternek kt fontos eleme van: a Pribnow-
box vagy -10 elem (TAAATA konszenzus szekvencia), ami 10 bp-ra tallhat 5-irnyban az els trand
bp-hoz kpest (amely a +1 pozcit jelenti). Ezen elem jelenlte esszencilis a transzkripcihoz. A msik
elem egy TTGACA konszenzus szekvencia, amit -35 szekvencinak is hvunk, mert a start ponttl 35 bp-ra
tallhat upstream, azaz 5-irnyban az trd szekvencitl. Jelenlte a promterben nem esszencilis, de
jelents mrtkben hozzjrul a gn trshoz. Vgl sok prokarita promterben a 35 elemtl 5-
irnyban tovbbi nem esszencilis szekvencik is tallhatk (UP elemek). Egy tipikus bakterilis promter
f elemeit a 12.4. bra mutatja be.
12.4. bra: Egy bakterilis promter smja
A bakterilis promterek lehetnek lland kifejezdst biztost, azaz konstitutv, vagy induklhat
promterek. Az indukci trtnhet hmrsklettel, vagy valamilyen kmiai genssel, induktorral. Az
indukci leggyakrabban IPTG-vel (izopropil-tiogalaktozid) trtnik, ami egy nem metabolizld laktz
analg. gy az indukci a lac-operon szablyozsi elvn alapul, azaz az expresszis vektor a promter
mellett tartalmazza a lac opertor szekvencit is (a -10 elem s az trd szekvencia kztt). Az induktor
(allolaktz vagy IPTG) hinyban a lac-represszor fehrje ktdik ehhez a szekvencihoz, gy nem
hozzfrhet az RNS-polimerz szmra a promter, teht nincs mRNS trs. Allolaktz vagy IPTG
jelenltben a lac-represszor levlik a promterrl, megtrtnik a gntrs. Radsul, az IPTG
mennyisgvel mg az trs mrtkt is szablyozni tudjuk.
Lac promter (lavUV5 promter): ltalnosan elterjedt, ilyen van a pUC katabolit, pTZ, pSK, pBluescript,
pGEM vektorokban. Br a promter viszonylag gyenge, mgis megfelel mrtk fehrje kifejezds rhet
el, mivel a plazmid nagy kpiaszm. Akkor mkdik a promter maximlisan, ha a baktrium kultra
mdiuma nem tartalmaz glkzt, ugyanis ekkor mkdik a cAMP/ aktivtor fehrje (CAP), ami szksges a
promter mkdshez.
Trp-lac (tac) promter: hibrid promter, -35 rgi tartalmazza a trp (trp operon) -35 szekvencijt, majd -
10-nl a lavUV5 promoter (lac-operon) szekvencijt s a lac-opertor szekvencijt. gy a promter
regullhat a lac-represszorral, azaz a gntrs induklhat IPTG-vel, s fggetlen a cAMP regulcitl.
Ers promter, nagymrtk expresszi rhet el vele. Ilyen promter tallhat a pGEX vektorokban,
amelyek sematikus felptst a 12.5. bra mutatja be.
160
12.5. bra: A pGEX-3X expresszis vektor trkpe
A pGEX vektorok replikonja (pMB1) a pBR322 vektorbl szrmazik, ezrt ezek alacsony kpiaszm
vektorok. ltalban ampicillin rezisztencijuk van, amit a |-laktamz enzim, a rezisztencia gn termke
biztost. A trp promterrel val hibridizci miatt sokkal ersebb induklhat expresszit biztost, mint a lac
promter, 3-szor ersebb a trp, s 10-szer a lac-promoternl. Ez egy GST-fzis fehrje termeltetsre
alkalmas vektor (ld.12.2.3.1. fejezet)
Trp-lac (trc) promter: szintn hibrid promter, a tac promter egyik vltozata. A klnbsg a kt
promter kztt a -35 s -10 elemeket elvlaszt tvolsgban van, a trc-promternl rvidebb. Ilyen
promter tallhat a pTrc vektorokban.
T7 promter: A legersebb promterek kz tartozik. A T7 bakteriofg specifikus promtere, 5-szr
ersebb, mint az E. coli baktrium konszenzus promtere, ezrt nagymrtk expresszit biztost. Specilis
baktriumtrzs kell hozz, amely kpes felismerni a T7 promtert, azaz termeli a T7 RNS-polimerz
enzimet (az E. coli RNS-polimerz enzim csak a sajt gnjei promtereihez ktdik, miknt a T7
bakteriofg RNS-polimerz csak a fg gnek promtereihez ktdik). Ezrt az E. coli BL21 baktriumtrzs
genomjba fg-fertzssel bejuttattk a T7 fg RNS-polimerz gnjt gy, hogy a lacUV5 promter
szablyozsa alatt legyen. Az gy kapott baktriumtrzset hvjuk BL21(DE3)-nak. A DE3 profg egy -fg
szrmazk, amelynek - a kromoszomlis integrcirt felels - int gnjbe juttattk be a T7 RNS-polimerz
s a lacI represszor fehrje gneket. Ebben a trzsben a laktz analg IPTG hatsra beindul a T7 RNS-
polimerz termelse, ami felismeri a plazmidon lv T7-promtert, s elkezdi trni a promter utn lv
inszertet.
Ilyen promter tallhat a pET vektorokban (plasmid for Expression of T7 RNA polymerase) (eredetileg a
Novagen biotechnolgiai cg termke), amelyet Studier s trsai fejlesztettek ki a 90-es vek elejn. Ezek a
vektorok colE1 origt (replikon) tartalmaznak, ami alacsony kpiaszmot biztost, s ltalban ampicillin
vagy kanamicin rezisztencia gnt hordoznak. A promterk vagy a T7 fg termszetes promtere, a 10
promter, vagy a termszetes 10 promter a lac opertorral (LacO) egytt. Az gy kapott T7lac promter
mr induklhat IPTG-vel, s nagyobb biztonsgot jelent, mert mind a polimerz, mind a termelend fehrje
gnje a lac opertor szablyozsa alatt ll, s IPTG-vel induklhat. Teht indukci nlkl elmletileg nincs
gntrs. De a BL21 pLysS s pLysE baktriumtrzsekben mg egy extra biztostk is van; ezek a trzsek
kln plazmidon (pLys) hordozzk a T7 RNS-polimerz termszetes inhibitornak, a lizozimnek a gnjt.
161
IPTG nlkl, az esetleg keletkez RNS-polimerzt a lizozim gtolja, gy biztos nincs trs. Ezt akkor
rdemes kihasznlni, ha toxikus a fehrje a baktrium szmra, gy csak az indukci hatsra kezd a fehrje
expresszldni. Nzzk meg a 12.6. bran az igen gyakran hasznlt pET-expresszis rendszer mkdst.
Itt tallhatk tovbbi elmleti s gyakorlati rszletek a legmegfelelbb vektorok kivlasztsrl.
12.6. bra: A pET-expresszis rendszer smja
pL promter: Magas hmrsklettel induklhat, mert hmrsklet rzkeny represszort tartalmaz. A -
fg represszor fehrje alacsony hmrskleten a promterhez ktdik, mg magasabb hmrskleten levlik,
gy elkezddhet a gntrs. A baktrium kultrt 30C-on nvesztjk, majd az indukci 42C-on trtnik.
Ez a promter klnsen hasznos toxikus fehrjk kifejeztetsnl. Ilyen vektorok a pHUB, pPLc, pKC30,
pAS1, pRM1, pTrxFus sorozatok. De ehhez a promterhez is specilis E. coli trzsre van szksg: az
M5219 trzs a -represszor gn hmrsklet rzkeny mutcijt hordozza.
araBAD promter: Az arabinz operon opertor helyt tartalmazza, gy arabinzzal induklhat, dzis-
fgg mdon. A promter, mivel arabinz hasznosts operon rsze, glkzzal gtolhat. Ilyen promterrel
a pBAD sorozat (Invitrogen) vektorai mkdnek.
lpp promter: Az expresszis vektor a kifejezend gn eltt egy kls membrn lipoprotein promtert
tartalmazza. Ez a fehrje nagy mennyisgben s llandan kifejezdik a baktrium sejtben, gy a promter
ers s konstitutv lesz.
phoA promter: A bakterilis alkalikus foszfatz gn (phoa) promtert s N-terminlis leader
szekvencijt tartalmazza. gy a fehrjnk olyan N-terminlis szekvencival fog kifejezdni, ami a
periplazmatikus trbe kldi. A promtert lehet induklni foszft megvonssal, vagy akr heztetssel. Ilyen
promter tallhat a pTA vagy pBAce vektorokban.
rrnB promter: Magyar vonatkozs promter; Venetiner Pl akadmikus s munkatrsai (MTA SZBK,
Szeged) fejlesztettk ki. Azon alapul, hogy a transzkripci mrtkhez nagyban hozzjrulnak a
promterhez kpest upstream irnyban lv szekvencik is. Ezrt az 5S rRNS gn promterhez, ami
magban is egy nagyon ers promter, mg egy extra 5-szekvencit adtak -40-60 rgiban. Ez az upstream
szekvencia (UP promter modul) az RNS-polimerz o-alegysg C-terminlis rsznek kthelyt
tartalmazza, gy rtelemszeren megnveli a gntrs hatkonysgt (kb. 30-szorosra).
162
12.2.1.2. Riboszma kthely (RBS)
Az RBS vagy Shine-Dalgarno szekvencia (amely az trt mRNS 5-UTR, azaz nem transzlld rgijban
tallhat) is nagyon fontos a gnek kifejezdshez. Ez az 5-9 nukleotidbl ll szekvencia komplementer a
16S rRNS 3 rgijval, gy segti a riboszma ktst s a transzlci inicilst. Az RBS s a transzlcit
inicil ATG (start) kodon tvolsga 3-11 nukleotid, s szintn jelentsen befolysolja az expresszi mrtkt
(azaz a tvolsg vltoztatsval is optimalizlni lehet a fehrjetermels szintjt ld. ksbb). Az expresszi
hatkonysgt a RBS-tl mg tvolabb lv 5-nem kdol rgik is befolysoljk s a gn 3-vgn
tallhat transzkripci termincis szekvencik is nvelhetik (br nem esszencilisak a legtbb
rekombinns fehrje ellltshoz).
A kereskedelemben kaphat expresszis vektorok tartalmazzk a megfelel szablyoz elemeket. Neknk
csak arra kell gyelnnk, hogy az expresszland gnnket a megfelel helyre klnozzuk be; a promter s
a riboszma kthely utn, ne vgjuk ki a riboszma-kthelyet, s a leolvassi keret se toldjon el. A
START kodont tartalmazhatja a vektor szekvencia (pl. az NdeI restrikcis enzim felismerhelyben van egy
START kodon: ATGCAT), de a cDNS-sel is bevihetjk a vektorba, csak az RBS-hez val tvolsgra kell
gyelni. A promter s a riboszma-kthely ltfontossgak a gnek expesszijhoz, a szablyoz elem
(opertor rgi) nlkl ugyan mkdhet az expresszis rendszer, de mgis ajnlott erre is gondolnunk, fleg
az expresszi optimalizlshoz (ld. albb). A kivlasztott expresszis rendszer vektorai tartalmazzk ezeket
az elemeket. Azt kell mg meggondolnunk, hogy a kvnt fehrje utols aminosava utn szeretnnk-e
befejezni a fehrje szintzist, vagy fzis cmkt akarunk a fehrje C-terminlis rszre. Els esetben
STOP kodont kell tennnk a cDNS vgre (termszetesen hasznlhatjuk a gn sajt STOP szekvencijt is),
a msodik esetben ki kell ezt hagyni. Ezutn csak az MCS (multiklnoz hely) megfelel helyre kell
bevinnnk az expresszland gn cDNS-t. Az gy elksztett vektort be kell juttatnunk a megfelel
gazdasejtbe (ld. 4.3. fejezet).
12.2.2. A prokarita fehrje expresszi optimalizlsa
Felttelezzk, hogy sikerlt kivlasztanunk a megfelel prokarita expresszis vektort s a vele kompatibilis
baktrium trzset. Az inszertnk (a kvnt fehrje cDNS-e) megfelel helyre bekerlt az expresszis
vektorba. Sikerlt a plazmid transzformlsa az expresszis trzsbe, a transzformlt baktriumok jl
osztdnak. Az indukcit is jl elvgeztk, de vagy nincs termknk, vagy nem megfelel a mrete, vagy
nem elegend a mennyisge. Mi lehet a gond, mi a teend?
1. Nzzk jra t a vektor trkpt, nem klnoz vektort hasznlunk-e, ami nem tartalmaz riboszma
kthelyet! Megfelel leolvassi keretben (frame-ben) van-e az inszert. Ez klnsen az N-terminlis
fzis cmkt tartalmaz konstrukciknl fontos (ld. 12.2.3.). A hrommal nem oszthat szm
hasthelyekkel vatosan kell bnni (ilyen pl. a NotI), mivel ezek knnyen eltolhatjk a leolvassi
keretet.
2. Szekvenljuk a plazmidban lv inszertet! Nincs-e benne delci, inszerci, ami frame eltolst vagy
STOP-kodon beplst okoz. A plazmid promtere s a transzkripcis termincis szekvencia kivl
primerl szolgl a szekvenlshoz. Ez a pET-plazmidoknl maga a T7-promter (T7forward), vagy a
T7Term (T7Term-reverse).
3. Kvessk nyomon a fehrjnk sorst! Vegynk mintt minden lpsnl, futassuk meg a mintkat
SDS-poliakrilamid glelekroforzissel (SDS-PAGE) s festssel, vagy Western-blottal ellenrizzk a
kapott termket. Legyen mintnk az induklatlan sejtekbl, majd az indukci utn is a sejtekbl, a sejt
feltrsa s centrifuglsa utn a fellszbl s a pelletbl (csapadk, ami a centrifugacs aljn
sszegylt), majd az sszes tiszttsi lps utn is. (A fehrjk tiszttst ld. 12.2.4. fejezet.)
4. Van fehrjnk, csak sajnos nem az oldhat frakciban, ami a sejt liztum fellszja, hanem a
csapadkban. Ez azt jelenti, hogy a fehrjnk oldhatatlan formban van a zrvny testben (ms nven
163
inklzis test). Ekkor kt lehetsg ll elttnk: az inklzis testbl preparljuk tovbb a rekombinns
fehrjt minden htrnyval s elnyvel egytt, vagy megprbljuk eltolni a fehrje termelst az
oldhat forma irnyba.
5. Nagyon kevs fehrjnk van. Mirt nem expresszldik a fehrje?
- Prbljuk optimalizlni az indukcis krlmnyeket; hmrsklet, id, indukcis gens
koncentrcija.
- Korai terminlds, mert ritka kodonok vannak az inszertben kzel egymshoz (olyanok,
amelyekre nincs elg antikodont hordoz tRNS a gazdasejtben) - pl. humn fehrjt szeretnnk
expresszltatni prokaritban, ahol ms bizonyos aminosavak kodon preferencija. Hasznljunk
olyan baktrium trzset, amely ritka kodonokat is hasznl (pl. Rosetta, a Novagen cgtl, vagy
CodonPlus, a Stratagene cgtl). Emlkezznk, fajonknt ms s ms a kdsztr kodon
hasznlati gyakorisga! Az E. coli s a humn kdsztrak kodon gyakorisgt a 12.1.
tblzatban hasonltjuk ssze. Srgval emeltk ki az E. coli ltal hasznlt ritka kodonokat.
- Rvid az mRNS letideje, hasznljunk olyan trzset, amelyben bizonyos RN-zok hinyoznak. (pl.
BL21Star)
- Nem elg stabil a fehrjnk s degradldik a tisztts sorn. Hasznljunk protez gtlszereket,
trjuk fel a sejteket vatosabban, s tartsuk minden tiszttsi lpsnl a prepartumot jgen, vagy
4C-on.
- Fejeztessk ki a fehrjnket expresszit s oldhatsgot segt N-terminlis cmkkkel, ilyen pl. a
GST illetve MBP cmke (ld. 12.2.3.).
- Gondoljuk meg, htha elg a cljainknak a fehrje kisebb rsze, N- vagy C-terminlis csonkolt
rsze, fragmentuma. Expresszltassuk a felteheten rendezetlen N- vagy C-terminlis rszeket
kdol rgi nlkli fehrjt. A fragmentumot kdol templt DNS-t szubklnozssal, in vitro
mutagenezissel, PCR mdszerrel llthatjuk el.
- Toxikus lehet a fehrjnk a gazdasejt szmra, ezrt hasznljunk olyan rendszert, amelyben nagyon
szigor szablyozs alatt van a promter. Ilyenek a pLysS s pLysE plazmidot tartalmaz trzsek.
- Prbljunk ki ms promterrel rendelkez expresszis vektorokat, ms baktrium trzseket.
- Hasznljunk msik tptalajt a baktrium kultra nvesztshez. ltalban LB tptalajban
fejeztetjk ki a fehrjt, de vlthatunk YT, 2YT, Terrific Broth, NzCYM, Nzamin tpra is.
Vltoztathatjuk a tptalaj NaCl koncentrcijt is: 0,2-0,6 M kztt. Adjunk a nvesztshez glkzt
(vigyzat, mert lac-opertort tartalmaz vektoroknl ekkor meg kell nvelni az IPTG
koncentrcijt!), vagy ms cukrot
- Fejeztessnk ki bakterilis dajkafehrjket (chaperonokokat) a fehrjnkkel egytt a hatkonyabb
folding rdekben. Pldul a DnaK-DnaJ chaperonokat vagy a GroEL-GroES chaperoninokat
hordoz expresszis vektorokkal egytt expresszltassuk a fehrjnket (ld. 12.2.2.4.). Elkpzelhet,
hogy a fehrjnket csak a klcsnhat partnervel egytt lehet expresszltatni ezt is rdemes
kiprblni.
- Vltsunk expresszis rendszert, pl. eukarita expresszis rendszerre trjnk t (ld. 0. fejezet).
164
12.1. tblzat: Az E. coli s a Homo sapiens kdsztr sszehasonltsa
Ne felejtsk el, hogy a rekombinns fehrjk expresszija, br vannak ltalnos elvek, mgis a tapasztalaton
alapul. Ksrletezni kell, hogy melyik krlmny, forma a legoptimlisabb az adott fehrje s az adott
konstrukci ellltshoz.
12.2.2.1. Az indukcis krlmnyek optimalizlsa
Az indukcis krlmnyek optimalizlsa az expresszis id, a hmrsklet s az induktor
koncentrcijnak a vltoztatst jelenti, mikzben monitorozzuk az expresszldott fehrje mennyisgt
mind a sejtliztum oldhatatlan (centrifugls utni csapadk), mind az oldhat frakcijban (fellsz). Az
expresszlt fehrje mennyisgt nyomon kvethetjk SDS-PAGE-val, vagy Western blottal. A Western blot
elnye, hogy a specifikus ellenanyag megmondja, melyik csk felel meg a glen a fehrjnknek. Ez akkor
klnsen nagy segtsg, ha nem vagyunk biztosak a fehrje elektroforetikus mobilitsban, vagy kevs a
mennyisge. Hasznlhatunk a fehrjnkre, vagy a fzis cmkre specifikus ellenanyagot (anti-His, anti-
GST, anti-MBP, anti-Flag, anti-HA). Ez a ksrlet arra a krdsre is vlaszt ad, hogy termeldik-e (nem
trtnt-e korai terminci) s mennyire stabil (degradldik-e) a fehrjnk.
Hogyan fgg a vizsglt hrom paramtertl az expresszi mennyisge, sebessge? Minl magasabb a
hmrsklet, s nagyobb az induktor koncentrcija, annl gyorsabban fejezdik ki a fehrje. Ez olyan gyors
lehet, hogy a fehrje megfelel feltekeredsre, harmadlagos szerkezetnek felvtelre nem lesz id, gy a
fehrje bels hidrofb magjai kvlre kerlnek, s ezen keresztl a fehrjk sszetapadnak, aggregtumokat
kpeznek s oldhatatlan formban kicsapdnak. Ezt ltalban el kell kerlnnk, mert nehz a fehrjt
visszaoldani, illetve renaturlni gy, hogy visszanyerje a biolgiai aktivitst (kivve, ha eleve
165
zrvnytestbl szeretnnk preparlni). IPTG-vel trtn indukci esetn, ami a legelterjedtebb indukcis
mdszer, ltalban 0,01-1 mM kztt vltoztatjuk az IPTG koncentrcijt. A hmrsklet hatsa is
knnyen rtelmezhet, hiszen minl magasabb hmrskleten trtnik az indukci, annl gyorsabban megy
vgbe minden folyamat, gy a transzkripci s a transzlci is a sejtben. ltalban 15-37C kztt trtnik
az expresszi. Az optimlis hmrsklet mellett rdemes belltani az induktor koncentrcijt s az
expresszi idejt is. Minl hosszabb ideig induklunk, annl tbb fehrje keletkezik, ami nveli az eslyt
annak, hogy oldhatatlan fehrjt kapunk. Szisztematikusan meg kell nzni a fehrje mennyisgt a
paramterek vltoztatsval mind az oldhat, mind az oldhatatlan frakciban.
12.2.2.2. Expresszis trzsek (BL21pLysS, BL21pLysE, Rosetta, BL21Star, stb.)
Sokszor segtsget jelent, ha ms trzsben fejeztetjk ki a fehrjnket. Ha pldul arra gyanakszunk, hogy
korai terminci miatt levlik a riboszmrl a mRNS, ezrt nincs megfelel mret termknk az
expresszi sorn. Ha a fehrjnk cDNS-nek bioinformatikai vizsglata is azt mutathatja, hogy tbb ritka
kodon van egyms utn, amin nem ll mdunkban mdostani, akkor rdemes olyan gazdatrzset
hasznlnunk, amely tartalmaz ritka kodon tRNS-eket. Ilyen a BL21 szrmazk Rosetta trzs (Novagene).
Ha rvid az mRNS letideje a sejtben, akkor fejeztessk ki a fehrjnket BL21(DE3)Star sejtekben. Ennek
a trzsnek a fenotpusa: F ompT hsdSB(rB, mB) gal dcm rne131 (DE3). Ebbl ltszik, hogy alkalmas
IPTG induklta gnexpresszira T7-promteren keresztl, az ompT- s lon- protezok inaktvak
(defektesek), ami fontos, hogy ne degradldjon a rekombinns fehrjnk. A fenti tulajdonsgok a
BL21(DE3) sejtekben is megtallhat, de a Star-nl mg a rne131 jelzs is szerepel, ami azt jelenti, hogy az
RNz-E gn csonkolt, ezrt inaktv. gy megn a sejtben a mRNS stabilitsa, letideje.
Ha toxikus a fehrjnk (pl. aktv protein-kinzt, foszfatzt, protezt fejeztetnk ki), hasznljunk pLysS
trzset, gy csak az indukci megkezdsvel expresszldik a fehrje, addig zavartalanul szaporodhatnak a
sejtek. A rekombinns fehrjk ellltsoz hasznlatos trzsekrl kitn sszefoglal olvashat itt. Az
emltett trzsek genotpusrl pedig ezen az oldalon tall az olvas tovbbi rszleteket.
12.2.2.3. Promter optimalizls
Amennyiben mindent kiprbltuk, de mg gy sem expresszldik megfelelen a fehrje, akkor rdemes
ms promterrel is prblkozni. Ez azt jelenti, hogy ms promtert tartalmaz expresszis plazmidba kell az
inszertnket szubklnozni. Lehet, hogy a T7lac promter olyan mrtk expresszit eredmnyez, ami sszes
fehrjnket zrvnytestbe viszi. Ilyenkor megoldst jelenthet a gyengbb tac vagy lac promter hasznlata.
Ne felejtsk el, a promterek csak a nekik megfelel expresszis trzsben mkdnek. Pldul a T7 promter
nem mkdkpes, ha nincs a baktriumban T7 RNS-polimerz, ezrt ehhez a promterhez mdostott
BL21 trzset kell hasznlnunk, mint a BL21(DE3) vagy a HMS174(DE3). (A DE3 profg hordozza a
lac-promter szablyozsa alatt a T7 RNS-polimerz gnjt.)
12.2.2.4. Koexpresszi
A koexpresszi azt jelenti, hogy egyszerre egy sejten bell tbb polipeptidlncot fejeztetnk ki. Szksgnk
lehet erre, ha pldul egy heterodimer fehrjt kell ellltanunk rekombinns formban. Tovbbi elny
lehet, hogy mr a sejten bell ltrejn a kt polipeptidlnc (vagy fehrje) kztti klcsnhats, ami segthet a
lncok feltekeredsben, vagy ha a bennnket rdekl fehrjvel egytt egy mdost enzimet
expresszlunk, a posztranszlcisan mdostott rekombinns fehrjt izollhatjuk a gazdasejtbl. J plda
erre, ha egy fehrjt aktv formban szeretnnk ellltani (pl. egyes MAPK enzimeket), de az aktivl
foszforilci nlkl ez nem sikerlhet. Megoldst jelenthet, ha a MAPK fehrjt az aktivl protein-kinzzal
(MAPKK) egytt fejeztetjk ki. gy megkapjuk a MAPK fehrjt aktv, foszforillt formban.
Koexpresszira prokaritkban tbbfle lehetsgnk van:
166
- Egy promter, tbb RBS s inszert cDNS, azaz egy policisztronos mRNS-t kapunk, amelyrl tbb
fehrje expresszldik (mint a bakterilis operonoknl). Ilyenkor a mRNS-hez tbb riboszma is
ktdik az RBS-eknek megfelelen, s egyszerre kezdi a fehrjk szintzist. Megjegyzend, hogy a
promterhez kzelebb elhelyezked ORF-rl tbb polipeptidlnc fog szintetizldni.
- Tbb azonos promter egy plazmidon, amelyrl gy tbbfle mRNS rdik t. A mdszert pldul
heterodimer fehrje ellltsra hasznlhatjuk.
- Tbb plazmid, amely klnbz inszertet hordoz. De ennek felttele, hogy ms legyen a plazmidok
replikonja, azaz klnbz kompatibilitsi csoportba tartozzanak s klnbz antibiotikum
rezisztencia gnt hordozzanak (ld. 7.2.1 fejezet).
- Egy promterhez fzis fehrjeknt kapcsoljuk a kt klnbz fehrjelncot. Azaz nem hasznlunk
STOP kodont az els fehrjt kdol szekvencia utn, hanem rgtn kvetkezik a msik polipeptidet
kdol szekvencia.
12.2.3. Fzis rekombinns konstrukcik
Sokszor az is megolds lehet a sikertelen expresszira, ha a kvnt fehrjnket fzis fehrjeknt fejeztetjk
ki. Ekkor a fehrjnk vagy N-, vagy C-terminlis rszre, vagy mindkettre tervezhetnk cmkt (tag-et).
Ezek a cmkk segthetik a
- fehrjnk oldhatsgt, expresszijt,
- olyan szignl szekvencikat tartalmazhatnak, amelyek megfelel kompartmentekbe irnytjk a
fehrjt,
- segtik a fehrje tiszttst affinits kromatogrfival
- lehetv teszik a fehrje nyomonkvetst is, pl. enzimaktivitsuk rvn vagy antignknt
szolglhatnak Western-blot esetn
A 12.1. videon egy fzis rekombinns fehrje tiszttsa mutatjuk be affinits kromatogrfival, FPLC
kszlk segtsgvel
12.1. video: Fzis rekombinns fehrje tiszttsa affinits kromatogrfival (FPLC)
167
12.2.3.1. GST-cmke
A GST, azaz a glutation-S-transzferz olyan enzim, amely glutation felhasznlsval a sejtben lv kis
toxikus molekulkat lebontja. A GST kompakt, globulris, nagyon stabil fehrje, 25 kDa molekulatmeggel.
Nagyon jl kifejezdik s oldatban marad prokarita sejtekben, radsul segti a hozz kovalensen kapcsolt
fzis partner kifejezdst is, ha a kifejezend fehrje N-terminlisra tesszk. Tovbb a GST-cmkn
keresztl a fehrje nagyon jl tisztthat affinits kromatogrfival. Az elre gyrtott glutation-agarz
gyanthoz (szmos cg rulja) ugyanis a GST nagyon nagy affinitssal ktdik (szubmikromlos a K
D
). A
gyanthoz nagy affinitssal ktd fehrjket szabad glutationt tartalmaz oldattal (10-20 mM) elulhatjuk.
gy elg tiszta fehrje prepartumot kapunk. A GST-gyanta nagy kapacitc; 1 ml tiszta gyanta kb. 6-8 mg
fehrjt tud megktni, s hasznlat utn regenerlhat. GST-cmkvel expresszlhatjuk a fehrjnket, ha pl.
pGEX expresszis vektorok valamelyikvel dolgozunk. Rszletesebben itt olvashatnak rla.
12.2.3.2. MBP-cmke
Az MBP (maltose-binding protein), vagyis a maltz-kt fehrje az E. coli malE gnjnek 42 kDa tmeg
termke. A fehrje a baktrium maltz transzportjban jtszik szerepet, ezrt ers affinitssal ktdik a
maltzhoz (a K
D
< 1 M). Ez a tulajdonsga lehetv teszi, hogy az agarz gyngyhz immobilizlt maltz
a sejtliztumbl megksse az MBP-fzis fehrjnket, amelyrl szabad maltzzal elulhat a fehrje. Az
elcis oldatunk kb. 10-30 mM maltzt kell tartalmazzon. Mivel a fehrje a baktrium sajt fehrjje, ezrt
az N-terminlisan hozzkapcsolt fehrje expresszis tulajdonsgait (pl. oldhatsg) is jelentsen javthatja.
MBP-fzis fehrjt a pMal sorozat (New England Biolabs) vektoraival lehet ellltani.
12.2.3.3. Polihisztidin-cmke
Taln a leggyakrabban hasznlt fzis rendszer. 6-10, de leggyakrabban 6 hisztidin aminosavbl ll
cmke, amit tervezhetnk a fehrje N-, vagy C-terminlis vgre is. Kismret cmke, ezrt felteheten a
legkevsb zavarja a fehrje mkdst. Nagy affinitssal ktdik a Ni-gyanthoz (Ni
2+
-ionokat ktnek
koordincis ktssel a gyanta specilis csoportjaihoz). A ktds azon alapul, hogy a Ni
2+
-ion koordincis
szfrjnak a felt foglaljk csak el a gyanta funkcis csoportjai, gy a hisztidin imidazol gyrjnek
nitrognatomja koordincis ktst hoz ltre a fmionnal is. Ez a kts elg ers, de fmkeltorokra (EDTA,
EGTA) nagyon rzkeny. Ezrt az affinits kromatogrfiai lpsek sorn ezeket a komponenseket kerlni
kell, mert leszedik a fmiont a gyantrl. Szintn kerlni kell a Ni-ionnal csapadkot kpez vegyleteket,
ilyenek a biokmiai reduklszerek, a DTT, vagy a bta-merkaptoetanol, mivel ezek tnkreteszik a gyantt,
illetve az oldat pH-ja sem lehet tl lgos, vagy savas. Viszont ezt az affinits kromatogrfis lpst lehet
ers detergens jelenltben, vagy denaturl krlmnyek kztt is hasznlni (pl. preparls inklzis
testbl). Nemcsak Ni
2+
-ion, hanem Co
2+
-ion is lehet az agarz gyanthoz koordinlva, ezrt ezt a tiszttsi
mdszert fm-affinits kromatogrfinak (metal-affinity chromatography) hvjuk.
Az elci itt is kompetcin alapul, imidazol oldattal (50-500 mM) szortjuk le a gyantrl a fehrjnket. Ez
a legelterjedtebb mdszer, de az elci megoldhat a pH cskkentsvel is. Ilyenkor lassan cskkentjk a
pH-t, elszr a kevsb specifikus ktsek, majd az ersebb ktsek sznnek meg. Az ok, hogy a pH
cskkensvel a hisztidin nem-kt elektronprral rendelkez N-atomja protonldik, s nem tud
koordinldni a Ni
2+
-hez. Ezltal fokozatos elcit rhetnk el, gy tisztbb lehet a fehrje prepartumunk (a
Ni
2+
-gyanta nemcsak polihisztidin-cmks fehrjket kt, hanem ms fehrjket is, ahol trkzelben vannak
hisztidin aminosavak, persze azokat kisebb affinitssal). A 12.7. bran lthat egy 85 kDa tmeg fehrje
Ni
2+
-affinits kromatogrfival trtn tiszttsa.
A tisztts klnbz lpseiben mintt vettnk, s megfuttattuk SDS-poliakrilamid glen, amit
fehrjefestkkel (Coomassie Brilliant Blue) hvtunk el. Lthat, hogy a 100 mM imidazollal trtn elci
nem elg ahhoz, hogy leszortsa a gyantrl a fehrjnket, mg 400 mM imidazollal nagy mennyisg,
viszonylag tiszta prepartumot kapunk.
168
A His-taget gyakran kombinljk ms cmkkkel is, pl. N-terminlis GST-, vagy MBP-fzival. A
tiszttsnl elszr Ni
2+
-affinits kromatogrfival izolljuk a sejtliztumbl a fehrjt, majd a msik cmke
felhasznlsval a msik kromatogrfis tiszttst is elvgezzk. Ezltal jelentsen megnvekszik a fehrje
tisztasga s ha a kt cmke a fehrje kt oldaln tallhat, ez lehetsget teremt arra is, hogy csak a teljes
hosszsg fehrje maradjon a prepartumban.
12.7. bra: Ni
2+
-affinits tisztts glelektoforetikus kpe. 1. sv: fehrje marker; 2. sv: a sejt nem oldhat frakcija
(centrifugls utni csapadk); 3. sv: a sejt oldhat frakcija (fellsz); 4. sv: elci 100 mM imidazollal; 5. sv:
elci 400 mM imidazollal
12.2.3.4. Egyb cmkk
Sok egyb expresszis vektorban van lehetsg cmkvel elltott fehrje kifejezsre (ld. 12.2. tblzat).
A krds csak az, mi a clunk. Nvelni akarjuk a fehrje oldhatsgt, expresszijt vagy nagyobb mrtk
tiszttst szeretnnk elrni? Nyomon szeretnnk kvetni a fehrjnk kifejezdst, lokalizcijt pl.
eukarita sejtekben? ltalban elmondhatjuk, hogy egy cmknek tbb funkcija is van, s csoportostsuk
egyik alapja ppen a felhasznls lehet. Ez alapjn beszlhetnk affinits, szolubilizcis, epitp, vagy
akr fluoreszcens cmkrl is. Egy-egy cmke tbb csoportba is besorolhat, pl. a GST-cmke nveli a
fehrje oldhatsgt, lehet affinits-alap tiszttsra hasznlni, s mg ellenanyag is kszlt r, amivel
nyomon lehet kvetni. Az alkalmazott cmkk ellen ltalban ltezik ellenanyag, gy Western-blottal vagy
eukarita sejtek esetn immunfestssel lthatv tehetk. Lteznek olyan eukarita vektorok is, amelyek
fluoreszcens fehrjket, vagy enzimaktivitssal rendelkez fehrjket knlnak fzis cmknek. Ilyen cmke
a GFP (green fluorescent protein) s vltozatai, vagy az enzimaktivitssal rendelkez -galaktozidz, illetve
luciferz. Ezeket azonban felhasznlsuk miatt az eukarita expresszis rendszernl trgyaljuk.
Az expresszis cmkk hasznlatrl itt tallnak tovbbi hasznos informcikat.
169
12.2. tblzat: Fzis cmkk s alkalmazsaik
12.2.3.5. A fzis cmkk eltvoltsa
A nagyobb mret cmke jelenlte befolysolhatja a fehrje biolgiai funkcijt pl. aktivitst, ktdst
ms fehrjhez, vagy a harmadlagos, negyedleges szerkezetnek kialakulst. Pldul a GST dimerizcira
hajlamos, gy mr eleve rknyszertheti a fzis partnert is, hogy dimerizljon. Ezen okok miatt rdemes
tisztts utn a fehrjrl valamilyen protezzal levgni a fzis cmkt. Szmos vektorban mr eleve
beterveztk a protez hast/felismerhelyt. Termszetesen olyan enzimeket kell hasznlni, amelyeknek
nagyon specilis hasthelye van, s ritkn fordul el a fehrjkben, gy nem hastja ms helyeken is a
rekombinns fehrjnket. Nhny esetben a kmiai hasts is szba jhet; pl. a brm-cin AspPro
aminosavak kztt hast. A 12.3. tblzat foglalja ssze a leggyakrabban hasznlt proteolitikus enzimeket
hasthelyeikkel egytt.
A protezzal val hasts trtnhet az elci utn, oldat fzisban. Ilyenkor a fzis cmktl, a nem hastott
fzis fehrjtl s a proteztl is meg kell tiszttanunk a fehrjnket valamilyen kromatogrfival.
Kismret (peptid) cmkket el lehet tvoltani dialzissel, vagy glszrssel. Msik lehetsg, hogy a
gyantra felkttt s mosssal tiszttott fehrjrl az oszlopon hastjuk le a fzis cmkt. Ilyenkor a cmke
az affinits oszlopon marad, mg a fehrjnk lecspg az oszloprl. Ekkor csak a proteztl kell
megszabadulnunk. Vigyznunk kell, hogy a proteznak s a fehrjnknek is megfelel puffert alkalmazzunk
a hasts sorn.
170
12.3. tblzat: Fzis cmke lehastsra alkalmas proteolitikus enzimek s jellemzik
12.2.4. Rekombinns fehrjk termelse s izollsa
Ha optimalizltuk fehrjnk expresszijt, s tudjuk azt is, hogy a sejt mely rszbl kell tovbb
tiszttanunk, akkor elkezdhetjk a nagyobb mennyisg fehrje termelst clz, nagy lptk expresszi
vgrehajtst, amely a kvetkez alfejezetekben ismertetett lpsekbl ll.
12.2.4.1. Indt (starter) kultra elksztse
Az elkszlt rekombinns DNS konstrukcit transzformljuk a megfelel expresszis trzsbe (pl.
BL21(DE3)). A transzformtumot megfelel antibiotikumot tartalmaz szilrd tptalajra szlesztjk s
37C-on inkubljuk. Msnap egy jl krlhatrolt telepet antibiotikumot tartalmaz 50 ml LB-tpba oltunk .
Ez lesz a starter kultra, amit 37C-on rzats mellett nvesztnk. 12-16 ra mlva, a starter kultra
megfelelen felszaporodik.10-20 ml-t 1l megfelel antibiotikumot tartalmaz folykony tptalajba oltjuk,
amivel elindtjuk az expresszis kultrnk nvesztst. A megfelel expresszis kln folyadkkultrban
felnvesztett szuszpenzija 10% glicerinnel (amely ez esetben a fagyll szerept tli be) elkeverve
lefagyaszthat s 80C-on hossz ideig trolhat. Ilyen glicerines expresszis klntr ltrehozsval
kivlthatjuk a gyakran hasznlt klnok expresszis sejtbe val transzformlst, elg a fagyasztott kultra
tredk rszt szilrd tptalajra inokullni.
12.2.4.2. Az expresszis kultra nvesztse s indukcija
A megfelelen inokullt (ld. 12.2.4.1.) baktrium tenyszetet 37C-on, folyamatos rzats (140-200 rpm)
mellett inkubljuk. Egy rzinkubtort a 12.8. bran mutatunk be. Inkubci kzben nyomon kvetjk az
osztd baktriumtenyszet srsgt. A tenyszet srsge jelzi az osztdsok elrehaladst, a
baktriumpopulci szaporodst s egyszeren, az optikai denzits 600 nm-en val mrsvel,
spektrofotomteren mrhet. OD
600 nm
= 0,8 krli rtknl a baktriumkultra kszen ll az indukcira. Ha
szksges, htsk le az indukci hmrskletre s vegynk belle mintt a ksbbi SDS-glfuttatshoz. Ez
lesz az indukci eltti minta. Ha a termoszttunk hmrsklete elrte az indukcihoz szksges rtket
tegyk bele a megfelel mennyisg induktort, ami a leggyakrabban IPTG. Inkubljuk s rzassuk a
megfelel ideig, majd vegynk belle mintt. Ez lesz az indukci utni minta. Az expresszis kultrbl a
kvetkez lpesek sorn tiszttjuk a termelt rekombinns fehrjt.
171
12.8. bra: Rzat inkubtor prokarita s eukarita szuszpenzis kultrhoz
12.2.4.3. A sejtek sszegyjtse (harvesting)
Ahhoz, hogy a sejtekbl a fehrjt a megfelel tiszttsi lpsekkel izolljuk, elszr ssze kell gyjtennk a
sejteket a tptalajbl. Ez a lps centrifuglssal trtnik (5000 g x 10 min, 4C-on). A tisztts sorn mindig
jgben, vagy 4C-on dolgozunk, hogy ne degradldjon a fehrje. A sejteket meg kell tiszttanunk a
tptalajtl, amit legtbbszr egy pufferrel (pl. PBS) val mosssal vgznk. A sejteket ezutn jra
centrifuglssal gyjtjk ssze.
12.2.4.4. A sejtek feltrsa
Az sszegyjttt sejteket lizlva a sejtben lev fehrje kinyerhet. A lzist a sejtek lzis pufferben val
inkublsval vgezzk. 1g baktrium sejtre ltalban 3-4 ml lzis puffert szmolunk.
A lzis puffer sszettele:
- Megfelel pH-t biztost puffer (ltalban 7-9 pH-tartomnyban): pl. 20 mM TRIS, foszft puffer.
- S, ami ionerssget biztost, ltalban NaCl, 0,15-0,5 M.
- Detergens, ami segti a sejtek feltrst, illetve a fehrjk oldatban tartst s cskkenti az aspecifikus
klcsnhatsokat, pl. 0,1-0,2% Tween20, CHAPs, TritonX 100.
- Glicerin 5-10%-ban, ami stabilizlja a fehrjket.
- Reduklszer, a nem megfelel diszulfidhidak reduklshoz: 2-10 mM bta-merkaptoetanol (a DTT-
re s DTE-re vigyzni kell fm-affinits kromatogrfia esetn).
- Protez gtlk, a sejtek degradldsnak kivdsre: pl. 1 mM PMSF, 1-5 mM benzamidin.
A lzist segti, ha tbbszrs fagyasztst-felolvasztst alkalmazunk, s/vagy ha a felszuszpendlt
sejtkultrhoz lizozimot adunk. A lizozim kpes a baktriumok sejtfalt bontani s ezrt alkalmas a lzisre.
Nagyon hatsos a Gram-pozitv baktriumoknl, de a Gram-negatv baktriumoknl is hasznos, ha
detergenssel, vagy ozmotikus sokkal egytt alkalmazzuk. Szoniklssal (a sejtek ultrahang segtsgvel
trtn feltrsval) is segthetjk a sejtek lzist, s a benne lv DNS darabolst. Vigyzzunk azonban,
mert szonikls hatsra melegszik az oldat, ami a prepartumban lv protezok aktivitsnak nvekedst,
gy a fehrjnk degradldst okozhatja, s emellett a fehrjnk denaturcijhoz vezethet. Ezrt ezt a
folyamatot jgben s sznetekkel vgezzk (1 perc szonikls meghatrozott frekvencival, majd egy perc
sznet). Ezt a lpst ismteljk 3-4-szer, mg a prepartum hgan folyss nem vlik. Ezutn DN-z I
172
enzimmel kezeljk, ami a DNS-t kisebb darabokra vgja. A sejtek feltrst vgezhetjk ers detergenssel
(TritonX 100 1-2%), deoxiklsavval vagy az n. French-Press kszlkkel is (ez utbbiban a nagy nyoms
trja fel a sejteket). A feltrs utn centrifuglssal elvlasztjuk az oldhat s az oldhatatlan frakcit. A
fellsz a lzispufferben oldd fehrjket, komponenseket, mg az oldhatatlan frakci (csapadk) a
sejttrmelket s az inklzis testet tartalmazza. A tovbbi lpsek attl fggenek, hogy hol tallhat a
fehrjnk; a fellszban oldhat formban, inklzis testben oldhatatlan formban, vagy a periplazms
trben.
12.2.4.5. Izolls oldhat frakcibl
Ha a fehrjnk az oldhat frakciban van jelen, felteheten natv formban, akkor ezt a protokollt kell
kvetnnk. A baktrium liztumban szmos fehrje van, kztk protezok is, amelyek emszthetik a
rekombinns fehrjnket. A tisztts sorn ezeket el kell vlasztanunk. A sejtek sszegyjtse utn a
fellszt visszk tovbb, s a cmknek megfelel affinits kromatogrfis tiszttsi lps kvetkezik.
Amennyiben a fehrjnk tartalmaz polihisztidin cmkt, ezt a legclszerbb alkalmazni, mert nagy affinits
s denaturl krlmnyek kztt is mkdik.
12.2.4.6. Preparls zrvnytestbl (inclusion body)
Ha a fehrjnk nem az oldhat fzisban, hanem a csapadkban van jelen, akkor fel kell oldanunk, amire
szmos lehetsg knlkozik: 5-8 M guanidin-HCl, 6-8 M urea, SDS-oldat, lgos pH. A csapadkot elszr
mossuk 1-2% Triton X 100 oldattal, majd centrifugljuk. A mosott csapadkot szolubilizl oldatban (5-8 M
guanidin-HCl vagy 6-8 M urea) vesszk fel. A csapadkot fel-le pipettzssal oldjuk, s 4C-on tbb rn t
llni hagyjuk. Inkubls utn tisztts cljbl ismt lecentrifugljuk az oldatot, de most mr a fellsz
tartalmazza a feloldott fehrjnket, igaz a denaturlszerben. Vlaszthatunk, hogy elvgezzk denaturl
krlmnyek kztt a fm-affinits kromatogrfit, vagy megprbljuk renaturlni a fehrjt, s utna
alkalmazzuk a tiszttsi lpst. Legclravezetbb az elszr alkalmazott fm-affinits kromatogrfia, hisz ez,
mint mr emltettk, denaturl krlmnyek kztt is jl mkdik, felttele viszont, hogy a fehrjnk
tartalmazzon His-cmkt. A gyantra felkttt s mosott fehrjt vagy olyan elcis pufferrel eluljuk, ami
mg tartalmazza a denaturlszert, vagy lecserljk a mos-elul puffert denaturlszer nlkli pufferre.
Amennyiben az elcis puffer is tartalmaz denaturlszert, akkor meg kell szabadulni tle, hogy a fehrjnk
renaturldni tudjon. Erre legjobb mdszer a dialzis. Ez trtnhet lpsenknt, azaz fokozatosan
cskkentjk a dializl pufferben a denaturlszer koncentrcijt, s kzben emeljk a NaCl mennyisgt,
hogy ne aggregldjon a fehrje. A dialzis sorn a fehrje visszanyeri a szerkezett, s remlhetleg a
biolgiai aktivitst is. Ezt persze fgg a fehrjtl, minl tbb domnbl ll egy fehrje, annl
remnytelenebb a renaturci. Szintn remnytelen a renaturci, ha a fehrjnk feltekeredshez az eredeti
sejtkrnyezetben dajkafehrjkre van szksg. A dialzis sorn a ciszteint tartalmaz fehrjknl
mindenkppen alkalmazzunk reduklszert: DTE, DTT, bta-merkaptoetanol, TCEP (Trisz-karboximetil-
foszfin). Ennl a mdszernl nagyon fontos, hogy a fehrje elg jl renaturldjon, s visszanyerje biolgiai
aktivitst. Elnye viszont, hogy nagy tisztasg s ltalban nagy mennyisg fehrjt lehet ellltani. Az
inklzis test nagyon kevs egyb fehrjt (s gy protezt) tartalmaz, a rekombinns fehrjnk akr az
sszefehrje 90%-a is lehet.
12.2.4.7. Izolls periplazmbl
A periplazms tr a Gram-negatv baktriumok kls s bels membrnja kztti tr. Itt jobb lehetsgek
knlkoznak a megfelel foldingra s a diszulfidhd kpzdsre. Ide megfelel N-terminlis szignl
szekvencit tartalmaz fehrjk jutnak el. Ilyen szekvencia az ompA, pelB, vagy a phoa-fzis fehrjk.
Ilyenkor a tiszttshoz hasznlt cmkt a C-terminlisra kell tenni.
A sejt feltrsa enyhbb krlmnyek kztt, nem szoniklssal, hanem ozmotikus sokkal trtnik. A
173
sejteket 80 ml puffer/1 g sejtcsapadk mennyisg lzis pufferben kell felvenni, amely tartalmaz 20%
szacharzt is. Az izoozmotikus oldatban lv sejteket centrifugljuk (8000 g x 20 min, 4C), majd
szuszpendljuk ket nagy mennyisg 5 mM MgCl
2
oldatban, vgl jabb centrifugls kvetkezik. Az gy
biztostott hipoozmotikus krlmnyek kztt a periplazms fehrjk mr a fellszba kerlnek.
Msik bevlt mdszer, hogy az sszegyjttt sejteket rgtn a MgCl
2
oldatban vesszk fel, ami
hipoozmotikus sokk a sejtnek, s vatosan lefagyasztjuk 20C-on, majd vatosan felengedjk. Ilyenkor a
sejt kls membrnja megsrl, de a bels pen marad. gy centrifuglssal elvlaszthatjuk a sejteket, mg a
fellszban marad a periplazmatikus tr tartalma.
12.2.5. A prokarita expresszi elnyei, htrnyai
Egyik legfontosabb elnye, hogy viszonylag gyors (ha ksz a konstrukci, 3-4 nap alatt termelhet a
fehrje), olcs, s nagy mennyisg fehrje llthat el vele. Htrnya, hogy a fehrjrl hinyzik az
esetleges poszttranszlcis mdosts (foszforilci, glikozilci, acetills), problms lehet az S-S hidak
kpzdse, illetve a fehrje feltekeredse. Sokszor a nagyobb, tbb domnbl ll fehrjket is rosszul lehet
kifejeztetni ebben a rendszerben. Vgl emlkeztetnk a kodon preferencira, ami ha nem megfelel, korai
terminci jhet ltre (br ez a veszly megfelel trzzsel cskkenthet (ld. 12.2.2. fejezet).
12.3. Tovbbi olvasnival a fejezethez
Sambrook, J and Russel, DW (2001) Molecular Cloning. A Laboratory Manual. CSHL Press, volume 1-3,
Third edition. ISBN: 0879695773.
Terpe K. (2006) Overview of bacterial expression systems for heterologous protein production: from
molecular and biochemical fundamentals to commercial systems. Appl Microbiol Biotechnol 72:211222
Graslund S.,Sagemark J., Berglund H., Dahlgren L. G., Flores A et al. (2008) The use of systematic N- and
C-terminal deletions to promote production and structural studies of recombinant proteins. Protein Expr
Purif. 58(2), 210-21.
Structural Genomics Consortium et al. (2008) Protein production and purification. Nature Methods
5(2):135-146
174
13. Eukarita expresszis rendszerek
Napjainkban a fehrjemrnksgnek egyre nagyobb jelentsge van nemcsak a kutatsban, hanem a
gygyszatban is. Biotechnolgiai cgek alakulnak, hogy ellenanyagokat, hormonokat, nvekedsi
faktorokat s egyb polipeptid tpus molekulkat lltsanak el (sokszor kzvetlenl gygyszati clbl; ld.
pl. 15.1.3. fejezet). A bakterilis expresszi ltalban ellt bennnket nagy mennyisg rekombinns
fehrjvel, de a fehrjnk nem biztos, hogy fel tudja venni a biolgiailag aktv formjt. Ennek oka lehet
egyrszt, hogy a baktriumban kevs s ms dajkafehrjk (chaperonok) mkdnek, gy nem lesz megfelel
a fehrjelnc feltekeredse (foldingja) s a szerkezete. Msrszt a poszttranszlcis mdostsok sem
rvnyeslnek, pl. foszforilci, glikozilci, stb. Harmadrszt, a citoplazma reduktv krnyezete miatt a
megfelel diszulfid-hidak sem tudnak kialakulni. Nagymret, tbb domnbl ll fehrjk ellltsa is
problms lehet prokarita rendszerben. Erre az in vitro rendszer rszben megoldst jelenthet, hisz elrhet
emls, vagy akr humn sejtmentes kivonat is. Ezek htrnya azonban, hogy kevs fehrje llthat el
velk. Ha ilyen problmval tallkoznunk, meg kell keresni a megfelel eukarita expresszis rendszert.
Milyen felttelei vannak egy j expresszis rendszernek?
Gyorsan s hatkonyan szaporodjon az organizmus
Nagy mennyisg fehrjt termeljen
Megfelel formban lltsa el a fehrjt
Knnyen kezelhet, olcs s biztonsgos legyen
13.1. leszt expresszis rendszer
A fejezet bevezetjben emltett cloknak majdnem teljesen megfelel az leszt, a legegyszerbb eukarita
gazdasejt. Genetikja, biokmija nagyon jl ismert, mr tbb mint 30 ve hasznljk rekombinns fehrje
termelsre. Nagyon sok leszt faj ismert (kb. 800), ebbl sok alkalmas fehrjetermelsre. A kt
leggyakrabban hasznlt leszt a Pichia pastoris, illetve a kznsges srleszt, a Saccharomyces
cerevesiae. Ezen a kt rendszeren keresztl mutatjuk be az leszt expresszis rendszerek jellemz
tulajdonsgait. Az lesztben hasznlhat vektor tpusokat mr rviden ttekintettk a 7.6. fejzetben.
Minden expresszis rendszer kt alapvet egysgbl ll: a megfelel gazdasejtbl s az expresszis
vektorbl. Az expresszis vektornak hordoznia kell azokat a szekvencikat, amely biztostja a gazdasejtben
a replikcit, s a kvnt fehrje kifejezdst. Az leszt vektorok shuttle (ingz) vektorok, mivel a
baktriumsejtek s az expresszis sejtjeink (leszt, rovarsejt, emlssejt) is repliklni tudjk. Ez gy rhet
el, hogy mindkt gazdasejt tpusra specifikus replikonnal rendelkeznek. Mivel minden fehrjetermels els
lpse az expresszis konstrukci ltrehozsa s a molekulris klnozs, a rekombinns DNS konstrukci
felszaportsa E. coli gazdban a legegyszerbb, leggyorsabb s legolcsbb. Ezt a mveletet brmilyen
expresszis gazdasejtet is hasznlunk, a bakterilis rendszerben vgezzk el.
Alapveten ktfle tpus leszt vektor ltezik: replikld s integrld. A replikld (episzomlis)
vektor extrakromoszomlis formban szaporodik a gazdasejtben. Ilyen vektor hasznlatakor ltalban csak
tmeneti (tranziens) expresszirl beszlnk s a vektornak tartalmaznia kell egy lesztben mkd
replikcis start szignlt is. A msik esetben a kifejezend fehrje cDNS-e homolg rekombincival az
leszt genomjba integrldik. Ekkor stabil expresszirl beszlnk, azaz a rekombinns transzformlt
trzs megrzi a transzgnt, a trzs fenntarthat akr hossz tvon is. A homolg rekombincit integrld
vektorokkal rjk el, amelyek tartalmaznak a genomi DNS szekvencival homolg szekvencikat. A
homolg rekombinci hatsfoka elg kicsi, ezrt mindenkppen ki kell vlogatni a transzformldott
sejteket. Erre a clra szelekcis markereket hasznlunk, amit a vektorunk kdol. Az expresszis kazetta
hordozza a kvnt fehrjt kdol szekvencit s annak kifejezdshez szksges elemeket; promter,
transzkripcis termincis szekvencia, riboszma kthely (Kozak szekvencia). Itt tallhat a multiklnoz
hely (MCS), ahov a klnozs sorn bevisszk a fehrjt kdol szekvencit.
175
sszefoglalva, az leszt expresszis vektorok f elemei:
1. bakterilis elemek: bakterilis replikcis orig, bakterilis antibiotikum rezisztencia gn
2. leszt genetikai elemek, amelyek a homolg rekombincirt vagy a vektor replikcijrt felelsek
(ARS: autonomous replication sequences)
3. szelekcis markerek
4. expresszis kazetta
13.1.1. Az expresszis kazetta
A fehrje expresszi legmeghatrozbb eleme a promter. Milyen legyen egy j promter? Nagymrtk s
specilis expresszit biztostson, amit lehet szablyozni, induklni. Erre legalkalmasabbak a glikolitikus,
vagy ms metabolikus utak enzimeit kdol gnek promterei. A kvetkezkben a leggyakrabban hasznlt
promtereket foglaljuk ssze:
S. cerevisiaepromterek:
- Nagyon ers, de csak gyengn induklhat promterek: PGK (foszfoglicert-kinz), GAPD (glicerin
aldehid-3-foszft-dehidrogenz); induktoruk a glkz
- Ers promter: GAL1 (galaktokinz), galaktzzal induklhat.
- Kzepesen ers promter: ADH2 (alkohol dehidrogenz), a glkz represszlja.
- Kzepesen ers promter: PHO5 (foszfatz), a foszft represszlja.
Pichia pastoris promterek:
- AOX1 promter: a Pichia pastoris alkohol-oxidz gnjnek promtere.
Az alkohol-oxidz enzim a leveg oxignjnek felhasznlsval a metilalkoholt formaldehidd oxidlja,
mikzben hidrogn-peroxid keletkezik. (A folyamat a peroxiszmban jtszdik le, gy nem kros a
sejtnek.) Ez a promter nagyfok expresszit biztost, metilalkohol hatsra akr 5% lehet az enzim mRNS-
nek a mennyisge a teljes mRNS mennyisgre vonatkoztatva, a fehrjeszint pedig az sszes fehrje 30%-t
is elrheti. Tudnunk kell, hogy a Pichia metilotrp leszt, azaz metanolt tud hasznlni egyedli szn-s
energiaforrsknt, ha nincs a mdiumban glkz s glicerin. Teht a glkz s a glicerin represszlja, a
metilalkohol pedig induklja a promter utn lv szekvencia trst. Ez egy idelis promter, hiszen
induklhat mdon nagymrtk expresszit biztost.
- AOX2: a msik alkohol-oxidz enzim gnjnek promtere. Szintn induklhat metilalkohollal, de 10-
szer kisebb expresszit biztost.
- DHAS: a dihidroxi-aceton-szintetz gn promtere. Ez a promter is a metanol metabolizmusban
jtszik szerepet, azaz metanollal induklhat, de nincs olyan ers, mint az AOX1.
- FLD1: a formaldehid dehidrogenz gn promtere szintn a metanol hasznostsban jtszik szerepet.
De metanol mellett metilaminnal is induklhat, gy a metilamin indukci esetn glkz s glicerin is
hasznlhat sznforrsknt.
- GAP1: a glicerinaldehid-3-foszft-dehidrogenz promtere lland expresszit eredmnyez, azaz
konstitutv promter. Akkor hasznlhat, ha a termelt fehrje nem toxikus a sejtre, illetve nem gtolja
a sejt osztdst.
- AOX1-GAP1: tandem promter, amellyel mg nagyobb expresszi rhet el.
Tovbbi szablyoz elemek:
A promter mellett ezeknl a vektoroknl is fontos, hogy az expresszis kazetta tartalmazzon
transzkripcis termincis szekvencit, valamint a mRNS processzlshoz s a poliadenilcihoz
szksges elemeket. Legtbbszr a PGK, GAPD s CYC1 gnek transzkripcis termincis szekvencijt
hasznljk. Fontos mg a transzlci inicicijhoz szksges szekvencik jelenlte is. Ezt a szekvencit
eukaritkban Kozak szekvencinak nevezzk, ami nlkl nem, vagy nagyon gyengn megy az expresszi.
Egyes vektorokban (klnsen N-terminl fzis konstrukcikban) ez mr adott, klnben neknk kell
beptennk.
176
13.1.2. Szelekcis markerek
Szelekcit kt klnbz elv alapjn vgezhetnk. Az egyik esetben az expresszis vektor bioszintetikus
utak enzimeit kdolja, pl. HIS3, HIS4, ADE1, URA3, LEU2, TRP1. Ebben az esetben olyan trzset kell
hasznlunk, amelyben az adott enzim defektes (mutns) s ezrt nem tud szaporodni olyan tpoldatban, ami
nem tartalmazza a szintzisben gtolt anyagot, pl. hisztidint, leucint, triptofnt vagy az uracilt (ezeket a
trzseket auxotrfnak hvjuk). Pldul HIS3 szelekcis marker gn hasznlata esetn a hisztidin
bioszintzisben gtolt trzset hisztidint tartalmaz tpoldatban tartjuk fenn. Transzformci utn azonban
hisztidin-mentes tpfolyadkban nvesztjk.. Ekkor csak azok a sejtek maradnak fenn (szaporodnak),
amelyek felvettk a vektort, s el tudjk lltani a hisztidin bioszintzishez szksges enzimet.
A msik lehetsg, ha a vektor antibiotikum rezisztencia gnt kdol. Azaz a baktrium trzsekhez hasonlan
a rezisztenciagn termke hatstalantja a mdiumban lv antibiotikumot (pl. G418, amely egy
aminoglikozid antibiotikum, s a neomicin-rezisztencia gnnel lehet inaktivlni, vagy zeocin, amely egy
glikopeptid s Zeocin rezisztencia gntermk inaktivlja). Ezek a szelekcis gensek minden eukarita
sejtben mkdnek, s a rezisztencia dzisfgg. gy az expresszis vektorbl tbb kpit tartalmaz trzsek
is szelektlhatak nvelve a mdium antibiotikum tartalmt.
13.1.3. Szekrci
Az leszt rendszer egyik legnagyobb elnye, hogy a fehrjk szekrcijt knny megoldani. Mivel az
leszt nem nagyon szekretl fehrjt, ezrt a rekombinns fehrje szinte az egyedli, ami megjelenik a
tptalajban. A szekrcis szignlt radsul le is hastja (szignl-peptidz), gy azt sem kell eltvoltanunk.
Ilyen szignl-szekvencia lehet a Saccharomyces cerevisiae -mating faktornak prepro-szignlja, vagy a
Pichia pastoris PHO1 szignlja. Szmos esetben a heterolg fehrje sajt szignl szekvencija a legjobb
megolds.
A szekrci nemcsak a tisztts szempontjbl kedvez, hanem a sejt intracellulris protezaitl is vdelmet
jelent. Intracellulris expresszi esetn protez-deficiens trzsek hasznlata jelenthet megoldst. (A kt
legfontosabb protez ebbl a szempontbl a proteinz-A s -B enzimek). A tpfolyadkban megjelen
protezok hatst pH optimalizlsval (minden enzim mkdsnek van pH-fggse), vagy a fermentcis
hmrsklet cskkentsvel lehet minimalizlni (alacsonyabb hmrskleten kevsb mkdnek az
enzimek, illetve kevesebb protezt szekretlnak.)
13.1.4. Poszttranszlcis mdostsok
Az eukarita leszt poszttranszlcis mdostsai kzelebb llnak az emlskhez. A termelt fehrjk
foldingja megfelel, a diszulfid-hidak kpzse is megtrtnik a megfelel helyen. A legnagyobb bajt a
glikozilci jelenti. Emlskben O-glikozilci trtnik, azaz Ser s Thr aminosavak hidroxil-csoportjn
keresztl, mg lesztben N-glikozilci aszparagin oldallncon keresztl. Radsul a cukor egysgek
mennyisge s fajtja is nagyon klnbzik. Emlskben a cukoregysg N-acetil-galaktzamin, galaktz s
szilsav, mg lesztben kizrlag mannz, s az leszt fehrjk hiperglikozilltak. gy az lesztben
gyrtott fehrjk emlskben nagyon ers antign tulajdonsggal rendelkeznek.
13.1.5. Az expresszi lpsei
Az eukarita expresszi lpsei alapveten megegyeznek a prokarita rendszer megfelel lpseivel (ld.
12.2.4. fejezet). Csak a klnbsgeket emeljk ki.
1. Az expresszis kazettban a promter s transzkripci termincis szekvencia kztt van az
177
expresszland fehrje kdol rgija. A termincis szekvencia ebben a rendszerben esszencilis.
2. Integrld vektor esetben a homolg rekombinci hatkonysgnak nvelsre a vektort
linearizljuk restrikcis hastssal. Fontos, hogy a hasts a vektor kromoszomlis szekvencijnl
legyen, hogy itt trtnjen meg a homolg rekombinci.
3. Az expresszis vektor bevitele az lesztsejtekbe. Az leszt cellulzt tartalmaz sejtfala miatt nehz
a transzformls, ezrt gyakran a szferoplasztot (a sejtfaltl megfosztott lesztsejtet)
transzformljk. Tbb transzformcis eljrs is ltezik, pl. a ltium-kloridos s polietiln-glikolos
transzformls. A leghatkonyabb gnbevitel azonban az elektroporls. A replikld vektoroknl a
fehrjnket kdol szekvencia extrakromoszomlis marad, mg integrld vektoroknl megtrtnik a
homolg rekombinci az leszt genomba.
4. A transzformlt trzsek kivlasztsa a szelekcis markerek segtsgvel, pl. hisztidin-mentes tptalaj.
5. Ellenrz PCR annak kimutatsra, hogy a genomban van-e a kvnt DNS. Ez a vektorban lv primer
szekvencik segtsgvel, vagy egy vektor-specifikus s egy inszert-specifikus primer pr segtsgvel
trtnik. A keletkezett PCR-termk jelenlte s mrete mondja meg, hogy a megfelel helyen van-e az
inszertnk.
6. Ha kszen van a rekombinns trzsnk, elkezdhetjk a sejtek nvesztst. Az leszt sejteket 28-
30C-on nvesztjk 220-250 rpm-es rzats mellett. A viszonylag nagy fordulatszmon val rzats a
megfelel levegztets miatt fontos.
7. Amennyiben a sejtek elrtk a megfelel sejtsrsget, induklhatjuk a tenyszetet. Pl. Pichia
sejteknl metanollal, kzben llandan mintkat vesznk (0, 6 12, 24, 36, 48 72, 96 rban), s SDS-
glelektroforzissel nyomon kvetjk a fehrjnk termeldst.
8. Ezt kveten kell a sejteket feltrnunk s a fehrjt izollnunk, tiszttanunk. A sejtek feltrsa,
amennyiben nem szekretlt fehrjrl van sz, a sejtfal jelenlte miatt nagyon nehz. A fel-
leolvasztgats s a savas-veggyngys ismtelt vortexels azonban sokat segthet. Alternatv
megoldsknt hasznlhatunk klnbz glikozilz enzimeket is (zimolz, lizozim stb.). Szekretlt
fehrjket a mdiumbl gyjtjk ssze.
13.1.6. leszt expresszis vektorok s rendszerek
Az leszt sejtekben a baktriumokhoz hasonlan elfordulnak plazmidok. Legismertebb a srleszt (S.
cerevisiae) 2-mikron plazmidja, amelyik egy 2 m tmrj cirkulris DNS, mely autonm mdon
replikldik. Replikonja az origbl s a REP (represszor) szablyoz gnbl ll. Amg a plazmid
kpiaszma magas, a kromoszomlis DNS-sel egytt replikldik. Amikor ez lecskken, beindul a plazmid
fggetlen replikcija, mg el nem ri a sejtenknti 30-50 kpit. Ezt a plazmidot YEp-nek (yeast episomal
plasmid) is nevezik. Ebbl szrmaznak a YEp sorozat vektorok, amelyek stabil plazmidok, egyenl
mennyisgben vlnak szt (szegregldnak) a lenysejtek kztt.
Egy msik lehetsg arra, hogy fggetlenl replikld leszt vektort kapjunk, hogy egy cirkulris DNS
tartalmazza azt a kromoszomlis szekvencit, ami a replikcirt felels. Ezt az elemet fggetlen
replikld szekvencinak hvjk (ARS: autonomously replicating sequnces). Nagy kpiaszmot
eredmnyez, de gyakran instabil, knnyen elveszthetik a sejtek a rekombinns plazmidot mitziskor. Az
ilyen tpus leszt vektorokat YRp-nek (yeast replicating plasmid) nevezzk. A YEp s YRp sorozat tagjai
a replikld plazmid-alap vektorok, mg a YIp plazmidok (yeast integrating plasmid) a genomba
integrldak. Ha az ARS-t tartalmaz plazmidba beptnk a kromoszma centromerjbl szrmaz CEN
szakaszokat, amelyek a kromoszmk mitotikus orshoz val kapcsoldsrt felelsek, ekkor stabilizlni
178
tudjuk vele a plazmidot, nem vsz el osztds sorn. gy kapjuk a YAC vektorokat, amelyek a replikcihoz
s az utdsejtbe jutshoz minden elemet tartalmaznak (ld. 7.5. fejezet).
Az ismertetett ngy leszt vektor tpust (integrld, replikld, episzomlis s leszt mestersges
kromszma) leszt expresszis vektorknt hasznlhatjuk (ld. 13.1. bra)
13.1. bra: Az leszt vektorok tpusai
A srleszt gazdasejtben hasznlhat expresszis vektorok pl. az Invitrogen cgtl beszerezhet pYES2
vektorok vagy a Novagen cg pYX vektorsorozata (sokszor a nv is utal a vektor fajtjra, pl. pYES2 egy
replikld yeast episomal plazmid). A Pichia rendszer plazmidjai ltalban integrld plazmidok, pl.
pHIL-D2. Ezen a linken szmos lesztben vagy ms gombban hasznlhat, klnbz elven mkd
vektorrl olvashatnak tovbbi rszleteket. Expresszis kitek is beszerezhetk, amelyek az leszt
rendszerben hasznlhatk. Ezek klnbz expresszis vektorokat, nmelyek leszt trzseket, a
szelekcihoz szksges anyagokat, szekvenl primereket s ms segdanyagokat tartalmaznak. Radsul
nagyon pontos lerst adnak arrl, hogyan kell lpsrl-lpsre vgrehajtani a rekombinns fehrjk
termeltetst. Rszletes ismertetjk itt tallhat.
13.1.7. Az leszt expresszis rendszer elnyei s htrnyai
Rviden sszefoglalva az leszt expresszis rendszer elnyei:
- olcs, knnyen kezelhet
- alkalmas fehrje szekrcira, s a mdiumbl knnyen kinyerhet a termelt fehrje
- nagy a kitermels; egy liter kultrbl 5-10 g fehrje is kinyerhet (a Pichia rendszerrel)
- ltalban j az emls fehrjk foldingja s a diszulfid-hidak kialakulsa is megfelel
A rendszer htrnyai:
- egyes poszttranszlcis mdosulsok, elssorban a glikozilci nem teljesen felel meg az emlsk
hasonl mdosulsainak; pldul hiperglikozilci lp fel, s ms oligoszacharid egysgek is
179
beplhetnek a rekombinns fehrjelncra (pl. mannz)
- bizonyos fehrjk heterolg expresszijra nem alkalmas
13.2. Bakulovrus expresszis rendszer
A bakulovrus expresszis rendszernl a gazdasejtek egy molylepke fajbl (Spodoptera frugiperda)
szrmaznak, a vektor pedig mdostott bakulovrus. A bakulovrusok rovarokat fertz ktszl cirkulris
DNS-vrusok, pl. Autographa californica s Bombyx mori nukleris polihedrzis (NPV). Genomjuk kb. 80-
100 kbp mret cirkulris DNS-bl ll, mely legalbb 154 fehrjegnt tartalmaz, amibl 20 virlis
struktrfehrjt kdol. A vrusrszecskt (virion) egy polihedrin nev fehrjbl ll mtrix burkolja be, ami
biztostja a vrus tllst a gazdasejten kvl. A polihedrin burokfehrje a vrus fertzs ksei szakaszban
termeldik extrm ers promterrl. Ezzel az ers promterrel (pPolh) indtjuk el a clgnnk
kifejezdst. A transzkripci inicicijhoz kulcsfontossg a TAAG-szekvencia (innen indul a
transzkripci), illetve a pPolh promter s a TAAG kztt lv 50 bp-nyi szakasz szekvencija is ersen
befolysolja az expresszis szintet. Errl a ksei promterrl a fertzs utn 20 rval kezd elindulni a
gnexpresszi, s a sejtek a fertzs utni 72-94 rig mg nem lizlnak. A vrhat legnagyobb expresszi
30-50 h kz tehet, ilyenkor a sejt legaktvabb promtere a polihedrin promter, s az ltala vezrelt
heterolg fehrjk mennyisge elrheti az sszfehrje tartalom 1-10%-t.
Az expresszi els lpse itt is az expresszis vektor, azaz a rekombinns vrus ellltsa. A clgnnket
beklnozzuk egy transzfer vektorba, amibl az expressszis kazettnk helyspecifikus transzpozicival
vagy homolg rekombincival tkerl a vrusgenomba. Majd a clgnnket tartalmaz vrusgenommal
megfertzzk a gazdasejtet, ahol a fertzs ksei szakaszban beindul a gnnk kifejezdse. Kt mdszert
fejlesztettek ki eddig a bakulovrus expresszis rendszer hatkony alkalmazsra.
13.2.1. Bac-to-Bac rendszer
A gnnket tartalmaz transzfer plazmiddal (pFastBac) mdostott E. coli trzset, n. DH10Bac trzset
transzformlunk. Ez a trzs tartalmazza a vrus genomjt (Bacmid), s egy tetraciklin rezisztencit hordoz
segdplazmidot, ami egy transzpozz enzimet kdol. Miutn a DH10Bac felvette a transzfer plazmidot, a
transzpozz segtsgvel megtrtnik a megfelel helyek kztt a helyspecifikus transzpozci, gy a
clgnnk a vrusgenomba kerl, elkszl a rekombinns vrus. A vrus szaportst E. coli-ban is
vgezhetjk, a vektor teht shuttle vektorknt szolgl. A rekombinns bacmidot hordoz baktrium
telepeket felszaports eltt szelektlni kell. Erre a clra antibiotikum s kk- fehr szelekcit alkalmazunk.
Transzformls utn a DH10Bac sejteket X-GAL-t, IPTG-t, kanamicint, tetraciklint s gentamicint
tartalmaz lemezen szlesztjk. (A transzpozci utn a transzfer vektor gentamicin rezisztencia gnje
tkerl a vrus genomba, ami eleve mr kanamicin rezisztencit hordozott.) A kk-fehr szelekci azon
alapszik, hogy a bacmid hordozza a LacZ azon rszt, ami hinyzik a baktrium genomjbl (o-
komplementci, ld. 7.2.3.1 fejezet), de a sikeres transzpozci hatsra ez a kdol rgi tnkremegy, gy
nem ll ssze a sejtben az aktv -galaktozidz enzim. A rekombinns bacmidot hordoz baktrium telepek
fehrek maradnak. Ezekbl a telepekbl bacmid-prepartumot ksztnk. (Vigyzni kell, mert a bacmid-
DNS a plazmidnl legalbb 1 nagysgrenddel nagyobb, knnyebben srl fizikai hatsokra.)
A rekombinns bacmiddal megfertzzk a gazdasejtet; a gazdasejt lehet SF9, SF21, HiFi5. Elszr
lipofekcival transzfektljuk a sejteket. A bacmidot felvett sejtekben idvel kialakulnak a fertzkpes
vrusok, amelyek kijutva a sejtbl (bimbzssal, vagy kizrssal) megfertzik az sszes sejtet. gy a sejtek
kzel 100%-a tartalmazza s szaportja a vrusokat. A felszaportott vrusok a transzformlst kvet 3-6
napban mr a mdiumban vannak, ezt hvjuk P1 vrus oldatnak. A P1-et miutn centrifuglssal s
sterilszrssel mentestettk a sejtektl, hosszabb ideig htben trolhatjuk. Ez az oldat mg kevs vrust
tartalmaz, s kicsi a trfogata, ezrt ebbl egy tbb vrust tartalmaz, n. P2 -t ksztnk. A P2 egy P1-nl
tbb vrust tartalmaz sejtmentes mdium, melyet nagyobb mennyisg sejt P1 vrus oldattal val
180
fertzsvel s inkublsval kapunk. A vrus mennyisgt tovbbi, megnvelt sejtmennyisg tenyszet
fertzsvel nvelhetjk, P3, P4, stb. A P3 oldat vrus tartalma mr megfelel a fehrje expresszihoz. Ezzel
fertzzk a sejteket, majd 36-72 ra kztt szreteljk (harvesting) a sejteket s izolljuk az expresszlt
fehrjnket. Itt is rdemes elszr kis trfogatban vgezni az expresszit, majd 36-72 ra kztt mintt
venni s megnzni termeldik-e fehrjnk (Western-blot). Az optimalizls sorn vltoztathatjuk a
hozzadott vrus oldat (P3) mennyisgt (0,1-10%), s a sejtek sszegyjtsig eltelt inkubcis idt.
A Bac-to-Bac expresszis rendszer smjt a 13.2. bra foglalja ssze. Az Invitrogen cg Bac-to-Bac kitjei
nagyon megknnytik a rekombinns vrusok ellltst, errl itt tallhat bvebb informci.
13.2. bra: A Bac-to-bac expresszis rendszer smja (a P2 vruspopulciig)
13.2.2. Kzvetlen bakulovrus (Direkt Bac) rendszer
Ennl a rendszernl a linearizlt deficiens vrus genomba a clgnnk a transzfer vektorbl homolg
rekombincival kerl be. Elszr elksztjk a rekombinns transzfer vektort, ami tartalmazza a gnnk
szekvencijt, majd a linearizlt vrus genommal egytt transzfektljuk a rovarsejteket. A sejten bell
ltrejn a homolg rekombinci, s csak azok a sejtek tudnak szaporodni, amelyeknl megtrtnt a
rekombinci, gy szelektlni sem kell. A reprodukcira kpes vrusok, mikor kiszabadulnak a sejtbl,
tovbb fertzik a sejteket, gy n a vrusok mennyisge, amit mg tovbb lehet szaportani, vagy
fehrjetermelshez lehet hasznlni. Bvebb informci itt olvashat.
A transzfer vektor szintn szaporthat prokarita sejtben, lehet benne tbb vrus is promter is, gy
egyszerre tbb polipeptidlncot is lehetsges expresszlni, pl. BaculoGold vektorok, vagy a PAA cg
BaculoOne vektorai. Az expresszihoz a pPolh promter mellett egy msik ksei promtert, a p10 promtert
is hasznljk, amely szintn ers promter. A bakulovrus expresszis kazettk is tartalmazzk a
181
transzkripcihoz s transzlcihoz szksges elemeket: transzkripcis termincis szekvencik, poli-A
szignl, Kozak szekvencia, N-terminlis fzis cmke.
13.2.3. A bakulovrus rendszer elnyei s htrnyai
Az E. coli sejtben rosszul kifejezd fehrjkre a kvetkez lehetsg vagy leszt sejtek vagy a
bakulovrus rendszer hasznlata. Az utbbival humn fehrjk is kifejezhetk aktv formban. A kitermels
nem lesz soha olyan j, mint amit el lehet rni E. coli rendszerben, de 1-50 mg fehrje kinyerhet 1 L
kultrbl. A fehrje foldingja feltehetleg j lesz (eukarita dajkafehrjk vannak jelen), a szekrcis,
kompartmentalizcis mechanizmusok mkdnek. A poszttranszlcis mdostsok (foszforilci,
proteolitikus mdosts, glikozilci, acetilezs, diszulfid-hidak) az emls rendszerekhez hasonlak. Mg
heterodimerizci is elrhet. Ennek mdja koinfekci, azaz fertzs egyszerre tbb vrussal, amelyek
klnbz clgnt tartalmaznak, vagy azt is megtehetjk, hogy a rekombinns vrusba tbb expresszis
kazettt ptnk be. A sejtek knnyen fenntarthatk, s gyorsan nnek szuszpenzis vagy letapad
kultrban is. Tenysztsk rzinkubtort ignyel (27-28C), s szksgnk lesz steril flkre s
mikroszkpora. Az utbbival kvetjk nyomon a sejtek llapott, mivel a fertztt sejtek megnnek s
lekerekednek. A tp viszont drga, mg az emlssejtekhez hasznlt bazlis (ld. ksbb) tphoz kpest is kb.
tszr drgbb. Msik htrny lehet, hogy a fertzkpes vrus oldat ellltsa munka s idignyes;
szerencss esetben is a ksz transzfer vektortl a P3 vrus oldatig trtn eljutsig kt ht szksges.
13.3. Emls expresszis rendszer
Emls expresszis rendszer esetn emls szvetekbl szrmaz sejtvonalakban fejeztetjk ki a kvnt
gnnket. Ennek a rendszernek is a gazdasejt s a vele kompatibilis expresszis vektor az alapja, ami
tartalmazza a kifejezend fehrjnket kdol szekvencit. A kvetkezkben sszefoglaljuk az emls
expresszis vektor lnyeges elemeit, az alkalmazott sejtvonalakat, a gnbevitel mdjt, s az expresszis
rendszer elnyeit s alkalmazhatsgt
13.3.1. Emls expresszis vektorok
Az emls expresszis vektorok is shuttle vektorok; a klnozshoz s szaportshoz E. coli rendszert
hasznlunk, gy a vektornak tartalmaznia kell a baktriumban val fenntartshoz s szaportshoz szksges
elemeket; E. coli replikon, antibiotikum rezisztencia gn (ld. 12.2. fejezet). Ezen kvl a transzkripcihoz
szksges promtert, a mRNS szintzis megfelel termincijhoz s a processzlsrt
(poszttranszkripcis mdostsok) felels elemeket, a transzlcihoz fontos szekvencikat. Ezeket a cisz-
regull szekvencia elemeket ismertetjk a kvetkezkben. A 13.3. bran egy ltalnos eukarita
expresszis vektort mutatunk be.
13.3.1.1. Emls promterek s enhanszerek
Az eukarita promterek fontos eleme a TATA-box, mely az els trand nukleotidhoz kpest (5'-irny)
30 s 25 bp-nl tallhat. Tovbbi, az 5'-irnyban elhelyezked elemek pl. a 50-tl 100-ig
elhelyezked GC-boxok, melyek szma s elhelyezkedse elgg eltr lehet gnrl-gnre, hinyuk, vagy
mutcijuk viszont bizonyos gnek esetn drasztikusan befolysolhatja a gn kifejezdst. Ezen elemek
vizsglatra fejlesztettk ki a riportergneket. A riportergnt a vizsgland promter/szablyoz elem utn
fuzionltatjk, majd valamilyen knnyen detektlhat mdszerrel nyomon kvetik a kifejezdst. A
kifejezds mrtke arnyos a promter/szablyoz elem mkdsvel. A riportergnek olyan fehrjt
kdolnak, amelynek aktivitsa mrhet (abszorbancia vagy fluoreszcencia alapon). A riportergnek fehrje
termkeit knnyebb nyomon kvetni, mint a gnrl keletkez mRNS-t, ami viszont kzvetlenebbl ad
informcit a promter aktivitsrl. Az elsk kztt alkalmazott riportergn a kloramfenikol-
acetiltranszferz (CAT) volt, amely kzmbsti (acetillssal) a sejtek szmra toxikus antibiotikumot
182
(azaz egy antibiotikum rezisztencia gn). Tovbbi riportergnek a -laktamz-t, -galaktozidz-t,
luciferzt, valamint a GFP-t s vltozait kdol gnek.
13.3. bra: Az eukarita expresszis vektorok ltalnos felptse
ltalnosan elmondhat, hogy az eukarita gnek promtere komplexebb, mint a prokaritk. Kevesebb
bennk a szablyszersg sokszor mg a TATA-szekvencik is hinyoznak , vltozatosabbak, s
rengeteg cisz- s transz-elem befolysolja a mkdsket. Az RNS-polimerz II sem kzvetlenl
kapcsoldik a promterhez, hanem a bazlis transzkripcis faktorokon keresztl. Vannak ktelezbb
szekvenciaelemek, vannak amelyek gnrl-gnre vltoznak, st olyanok is, amelyek tbb mint 1000 bp-ra is
lehetnek a struktrgntl, s mgis jelentsen befolysoljk a gntrst. Ezeket az elemeket hvjuk
enhanszereknek (az enhancer sz jelenetse megnvel, megemel). Az enhanszerek lehetnek 5' vagy 3'
(upstream vagy downstream) irnyban is a gn promtertl, st a gn egy intronjn bell is. A tvolsguk
is vltozhat, a promtertl akr tbb ezer bp-ra, de akr ms kromoszmn is lehetnek. Mkdsk lnyege,
hogy aktivitsuk kifejtsekor trben kzel kerlnek ahhoz a promterhez, amelynek a mkdst
befolysoljk. Az emls expresszis vektorok ezrt a megfelel mrtk expresszi rdekben az
enhanszerek jelentsge miatt nemcsak a megfelel promtert, hanem annak enhanszert is tartalmazzk.
De milyen legyen a clgnnk promtere? A vlasz abban rejlik, hogy mit szeretnnk vizsglni.
Amennyiben a gn kifejezdst, mkdst szeretnnk vizsglni, mindenkppen a sajt promtert
rdemes hasznlni, radsul a sajt krnyezetben. Ha viszont az a clunk, hogy nagyobb mennyisgben
lltsuk el a gntermket, a fehrjt, akkor nagy expresszit biztost, ers promtert hasznljunk. Erre
legalkalmasabbak a vrus promterek, illetve olyan endogn promterek, amelyek llandan aktvak s nagy
mennyisg fehrje expresszit tesznek lehetv. Nzzk meg az emls expresszis rendszerekben
leggyakrabban hasznlt promtereket:
- SV40 promter: SV40 (Simian vacuolating virus 40) egy majmokat s az embert is megfertz DNS
vrus. Ezt a polima csaldba tartoz vrust Rhesus majom vese sejttenyszet vizsglata kzben fedeztk
fel 1960 krl, s kiderlt rla, hogy szmos klnfle tumor kpzdst kpes elindtani. A vrus a
gazdasejt MHCI receptorn keresztl a VP1 glikoproteinjnek segtsgvel jut be a sejtbe. A sejtmagban a
sejt II-es tpus RNSpolimerz enzime ktdik az 5 kb nagysg vrusgenom SV40 promterhez, s
183
elkezdi trni a vrus korai gnjeit. Ezek a gnek kt fehrjt kdolnak: kis antignt, s a nagy T-antignt.
A nagy T-antignnek tbb szerepe is van: kikerl antignknt a sejt plazmamembrnjba; szablyozza a
virlis gnek mRNS szintzist; s ktdik a vrusgenom replikcis origjhoz, inicilva ezzel annak
replikcijt. Az SV40 promter TATA-szekvencija, s a tle 5' irnyban lv GC-boxok s az enhanszer
szablyozza a vrus korai, majd a ksei gnjeinek az expresszijt. (A ksei gnek a korai gnek
komplementer szlain tallhatk ellenttes leolvassban; ugyanannak a promternek a szablyozsa alatt,
s a GC-boxokhoz ktd fehrjk dntik el a szintzis idejt s irnyt.)
- CMV promter (cytomegalovirus immediate-early promter): a citomegalovrusok a herpesz vrusok
csaldjba tartoznak. Promterk nagyon ers, nagymrtk expresszit biztost, ezrt is hasznljuk az
expresszis vektorainkban. lland kifejezdst biztost, de a tapasztalatok szerint mkdse elgg
szvet- s sejtfgg.
- CAG promter: Egy hibrid promter, amelyben a csirke -aktin promtert a CMV korai enhanszervel
fuzionltattk. Ez a promter a CMV promtertl eltren nem sejtspecifikus, gy brmelyik sejtvonalban
hasznlhat. Emellett a sejt magas aktin szintje s CMV enhanszer aktivl hatsa miatt erteljes
expresszit eredmnyez.
- UbC promter (human Ubiquitin C): Egy szintn magas szinten expresszld, minden sejttpusban
kifejezd promter. Akkor hasznljk, ha a CMV promter nem mkdik.
- PGK (egr 3-foszfoglicert kinz 1 promter): minden sejtben mkdik a glikolitikus t, ezrt ez a
promter minden sejttpusban kifejezdik, csak a kifejezds mrtkben van klnbsg. Azokban a
sejtekben, amelyekben nagyobb a glikolzis sebessge, aktvabb a promter is, ezrt nagy expresszit
eredmnyez. Transzgenikus egerekben s transzdukcis vektorokban hasznljk (ld. ksbb).
- EF1A (humn elongcis faktor 1 promter): Szintn akkor hasznljk ezt a promtert, amikor a CMV
promter nem mkdik (embrionlis ssejtek) vagy cskkent az aktivitsa.
Az eddig felsorolt promterek mind konstitutv, ers expresszit biztostanak, de lteznek ezen kvl
szablyozhat s induklhat promterek is.
13.3.1.2. Transzkripci terminci s poliadenilcis szignl
A prokarita expresszis vektorokban tallhat transzkripci termincis szekvencia nem felttlenl
szksges az expresszihoz, viszont az eukarita rendszerekben a mRNS megfelel processzlshoz ez a
szekvencia esszencilis. Az eukarita mRNS vgt a gn STOP kodonja utn kvetkez 3' UTR
szekvenciban (3' untranslated region) tallhat elemek jellik ki. A legfontosabb elem a poliadenilcis
szignl, ami az trdott RNS-en AAUAAA szekvencinak felel meg (ld. 13.4. bra)
13.4. bra: A poli-A farok s kialakulsa
184
Ez a konszenzus szekvencia jelzs egy RN-z komplex szmra, hogy a szekvencia utn 10-30 bzissal
hastson bele az RNS-be, majd a kpzdtt pre-mRNS gy kialakult 3-vgre a poli-A-polimerz (PAP)
szintetizl egy kb. 200 bzisnyi poli-A farkat. A poli-A szekvencit nem a vektorunk, s nem az inszertnk
kdolja, hanem a sejt enzimei helyezik fel a megfelel poliadenilcis szignl felismerse utn. A poli-A
szignl, de klnsen a poli-A hely krli szekvencik is vltozatosak az eukaritkban. Az alkalmazott
eukarita vektorokban a leggyakoribb az SV40 ksei poliadenilcis szignlt (SVLPA) s a Herpes
simplex virus timidin kinz (HSV-TK) poli-A szignlt hasznljuk, amelyek be vannak ptve a
vektorunkba. A poli-A farok s a hozzktd fehrjk stabilizljk a mRNS-t, ezek nlkl hamar
degradldna. Szerepe van az RNS stabilizlsn tl az rett mRNS citoplazmba val kijutsban s a
transzlciban is. A poli-A farok idvel egyre rvidl a sejtben, gy egyre cskken a mRNS stabilitsa s a
transzlci mrtke.
13.3.1.3. Splicing szignl
Az eukarita gnek az 5' s 3' UTR szekvencik mellett intronokat is tartalmaznak. Az intronok kivgsa s
a pre-mRNS rse a sejtmagban trtnik. Csak az rett mRNS jut ki a citoplazmba, ahol elkezddhet a
transzlci, a fehrje szintzise. Minden szablyoz elem, ami segti a mRNS rst hozzjrul a fehrjnk
expresszijnak a nvekedshez. Fehrjetermels cljbl nem a teljes gnt, hanem az intron-mentes cDNS
szekvencit szoktuk klnozni az expresszis vektorba, ami gy nem tartalmaz splice-helyeket. A splice-
helyek azonban szerepet jtszanak a mRNS rsben, meggyorstjk a mRNS kpzdsnek sebessgt.
Ezrt szmos expresszis vektor tartalmaz intron szekvencikat 5' s 3' splice-helyekkel, ami megnveli a
fehrje expresszi mrtkt
13.3.1.4. Transzlci inicicis (Kozak-) szekvencia
Az eukarita gn transzlcijnl is nagyon fontos a mRNS szekvencija az inicicis kodon krnyezetben.
Ezek a szekvencik segtik, hogy jl beilleszkedjen az inicicis Met kodon a riboszma kthelyre.
Marilyn Kozak vizsglta az eukarita gnek transzlcijnak inicicijrt felels szekvencikat, s azt
tallta, hogy vannak bizonyos helyek, ahol fontos, hogy milyen nukleotid tallhat. Vizsglatainak
eredmnyeknt megllaptott egy konszenzus szekvencit, amely nagy valsznsggel kedvez az
inicicis kodon (AUG) riboszmhoz val ktdshez. Ezt a szekvencit hvjuk Kozak-szekvencinak.
Ezek alapjn az inicicis AUG mellett nagyon fontos, hogy a +4 helyen G, 3 helyen purin bzis (A vagy
G) legyen: (gcc)gccRccAUGG. A 12.13. brn lthat az a szekvencia log, ami feltnteti, hogy az
inicicis kodon krnykn az eukarita gnek milyen nukleotidokat tartalmaznak. Lthat az brn, hogy
az inicicis kodon a DNS templtban szinte mindig ATG (egyes esetben CTG is lehet helyette), +4 helyen
leginkbb G tallhat, mg a 3 helyen A vagy G nukleotid. rdemes teht a nagyobb expresszi rdekben
betervezni a felteheten ers konszenzus Kozak-szekvencit. Amennyiben az inicicis szekvencik
krnyke nem elg j, akkor a riboszma onnan fogja indtani a transzlcit, ahol ersebb Kozak-
szekvencit tall. Ha N-terminlis fzis fehrjt fejeztetnk ki, akkor a vektor mr tartalmaz a fzis-tag
kdol szekvencija eltt egy ers Kozak-szekvencit (ld. 13.5. bra), amiben megbzhatunk. Ha nincs a
vektorban, akkor a gyrt ezt kzli velnk, s neknk kell betervezni.
185
13.5. bra: A Kozak-szekvencia logja (a konszenzus szekvencia egyes pozcikban megtallhat nukleotidok
gyakorisga)
Az eukarita gnek monocisztronosak, de elfordul, hogy egyszerre kt polipeptidlncot szeretnnk
kifejeztetni egy promter irnytsa alatt. Ilyenkor policisztronos vektort kell hasznlni, amiben a msodik
fehrjt kdol szekvencia eltt bels riboszma kthelynek kell llnia. Ezt a szekvencit hvjuk IRES-
nek, azaz angolul internal ribosome entry site-nak. Ebben az esetben a transzlci az 5'-sapka felismerse
nlkl indul a mRNS kzeprl.
13.3.1.5. Szelekcis markerek
Az emls sejtek szelektlsnak legelterjedtebb mdja az antibiotikum szelekci. A szelekcis marker gn
(miknt a prokarita sejteknl is) az antibiotikum talaktst s ezzel kzmbstst vgz enzim, amely
az expresszis vektorrl egy ers emls promter irnytsa alatt termeldik. A leggyakrabban hasznlt
antibiotikum a geneticin vagy G418, higromicin, zeocin s blaszticidin. A G418, egy aminoglikozid-tpus
antibiotikum, amely gtolja mind prokarita, mind eukarita sejtekben a fehrjeszintzist. Ebbe az
antibiotikum csaldba tartozik mg a gentamicin, neomicin s a kanamicin is. Ezek semlegestst a
neomicin gn ltal kdolt aminoglikozid-3'-foszfotranszferz (APH) vgzi, amely foszftcsoportokat visz fel
az antibiotikumokra, gy azok nem tudnak tbb ktdni a riboszmhoz. A higromicin-B is egy
aminoglikozid tpus antibiotikum, amely szintn fehrjeszintzist gtol s hasznlhat prokarita, eukarita
sejtekben egyarnt. Kzmbstshez higromicin-foszfotranszferz gnre (hpt) van szksg. A
hatsmechanizmus azonban ugyanaz, az antibiotikum foszforilldik, gy nem tud tbb ktdni a
riboszmhoz. Az antibiotikum szelekci sorn meg kell keresnnk azt a koncentrcit, amely elpuszttja a
nem transzfektldott sejteket, mg a transzfektlt sejtek tllnek s szaporodnak benne. Antibiotikum
szelekci felhasznlsval kivlogathatjuk azokat a sejteket, amelyek felvettk az expresszis vektort s gy
rezisztencit szereztek.
13.3.1.6. Az emls expresszis vektorok tpusai
Az emls expresszis vektorok legtbb eleme klnbz emls sejteket fertz vrus genombl szrmazik,
st egyes tpusoknl magt a rekombinns vrust hasznljuk gnhordoznak. Ez alapjn csoportostva
nzzk t a legelterjedtebb emls vektorokat.
Plazmidok: ltalban vrus genetikai elemeket hasznlnak bakterilis elemekkel egytt, valamint ers
promtereket tartalmaznak, amelyek a legtbb sejttpusban mkdnek. ltalban nem integrldnak a
gazdasejt genomjba, lehet viszont replikcit biztost origjuk (SV40, vagy EBV orig).
- pCDNA: CMV promter
- pEGFP-N1: CMV promter, eGFP fluoreszcens fzis cmke kerl a fehrjnk C-terminlisra.
- pEGFP-C1: CMV promter, eGFP kerl a fehrje N-terminlisra (ld. 13.6. bra).
186
A kvnt gnnket CMV promterrel fejeztetjk ki, SV40 PA termintor szekvencival. Mivel ez egy shuttle
vektor, prokaritban a replikcijt a pBR322 replikon teszi lehetv; a szelekcit pedig a prokarita
AmpR-promter vezrelte NeoR rezisztencia gn termke biztostja (kanamicin antibiotikumot hasznlva).
A rezisztencia gn emls sejtekben val kifejezdst az SV40 promter s a TK_PA szignl biztostja
(ilyenkor G418 antibiotikumot hasznlunk). Szmos (kb.16) klnbz restrikcis hellyel lehet a cDNS-
nket bevinni az eGFP-fzis cmke mg. Az inszertnket EGFP_C_primerrel tudjuk forward irnybl
szekvenlni, de ms szekvenls lehetsget is knl a vektor.
13.6. bra: pEGFP-C1 expresszis vektor trkpe. A vektor trkpet az Addgene Vector Database kszletbl
tltttk le. Ez egy szabad vektor megoszt kzpont, amely lehetsget teremt a kereskedelmi forgalomban nem lv
vektorok csere-berjre minimlis kezelsi kltsggel, valamint a sajt vektorunk trkpt is el tudjuk kszteni.
Lteznek olyan vektorok is, amelyek a GFP klnbz varinsait kdoljk fzis cmkeknt, pl. YFP, CFP;
vagy ms fluoreszcens fehrjt (mCherry, DsRed). Ezek a fzis cmkk ms-ms hullmhossz fnnyel
gerjeszthetk, s mshol van az emisszijuk. Segtsgkkel a fehrjnk expresszijt, az eukarita sejten
belli lokalizcijt (kololakizcijt) knnyen nyomon tudjuk kvetni. Egy ilyen ksrlet eredmnyt
mutatja be a 13.7. bra.
187
13.7. bra: Fehrje expresszi nyomonkvetse fluoreszcens fzis cmkvel. HEK293T sejteket transzfektltunk
egyszerre kt klnbz fluoreszcens cmkt hordoz plazmiddal (kotranszfekci), majd transzfekci utn 36 rval
floureszcens mikroszkppal kvettk a plazmidokban kdolt fehrjnk expresszijt. Az els kpen lthat, hogy a
sejtek kifejezik CFP-cmkt hordoz fehrjt (gerjeszts: 456 nm, emisszi: 486 nm), a msodik kpen pedig a YFP-
fehrjt kifejez sejtek vilgtanak piros sznnel (gerjeszts:510 nm, emisszi:535 nm). A harmadik brn egymsra
vettettk a kt kpet, gy lthat, hogy a narancssrga sejtek felvettk mindkt plazmidot. Ez a mdszer alkalmas in
vivo fehrje kolokalizci vagy klcsnhats kimutatsra.
Rekombinns vrusok: nagy hatkonysg, replikci-inkompetens virlis rszecskk. Ezek a rendszerek
hasznlhatk fehrjk expresszijra, vagy gncsendestsi ksrletekre is. A gnterpiban is a rekombinns
vrus rendszereket hasznljk.
- SV40: 5 kbp nagysg genom, kb. 5 kbp nagysg inszertet tud befogadni, transzdukl vektor, de
specilis gazdasejt kell hozz, pl. CV-1 vagy COS sejtek.
- Papillomavrus: 8 kbp nagysg cirkulris ktszl DNS vrus. Stabil extrakromoszomlis a
replikcija, 20-50 kpia/sejt.
- Retrovrusok: RNS-vrusok, pl. Rouse szarkma (RSV), egr leukmia (MLV), egr emltumor
(MMTV) vrusok. Integrldnak a gazdasejt genomjba, stabil transzfekcira, ezltal permanens
expresszi kpesek.
- Adenovrusok: 36 kbp nagysg genom, extrakromoszomlis a replikcijuk, tranziens expesszihoz,
gnterpihoz hasznljk.
- Lentivrus: RNS-vrus, stabil integrci a genomba, permanens expresszira alkalmas.
13.3.1.7. Stabil vagy tranziens transzfekci
Az expresszis vektorok msik csoportostsa azon alapul, hogy kpes-e a vektor, vagy valamely rsze
integrldni a gazdasejt genomjba, s ezzel stabil klnokat ltrehozni. Ezeket a vektorokat hvjuk (ld.
lesztnl) integrld vektoroknak. Az integrld vektorbl ltalban homolg rekombincival
trtnik meg az expresszland fehrjnk szekvencijnak beplse a gazdasejt genomjba. Ennek a
folyamatnak a hatsfoka nagyon kicsi, ezrt mindenkppen szelektlni kell szelekcis markerek
segtsgvel. A szelekcit hosszabb ideig fenn kell tartani, gy kzel 100% lesz a transzformldott sejtek
mennyisge. A stabilan transzfektlt sejtek mr egy nll sejtvonalat alkotnak s fenntarthatk,
lefagyaszthatk. Elnyk a homogenits, a stabilits (nem vsz el a transzgn), illetve a nem tl magas
expresszis szint. A nem tl magas expresszis szint sokszor elnyt jelent, mert kevsb szl bele a sejt
norml mkdsbe, s nem pusztul el a sejt. Tranziens transzfekcinl sok fehrje termeldik, ez
jelentsen befolysolja a sejt mkdst, ami stresszt jelent a sejtnek s ez sokszor problmt okoz. A
tranziens transzfekci elnye viszont, hogy nagyon gyors, a transzfekci utn 12-72 ra elteltvel mr lehet
vizsglni a sejtet, vagy izollni a kifejezdtt fehrjt.
A transzfekci hatsfokt s a fehrje kifejezdst fzis fehrjkkel lehet nyomon kvetni. Ilyenkor N-
vagy C-terminlisan egy enzimaktivitssal (luciferz, -laktamz, -galaktozidz ) rendelkez fehrjvel
vagy fluoreszcens fzis fehrjvel egytt fejeztetjk ki a fehrjnket, ezltal detektlhatjuk az expresszi
mrtkt, hatsfokt (a sejtek hny szzalka transzfektldott), valamint a kifejezd fehrje lokalizcijt.
188
A tranziens transzfekci elnye a gyorsasg s a magas expresszis szint, gy kivlan alkalmas fehrje
termelsre, illetve nagyszm klnbz fehrje vizsglatra. 3-4 nap mlva viszont a sejt vagy elpusztul a
nagy expresszis szinttl, vagy annyira kihgul benne az expresszis vektorunk, hogy jelentsen
lecskken a transzformlt sejtek mennyisge. Ennek oka, hogy a vektorunk nem replikldik, gy mitziskor
kihgul, vagy degradldik. Ennek kikszblsre hasznlhatunk replikatv episzomlis vektorokat, mint
pl. a pSV-vektorok. Ezek a vektorok virlis replikcis origt hordoznak, s ha a sejtben kifejezdik a
replikcit szablyoz fehrje is, akkor a vektorunk extrakromoszomlisan fog replikldni. Ennek
kvetkeztben kevsb hgul ki, radsul antibiotikum szelekcit alkalmazva mg fel is lehet dstani a
transzfektldott sejteket. Ez egy kztes megolds az tmeneti s a stabil transzfekci kztt, azaz a
sejtvonal szelektlhat s fenntarthat hosszabb ideig, de nem stabil. Az antibiotikum rezisztencit, amit a
szelekcinl kihasznlunk, bejuttathatjuk ugyanazon a vektoron, ami a kvnt fehrje cDNS-t hordozza, de
egy msik expresszis vektoron is. Ilyenkor egytt transzfektlunk a kt plazmiddal, azaz ko-
transzfektlunk, s azzal a feltevssel lnk, hogy ha egy sejt felvette a szelekcis markergnt tartalmaz
plazmidot, akkor nagy valsznsggel felvette a msikat is.
13.3.2. Sejtvonalak
A fehrje expresszira hasznlt sejtvonalakat primer sejttenyszetekbl nyerik, tbbszrs passzls utn. A
kiindulsi szvet lehet nem transzformlt felntt szvet, azonban az ezekbl szrmaz sejtek csak ~30
osztdst brnak ki. Lehet norml embrionlis szvet, amelybl szrmaz sejtek ~50 alkalommal kpesek
osztdni. Ezeket a sejttenyszeteket teht nem lehet korltlan ideig fenntartani. Expresszis kultraknt
hasznlnak mg daganatos sejtekbl kivont immortalizlt, vagy mestersgesen immortalizlt sejtvonalakat
is. A mestersgesen immortalizlt sejtvonalakat vrus ltali fertzssel lehet ellltani, ilyen pldul a
COS1 s a COS7 sejtvonal. Ezeket transzformlt sejtvonalaknak hvjuk, s elnyk, hogy korltlan ideig
kpesek osztdni. A nem transzformlt sejtvonalak is idvel spontn transzformldnak, gy korltlan ideig
fenntarthatv vlnak. Ennek oka, hogy nincs immunrendszer, ami kordban tartan ket, s gyorsan
mutldnak, szelektldnak az in vitro krlmnyek hatsra.
A leggyakrabban hasznlt sejtvonalak:
- CHO: (Chinese hamster ovary) knai cskos hrcsg petefszek sejtek; monolayer kultrban
(letapadva) tarthatk, gyorsan nnek s hatkonyan termelik a rekombinns fehrjt; az emls sejtek
klija. Az ipari termelsre leggyakrabban hasznlt emls expresszis rendszer.
- COS: afrikai zld majom vesbl szrmaz fibroblaszt-szer sejtvonal, amelyet CV-1 sejtek SV40
vrussal val fertzsvel nyertk. (A CV-1 sejtek afrikai zld majom vese fibroblaszt sejtek.)
Gyakran hasznljk rekombinns fehrjk ellltsra. Amennyiben SV40 vektorral fejeztetjk ki a
fehrjnket, a vektor replikcijt a nagy T-antign szablyozza, gy nllan replikldik.
- NIH-3T3: egr embrionlis fibroblasztbl szrmaz, letapad (monolayer kultra) immortalizlt
sejtvonal.
- HeLa: a legrgebben fenntartott humn sejtvonal, mhnyakrk sejtekbl szrmazik (Henrietta Lack
amerikai n tumorjbl 1951-ben vettk ki az eredeti sejteket). Rendkvl gyorsan osztd letapad
sejtvonal, a rkkutats leggyakrabban hasznlt sejtvonala.
- L6: patkny vzizombl izollt sejtvonal
- HEK293: embrionlis vesesejtekbl szrmaz immortalizlt sejtvonal. Norml embrionlis
vesesejteket fertztek adenovrussal, amelynek genomja integrldott a sejt genomjba. Nagyon
knnyen fenntarthat, s transzfektlhat. Elszeretettel hasznljk sejtbiolgiai kutatsokban s
biotechnolgiban terpis fehrjk s vrusok ellltsra. A HEK293T sejtekben kifejezdik az
SV40 nagy T antign, gy SV40 replikcis origj expresszis vektort hasznlva sokig fenntarthat
a vektor replikcija s gy a fehrje expresszi is.
A megfelel krlmnyek kztt tartott sejtek viszonylag gyorsan osztdnak, gy knnyen vltozhat a geno-
s gy a fenotpusuk. gyelnnk kell arra, hogy ne vltozzon a genotpus a ksrleteink sorn (ugyanazzal a
sejttel kezdjk s fejezzk be a ksrleteinket), ezrt mindig fagyasszuk le a kultrt, mikor elszr kzhez
189
kapjuk a sejteket. gy brmikor visszanylhatunk az eredeti, ismert genotpus kiindulsi sejthez. Ehhez be
kell tartani a fagyaszts s a felolvaszts szablyait, s meg kell tallni a sejteknek a legmegfelelbb
fagyasztsi mdiumot. ltalban jellemz, hogy a fagyasztst magas szrum (20-40%), s kb. 10% DMSO
mellett vgezzk. A fagyaszts lassan trtnik, mg a felolvaszts gyorsan s utna gyorsan meg kell
szabadulni a DMSO-tl, mivel knnyen tjut a plazmamembrnon, s toxikus hats a sejtekre.
13.3.3. Gnbevitel emls sejtbe
Az expresszis vektor bevitele a sejtekbe biokmiai, fizikai mdszerekkel s vrusfertzssel trtnhet.
Ezekkel a mdszerekrl a 3. fejezetben foglalkoztunk rszletesen. Az emls sejtekhez hasznlt gnbeviteli
lehetsgek sszefoglalva:
- DEAE-dextrn-medilta transzfekci
- transzfekci Ca
2+
-foszftos/DNA csapadkkal
- kationos-lipofekci
- elektroporls
- transzdukci
- mikroinjektls
Nagyon fontos a beviend gn tisztasga. Minl tisztbb s tmnyebb a rekombinns DNS, annl nagyobb
a transzfekci hatkonysga. ltalban a szilika oszlopos tisztts elegend (kaphatk nagytisztasg,
mikoplazmamentes DNS-t gr kitek is), de mg jobb hatsfok rhet el alkoholos-lecsaps utn, illetve
CsCl-os gradiens centrifuglssal.
13.3.4. Induklhat emls expresszis rendszerek
Minden expresszis rendszernl nagy elnyt jelent, ha a kvnt gn (target vagy clgn) expresszijt
szablyozni, induklni lehet. Ez klnsen akkor j, ha a termelend fehrje toxikus, vagy ersen
befolysolja a sejt mkdst. Az emls expresszis vektorok indukcijt klnsen a transzgenikus llatok
esetben hasznljk ki. Ennek egyik mdja, ha a gnnk promterbe olyan elemeket ptnk, amelyek a
megfelel faktorok megktse utn a gn transzaktivcijt idzik el. Ezek az elemek lehetnek a
gazdasejtben mr eleve megtallhatak, vagy mestersgesen bevittek is. (bakterilis, ms eukaritbl
szrmaz elemek). Az albbiakban nhny pldt sorolunk fel:
- Glkokortikoid hormon hatsra aktivld elem, GRE (glucocorticoid response element): A hormon
vlasz elemek vagy angolul Hormon Response Element (HRE) nagyon elterjedtek a humn genomban, tbb
szz tallhat bellk s nagyon fontos folyamatokat szablyoznak. Mkdsk a kvetkez: a megfelel
hormont megkti a sejtben tallhat receptora, ezutn a receptor-hormon komplex dimerizl s
transzlokldik a sejtmagba. Itt hozzktdik a DNS-en tallhat megfelel HRE konszenzus DNS-
szekvencijhoz, majd klcsnhatsba lp a promterhez ktd ms transzkripcis faktorokkal s elindtja
a target gn transzkripcijt. Ilyen HRE a GRE is, amelyet klnbz szteroid-hormon receptorok kpesek
felismerni, majd hozzktdve transzaktivcit elindtani. Induklhat expresszis vektorokban adenovrus
late promterben GRE szekvencikat helyeznek el a megfelel mdon, amely a hormon, vagy
szrmazkainak a hatsra a promter utn kapcsolt gn expresszijt akr 1000-szeresre is nvelheti.
rthet, hogy azok a sejtek mutatnak nagyobb gnexpresszit, amelyek tbb hormon receptort tartalmaznak.
Ezrt a gazdasejt egy glkokortikoid receptor tltermel sejt (pl. CHO), amelyet dexametazonnal induklnak
a megfelel gnexpresszi rdekben.
- Ekdizon-indukci: Az ekdizon egy zeltlb hormon, amely nagy szerepet jtszik az llat
egyedfejldsben, s ekdizon vlasz elemeken (response factor) keresztl kpes szablyozni bizonyos
gnek kifejezdst. Emlssejtek indukcija esetn be kell vinni ezeket az elemeket s kln a receptort is
190
be kell pteni a promterbe. gy az indukci kt vektorral oldhat meg:
1. vektor: HSP promter + ekdizon response elem + inszert
2. vektor: CMV s RSV promter + ekdizon receptor kdol rgi
- Bakterilis elemmel is lehet emlssejtekben induklt gnexpresszit elrni, mghozz a jl ismert lac-
opertor segtsgvel. Az indukci IPTG-vel trtnik, de meg kell oldani az opertor s a lac-represszor
fehrje szekvencijnak a bevitelt a sejtekbe, ami ltalban szintn kt vektor hasznlatval oldhat meg:
1. vektor: RSV-LTR promter + lac opertor (3x) + inszert
2. vektor: CMV promter + lacI
- Tetraciklin indukci: A tetraciklin nagyon hatsos antibiotikum Gram-pozitv, Gram-negatv
baktriumok s protozok ellen is. Legalbb 1000 szrmazkt lltottk el s ismert a hatsmechanizmusa
is. Knnyen bejut a prokarita sejtekbe, ott hozzktdik a riboszmhoz s tnkreteszi a kodon-antikodon
klcsnhatst. A rezisztens baktrium egy multimer antiporter fehrjvel (Tet) kipumplja az antibiotikumot
a citoplazmbl. Szmos Tet fehrje ltezik, tbbek kztt a Tn10 transzpozon ltal kdolt TetA. A TetA
nagy mennyisge esetn, mivel a fehrje mkdse kzben kationokat pumpl ki a sejtbl, a membrn
depolarizldik, ami a sejt pusztulshoz vezethet. Ezrt a sejt ersen szablyozza a TetA expresszijt egy
TetR represszor fehrjvel. Tetraciklin hinyban a TetR ersen ktdik a tetA s tetR gnek opertor
szekvenciihoz, meggtolva a fehrjk expresszijt. Tetraciklin hatsra azonban a TetR levlik az
opertorhelyrl s beindul az expresszi. Ez utbbi indukcis rendszert rszletesen is ismertetjk (ld.
13.3.4.1.)
13.3.4.1. A Tet-represszoron alapul indukcis rendszerek
A Tet operon mkdst kihasznlva fejlesztettek ki tbb frappns s szles krben hasznlt induklhat
emls expresszis rendszert. A szablyozott rendszer elnye, hogy az elemei bakterilisak, teht nem
interferlnak a gazdasejttel. Ezekben a rendszerekben a clgn transzkripcijt a TetR szablyozsa al
helyezik gy, hogy nhny kpiban tetO (opertor) szekvencik tallhatk a promter s a transzkripci
kezdhelye kztt. gy tetraciklin (vagy szrmazkai) nlkl nincs expresszi. Megfelel szvetspecifikus
promter s a tetO elem kombincijval szvetspecifikus s induklhat gnexpresszi rhet el. Ez az n.
Tet-represszor rendszer jl mkdik transzgenikus nvnyekben, de kevsb sikeres emlssejtekben.
Ennek oka, hogy emlssejtekben nem elg nagy a represszor koncentrcija, ami gtolni tudnl az ers
promtert.
Kreatv kutatk elksztettk az elbbi rendszer a fordtottjt, ahol a TetR nem represszor, hanem aktivtor
lesz. Elszr fuzionltattk egy transzaktivtor fehrjvel, a HSV-1 (Herpes Simplex Virus-1) VP16-tal, gy
mikor a represszor kt a promterhez, akkor a transzaktivtor fehrje gntrst indt el. Amennyiben
megjelenik a sejtben az effektor (tetraciklin), akkor a VP16-TetR transzaktivtor (tTA) kimra levlik a
promterrl s jelentsen lecskken a gntrs. Ez a rendszer akkor mkdik jl, ha stabil transzfekci
sorn a transzaktivtor s a target gn tbb kpiban van jelen a genomban. A tTa rendszerben teht akkor
indul el a gntrs, ha nincs a sejtben tetraciklin, ezrt ezt Tet-Off rendszernek is hvjk. Az induklatlan
llapot fenntartshoz alacsony-kzepes koncentrciban kell az effektort (tetraciklin, doxiciklin) adni a
sejtekhez.
Ksbb a rendszert megfordtottk, s ebbl alakult ki a Tet-reverz rendszer mutns TetR fehrjvel, ahol a
represszor csak az effektor jelenltben indtja el az expresszit, annak hinyban nem. Ez a Tet-On
rendszer sokkal rzkenyebb doxiciklinre s anhidro-tetraciklinre, mint tetraciklinre. A rendszer jl mkdik
ebben a formban is, de mg tovbbfejlesztettk az expresszis szint nvelse s az llandan termeld tTa
toxikus hatsa miatt. A vad-tpus tTa kimra represszor fehrjt is a tetO elem szablyozsa al tettk, gy
az effektor nemcsak a target gn, hanem a tTA gn expresszijt is szablyozza: antibiotikum jelenltben
alacsony a szabad tTa szintje, gy nem tud ktdni az opertorhelyre, nincs gntrs. Mikor nincs jelen az
antibiotikum, akkor viszont hozzktdik s elindtja nmaga s a target gn szintzist. Radsul minl
191
tbb tTA termeldik, az annl jobban induklja nmaga s a target gn termeldst. Ezt a rendszert
autoregultor Tet rendszernek hvjuk.
Szmos biotechnolgiai cg knl tetraciklin regullta emls expresszis rendszert. Pldul az Invitrogen T-
Rex rendszere Tet-On rendszer, teht tetraciklin s szrmazkaira kapcsol be az expresszi. Bvebben itt
lehet olvasni rla. A Tet-On s Tet-Off rendszer smjt a 13.8. bran mutatjuk be.
13.8. bra: A Tet-On s Tet-Off rendszer smja
13.4. Egyb eukarita expresszis rendszer
13.4.1. Dictyosteliumdiscoideum expresszis rendszer
A Dictyostelium discoideum egy sejtes nylkagomba. A talajban l, tbbnyire baktriumokkal tpllkozik.
Laboratriumban knnyen tarthat akr folyadkkultrban, akr szilrd tptalajon. Rvid az letciklusa, a
genomja (34 Mbp haploid genom, 6 kromoszma, 12500 fehrje gn) teljesen ismert, sok gnje homolg
humn gnekkel, a gnek szablyozsa is hasonlan trtnik. Gnjeinek szekvencija a DictyBase
adatbzisban tallhat. Nagyon j modell organizmus genetikai, sejtbiolgiai folyamatok tanulmnyozsra,
de a rkkutatsban, immunfolyamatok megrtsben is nagy hasznt veszik.
A rekombinns fehrje expresszijhoz itt is shuttle vektorral visszk be a kvnt fehrjnk cDNS-t a
gazdaszervezetbe. A vektor tartalmazza a baktriumban trtn szaporodshoz szksges elemeket (orig,
192
rezisztencia gn), s a Dictyostelium sejtben trtn replikcirt felels szekvencikat. Ennek az eukarita
llnynek is van termszetes plazmidja, aminek a replikcis origjt hasznljk ki az expresszis
vektorok. Az leszthz hasonlan vannak integrld s replikld expresszis vektorai. A
Dictyostelium expresszis rendszert leginkbb a citoszkeleton s fehrjinek tanulmnyozsra hasznljk.
Kivlan alkalmas rekombinns miozin fragmentumok ellltsra. Amennyiben a rekombinns fehrje
sejtbiolgiai szerept vizsgljk, akkor GFP-fzis cmkvel ltjk el, fehrje preparls cljbl pedig a
szoksos affinits cmkkkel (pl. His, GST, Flag). A pDXA-3H sorozat plazmid vektorokat kimondottan
fehrje expresszira dolgoztk ki.
13.4.2. Drosophila melanogaster expresszis rendszer
A gymlcslgy (Drosophila melanogaster) Schneider 2 sejtek (S2) 20-24 rs lrva primer
sejttenyszetbl szrmaznak. Knnyen kezelhetek, nem ignyelnek szndioxidot, 25-28C-on letapad s
szuszpenzis kultrban egyarnt knnyen szaporthatk. Kivlan alkalmasak tranziens s permanens
heterolg fehrje expresszira. A sejtek transzfektlsa ltalban kationos-liposzms (Cellfectin) vagy
Ca
2+
-foszftos mdszerrel trtnik. Tranziens transzfekcinl 1-4 nap mlva lehet vizsglni a transzfektlt
sejteket, vagy izollni az expresszlt fehrjt. Stabil (permanens) transzfekcinl szelektlni kell a megfelel
antibiotikum rezisztens klnokat. Szelekcira leggyakrabban higromicin s blaszticidin antibiotikumot
hasznlnak, melyek eukarita s prokarita sejtekre egyarnt toxikusak. A blaszticidin kzmbstsre
hasznlt rezisztencia gnt (blaszticidin-S-dezaminz, bsd) a pCoBlast nev plazmid, mg a higromicin
rezisztencia gnt (hpt) a pCoHygro plazmid kdolja. Mint a nvbl is ltszik, a rezisztencia gnt az
expresszis vektorral val ko-transzfekcival lltjk el. A stabil sejtvonal ltrehozsa 2-4 hetet vesz
ignybe. A stabil klnok eltarthatak, le lehet ket fagyasztani. Az expresszlt fehrje mennyisg viszonylag
magas (1-20 mg/L kultra). Az emls szervezetekben tallhat glikozilci s a megfelel diszulfid-hidak
kialakulnak. A szekrci mkdik mind az inszert sajt, mind a vektor BiP-szignljval. Hasznlhat akr
virlis fehrjk, akr humn fehrjk ellltsra, transzkripcis faktorok, vagy nem Drosophila-homolg
transzkripcis faktorok tanulmnyozsra
Drosophila expresszis vektorok: a vektoroknak hordozniuk kell az eukarita vektorok ktelez elemeit
(promter, poliA szignl, Kozak szekvencia, stb.), illetve mivel szintn shuttle vektorok, a megfelel
bakterilis elemeket is. Nhny plda: pMT/V5-His (metallotionein promtert tartalmaz, amely fmionokkal
induklhat), pCoBlast s pCoHygro vektorok (rezisztencia gnt kdolnak egy ers, konstitutv promter)
13.5. Eukarita sejttenyszts
A sejttenyszetek manipullst steril krlmnyek kztt kell vgezni. Erre alkalmas a laminris flke,
mivel nagyon kis csraszm lgteret biztost (ld. 13.9. bra).
A tenysztshez hasznlt ednyeknek s eszkzknek megbzhatan sterilnek kell lennik. Ezrt elre
csomagolt, ltalban ionizl sugrzssal sterilizlt tenysztednyeket, szerolgiai pipettahegyeket
hasznlunk. Ha erre nincs md, pl. nagy lptk szuszpenzis kultrnl, vagy nagyon kis trfogatok
kimrshez pipettahegyre van szksg, akkor tbbszri vzgz-sterilizlst hasznlunk (20 perc, 121C, 2
atm nyoms). A laboratriumban lv felleteket tartsuk tisztn, ferttlentsnk gyakran. A sterilflkt
hasznlat eltt s utn trljk t 70%-os alkohollal (etanol, izopropanol), hasznljunk gumikesztyt
magunk s a sejtek vdelmben is.
Alapveten ktfajta tenysztsi md ltezik; szuszpenzis kultra s letapad (monolayer) sejttenyszet.
Egyes szuszpenzis kultrkat llandan rzatni kell, pl. Sf9 s leszt sejtek. Az leszt sejtek nevelse
egyszer, hasonl a bakterilis sejtekhez. A tptalaj sszettele egyszer, ltalunk is sszellthat. A
rovarsejtek s az emlssejtek azonban ltalban drga, komplex tptalajt ignyelnek. Jobban jrunk, ha
megvsroljuk ket a megfelel gyrttl. Neknk csak antibiotikumot, tptl fggen L-glutamint, s
szrumot kell beletenni hasznlat eltt.
193
13.9. bra: Munka a sterilflkben
Az alap vagy bazlis tptalajokat kevsb ignyes sejtekhez hasznljuk, pl:
- MEM (Minimum Essential Medium);
- BME (Basal Medium; Eagle),
- DMEM (Dulbeccos modified MEM, emelt aminosav/ s vitaminszint),
A komplex mdiumok tbb komponenst is tartalmaznak, magasabb ignyhez igazodnak, ilyen pl. az
RPMI1640: nagyon sok sejtflesghez hasznlhat.
A tptalajok pufferolt (bikarbont-HEPES rendszer, pH 7,2-7,4) krlmnyek kztt aminosavakat
(esszencilisakat, vagy az sszeset), szervetlen skat (Na
+
, K
+
, Mg
2+
, Ca
2+
), nyomelemeket (Fe, Cu, Zn
szerves vegyletek formjban), vitaminokat, D-glkzt (esetleg fruktz, galaktz, mannz formjban) s
a megfelel pH nyomon kvetsre fenolvrs sav-bzis indiktort tartalmaznak, amihez mg szrumot
adhatunk. A szrum tartalmazza a sejtek tllshez s szaporodshoz szksges nvekedsi faktorokat s
hormonokat. Bizonyos sejtek berik felntt marha/l vrszrummal, ignyesebbeknek magzati szarvasmarha
(borj) szrumra van szksgk (FBS: Fetal Bovine Serum), st nhny humn sejt fenntartshoz emberi
vrsavra van szksg. A vrszrum tartalmaz mg zsrsavakat, lipideket, szlltfehrjket az ionok s
hidrofb molekulk szmra (pl. transzferrin a vas szmra). A szrum (minimum 5-20%-ban) bizonyos
sejteknek esszencilis, de jelenlte minden sejtnek kedvez. Vgl igen fontos, hogy a mdium tartalmazzon
antibiotikumot. A fertzsek elkerlsre ltalban penicillint s sztreptomicint (Pen-Strep 0,5-1%-ban)
adunk a mdiumhoz, de hasznlhatunk gentamicint, s (ritkbban) antimikotikumot is.
13.6. Tovbbi olvasnival a fejezethez
Romanos MA, Scorer CA, Clare JJ (1992) Foreign Gene Expression in Yeast: a Review. Yeast. 8:423-488.
Hartley, JL (2006) Cloning technologies for protein expression and purification. Current Opinion in
Biotechnology 17:359366
Barnes, LM and Dickson, AJ (2006) Mammalian cell factories for efficient and stable protein
expression. Current Opinion in Biotechnology 17:381386
Structural Genomics Consortium et al. (2008) Protein production and purification. Nature Methods
5(2):135-146
194
Knetsch ML, Tsiavaliaris G, Zimmermann S, Rhl U, Manstein DJ, (2002) Expression vectors for studying
cytoskeletal proteins in Dictyostelium discoideum. J Muscle Res Cell Motil. 23 (7-8): 605-11.
Kato T, Kajikawa M, Maenaka K, Park EY (2010) Silkworm expression system as a platform technology in
life science. Appl Microbiol Biotechnol. 85(3):459470.
195
14. Clzott gnmdosts (gn-targeting) mdszerek
14.1. Bevezets
Az eddigi fejezetekben megismerkedtnk a gntechnolgia sokfle mdszervel. Az eddig lert mdszerek
azonban az l rendszer egszt tekintve csak korltozott alkalmazsokat tesznek lehetv. Plazmidokkal s
egyb kvlrl bevitt, genetikailag nem stabil elemekkel nem lehet a legtbb organizmus sajt, bels
mkdst tartsan megvltoztatni. Ehhez olyan technolgikra van szksg, amelyek lehetv teszik az
llnyek sajt gnjeinek DNS-szint talaktst. A genomilis DNS mdostsa viszont minden
tekintetben sokkal nehezebb, mint - a viszonylag kicsi - plazmidok s mestersges kromoszmk szabsa-
varrsa. A legnagyobb problma a kromoszmk mrete. Egy sok megabzis (milli bzispr) vagy esetleg
gigabzis (millird bzispr) mret DNS-szekvenciban nem tudunk kellen rvid, de mgis egyedi
szekvencikat tallni. A hagyomnyos, restrikcis endonuklezokon alapul technikk itt egyszeren csdt
mondanak. Teht a kromoszmk DNS-nek mdostshoz teljesen ms, jszer mdszereket kell
hasznlnunk. Ezek nem 5-10 bzispr szekvencijnak azonossgra plnek, hanem jval hosszabb
darabokra, motvumokra. A msik problma a genomilis gnek s kromoszma-darabok fizikai mrete:
egy-egy ekkora makromolekula manipullsa, s bejuttatsa a sejtbe nmagban hatalmas kihvst jelent.
Ezen problmk mg ma sem teljesen megoldottak, de a genom-szint mdost mdszerek vrl-vre
fejldnek, s mint ltni fogjuk, az alkalmazsok egsz trhzt nyitjk meg a molekulris biolgia szmra. A
"gene-targeting" kifejezst (magyarul clzott gnmdostsnak fordthatjuk) itt most tg rtelemben
hasznljuk: belertjk exogn DNS-darabok, vagy egsz gnek bejuttatst a genomilis DNS-be spontn
integrcis mechanizmusok rvn is.
14.2. DNS hibajavts s homolg rekombinci
Hogy megrtsk a genomilis DNS-mdost eljrsok mkdst, elbb a DNS-hibajavts
mechanizmusait kell ttekintennk. Az rktanyagban sokflekppen keletkezhet hiba, ennek megfelelen
szmos mechanizmus ltezik a kijavtsukra is. Az egyszer bzis-cserket viszonylag knny kijavtani.
Attl fggen, hogy a bzis kmiai mdosulsrl, hidrolzisrl vagy egy (a replikcis sorn keletkez)
hibs beplsrl van sz, klnfle bzis vagy nukleotid kivg (exczis) mechanizmusok llnak
rendelkezsre. Ha a DNS-dimer egyik felben a cukor-foszft gerinc "eltrik" (hidrolizl), akkor ezt egy
megfelel DNS-ligz enzim knnyedn helyre tudja lltani. Ms a helyzet, ha nhny nukleotid tvolsgon
bell mindkt lnc eltrik. Ilyenkor a hmozgs kvetkeztben mr nhny msec elteltvel igen messze
kerlnek a szabad vgek egymstl. Ahhoz, hogy ilyenkor is helyre lehessen lltani a DNS-t, sszetett
javt enzim-rendszerekre van szksg. Elszr is az sszetartoz vgeket (hosszas keresssel) meg kell
tallni, utna pedig lehetsg szerint hiba nlkl egyesteni kell ket.
A ketts trsek utni javtsra is tbbfle in vivo mechanizmus ll a sejt rendelkezsre. A gntechnolgiai
alkalmazsai miatt a kt legfontosabb tvonalrl rszleteiben is kell beszlnnk. Az egyik a nem-homolg
vg-a-vghez illeszts (NHEJ: Non-homologous end joining). Ilyenkor a kvetkezrl van sz: ha a kt
trvget (eredetileg a csonttrsekre hasznlt kifejezs) meg tudja tallni az enzimkomplex s azok
tkletesen illeszkednek, akkor az NHEJ javt rendszer DNS-ligz aktivitsa rvn egyesteni fogja ket. A
nem-homolg hibajavtst (ami sok baktriumban elgg alrendelt, de emlskben dominns szerep) a
bzisprosodsok vezrlik. Amennyiben erre nincs md (pl. tompa vggel vlt szt egymstl a kt DNS
vg, vagy a nukleotidok kmiailag megvltoztak), akkor ms mechanizmust kell vlasztani. Ilyenkor
elkezddik a trvgek 5' szlnak visszavgsa, megfelel exonuklezok ltal. Mg mindig van lehetsg
nem-homolg egyeslsre (MMEJ: Microhomology-mediated end joining), de a tkletes javts csak a
vgek egyestsvel ilyenkor mr nem lehetsges. Minden remny azonban nem veszett el. Ha a sejtnek
sikerl egy megfelel, p ketts szl DNS templtot tallnia a javtsra, akkor kiptolhatja az elveszett
szakaszokat, s hibtlanul helyrellthatja a srlt molekult. Ez az alapja a homolg rekombincinak (ld.
14.1. bra).
196
14.1. bra: DNS kettstrsek javtsa: nem homolg vg-a-vghez illeszts s homolg rekombinci
Ilyenkor a trvgeket felismer fehrjekomplex elbb hosszan szttekeri a DNS-t, s lebontja az 5'- vg
szlat. Az egyszl DNS-t erre specializlt fehrjk burkoljk be, hogy lineris maradjon. Ezzel egyidejleg
elkezddik a homolgia-keress. Ha sikerl egy, a trvghez hasonl szekvencij ketts szl DNS-t
tallni, akkor azt a megfelel fehrjk szttekerik, s a trtt 3' szl benyomul az p prjnak a helyre
(strand invasion). Ez utn a DNS-polimerz segtsgvel megkezddik a srlt szl kiegsztse. A
rekombincis pont mgtt a ngy DNS-szl egy furcsa, "vasti keresztvltra" emlkeztet keresztezdst
alkot (Holliday junction). Miutn minkt szl megtallta a homolg prjt, elegenden hossz szintzis
utn az sszes nukleotid visszaptldik. DNS-ligzok ezutn bezrjk a nukleotidszlak cukor-foszft
gerinct. Marad azonban egy kis problma: a kt kromoszma kt helyen mg mindig keresztezdik
egymssal. Ezen pontok feloldsra specilis reszolvz enzim ll rendelkezsre (Holliday junction
resolvase). A reszolvz elvgja a ngyes DNS-t majd tellenben egyesti, ezltal kt kln prt hoz ltre.
A keresztezdsek egybknt a keletkezsk utn vndorolhatnak is: ez segthet akkor, ha csak az egyik 3'-
vg tallta meg a homolgjt. A hibrid ilyenkor sztvlhat, s gy a kiegsztett trtvg is megkeresheti a
prjt (SDSA: Synthesis dependent strand annealing). Ebben az egy esetben nem gond az eredeti viszonyok
visszalltsa. Minden egyb esetben viszont mivel a Holliday junction tkletesen szimmetrikus
kpzdmny a reszolvz enzim hastsa a kt eredetileg klnbz kromoszma hibridjt hozhatja ltre
(crossing over). Ha a kt kromoszma valban teljesen homolg, akkor ez nem problma. Ms esetekben
viszont rekombincihoz fog vezetni. Ilyen rekombincis esemnyeket hasznlnak a meizis sorn az
eukarita sejtek (szndkosan eltrve a kromoszmkat) hogy az apai s anyai eredet gnjeikbl j
kombincikat hozzanak ltre. Ugyanezt a jelensget hasznljk a homolg rekombincira alapozott
gnmdost mdszerek is.
A homolg rekombinci vzlatos mechanizmusait a 14.2. bra mutatja be.
197
14.2. bra: A homolg rekombincis javts tjai s vzlatos mechanizmusaik
A sejtekbe juttatott linearizlt rekombinns DNS-sel sokkal nagyobb hatkonysg rekombincit lehet
elrni, mint a cirkulris eredetivel. A vgeket ugyanis mivel nincs rajtuk a telomerekre jellemz vd
198
szekvencia az eukarita sejtek trvgekknt fogjk rzkelni, s ez aktivlni fogja a kettstrst javt
mechanizmusokat. Kis szerencsvel a sejt a vgek visszabontsa utn meg fogja tallni a hossz homolg
rszek egyikt, s keresztezdst kpez a sajt kromoszmjval. ltalban ez a kritikus lps: ha az egyik
vget sikerlt megillesztenie, akkor a tbbi homolg szakaszt is nagyon knnyen megtallja. Br ilyenkor a
"javts" igazbl lehetetlen feladat - hacsak a sejt nem kapcsolja ssze a plazmidok vgeit - a Holliday-
junkci gy is bizonyos valsznsggel feloldsra kerl, gy a sejt a sajt, j genomilis szakaszt adott
esllyel eldobhatja egy rossz templt kedvrt. Az eredmny egy genomjban clzottan mdostott sejt
lesz.
14.3. Gn-targeting konstrukcik ellltsa
A legtbb ma hasznlatos clzott gnmdost eljrs a homolg rekombincin alapul. Ez azonban nem
hasonlt az in vitro klnozshoz. Sosem szabad elfelejteni, hogy itt egy spontn folyamatrl van sz,
amelynek hatsfoka mg idelis esetben is meglehetsen alacsony. A leghatkonyabb ma hasznlatos
technikk is csak kb. 1% valsznsggel eredmnyeznek "j" clegyedeket, benne a clmolekulval.
Ahhoz, hogy ezt ki tudjuk hasznlni, nem elg a megfelel DNS-darabot egyszeren csak bejuttatni a
clsejtbe. A valsgban a klnbz pozitv s negatv szelekcis stratgik ravasz kombincijra van
szksg. A gyakorlatban nagyon sokfle technikval lehet gn-targeting konstrukcikat ellltani. Itt csak
nhny fbb mdszert fogunk bemutatni, a teljessg ignye nlkl.
14.3.1. A recombineering alapjai. A Red rekombincis rendszer
A homolg rekombincit nemcsak eukarita szervezetekben lehet hasznlni: ilyen folyamatok
prokaritkban is lteznek. Ezt a jelensget fel lehet hasznlni a plazmidok s mestersges kromoszmk
kztti DNS-darabok csereberlshez. A homolgit mutat DNS-darabok rekombinci rvn pldul
egyesthetnek kt klnfle DNS-darabot, vektort (klnsen ha csak egy homolg szakasz van). Ha a kt
DNS-darab tbb homolg szakasszal is br, akkor a rekombinci tviheti a kzttk lv darabot az
egyikbl a msikba ("bepattints", angolul "pop in"). Ugyangy, kt homolg szakasz vektoron belli
prosodsa a kztes darab kivgdshoz, esetleg elvesztshez vezethet ("kipattints", "pop out"). Pozitv
(pop in esetn ) vagy negatv (pop out esetn) szelekcis markerek beptse a krdses darabba felgyorstja
a folyamatot . Ezeket a mdszereket szoktk "recombineering"-nek (recombinogenic engineering) nevezni .
Noha a baktriumok rekombincis kpessge nmagban viszonylag alacsony, az ket megfertz vrusok
nmelyike jelentsen fokozza a homolg rekombinci eslyt: olyannyira, hogy akr a transzformcival
bejuttatott rvid, lineris DNS-darabok is rgtn beplhetnek a megclzott plazmidba. Ezt bizonyos trzsek
mdostsval nagy hatkonysg in vivo klnozsra lehet hasznlni.
A legelterjedtebb a Red rekombincis rendszer. Ennek mkdshez a -fg hrom klnbz gnjre
van szksg (Exo, Bet s Gam). Az Exo gn egy exonuklezt kdol, ami a bejuttatott ktszl DNS-seket
5'3' irnyban visszanyesi, ragads vgeket hozva ltre. A Bet fehrje a szabad, egyszl DNS-vgekhez
ktdik, s megvdi ket a degradcitl. Vgl, a Gam gn termke blokkolja a baktrium sajt RecBCD
javt enzimt, amely egybknt sztszedn a bejuttatott lineris DNS-t. A rekombinci ltrejtthez a
sejteknek aktvan nvekednie kell, a bepls ugyanis a DNS-szintzis kzben, kzvetlenl a replikcis
villban trtnik. Mivel a virlis gnek aktivldsa akadlyozza a baktrium normlis letciklust, ezrt
hmrsklet-szenzitv rendszert hasznlunk. Az E. coli tenyszetet 32
o
C-on tenysztve a (defektv) profg
formjban beplt -fg gnek teljesen ki lesznek kapcsolva, de egy rvid hsokk rvn (42
o
C)
aktivlhatak. Ezutn a baktriumokat azonnal transzformlni kell. A Red rendszert fel lehet hasznlni in
vivo mutagenezisre is: ha egyszl DNS-t juttatunk a baktriumba (pldul elektroporcival), akkor az be
fog plni a szlet szl helyre. A mdszer akkor a leghatkonyabb, ha az oligonukleotidunkat gy
tervezzk meg, hogy a szintzis sorn elmarad szllal legyen homolg. A Red rekombincis rendszer akr
plazmiddal is bevihet a clsejtbe (a pSIM plazmidcsald rvn), ezrt alkalmas arra, hogy bakterilis
mestersges kromoszmkbl (BAC klnokbl, illetve az azokat hordoz baktriumokbl) genomilis
199
darabokat klnozzunk t egy ltalunk meghatrozott vektorba. gy akr egr vagy emberi kromoszmk sok
ezer nukleotidos darabjai is knnyen tvihetek a kvnt plazmidba. A Red rendszer bevitele utn csupn
egy feladatunk van: A megfelel, a tervezett vgekkel homolg kicsi szakaszokat kell beptennk a
vektorunkba. De a clplazmidot a bejuttats eltt linearizlni is kell, gy, hogy a klnozni kvnt rsz
vgeivel homolg rvid darabkk a vektor kt szabad vgre kerljenek. Ezrt a legknyelmesebb
megolds, ha a teljes vektor PCR termkt transzformljuk, amit megfelel (a clgnnel homolg) tlnyl
vgekkel lttunk el, a PCR primerek j megvlasztsval. A rekombinci ezek utn spontn ki fogja szedni
a kvnt darabot a BAC klnbl, s bepti a vektorba, bezrva a plazmidot. Ugyangy, a kvlrl bevitt,
PCR-rel ltrehozott inszertek is egy lpcsben (mindenfle restrikcis emszts nlkl) "bepattinthatak" a
kvnt vektorba, ha a tervezett beplsi hellyel megfelel homolgia van minkt vgen. Ezen elnyk miatt
a Red rendszer a targeting vektorok ptsnl ma az egyik leggyakrabban hasznlt technika.
14.3.2. Gateway klnozs
A targeting vektorok ptsnl gyakori problma, hogy vektor-alapvzat kell cserlni a klnozs sorn. Ha
itt is el szeretnnk kerlni a restrikcis emsztseket, erre a leggyorsabb s leghatkonyabb technika az n.
"Gateway" klnozs. Ezt az Invitrogen cg ltal kifejlesztett mdszert, mint hastsmentes klnozst rviden
mr emltettk a 4.2.6. fejezetben. Itt is a -bakteriofg letciklust hasznljuk ki: mikor lizogn fzisba lp,
a fg integrcijt a gazdakromoszmba egy specifikus enzim (integrz, Int) irnytja, amely a fg
cirkulris DNS-st egy adott helyen (AttP) felnyitja s egyesti a bakterilis genom egy specifikus helyvel
(AttB). Az AttP s AttB helyek sszekapcsoldsval hibrid szekvencik keletkeznek: AttL ("bal vg") s
AttR ("jobb vg"). A reakci maga egyirny, de megfordthat: mghozz a fg exczis enzime (Xis) ltal.
Ez az enzim a profg kt vgn tallhat AttL s AttR szekvencikat ismeri fel, sztvgja a DNS-t s
keresztben jraegyesti. Ezzel kivgja a fg-genomot s cirkularizlja azt, helyrelltva az eredeti AttB s
AttP helyeket (ld. 14.3. bra).
14.3. bra: A -fg termszetes lizogn letciklusa (A) s a Gateway klnozs smja
200
A reakci mechanizmusa hasonlt a restrikcis klnozsra: a hastskor itt is "ragads" vgek keletkeznek,
amelyek a bzis-komplementarits segtsgvel fognak jra egyeslni. Az AttB helyek ltalban rvidek, a
bepls sorn az AttP hely hossz, nem szimmetrikus 5'- s 3'-vgei megoszlanak az AttL s AttR kztt.
Fontos szrevennnk, hogy egyik felismer hely sem teljesen azonos a msikkal, mivel nem palindrom
szekvencikrl, s csak rszben komplementer prokrl van sz. Viszont az enzimek rzkenyek a felismer
helyek homolgia viszonyaira: ha az sszetartoz pr egyikben pldul az AttP-ben) a homolg szakaszt
kicserljk, akkor a reakci csak akkor fog mkdni, ha ugyanezt a csert az AttB-ben is vgrehajtjuk. Az
egsz technolgia ezen az szrevtelen alapszik: a megfelel, kompatibilis prokat szmozssal szoktk
jellni. Ha teht a plazmidunk tartalmaz kt darab, megfelelen orientlt AttL helyet (AttL1 s AttL2),
amelyek egy "picikt" klnbznek egymstl (a komplementer szakaszuk ms), de pontosan megfelelnek
egy msik vektor AttR helyeinek (AttR1 s AttR2), akkor az sszetartoz helyek pronknti egyestsvel a
kztes darabok tkerlnek az egyik vektorbl a msikba. A reakci in vitro kivitelezhet: ehhez csak a
megfelel LR enzimkeverkre van csak szksg (a valsgban nemcsak a Xis enzim kell, hanem az E. coli
sajt IHS Integration Host Factor fehrjjre, st az Int integrzra is). A vgtermk vektorokban az
inszert kt vgn AttP1, s AttP2, illetve AttB1 s AttB2 helyek keletkeznek. Termszetesen, ha a msik
fajta, BP enzim keverket hasznlunk a vgtermken (ami csak az IHF s az Int fehrjket tartalmazza, Xis
nlkl), akkor a reakci irnya megfordul, s visszakapjuk az eredeti konstrukciinkat. (ld. 14.3. bra) Nem
szabad elfelejteni, hogy az AttL, AttR, AttB s AttP vgek mind-mind rzkenyek az irnytsra: ha az
egyik vget vletlenl fordtva ptjk be, akkor a kt vektor fog egyeslni egymssal, ahelyett hogy az
inszertet vinnnk t ezrt nagyon figyeljnk oda a tervezsnl!
A Gateway klnozs klnsen akkor elnys, ha az inszertnket ksbb nagyszm, klnfle vektorba
szeretnnk tvinni. Ilyenkor az inszertet elbb egy alapvektorba (entry vector) ptjk be, amely tartalmazza
a megfelel AttL1 s AttL2 vgeket. A bevitel trtnhet magval a BP reakcival is (ligls-fggetlen
klnozs, ld. 4.2.5. fejezet): ilyenkor a PCR-termk tlnyl vgei tartalmazzk az AttB1 s AttB2
helyeket, a plazmid pedig az AttP1 s AttP2 clszekvencikat. Az inszertet utna nagyszm klnbz,
AttR1 s AttR2-tartalm clvektorba lehet tvinni - pldul a fehrjetermels optimalizlsa cljbl. Az
AttP, AttL, AttR helyeket tartalmaz "gyri" vektorokat gy alkottk meg, hogy a kt rekombincis hely
kztt egy specilis negatv szelekcis marker legyen: a ccdB gn (F-plazmid eredet DNS-girz inhibitor)
ha a helyn marad akadlyozni fogja az tlagos E. coli sejtek nvekedst, gy a csak a kicserldtt
inszertet tartalmaz klnokat fogjuk visszakapni. A klnfle AttR s AttL prok sszetettebb szublnozst
is lehetv tesznek: trkks felhasznlsukkal akr kis inszertek sorozatbl is pthetnk egy nagy
inszertet. A Gateway klnozs a targeting vektorok esetben a negatv rezisztencia-gnek beptsnl
klnsen hasznos: ezeket a vgs clvektor tartalmazza, s ide lehet az sszes klnbz clz (targeting)
konstrukci magjt berakni, mindenfle restrikcis emszts nlkl, LR klnozssal.
14.3.3. Targeting vektorok tervezse
Az sszes szksges fbb mdszer ismeretben most mr abban a helyzetben vagyunk, hogy akr meg is
tervezhetjk a sajt targeting vektorunkat. Elsknt a kvetkez felttelt rdemes szem eltt tartani: az
eukarita rendszerek homolg rekombincis mdostshoz nagyon hossz homolg szakaszok kellenek.
Akr gnkitst terveznk, akr gnt akarunk clzottan bevinni egy organizmusba, a konstrukcink kt
homolg vgnek kln-kln legalbb 1,5-2 kbp mretnek kell lennie. Br a kt vg nem kell hogy
egyforma hossz legyen, j ha egyttes hosszuk legalbb ~6 kbp. Egy msik fontos feladat a szelekcis
markerek megvlasztsa. A tervezett konstrukci belsejbe (a homolg "karok" kz) legalbb egy olyan
rezisztencia-gn beptse szksges, amely a clszervezetben is aktv: ez lesz a pozitv szelekcis
markernk.
Eukarita sejtek szelekcijra termszetesen nem hasznlhatunk olyan vegyleteket, amelyek csak a
baktriumokra hatnak (pl. ampicillin): neomicin, blaszticidin, puromicin vagy zeocin antibiotikumokat
szoktunk alkalmazni. Ezek tbbsge mind prokaritkban, mind eukaritkban hatkony: teht lehetv
teszi, hogy olyan rezisztencia-gnekkel szelektljunk, amelyeket gy terveztnk meg (dupla promterrel,
Shine-Dalgarno s Kozak szekvencikkal), hogy mind a klnozsra hasznlt E. coli-ban, mind pl. egr
201
sejtekben expresszldjanak. A pozitv szelekcis marker azonban nmagban nem elegend. A vektorbl
ered, a homolg karokon tlnyl vgekre kell legalbb egy negatv szelekcis marker, hogy a nagyon
gyakori nem-homolg rekombincis esemnyeket (NHEJ) megprbljuk kiszrni. A homolg
rekombinci a rezisztencit hordoz kazetta (kazettk) kt vgn lv hossz homolg karokon fog
bekvetkezni, gy a negatv szelekcis marker (rzkenysgi gn) ilyenkor (s csak ilyenkor) kiesik (ld.
14.4. bra).
14.4. bra: Gn targeting vektorok vzlatos felptse s a kromoszmba val bepls lehetsges mdjai: homolg
rekombinci (A) s random bepls (B)
A gyakrabban hasznlt rzkenysgi gnek kz tartozik a diftria toxin A-alegysg (nvnyekben is
hasznlhat), vagy a citozin-dezaminz enzim. Emls rendszerekben leginkbb a herpeszvrus
timidilt-kinz (TK) gnt hasznljk, ez ganciklovir jelenltben a sejtek pusztulshoz vezet. Mivel az
egyoldali homolg bepls nagyon ritka folyamat, ezrt a legtbbszr elegend, ha csak az egyik nem
homolg karon tallhat egy negatv szelekcis marker.
Vgl, de nem utolssorban a gnmdostst ellenrz tesztekrl (assay) kell gondoskodnunk. Ezekkel
tudjuk ugyanis bebizonytani, hogy a targeting vektorunk megfelelen clba tallt-e. A legtbb vektor-ptsi
lps ellenrzsre a PCR is megfelel, a clszervezetben azonban praktikusabb Southern-blot eljrst
hasznlni. Egy j stratgia lehet pldul a kvetkez: a prbinkat tervezzk gy a clszervezet
kromoszmjra, hogy ppen kvl essenek a targeting vektorban hasznlt hossz karokon. Vlasszunk
olyan restrikcis enzimet, ami belehast az ltalunk bevitt kazettba, de az eredeti genomilis szakaszba
nem. Az emsztett kromoszomlis DNS-hez gy a helyes s rossz bepls esetn mshol fog hibridizlni a
prbnk. Mivel a vektor ptse is meglehetsen bonyolult, ezrt mindenkppen ellenrizzk a
konstrukcinkat a clszervezetbe juttats eltt! Csak teljesen szekvenlt vektorral ajnlatos dolgozni, s a
homolg karok, valamint a beptett kazettk hosszt s orientcijt is mindig ellenrizni kell, megfelelen
tervezett Southern-blot prbk, restrikcis trkpezs s/vagy PCR segtsgvel.
202
14.3.4. A gn-targeting konstrukcik elksztse
Egy targeting vektor ptse nem egyszer feladat. Ehhez szksgnk van a clszervezet genomilis DNS-
snek megfelel szakaszra. Egy megfelel, genomilis DNS-t tartalmaz mestersges baktrium-
kromoszma (BAC kln) megvsrlsa ilyenkor nagy segtsg lehet. Ha a hagyomnyos, PCR-alap
eljrst vlasztjuk, akkor keresnnk kell olyan restrikcis helyeket, amelyek nincsenek jelen a megclzott
genomilis szakaszon. Ezutn hrom kln PCR-rel felszaportjuk a kt homolg karnak megfelel szakaszt,
tovbb a kzjk beptend (szelekcis s mdost) kazettt. A restrikcis emsztsek utn (amely
helyeket a primerekkel vittk be) egy hrmas liglst kell vgrehajtanunk! Haladhatunk lpsenknt is, de
akkor nincs md sehol a szelekcira, szrni kell a klnokat; ezrt ez az eljrs meglehetsen fradsgos s
lass. Ha azonban sikerlt a ligls, akkor a plazmid elkszlt, mivel tartalmazza a negatv szelekcis
markert s a linearizcihoz szksges extra hasthelyet. A hagyomnyos mdszer gyengesge a restrikcis
hasthelyekben rejlik: nem minden esetben van md ugyanis ezek alkalmas megvlasztsra. Tovbb a
nem-kdol genomilis szekvenciban polimorfizmusok lehetnek, amelyek elre nem lthat mdon
hasthelyeket hozhatnak ltre. Szintn fontos hogy a PCR utn minden klnt elejtl-vgig ellenrizni kell
(szekvenlssal), hogy ne vigynk be a rekombincival nem kvnt mutcikat.
A modernebb, recombineering-alap eljrsok ezen htrnyokat jrszt kikszblik. Ilyenkor a Red
rekombincit hasznljuk a konstrukci megptshez. A BAC-klnt tartalmaz baktriumokat a pSIM
plazmiddal transzformlva bevisszk a Red rendszert. A mdost kazettk beptse s a kiszemelt
vektorba val temels egyarnt in vivo trtnik, a hsokkolt baktriumok PCR termkekkel val
elektroporlsa utn. A kazettk beptst egyszeren antibiotikum-szelekcival ellenrizhetjk. Ezutn a
vektoron is PCR-t hajtunk vgre a tervezett homolg karok kt szlvel rviden azonos, kb. 40-50
bzispros tlnyl vggel s ezzel transzformlunk. gy tudjuk kiemelni a BAC klnbl a kvnt
szakaszt. Ennl az egy lpsnl nem tudunk szelektlni: ezrt plazmidot kell preparlnunk s ellenrzs utn
jra transzformlnunk. Ezt a lpst ki lehet vltani kztes vektor hasznlatval (amely pl. lehetv teszi a
kk-fehr szelekcit az temelskor). Ebben az esetben megcserlhetjk a klnozsi sorrendet, s a
kiemelssel kezdhetnk. Ha az sszes kvnt elemnk a helyre kerlt, akkor kvetkezhet a vektor-alapvz
cserje, gy a rendszerbe belekerl a negatv szelekcis marker, s egy vagy tbb megfelel, ritka restrikcis
hasthely is. Ha az els lpsben olyan vektort hasznltunk, amely Gateway-kompatibilis, pl. AttL vgeket
tartalmaz a klnoz hely kt vgn, akkor ezt a vgs lpst nagyon egyszer lesz vgrehajtani: az
inszertnk a vgleges vektor AttR vgeivel fog rekombinldni egy in vitro LS klnozsi reakci utn. A
clszervezetbe val bejuttats eltt azonban restrikcis emsztssel linearizlni kell a vektort.
14.4. A targeting-konstrukci bejuttatsa a clszervezetbe
14.4.1. Sejtek s sejtvonalak transzfektlsa. Emls embrik manipulcija
Ha a gnmdostst llati sejttenyszeten kvnjuk vgrehajtani, akkor a DNS bejuttatsa viszonylag
egyszer feladat. Akr embrionlis ssejteket (ESC: embryonic stem cell), akr daganatos sejtvonalakat
kvnunk megclozni, a protokoll minden esetben nagyon hasonl. Ugyangy kell eljrnunk, mint a
plazmid-alap fehrje expresszikor (ld. 4.3.2 fejezet). A sejteket lehetsgnk van elektroporlni is, de
ennl gyakrabban hasznljuk a kmiai genseken alapul transzfekcis mdszereket. Ilyenkor vagy
kationos lipideket vagy kationos, elgaz szerves polimereket (dendrimereket) kevernk a linearizlt
plazmidhoz, s a sejtekhez. Ezek komplexet kpeznek a DNS-sel, de egyttal destabilizljk a sejtmembrnt
is, gy a plazmid-reagens komplex be tud jutni a membrnon keletkez lyukakon.
A transzfekci utn antibiotikum (pl. a neomicin-analg G418) hasznlatval szelektlnunk kell a
transzfektlt sejteket. A be nem plt plazmidok nem szaporodnak, gy az osztdsok sorn elbb-utbb
kihgulnak a tenyszetbl: csak a kromoszmba beplt rezisztencia-gn fog stabilan megmaradni. Mivel a
vletlen integrci (NHEJ) lesz a bepls leggyakoribb mdja, a pozitv mellett negatv szelekcira is
szksgnk lesz: ezt llati sejteken leginkbb a mdiumhoz adott ganciklovirrel szoktk vgezni (a vektorok
203
timidilt-kinz gnt tartalmaznak). Csak az a sejtpopulci eslyes arra, hogy hordozza a transzgenikus
kazettt a genom megfelel helyn, amely tllte a dupla szelekcit. Ha knock-out vagy knock-in egeret
szeretnnk ltrehozni, a kvetkez lpsben az embrionlis ssejteket 3,5 napos blasztociszta stdium
embrikba kell injektlnunk (mikroinjektorral). Az embrikat ltalban in vitro fertilizcis eljrssal
lltjuk el, de hogy a folyamat sikeres legyen, a beltetsrl is gondoskodnunk kell. Steril hmmel val
proztatssal a befogad nstny egr mht a megfelel fzisba hozzuk (lterhessg).
14.5. bra: Clzott gnmdosts (A) s clzs nlkli gnmdosts ltrehozsa egrben (B). Az utbbi eljrssal
transzgenikus egeret hoztunk ltre.
204
A kezelt embrikat a befogad, lterhes egr uterusba fecskendezve valdi terhessget hozunk ltre. A
szlet kisegerek genetikailag kimrk lesznek, amelyek szerencss esetben a csravonalukban is hordozzk
az eredeti, mdostott sejtek utdait. Az egerek proztatsval, majd (szksg esetn) beltenysztsvel
hozhatak ltre a tisztn transzgenikus llatok (az llatokat termszetesen genotipizlni kell, pl. Southern-
blottal vagy PCR-rel). Az eljrs smjt a 14.5. bra foglalja ssze.
14.4.2. Stabil transzfekci. Transzgnek clzs nlkli bevitele
Amennyiben a transzgnt clzs nlkl szeretnnk bepteni a clszervezet genomjba, a fentieknl jval
egyszerbb dolgunk lesz. Ilyenkor nincs szksge sem homolg vgekre, sem negatv szelekcira:
egyszeren a cl-kazettval (ill. az azt hordoz plazmiddal) transzfektlunk, amely tartalmazza a bevinni
kvnt gnt s egy megfelel rezisztencia-gnt. Az antibiotikum-szelekci ki fogja szrni azokat a klnokat,
ahol (fleg NHEJ rvn) a genomilis DNS-be beplt a kazettnk. Sejtvonalak esetn ezt hvjk stabil
transzfekcinak: ennek fleg a gygyszeripari biotechnolgiban van nagy jelentsge (ld. a kvetkez
fejezetet). A leggyakrabban hasznlt CHO (Chinese hamster ovary) sejtekbl pldul hinyzik a
dihidrofolt-reduktz gn. Ha ezt a vektorunkkal bevisszk, akkor metotrext jelenltben csak azok a
sejtek lesznek kpesek tartsan nvekedni, amelyek genomjba integrldott a konstrukcink. gy
elkerlhet a drga antibiotikumok hasznlata is. Mivel a nem-homolg rekombinci emlskben nagy
hatkonysg folyamat, ez knnyv teszi a clzs nlkli transzgn egerek ltrehozst. Ilyenkor nincs is
szksg az elzetes szelekcira: A vektor DNS-t kzvetlenl az in vitro megtermkenytett petesejtbe
juttatjuk be (mikroinjektorral). A beltets itt is a megfelel lterhes egrbe trtnik, s a megszletett
kisegereket alkalmas markerekkel genotipizlva lehet megtallni a sikeres transzformnsokat.
14.4.3. Nvnyi s gomba sejtek transzformlsa. Homolg rekombinci
nvnyekben
Az llati sejtekkel ellenttben, amelyek gyakran "csupaszak", a tbbi eukarita llny membrnjt kvlrl
vastag sejtfal burkolja. Ez a DNS bejuttatsa szempontjbl is komoly akadlyt jelent. gy nvnyek s
gombk genetikai mdostshoz a DNS-t nem lehet nmagban csak az eddig emltett kmiai
mdszerekkel bevinni. A sejteket termszetesen elektroporlhatjuk, st, a (ksbb emltsre kerl)
gnpuskt is bevethetjk rajtuk, de van ennl egyszerbb megolds is: el kell tvoltani a sejtfalat.
Gombknl ezt hvjuk szferoplaszt mdszernek. Ilyenkor enzimatikus emsztssel, kitinzzal
szabadulunk meg rszben a sejtfaltl; a keletkez sejteket nagy ozmolarits cukoroldatban (1 M szorbitol)
kell reszuszpendlni, s nagyon vatosan szabad csak kezelni (spontn kilyukadhat a membrnjuk).
lesztgomba sejtek (pl. Saccharomyces cerevisiae, Pischia pastoris) sikerrel transzformlhatak a sejtfal
leemsztse nlkl is, mghozz ltium-acett, nagy molekulatmeg polietiln-glikol (PEG 4000) s
hsokk egyttes alkalmazsval (ltium-mdszer). Nvnyek transzformlsakor szintn elbb a sejtfalat
tvoltjuk el: cellulz s pektinz egyttes alkalmazsval. A (pldul levelek sztdarabolsa utn)
keletkez, emsztett sejteket itt is megfelel ozmolarits oldatban (pl. 0,6 M mannitol vagy 0,25 M CaCl
2
)
kell tartani. A gombkhoz hasonlan, a lecsupasztott nvnyi sejtek (pl. Arabidopsis protoplasztok)
knnyen transzformlhatk csupn a plazmid DNS s polietiln-glikol hozzadsval (pl. 25% PEG 6000)
is. A nvnyi sejtek azutn megfelel krlmnyek mellett visszaptik a sejtfalat, osztdsnak indulnak
(protoplaszt regenerci), majd teljes nvnyi embriv alakulhatnak t (szomatikus embriogenezis). A
regenerci kzben a sejteket a bevitt kazetta rezisztencia-gnjvel szelektlni lehet, de egyb szrs is
megvalsthat (pl. GFP gn bevitelvel). Maga a protoplaszt regenerci alacsony hatkonysg folyamat
(nagyjbl 10000, vagy tbb sejtbl lesz egy teljes nvny). A homolg rekombincis megkzelts
sikerrel hasznlhat pl. mohk (Physcomitrella patens) genetikai mdostsra, de a magvas nvnyekben
ezek a mdszerek sajnos csak alacsony rekombincis hatkonysgot tesznek lehetv: ma is van igny a
clzst elsegt j mdszerekre.
205
14.4.4. Nvnyek genetikai mdostsa Ti plazmid segtsgvel
Nvnyi sejtek genetikai mdostsra a protoplaszt-regenercinl hatkonyabb mdszerek is lteznek. A
legrgebben ismert, s ma is a leggyakrabban hasznlt eljrs egy klnleges nvnyi parazita, az
Agrobacterium tumefaciens tumor indukl (Ti) plazmidjt hasznlja. Ez a baktrium tbbfle ktszik
nvny gykern lskdve, az E. coli-bl ismert F-plazmidhoz hasonl konjugcis rendszert hasznl a
gazda megbetegtsre. Ebben az esetben a konjugci nem kt baktrium kztt kvetkezik be, hanem az
Agrobacterium a gazdanvny sejtjbe viszi t a plazmid egy rszt, ahol az a genomba integrldik. A Ti
plazmid nagymret (~200 kbp), s szmos operont tartalmaz. A daganatkpzsrt illetve a baktriumot
ellt tpanyagok szintzisrt felels (eukarita rendszer) gneket a mestersges konstrukcikban
ltalban eltvoltjuk (disarming), ezek helyre lehet bepteni a bevinni kvnt gneket. Az tvitelhez illetve
a beplshez csupn a plazmid kt specilis szekvencijra ("bal szl", LB s "jobb szl", RB ) valamint a
virulencit biztost Vir operonra van szksg. A Vir operon valjban legalbb 18 klnbz gnt
tartalmaz: a plazmid tvitele ezek koopercijval valsul meg. A VirA gn egy receptor-hisztidin-kinzt
kdol, ami rzkeli a nvny srlsekor felszabadul anyagot (acetosziringon). A VirG fehrje
foszforilcija rvn aktivldik s bekapcsolja az operon tbbi gnjt. A VirC1 (felismer) s VirD1/2
(endonuklez) fehrjk a plazmid megfelel vgeihez (LB s RB) ktdve annak hastst eredmnyezik. A
letekered, egyszl DNS-t a VirD2 s VirE2 fehrjk vdik meg a degradcitl, egyben a VirB gn
termke ltal ltrehozott prushoz is irnytjk, amelyen keresztl az a nvnyi sejtbe exportldik. A VirD2
s VirE2 fehrjk tovbbra is kapcsoldnak a DNS-hez: ezek a nvny sejtmagjba irnytjk a DNS-
darabot, s lehetv teszik az integrcijt (a VirD2 a gazda DNS-javtsba is beleszl). Ez jrszt vletlen
rekombinci rvn megy vgbe. A bal szl s jobb szl kz (az gynevezett T-DNS rgiba) beptett
gnek gy a gazdanvny kromoszomlis DNS-be integrldnak (ld. 14.6. bra).
14.6. bra: Ti plazmid trkpe. A T-DNS rgi helyettesthet az inszerttel.
Az tviteli mechanizmus azonos a nopalin s oktopin tpus Ti plazmidoknl, amelyek egybknt sokban
klnbznek egymstl, de mindkettt lehet gnbevitelre hasznlni. Br a Ti plazmid tl nagy a kzvetlen
klnozshoz, az e clra tenysztett Agrobacterium trzsek plazmidjait manipullhatjuk tbbfle mdon is:
bakterilis homolg rekombincival (pop-in) be lehet vinni a kvnt gneket a "lefegyverzett" (disarmed)
Ti plazmid T-DNS rgijba egy kisebb kztes vektorbl is, amit E. coli-ban szaportunk. De e helyett ma
mr inkbb dupla vektorrendszert (binary vector) hasznlunk: ilyenkor az Agrobacterium trzs az eredeti Ti
plazmid egy kis darabjt tartalmazza, amely szinte csak a Vir operonbl ll (helper plazmid). Az RB s LB
vgeket csak a msik plazmidba ptjk be, ami a clgnt is tartalmazza, s E. coli-bl preparlhat (ld.
14.7. bra) Ezt a plazmidot Agrobacterium-ba transzformlva, a baktriumokat antibiotikummal
206
szelektlva, majd a nvnyi sejttenyszeteket fertzve nagy hatkonysg gnbevitel rhet el. A
megtmadott sejteket tartalmaz kalluszokbl pedig transzformlt embrik nyerhetek.
14.7. bra: Az Agrobacterium ketts vektorrendszere
A fejld virgok fertzsvel a csrasejtek direkt mdostsa is megvalsthat ("virgbemrts", floral dip
mdszer). A legutbbi idkben sikerlt olyan Agrobacterium trzseket ltrehozni, amelyek egyszik
nvnyeket (pl. gabonkat) is kpesek fertzni. Br a rendszer nmagban clzs nlkl mkdik, ez nem
jelenti azt, hogy nem lehet homolg rekombincira is hasznlni. Megfelel pozitv-negatv szelekcis
konstrukcikkal elfogadhat hatkonyg (>0,1%) homolg rekombinci s clzott gnmdosts rhet el.
Mindezt azonban a jelenlegi nvnyi gntechnolgia alig-alig hasznlja ki: a mezgazdasgi biotechnolgia
legtbb mai cljra a clzs nlkli gnbevitel is ltalban megfelel.
14.5. Knock-out s knock-in technikk
A clzott gnmdost eljrsok egyik els clja (s ma is az egyik f felhasznlsa) a gnjeikben elrontott,
null mutns (KO: knock-out) llnyek ellltsa volt. Ezen mutnsok tanulmnyozsa sokat segti a
molekulris biolgiai folyamatok megrtst. Tovbb a genetikailag mdostott emlsllatok szmos
genetikai eredet emberi betegsg modelljl szolglhatnak.
14.5.1. Homing endonuklezok. Cre/Lox s Flp/Frt rendszerek
A modern gnkitsi technikk specilis endonuklezok hasznlatn alapulnak. Jllehet egyszer
funkcivesztses mutnst ltre lehet hozni csupn homolg rekombincival is, a rezisztencia-gn jelenlte
az eukarita genomban nem kvnatos jelensgeket eredmnyezhet (a kromatin mdostsa miatt
befolysolja a krnyez gnek expresszijt). gy mindenkpp szksg van olyan enzimekre, amelyek in
vivo is kpesek a bakterilis restrikcis enzimeknl jval nagyobb clzsi pontossggal specifikus
mdon szabni-varrni a clszervezet genomilis DNS-st. Az ilyen tulajdonsgokkal rendelkez,
termszetben is megtallhat enzimeket hvjuk homing endonuklezoknak. Ellenttben a bakterilis
restrikcis enzimekkel, ezek hossz (14-44 nukleotidos) DNS-szakaszokat ismernek fel, s nagyon
specifikus folyamatokban jtszanak szerepet. J nhnyuk "nz" genetikai elemek: vrusok s
transzpozonok rszt kpzi. Ilyen pldul a Chlamydomonas zldalga I-CreI enzime (nem keverend ssze
207
a Cre-rekombinzzal): ez abbl az intronikus szekvencibl rdik t, amely a sajt aktivitsa kvetkeztben
tud integrldni a genomba (transzpozon-szeren). A homing endonuklezoknak szmos csaldja ltezik, a
mindennapi gyakorlatban kt ilyen fehrjt hasznlunk a clzott gnmdostsokhoz: a Cre-rekombinzt (ld.
14.8. bra) s az Flp ("flippz") enzimet.
14.8. bra: A Cre-rekombinz katalitikus ciklusa
A Cre-rekombinz eredetileg a P1 bakteriofgbl ered, szerkezetileg hasonl a -fg integrz enzimhez. A
felismer helynek kln neve van: LoxP (locus of crossover-P1). Ez a kt szln palindrom, kzpen
viszont aszimmetrikus nukleotid szekvencit jelent (ATAACTTCGTATA-GCATACAT-
TATACGAAGTTAT), ezrt a LoxP helyek nem szimmetrikusak, irnyultsguk van. A hasts a nem
palindrom szakaszon bell fog bekvetkezni. A Cre-enzim azonban nem csak endonuklez aktivitssal
rendelkezik, hanem (a tetramerizci rvn, sajt DNS-ligz aktivitsa rvn) elsegti a szabadd vlt
vgek egyeslst is (site-specific recombination). Ez ltal a kt (megfelelen irnytott) LoxP hely kztti
DNS-darab a Cre-enzim hatsra kivgdik s cirkularizldik. A kivgott darab az osztdsok sorn
ltalban elvsz, delcit hozva lre. A reakci "keresztben" is vgbemehet: kt kromoszma karjait pldul
fel lehet cserlni, ha mindkett tartalmaz egy-egy LoxP helyet (transzlokci). Az egy kromoszmn belli
kt fordtott LoxP hely rekombinlsa pedig inverzihoz vezethet. Ily mdon a Cre gnt hordoz plazmid
tmeneti bevitele egy sejtbe vagy sejtvonalba (tranziens transzfekci) permanens genetikai vltozsokat
tud okozni a szervezet genomjban, radsul clzottan, a LoxP helyek pozcijtl fggen. Ezen helyek
gyes beptsvel teht kpesek vagyunk ksleltetett in vivo rekombincis folyamatokat vezrelni.
Egyszer ksrletekhez egy rekombincis rendszer is elegend, de az sszetettebbekhez (mint a feltteles
gnkits) tbb, fggetlen enzimrendszerre van szksg. A msik gyakran hasznlt rendszer az Flp
("flippz") enzimen alapszik. Ez a srlesztbl izollt enzim felels a Saccharomyces trzsek plazmid
szer trpe DNS-gyrinek (2-mikron plazmid, ld. 13.1.6. fejezet) fenntartsrt. A felismer helyeinek
neve Frt (Flp recognition target), ez a LoxP helyekhez hasonlan kzpen nem szimmetrikus, a kt szln
viszont majdnem vagy teljesen palindrom (GAAGTTCCTATTC-TCTAGAAA-GTATAGGAACTTC). Az
Flp-enzim is dimerizldik a cl DNS-en, s kzpen, a nem szimmetrikus szekvencinl hast. A Cre-
rekombinzhoz hasonlan, a kzps szakaszra igazbl csak a rekombincihoz van szksg, az
208
endonuklez aktivitshoz nem kell. gy ezen szekvencia megvltoztatsval lehetsg van egy-egy
rendszerbl nmagban is tbb, keresztben nem kompatibilis felismer helyet ltrehozni (hasonlan a
Gateway vektorok AttR s AttL helyeihez). Ezeket a mestersgesen ltrehozott, tervezett rekombincis
helyeket az eredeti neve mg (mnusz egy betvel) tett szmozssal szoktk jellni. gy pldul egy Fr3
hely csak egy msik Fr3 hellyel tud rekombinldni (egy Fr5 hellyel nem), de ugyangy az Flp-enzim
irnytja a folyamatot, mint az eredeti Frt helyen. gy egy enzim (tmeneti) expresszijval potencilisan
tbb, jl irnytott rekombincis esemnyt is tudunk vezrelni. A mdszer egyetlen korltozsa a felismer
helyekben rejlik: ezeket a helyeket elbb be kell ptennk a genomba (megfelel targeting vektorral), hogy
kpesek legynk a clzott gnmdostsra. Ezrt az utbbi idben komoly erfeszts trtnt tervezetten
talaktott homing endonuklezok ltrehozsra (pl. I-CreI mutnsok), amelyekkel a genomilis szekvencik
sokkal nagyobb trhza clozhat meg; akr termszetes genomilis szakaszok is clba vehetek. A homing
endonuklezokkal kivlthat mutcik smjt a 14.9. bra foglalja ssze.
14.9. bra: Kromoszomlis mutcik kivltsa homing endonuklezokkal
14.5.2. Clszekvencira tervezett hast enzimek. Cink-ujjas s TALE-
nuklezok
A kromoszomlis DNS clzott tszabsa irnti nagy igny egszen jszer mdszerek kifejlesztshez
vezetett. A 2010-es vekben jelentek meg elszr olyan technolgik, amelyekkel md van lnyegben
tetszleges genomilis rgi hastsra illetve rekombinlsra. Erre a homing endonuklezok ltalban
nem alkalmasak, hiszen a fehrje szubsztrtfelismer s katalitikus rgija egymstl nem vlaszthat el. E
helyett olyan mestersges enzimeket kellett tervezni, amelyek egy DNS-felismer elem s egy laza
specificits endonuklez katalitikus domn fzijval hozhatak ltre (modulris felpts). Jelenleg kt
ilyen megkzelts ltezik, amelyet a gyakorlatban is hasznlnak: az egyik kzlk az gynevezett
cinkujjas nuklezokon (ZFN: Zinc finger nucleases) alapszik (ld. 14.10. bra). A termszetes cinkujjas
transzkripcis faktorok a DNS-hez jl meghatrozott szekvencia-specificitssal ktnek, mghozz
leggyakrabban hrom cinkujjal. A cinkujjak irnytott mutciival ez a specificits megvltoztathat, gy a
fehrjk nagyon sokfle clszekvencihoz hozzidomthatak. Hosszabb "cinkujj-fzrekkel" mg nagyobb
specificits hozhat ltre: akr a genom egyedi szakasza is clba vehet. Ilyenkor a megfelel nuklezzal
(pl. FokI) kpzett fzis fehrje clzottan el tudja vgni a kromoszomlis DNS-t a felismer hely kzelben.
A ZFN technolgia teht szksgtelenn teszi a mdost helyek beptst: a vad tpus genomokban is
209
mkdik. A mestersges nuklezok tmeneti bevitele (pl. plazmiddal) nmagban is rekombincikat okoz:
tartsabb expresszi esetn a nagyszm hasts-javts ciklussal jr hibkkal knny clzott
pontmutcikat vagy delcikat ltrehozni. Tbb, klnbz clszekvencira tervezett nuklezzal pedig
komplex trendezseket lehet vgrehajtani a illet organizmus genomjban. A mdszer kombincija a
targeting vektorokkal (miszerint clzott kettstrst okozunk a kiszemelt gnben, amihez a bejuttatott DNS
tkletesen passzol) nagysgrendekkel emeli a homolg rekombincis mdostsok hatkonysgt is.
14.10. bra: A cink-ujjas nuklezok felptse
A mdszer htultje, hogy itt minden egyes genomilis szakaszra kln tervezett enzimre van szksg.
Maguk a cinkujjas nuklezok is bizonyos szempontbl korltozottak, egyes DNS-szekvencikon nem elg
szelektv a mkdsk. Ez abbl a tnybl fakad, hogy a cink-ujjak a clszekvencit blokkokban ismerik fel,
nem pedig egyedi nukleotidonknt. Lteznek viszont olyan termszetes fehrjk, amelyek ezen a szinten is
tkletesen modulrisak. Az erre ptett technolgit hvjk TALE-nuklezoknak (TALEN: transcriptional
activator-like effector nucleases; ld. 14.11. bra). A fzis fehrje alapja itt egy, a parazita Xanthomonas
baktriumokbl izollt fehrjecsald. Ezeket a fehrjket a baktrium termeli, s juttatja be a gazdanvnybe
azrt, hogy ott bizonyos gneket clzottan aktivljanak. Innen kaptk a nevket. A szerkezetk ersen
repetitv: minden egyes rvid, 34 aminosavas szerkezeti blokk (repeat) egy-egy nukleotid ktsrt felels,
mgpedig nagy specificitssal. gy az ltalunk megtervezett repeat-sorrenddel az egsz TALE fehrje a
kvnt DNS-szekvencia "tkrkpe" szerint pthet fel (ltalban prban, hogy mind a kt DNS-szlat
elhastsuk). Mindezt nem-specifikus endonuklez domnekhez (FokI) kapcsolva egy j fajta mestersges
endonuklez lesz az eredmny. Az egyetlen nehzsg a gn mestersges ellltsval (gn-szintzissel) van:
ez ugyanis a repetitv DNS-szekvencik miatt nem a legegyszerbb feladat, de ltalban megoldhat.
14.11. bra: TALE-nuklezok s felismerhelyk
210
14.5.3. Gnkits (knock-out) s j gnek clzott beptse (knock-in)
Ahogy azt lttuk, a gnkitsi (knock-out) technikk ma mr tlmutatnak a genomilis szekvencik
egyszer elrontsn. A gn tnkrettele cljbl elegend csupn egyetlen exont valami egybbel, pl. a
rezisztencia-gn kazettjval kicserlni. A mdszer akkor biztos, ha frameshift-et (leolvassi keret
eltoldst) is okozunk az exon kiessvel. Ez az eljrs hatkony, de sokszor nmagban mg nem elegend.
14.12. bra: A gncsapdzs vzlata. Kombinlt knock-out s knock-in mdszerek
211
Felmerlhet az az igny, hogy a clszervezetben csak a kvnt mdostst hajtsuk vgre: ne hagyjunk
magunk utn sok "DNS-szemetet", pldul a rezisztencia-gneket. Erre a clra (amelyet nha a "delitto
perfetto" olaszul a "tkletes bntny" elvnek is neveznek) a rezisztencia-gnek kr ltalban egy Frt
vagy LoxP prt ptnk be. A megfelel stdiumban (pl. az embrionlis sejtek szelekcijnak megtrtnte
utn) a Cre vagy Flp gnt hordoz plazmid tmeneti bevitelvel a szelekcis gnt vagy gneket eltvoltjuk,
gy azok nem szlnak bele sem a splicing folyamatba, sem az organizmus fenotpusnak kialaktsba.
Ugyanez rhet el, ha a megfelel mutns egernket egy olyan trzsbli egrrel keresztezzk, amely mr a
korai embrionlis fejlds sorn is expresszlja a Cre- vagy Flp-enzimet (deleter strain).
Termszetesen vannak olyan helyzetek is, amikor kifejezetten szeretnnk beavatkozni az eredeti gn
mkdsbe: pldul ha j genetikai elemeket visznk be a kromoszomlis DNS-be (knock-in). Ez
kombinlhat a gnkitssel is: ha a targeting vektorunk nemcsak a rezisztencia gnt tartalmazza, hanem
eltte egy msik, riporter-gnt is, akkor az megfelel bepls esetn trhatv vlik. Ilyet eredmnyez, ha
a riporter-gnt gy alaktjuk ki, hogy kpes legyen splicing rvn fzis fehrjt alkotni az eredeti fehrje
elejvel ez a gncsapda (gene trapping) (ld. 14.12. bra). Ugyangy, a riporter (pl. GFP, bta-
galaktozidz) bepthet az els exon helyre is (promter trapping), st, ha van sajt promtere, akr az
eredeti promter helyre is (enhancer trapping). Ezek a konstrukcik nemcsak a clzs sikeressgrl adnak
egyrtelm visszajelzst, de mg az eredeti gn expresszis mintzatt is nyomon kvethetjk velk. Ha a
kt bevitt (csapda s rezisztencia) gn mrett szeretnnk minimalizlni, a msodik gn trsa sajt
promter nlkl is megoldhat, IRES elemekkel (bicisztronos eukarita konstrukci).
Amikor az egrtrzsnk genomjban egy adott helyen mr van egy alkalmas rekombincis helyeket (pl.
egy Frt/Fr3 prt) tartalmaz kazetta, ezt clzott gnbevitelre (knock-in) is felhasznlhatjuk. Ilyenkor a
meglv kazettt egy tranziensen bevitt plazmid j kazettjra lehet kicserlni (feltve hogy ugyanazokat a
rekombincis helyeket tartalmazza, azonos orientciban, mint a kromoszma). A Cre vagy Flt rekombinlt
embrionlis ssejtekbl pedig a szoksos mdon lehet kimrkat majd genetikailag tiszta egereket ltrehozni
(Recombinase-mediated cassette exchange).
14.5.4. Feltteles gnkits, gnjavts
A homing endonuklezok vezrlse lehetv teszi a rekombincis esemnyek id- s trbeli szablyozst
is. Ezt ki lehet hasznlni akkor, amikor csak a fejlds adott pontjn szeretnnk elrontani a megclzott gnt,
vagy esetleg szvetspecifikus genetikai mdostst akarunk vgrehajtani. Erre szolglnak a feltteles
gnkitsi ("conditional knock-out") technikk. Ilyenkor olyan organizmusokat (pl. egrtrzseket)
hasznlunk, amelyek genomjba a Cre- vagy Flp-rekombinzt elzleg induklhat promterrel ptettk
be. A gyakorlatban az egyik legnpszerbb a tetraciklin-induklhat rendszer - ilyenkor a Cre gn
promtert egy Tet-represszor ktse tartja kikapcsolva (aminek gnjt szintn beptettk a rekombinz
mellett). A rekombinci a tet rendszerben az egerek doxiciklinnel trtn etetse utn valsul csak meg.
Termszetesen a feltteles gnkits esetn gy kell megterveznnk a targeting vektort, hogy a gn a
rekombinci nlkl mg tkletesen mkdjn. Ezrt ilyenkor legalbb kt kazettt kell beptennk (kt
kln antibiotikum-rezisztencival), mghozz a megclzott exon(ok) kt oldalra. A kazettknak szigoran
az intronikus rgiba kell kerlnik, gy, hogy a splicing folyamatt ne zavarjk (150-200 nukleotidra az
exon-intron hatroktl). A rezisztencia-gnek kt oldalra egy-egy kompatibilis felismer hely-pr kerl: az
egyiket pl. Frt helyekkel, a msikat Fr3 helyekkel vesszk krl. Melljk pedig egy-egy LoxP helyet
tesznk. A hrmas (ktszeresen pozitv, egyszeresen negatv) szelekci megtrtnte utn a kt kazettt a
tranziensen bevitt Flp-rekombinzzal eltvoltjuk: csak a LoxP helyek maradnak meg srtetlenl a
genomban.
Az ilyen genotpus egr ltalban megklnbztethetetlen lesz az eredetitl: egsz addig, amg a Cre-Tet
trzzsel nem keresztezzk, s az utdokat elkezdjk doxiciklinnel kezelni. Ekkor meg fog trtnni a
rekombinci, s a kiszemelt gn mkdskptelenn vlik. Ez klnsen akkor hasznos technika, ha tudjuk
hogy az illet gn az embrionlis fejldsben ms szerepet tlt be, mint felnttben (korai kitse esetleg
letlis). A Cre-Tet rendszer azonban csak egy a sok lehetsges vltozat kzl: lehetsg van sejttpus
212
specifikus rekombinz promterek ellltsra is: ezek csak az adott, differencilt sejttpusban fogjk
vgrehajtani a rekombincit. Mg arra is van md, hogy a gnkits ellenttt vgrehajtsuk, s szablyozott
mdon megjavtsuk a krdses gnt. Ez gy lehetsges, hogy az elzleg az intronba bevitt, a gnt elront
(pl. STOP kodont tartalmaz vagy egyb mdon gn-csapdz) kazettt a rekombinzzal utlag kivgjuk,
gyakorlatilag tkletesen helyrelltva az eredeti viszonyokat. A feltteles gnkits smjt, sszevetve az
egyszer gnkitssel, a 14.13. bran szemlltetjk.
14.13. bra: Cre/Lox s Flt/Frt rekombinz-rendszerek hasznlata gnkitses llnyek ellltsra
14.5.5. Genetikai elemek beptse transzpozonok segtsgvel
14.5.5.1. A transzpozonok molekulris biolgija
Gnek tbb-kevsb clzott bevitelre vagy mdostsra nemcsak a homolg rekombincit vagy a
homing endonuklezokat lehet hasznlni. Erre a clra az olyan termszetes genetikai parazitk, mint a
vrusok s transzpozonok is sokszor megfelelnek. A mobilis genetikai elemeknek nevezett
transzpozonoknak szmos fajtja ltezik: a "szaporodsi" (transzpozcis) mechanizmusuk alapjn kt f
tpus klnthet el: az letciklusuk sorn RNS-re kird majd DNS-re visszamsold
retrotranszpozonok (I. tpus), valamint a DNS-darabok kivgsval s tvitelvel operl DNS-
transzpozonok (II. tpus). A tovbbi, ritka s komplex tpusok trgyalstl (III - "politronok", IV -
"helitronok") itt most eltekintnk. A transzpozonok fontosabb tpusait a 14.14. bra mutatja be:
A retrotranszpozonok viszonylag komplexebb genetikai felptssel rendelkeznek, s minden esetben
msols-beilleszts (copy-paste) mdszerrel mozognak a genomban. Egy rszk esetben (LTR: Long
terminal repeat, retrotranszpozonok) az mRNS visszarsa DNS-re, majd annak integrcija a gazda-
213
genomba (a transzpozon-DNS kt vgn tallhat LTR szekvencikat felismer integrzok ltal) nagyon
hasonlt a vrusokra. A hatr a retrovrusok fel semmikppen sem les: klnsen, mivel egyes
retrotranszpozonok genomja burokfehrjket is kdol. Ms rszk esetben (non-LTR retrotranszpozonok) a
reverz transzkripci s az integrci egyszerre kvetkezik be: Ilyen pldul az emberi genomban is
megtallhat LINE1 retrotranszpozon. A LINE1 eredeti (aktv) formja sszesen kt gnt tartalmaz. Az
egyikk fehrje-termke a transzpozon RNS-hez ktdik, s annak a magba trtn visszaszlltst
irnytja. A msik fehrje pedig egyszerre rendelkezik DNS-endonuklez s RNS-fgg DNS-polimerz
aktvitssal. gy a gazda DNS adott helyen trtn hastsa utn kpes azt a fehrjhez kapcsold RNS-
szlrl kiegszteni, bemsolva a transzpozont a kpzett rsbe.
14.14. bra: A gntechnolgiban alkalmazott transzpozonok legfontosabb tpusai
A DNS-transzpozonok szaporodsi ciklusa ennl is egyszerbb. Ezek mindig a kivgs-beilleszts
mdszerrel mozognak. Ilyenkor a transzpozon ltal kdolt egyetlenegy fehrje homing endonuklez
aktivitsnak ksznheten kpes felismerni s kivgni a transzpozon kt, specilis szekvencikkal (inverted
repeat) rendelkez vgt. Ezen enzimek a kivgott darab vgeihez kapcsoldva a gazda DNS-st is kpesek
bizonyos helyeken hastani (ilyenkor a specificitsuk jval kisebb, mint a transzpozon kivgsakor).
Radsul ligz aktivitssal is rendelkeznek, gy a transzpozon s a gazda genom trvgeit mindkt oldalon
214
egyesteni tudjk, legalbbis az egyik szlon. A msik szlat a gazda sajt javt rendszere fogja kiptolni s
bezrni, gyakran megkettzve ezzel a transzpozon felismer helyt (ld. 14.15. bra).
14.15. bra: DNS-transzpozonok szaporodsi ciklusa
14.5.5.2. Genetikai mdosts transzpozonokkal
A transzpozonok jl alkalmazhatak idegen genetikai elemek clszervezetbe trtn bevitelre is, ehhez
azonban a kvetkez nhny szempontot kell szem eltt tartanunk. Elszr is, a transzpozonok beplse
meglehetsen aspecifikus. A felismer szekvenciik mind az RNS, mind a DNS-alap transzpozonok
esetben ltalban rvidek, lehetv tve hogy a transzpozon potencilisan nagyszm helyre plhessen
be. gy br az integrci nem teljesen vletlenszer a bevitt konstrukci elre nehezen megjsolhat
hely(ek)re fog beplni. Msrszt, a transzpozcis aktivitst valahogyan irnytani kell. Az endogn
transzpozonok aktivitsa ltalban alacsony - mivel msklnben a gazdaszervezetet veszlyeztetnk - s
sok a csonkoldott vagy mskppen inaktivldott kpia a genomban. A gyakorlatban ezrt inkbb olyan
transzpozonokat hasznlunk, amelyek nincsenek jelen a clszervezetben: ilyenkor md van a transzpozz
aktivits mestersges megnvelsre, irnytott mutcik rvn. A vektorunk csak a transzpozcihoz
szksges felismer vgeket tartalmazza (nem nll transzpozon). Az enzim(ek)et kdol (helper)
plazmidot kln juttatjuk be a sejtbe, hogy csak tmenetileg legyenek jelen. Petesejtek genetikai mdostsa
esetn md van a transzpozz mRNS-nek mikroinjekcijra is. A transzpozon csak addig mozoghat, amg
az t mozgat fehrjk jelen vannak, utna stabilan rgzl a genomban ezzel elkerlhetek a ksbbi, nem
kvnatos rekombincik. De az elem irnytott mdon brmikor jra mobilizlhat, a megfelel,
transzpozzt kdol plazmid tmeneti bejuttatsval
14.5.5.3. Transzpozonok gntechnolgiai alkalmazsai
j genetikai elemek beptsre retrotranszpozonok is hasznlhatak: ilyen pldul a nvnyi
gntechnolgiban alkalmazott Tnt1 (LTR tpus) transzpozon, amely a dohnybl (Nicotiana tabacum)
ered, s tbb, magasabb rend nvny genomi mdostsra alkalmas. A vletlen beplse sorn okozott
mutcikkal (inszercis mutagenezis) pldul feltrkpezhet szmos gn mkdse. De a DNS-
transzpozonok egyszersgknek ksznheten nagyobb npszersgnek rvendenek. Ilyenek pldul a
Tol2, a PiggyBac s a Sleeping Beauty elemek.
215
A Tol2 transzpozon, amely a japn rizshalbl (Oryzas latipes) szrmazik, nem rendelkezik semmifle
szekvencia-preferencival, ami a beplst illeti. Viszont elszeretettel integrldik gerincesek mkd
gnjeinek kzelbe vagy belsejbe, ezrt jl alkalmazhat funkcivesztses mutnsok ltrehozsra
(gncsapdz mdszerekkel). A petbe injektlt, riporter konstrukcit (pl. GFP-t) tartalmaz plazmid s
Tol2 mRNS segtsgvel gnkittt llatok llthatak el: st, mg az eredeti gn expresszis mintzata is
kvethet. Az eltallt gn azonban sokszor csak szekvenls segtsgvel azonosthat.
A Drosophilban mr rgta ismert P-elem hasonlkppen hasznlhat rovar genomok mutagenezisre,
genetikai trkpezsre (inszercis mutagenezis, enhancer trapping mdszerekkel). A Sleeping Beauty
("Csipkerzsika") transzpozon viszont egy teljesen mestersgesen ltrehozott rendszer. Lazacflk
genomjban tallhat, fosszilis Tcl1/mariner tpus genetikai elemek (kihalt, egykori transzpozonok) alapjn
lett rekonstrulva, majd vatos mutcikkal nagy aktivitsra nvelve. Jl hasznlhat klnfle gerinces
genomokba trtn (jrszt clzs nlkli) gnbevitelre, gy a gnterpis prblkozsokban is egyre
gyakrabban alkalmazzk. Induklt ssejtek ltrehozsra is hasznlhat. Rvid clszekvencija (TA
dinukleotid) miatt szinte brhol beplhet a genomba, de a Tol2-tl eltren csak ritkn kerl be mkd
gnekbe. A PiggyBac transzpozon eredetileg molylepkkbl ered, de a legtbb llati genom mdostsra
alkalmas. A felismer helye (TTAA) rvid, de az integrci mindig precz (nincs clhely-duplikci),
ellenttben a legtbb egyb transzpozonnal. Ezrt a PiggyBac rendszerrel beptett elem nyom nlkl
vgdik ki a genombl a transzpozz hatsra: gy felhasznlhat reverzibilis gnmdostsra is. Htrnya
viszont, hogy a PiggyBac rendszer szintn hajlamos a mkd gnek kzelbe beplni. Hogy az ltalunk
bevitt s az endogn gnek interakciit minimalizljuk (ha ezt szeretnnk elkerlni), a gnbevitelre sznt
transzpozon vektorokat jabban inzultor elemekkel is elltjk. Az inzultorok gtat vetnek a kromatin
mdostsnak, gy az egymshoz tl kzel es promterek nem fogjk zavarni egymst (ld. 14.16. bra).
14.16. bra: Plda a transzpozon alap vektorokra: j gnek bevitelre sznt PiggyBac vektorrendszer
14.6. Gncsendests (knock-down) RNS interferencival
Br a gnkits hatkony mdszer egy-egy gn mkdsnek befolysolsra, ma mr ennl finomabb
mdszerek is lteznek, amelyek radsul kevsb munkaignyesek. Ezek ltalban nem genomilis, DNS-
szint mdostsokat, hanem az RNS szintjn trtn beavatkozst jelentik. A mdszereket sszefoglal
216
nevkn RNS interferencinak (RNAi) nevezik. Itt egy termszetes jelensget hasznlunk ki. Mr tbb
vtizede ismert, hogy egy-egy fehrjekdol gnt RNS-szinten ki lehet kapcsolni, ha a megfelel RNS szl
komplementert (antiszensz oligonukleotidot) bevisszk a sejtbe. Rvid, ketts szl RNS-darabok
(siRNS: short interfering RNA) segtsgvel mg nagyobb hats rhet el. A pontos mechanizmusok
feltrsa ma mr lehetv teszi a clzott gncsendestst (knock-down) is. A legtbb sejt szmra a stabil
ktszl RNS teljesen idegen molekula: az ket megfertz vrusokban, illetve azok letciklusa sorn
viszont gyakran elfordul. A ktszl RNS-sek lebontsra eukaritkban ezrt egy specilis rendszer
szolgl. Ez alkalmasint lebontja a szervezeten bell keletkez ktszl RNS-seket is. Az egyes RNS-sekben
tallhat hossz (20-30 nukleotidos) hajtkanyarok (stem-loop structures) hurkon belli hastsval
normlisan is keletkezhetnek ketts szl RNS-sek (miRNS: micro-RNA), amelyeknek a termszetes
gnexpresszis szablyozsban van szerepk. A szervezetben a ktszl RNS-sek feldaraboldnak, s a
keletkezett egyszl darabkk (katalitikus mdon) segtik a velk komplementer mRNS-sek hastst, vagy
a transzlci gtlst.
Nvnyek rendelkeznek olyan RNS-fgg RNS-polimerzokkal is, amelyek kpesek a hastott darabkkat
kiegszteni. gy a felismer templt szaporodhat, s a plazmodezmkon keresztl az egsz szervezetben
sztterjedhet, szisztms RNAi vlaszt hozva ltre. Szisztms RNS-interferencia megvalsulhat a
Caenorhabditis elegans nev fonlfregnl is. Mivel rendelkezik a hossz, ketts szl RNS-sek (>400
bzispr) felvtelre szolgl receptorokkal s a szlltsukhoz szksges fehrjkkel, az RNAi vlasz az
llat ketts szl RNS-sel val etetsvel is kivlthat. Gerincesekben azonban nincs ehhez hasonl
szisztms RNS interferencia: a ktszl RNS hatsa az egyes sejtekre korltozdik. Emls sejtekbe
termszetesen nem juttathatunk be hossz antiszensz nukleotidokat kvetkezmnyek nlkl: a 25-30
nukleotidnl hosszabb ktszl RNS-sek ugyanis a termszetes immunits antivirlis rendszert is
aktivljk, s a transzlci teljes blokdjhoz vezetnek. Ezrt a mikro-RNS-eknek megfelel, rvid
nukleotidokkal kell a gncsendestst vgrehajtani.
A megfelel RNS-sek bejuttatsra tbb md van: transzformlhatunk olyan plazmiddal, amibe ers
promter (pl. U6 splicing alegysg snRNS) mg ptjk be a hajtkanyar-kpz szekvencit. A kzps,
hurok rgi mindig azonos maradhat: az nmagval prosod szr szekvencijt kell a cl RNS-hez szabni.
Br az ilyen konstrukcik szekvenlsa gyakran problms (a hurok a DNS-ben is megjelenhet a PCR
kzben s elakad rajta a DNS-polimerz), ezeket a rvid hajt RNS-seket (shRNS: short hairpin RNA)
kdol plazmidokat szles krben alkalmazzk gncsendestsre (gene silencing). A kis hajtkanyart
tbbsejt llatokban a Drosha s Pasha endonuklezok ismerik fel, s vgjk ki a krnyez, hosszabb RNS-
szakaszbl, akrcsak a termszetes miRNS gnek esetn. Ezutn a Dicer endonuklez lehastja a hurkot, gy
az siRNS valdi dimerr vlik. A mretre vgott (nagyjbl 21 nukleotid hossz) siRNS-darabka vgl a
RISC komplexbe (RNA induced silencing complex) kerl. A komplex magjt alkot Argonaute
endonuklez a kt siRNS szl egyikt (guide strand) stabilan megkti, a msik szlat (passanger strand)
pedig kiveti. A komplex ezutn a megkttt siRNS-szllal prosthat, hosszabb, egyszl RNS
molekulkat keres. Tkletes komplementarits esetn az Argonaute endonuklez az mRNS szlat kzpen
elhastja. Ezzel megakadlyozza a transzlcit, s tovbbi, sejten belli ribonuklezok szubsztrtjv
teszi, amelyek elbb-utbb teljesen lebontjk a hastott mRNS-t. Abban az esetben, ha a vezet siRNS szl
s az mRNS kztti bzisprosods nem tkletes (a kt szl a kzepn nem teljesen komplementer) vagy
inaktv fehrjket tartalmaz komplexrl van sz (az emls Argonaute fehrjk kzl pldul egyedl az
Ago2-nek van mrhet enzimaktivitsa), a hasts nem megy vgbe. A transzlci azonban ilyenkor is
gtlst szenved. Az siRNS-sek szmos eukarita llnyben szablyozzk a transzkripcit (RITS komplex),
a transzpozonok expresszijt (PIWI-kt RNS-sek, piRNA), st a kromatin mdostst is. Ezen
folyamatok molekulris szint rszleteit azonban ma mg csak kevss ismerjk.
Az RNS-interferencira egy msik lehetsg, hogy szintetikusan ellltott siRNS-eket jutattunk a sejtekbe.
A tervezskor csak arra kell gyelni, hogy az oligonukleotid valban egyedi legyen (a teljes transzkriptom
ellenrzsvel). Gyakorlatilag a clgn brmelyik szakaszt megclozhatjuk (nem csak a kdol szakaszt,
hanem az 5'- vagy 3'-UTR vgeket is). Erre automata tervezprogramok is rendelkezsre llnak. Br
optimlis gncsendests nha elrhet akr egyetlen fajta ktszl RNS-darab bejuttatsval is, ltalban
217
rdemes legalbb 3-4 klnfle szekvencit kiprblni, hogy a "szerencse kisasszonyt" kiiktassuk a
ksrletbl. A gncsendests smjt a 14.17. bran mutatjuk be.
A gncsendests a gygyszeripar rszrl is hatalmas rdekldsre tart szmot: a cl az RNS interferencia
alap terpik megvalstsa. Ilyenkor nem termszetes nukleotidokat, hanem pldul foszfotiot ktst
tartalmaz (ltalban egyszl) nukleotid analgokat hasznlnak, amelyek ellenllak a ribonuklezokkal
szemben. Br a az egyszl RNS-sekkel nehezebb a RISC komplexet megclozni (mivel az Argonaute
fehrje ktshez elbb 5' pozciban foszforilldnia kell a nukleotid analgnak), ma mr tbb antiszensz
RNS-szrmazkokat hasznlnak sikerrel klnfle betegsgek kezelsre. Ilyen pldul a rgta
forgalmazott fomiversen (a citomegalovrus IE2 gnje ellen, antivirlis szerknt) vagy a mipomersen
(apolipoprotein-B ellen, hiperlipidmia kezelsre). Az RNAi alap terpik fejlesztse azonban nem
knny feladat, mivel a megfelel nukleotid-analgok gyakran instabilak, tovbb hajlamosak gyulladst s
egyb nem kvnatos (off-target) vlaszokat okozni. De az j RNS-analg gygyszerek ellltsnak
legnagyobb nehzsge, hogy a testi sejtekbe egyelre nem tudjuk igazn hatkonyan bejuttatni a megfelel
nukleotid-analgokat.
14.17. bra: A gncsendests sejttenyszetben, RNS interferencia alap mdszerekkel
14.7. Stabil episzomlis rendszerek
Jegyzetnkben eddig csak stabil genetikai elemekrl beszltnk, s csak a szervezet sajt kromoszmirl
esett sz. Mita azonban tudjuk hogy mi kell egy kromoszma fenntartshoz, ltre tudunk hozni
mestersges kromoszmkat is. A plazmidokkal ellenttben, amelyeknek nincsenek rktst segt elemei
(centromri), de legtbbszr mg eukarita replikcis origi sem, a mestersges kromoszmk
genetikailag stabilnak tekinthetk. leszt esetn a technolgit mr rgta hasznljk (YAC), de ma mr
lteznek mestersges emls, st akr humn kromoszmk is (HAC). Ez lehetv teszi nagymret gnek
sejtekbe trtn stabil bevitelt, genomilis integrci nlkl. A technolgia egyelre mg retlen, de a
mdszer megoldst knlhat sok, reverzibilis gnmdostst kvn feladatra is. Pldnak emltjk az
induklt ssejtek ellltst. Ezek ellltshoz a ma ltez sszes protokoll megkveteli hrom vagy
ngy gn bevitelt a pluripotencia induklsra (pl. Sox2, Klf4, Oct-4 s Myc). Ha viszont ezek az rett
218
szvetben tovbbra is expresszldnak, problmkat okozhatnak (pl. a Myc gn magas aktivitsa
daganatokra hajlamost). Megoldst knlhat, ha ezeket a gneket egy kln mestersges kromoszmn
visszk be, ahol a gnek aktivitst knnyen szablyozhatjuk, akr blokkban is. De ha ez a minikromoszma
szelektven eltvolthat (erre egyelre csak a konvencionlis negatv szelekcis technikk, pl
TK/ganciklovir mdszer llnak rendelkezsre), akkor megvalsthat az ssejtekk programozs brmilyen
genetikai elem tarts beptse nlkl, genetikailag tiszta rendszerben, stabil episzomlis gnek rvn.
14.8. Tovbbi olvasnival a fejezethez
Alexandra Joyner (1999) Gene targeting: A Practical Approach. 2nd edition. Oxford University Press,
ISBN: 978-0-199-63792-8
Recombineering 2012: http://redrecombineering.ncifcrf.gov/ (the Court lab official recombineering website)
Hafez, M, Hausner, G (2012) Homing endonucleases: DNA scissors on a mission. Genome 55(8): 553-69.
Zayed H, Izsvk Z, Walisko O, Ivics Z. (2004) Development of Hyperactive Sleeping Beauty Transposon
Vectors by Mutational Analysis. Molecular Therapy, 9: 292-304.
Hutvagner G & Simard MJ (2008) Argonaute proteins: key players in siRNA silencing. Nature Reviews,
Molecular and Cell Biology 9(1): 22-33.
219
15. Transzgenikus llnyek. Gnterpia
A genetikailag mdostott llnyek (GMO: Genetically Modified Organism) magukba foglaljk az sszes
olyan szervezetet, melyek genetikai anyagt mdostottk valamely gntechnolgiai mdszerrel. A
transzgenikus llny pedig egy olyan GMO, melybe egy msik szervezetbl izollt gnt juttatunk be,
amit eredetileg az nem tartalmazott. Az gy kvlrl bejuttatott, exogn eredet transzgn rkldik az
utdokban, ha az a csravonalba kerlt be. Transzgenikus llnyek ellltsa sokfle mdszerrel trtnhet,
amelyeket az elz fejezet (0. fejezet) rszletesen trgyalt.
Az idegen gn (transzgn) termkt a gazdaszervezet ugyangy termeli, ahogy a sajt fehrjit. Az
expresszi mrtke a gnnel egytt bevitt egyb DNS szakaszoktl fggen (promter rgi, 5 upstream
elemek, 3 UTR) vltozhat, illetve szvetspecifikussga is ettl fgg. Clunk A transzgn expresszlsa
mellett a gazdaszervezet gnexpresszis mintzatnak megvltoztatsa is cl lehet. Tgabb rtelemben
transzgnnek nevezhetnk minden olyan, nem felttlenl gnt kdol DNS szakaszt, vagy mestersgesen
ellltott gnt, melyeket olyan llnyekbe vagy vektorokba juttatunk be, ahol azeltt nem fordultak el.
Praktikussgi szempontbl elklntjk a genomilis transzgneket a cDNS transzgnektl, mely utbbiak
nem tartalmaznak intronokat s a gn krli szablyoz rgikat. A kifejezetten nagymret klnok
trolsra/manipullsra kifejlesztett BAC, YAC s kozmid knyvtrak (ld. 7. fejezet) ellltsval a
genomilis transzgnek szablyoz elemeivel egytt trtn klnozsa knnyen megvalsthat. A
transzgenikus llnyek ellltsa j tvlatokat nyitott a kutatsban, gygyszeriparban, mezgazdasgban
s szmos egyb ipargban.
A fejezeten bell elszr pldkon keresztl bemutatunk klnbz transzgenikus llnyeket (nvnyeket,
llatokat, mikrbkat) s a legfontosabb felhasznlsi terleteiket. Rviden kitrnk a GMO-kal kapcsolatos
tudomnyetikai s krnyezetbiztonsgi (biosafety) krdsekre.
15.1. A transzgenikus llnyek tpusai s felhasznlsuk
A transzgn gazda s a felhasznlsuk lehetsgei alapjn clszer kln trgyalni a transzgenikus
nvnyeket, llatokat s mikrobkat. A transzgenikus nvnyek f alkalmazsi terlete rtelemszeren a
mezgazdasg s lelmiszeripar, br megjegyzend, hogy ma mr gygyszerek ellltsra is be lehet ket
vonni. Transzgenikus baktriumokat hasznlnak gygyszerfehrjk ellltsra, a bioremediciban s a
krnyezeti biotechnolgia tbb ms terletn is. Rviden sszefoglaljuk a transzgenikus llatok szerept az
alapkutatsban, a gygyszeriparban s a gygyszatban is.
15.1.1. Transzgenikus mikrobk
A baktriumok voltak az els olyan szervezetek, melyek genetikai anyagt mdostottk laboratriumi
krlmnyek kztt. A transzgenikus mikrobk szerepe ma mr a bioremediciban nlklzhetetlen. A
higanyszennyezsek eltakartsban pldul egy olyan E. coli trzs bizonyult hatkonynak, ami egr
metallotionein (mt-1) s E. coli polifoszft-kinz (ppk) gneket tartalmaz dohny 16S riboszomlis RNS gn
konstitutv promtere mgtt. Ezek az enzimek higany rezisztencit s annak felhalmozdst eredmnyezik
a baktriumban. Egy msik alkalmazsban E. coli DH5 trzs liztumt hasznltk bioriporterknt arznt
tartalmaz vz kimutatsra. A baktrium plazmidja egy arzn-induklt promtert tartalmaz, amely mg a
luciferz enzim gnjt klnoztk be. Arzn jelenltben a luciferz szubsztrtja jratermeldik. A
baktriumkultrbl szuszpenzit ksztettek, amit csvekben liofilizltak. A teszt kit egy-egy csvhez
vizet adva luminomterrel detektltk a minta lumineszcencijnak, gy arzntartalmnak a mrtkt.
220
15.1. bra: Humn inzulin termelse E. coli baktriumban. (A) Baktriumbl izollt plazmidot s a humn inzulin
gnjt (izollt vagy szintetikus) ugyanazokkal a restrikcis enzimekkel hastjuk, majd a ragads vgeikkel a humn
inzulin gnjt a plazmidba ligljuk. Szelekci utn a plazmidot a megfelel E. coli trzsekbe transzformljk, ahol
folyamatos a -galaktozidz promtere utni proinzulin transzkripcija s transzlcija. Klnbz tiszttsi lpsek
utn trtnik a C-peptid tripszines hastsa, ami az inzulin vgleges formjt eredmnyezi. (B) Az inzulin tiszttshoz
hasznlt HPLC oszlop. (C) Az inzulin termels folyamata. (a mdostott bra forrsa: Walsh, Gary. "Therapeutic
insulins and their large-scale manufacture." Applied microbiology and biotechnology 67.2 (2005): 151-159.)
A gygyszatban is alkalmaznak transzgenikus mikrbkat, rekombinns fehrjk termelsre. Az inzulin
az egyik leggyakrabban hasznlt gygyszati cl fehrje, olcs s nagy mennyisg termelse rendkvl
fontos. Humn inzulint nagy mennyisgben elszr Escherichia coli trzsek felhasznlsval lltottak el
(a humulin fantzianev rekombinns inzulint a Genentech cg fejlesztette ki 1978-ban, gygyszerknt az
Ely Lilly kezdte forgalmazni 1982-ban). A humn inzulin A s B lnct kln trzs termelte szintetikus
nukleotid szekvencikrl, ezeket aztn kln tiszttottk, majd oxidatv krnyezetben egytt inkubltk, gy
a kt szl kztt kialakult kt diszulfid-hd ktssel jtt ltre az intakt inzulin. Az egyes inzulin lncokat egy
lac konstitutv promter mg klnoztk, a -galaktozidz gnjvel egytt. A pozitv klnokra kk-fehr
szelekcival s ampicillin antibiotikummal szelektltak. Transzlcit kveten a -galaktozidz C-
terminlishoz egy metioninnal kapcsolt inzulint cianogn-bromidos kezelssel szabadtottk fel, elhastva a
metionin utni peptid ktst. Egy msik mdszernl a humn proinzulin egyetlen szintetikus szlrl rdik
t, a polipeptidbl pedig tripszinnel hastjk ki a C-peptidet (ld. 15.1. bra). Rekombinns humn inzulin
termelsre lesztt (Saccharomyces cerevisiae) is hasznlnak. Helyspecifikus mutagenezissel mdostott
inzulin analgokkal mra mr szmos eltr hatidej s stabilits inzulin van forgalomban.
Genetikailag mdostott baktriumokkal vralvadsi faktorokat, s nvekedsi hormonokat is ellltanak
(ld. 15.1. tblzat). A baktriumok ltal termeltetett fehrjk jval biztonsgosabbak, mint a korbban
221
alkalmazott mdszer, amikor is kadaverekbl vontk ki a mg le nem bomlott fehrjket (pl.
hasnylmirigybl inzulint, mely egy cukorbeteget kt-hrom napig lt el). Egyrszt gy a szerben jelenlev
krokozk is tovbbjuthattak (AIDS, hepatitis-C, Creutzfeldt-Jakob szindrma), msrszt a megnvekedett
ignyeket ezekbl nem lehetett kielgteni.
Egyes orszgok katonai hadviselsnek rszt kpezi a mikrobilis biolgiai fegyverek ellltsa s
esetleges hasznlata. Ezeket a nemzetkzi szerzdsekben tiltott biofegyverek egy rszt transzgenikus
baktriumok formjban lltjk el.
15.1.2. Transzgenikus nvnyek
A mezgazdasgban termesztett transzgenikus nvnyek az egyik leggyakrabban emlegetett pldi a
genetikailag mdostott (GM) szervezeteknek. Az olyan gnmdostsok, melyek nagyobb termshozamot,
kevesebb rovarirtszer hasznlatt, nagyobb tprtk termst vagy betegsgeknek ellenllbb fajtt
eredmnyeznek, szmos elnyt jelentenek a mezgazdasgban. Nvnyek, melyek gyorsabban bernek,
tolerljk a klnbz talajszennyezseket, st, szrazsgot, fagyot vagy egyb szlssges idjrst olyan
vidken is meg tudnak lni, ahol eltte nem, illetve ahol eltte nvnytermesztsre nem volt lehetsg.
Fldnk egyre nvekv emberi populcijnak ezek a tulajdonsgok a jvben ltfontossgak lesznek.
Hagyomnyos nvnytermesztk kereszteztek elszr olyan nvnyeket, melyek termszetes szaporodssal
nem jhettek volna ltre. Ilyen volt az 1875-ben ellltott bza-rozs hibrid, a tritikl. Hamar rjttek, hogy
a hibrid tartalmazza mindkt faj hasznos tulajdonsgait, amire szelektlni lehetett. Az els genercis GM
nvnyeket mutcis szaportssal lltottk el, ahol a nvnyek sugrzsnak, illetve vegyszereknek voltak
kitve. Ilyen krlmnyekkel nveltk a mutcis rtjukat, s utdaik kzl vlogatni lehetett a klnbz,
stabilan megmarad s hasznos tulajdonsgokra. Ehhez a nem specifikus mdszerhez kpest a transzgnek
bevitele egy sokkal pontosabb s szablyozhatbb mdja a kvnt tulajdonsgok elrsnek.
15.1.2.1. Transzgenikus nvnyek ellltsa
Az els transzgenikus nvnyt 1983-ben lltottk el, amikor az aminoglikozid tpus antibiotikumok (pl.
kanamicin, neomicin, geneticin) rezisztencia gnjt petnia s dohny nvnyekbe juttattk be [1]. A kimra
gn a neomicin I-es vagy II-es tpus foszfotranszferz enzim gnjt illetve a nopalin-szintz gn szablyoz
rgiit tartalmazta (ld. 15.2. bra).
15.2. bra: Agrobacterium-kzvettett gntvitel. A transzgenikus nvnyek ellltsnak egyik tpusa az
Agrobacterium tumefaciens talajbaktriummal trtn fertzs, mely segtsgvel a nvnyi genomba bepl T-
DNS-rl trtnik a transzgn trsa. A mdszer jl alkalmazhat olyan nvnyeknl, amit az Agrobacterium
hatkonyan kpes fertzni (pl. dohny, paradicsom, burgonya). Szemlltet vide itt nzhet meg.
222
A neomicin-foszfotranszferz foszforilcival inaktivlja az aminoglikozid antibiotikumokat, mg a nopalin-
szintz konstitutv promtere biztostja az lland expresszit a nvnyi sejtekben. A kimra gnszakaszt
elszr egy kztes plazmidba klnoztk, amirl rekombincival kerlt be a transzgn egy tumort
indukl plazmidba (Ti plazmid), melyet Agrobacterium tumefaciens talajbaktriumba transzformltak
(ld. 14.4.4. fejezet). Ez a talajbaktrium a termszetben is sokfle Ti plazmidot tartalmaz. A baktriummal
fertzve a nvnyi sejteket, a Ti plazmidbl a nvnyi sejtek genomjba pl be egy DNS-darab (T-DNS),
mely tartalmazza a transzgnt is. A bepls clzottan trtnik, a T-DNS kt vgn lv ismtld
szekvencik segtsgvel. A megfelel plazmiddal transzformlt nvnyi sejtek antibiotikum jelenlte
mellett szelektlhatak.
Az olyan nvnyeknl, amik nem rzkenyek az Agrobacterium ltal kzvettett folyamatokra, gyakran
alkalmazott gnbeviteli mdszerek a gnpuska, a direkt gntvitel protoplasztokba (pl.
elektroporcival) s a mikroinjektlsos gnbevitel. A protoplaszt (izollt nvnyi sejt sejtfal nlkl)
transzformlsa nagyon hatkonyan mkdik brmely felsorolt fizikai folyamaton alapul technikval,
hiszen nem szksges biolgiai vektor a transzgn kzvettshez, gy elkerlhetek a nem-kompatibilis
gazda problmk. Homolg rekombincival pedig specifikusan pthet be a transzgn az ismert nvnyi
genomba. A protoplaszt transzformlsval az egyetlen problma, hogy a nvny regenercija
protoplasztbl egy rendkvl knyes folyamat, ami sok problmval jr. A gnpuska (ld. 15.3. bra)
szmos elnnyel rendelkezik (egyszer hasznlat, egy lvsbl sok transzformlt sejt, a legklnbzbb
szvetek/sejtek transzformlsa, stb.), s akkor is hasznosnak bizonyul, amikor ms mdszer nem mkdik
egy transzgenikus nvny ellltsnl.
15.3. bra: Nvnyek transzformlsa fizikai mdszerekkel. Protoplasztok, vagy sejtfallal rendelkez nvnyi
sejtek transzformlsra is alkalmas a gnpuska, vagy a mikroinjektor, ami a DNS-t nagy nyomssal juttatja t a
sejtfalon s a sejtmembrnon.
Az els transzgenikus szja ltrehozsnl a gnpuska sokkal sikeresebbnek bizonyult, mint az
Agrobacterium-kzvettett transzformls. A mdszer htrnya, hogy a DNS mennyisge nem
szablyozhat, illetve a transzformlt nvnyek kis szzelkban trtnik csupn genomilis integrci, a
citoszolikus plazmid-transzgnek pedig hossz tvon nem fenntarthatak..
223
15.1.2.2. Transzgenikus nvnyek a mezgazdasgban s az lelmiszeriparban
Transzgenikus nvnyek els szabadfldi termesztse Franciaorszgban s az Egyeslt llamokban 1986-
ban kezddtt, nvnyirtszerekre rezisztens dohnnyal. 1987-ben alaptottk az els cget, mely Bacillus
thuringiensis baktriumbl izollt, rovarra toxikus fehrjt termel transzgnt tartalmaz dohnynvnyt
lltott el (Bt dohny), szintn Agrobacterium-kzvettett technolgival. A dohnymoly lrvjt l hatst
elsknt Bacillus thuringiensis berliner baktriumban termeld endotoxin (bt2) gnjnek a bevitelvel
rtk el. A baktrium citoszolikus plazmidjbl izollt bt2 vagy cry gn (crystal protein) termke egy
protoxin, mely kristlyknt jut be a rovar emsztrendszerbe, itt oldatba kerl, majd protezok kihastjk
az aktv toxint belle. Ksbb ezen baktriumok plazmidjaibl tbbfle cry gnt izolltak, gy mra a
biolgiai rovarl szerek szles spektrumval rendelkeznk (pl. Lepidoptera, Diptera, Coleoptera vagy
Hymenoptera fajok ellen). A Bt nvnyek alkalmazhatsga megosztja a kutatkat. Mivel az ilyen
nvnyeket nemcsak a krokozk, hanem a kzelben l rovarpopulcik is elfogyaszthatjk, a toxin ezek
populciit is pusztthatja. Egyesek szerint a Bt kukorica (amelyet ma mr nagy terleten termesztenek)
pollenje ll kirlylepke populcik, illetve mh kolnik nagyfok pusztulsnak htterben, azonban
egyikre sincs egyrtelm bizonytk. Szmos kutats vizsglja a vad tpus s a Bt kukorica
gnllomnynak keveredst is, a transzgnek tjutst a vad tpusba. Aggodalomra adhat okot az is, hogy
egy Bt kukorica a nvnyvdszerekben megengedett maximum toxin mennyisg ezerszerest termelheti.
Az els GM termny az Egyeslt llamokban 1994-ben kerlt forgalomba, egy hosszabb eltarthatsgi
idej paradicsom formjban (FlavrSavr nven). A gnmdostott paradicsomot antiszensz RNS
technolgival lltottk el. A poligalakturonz enzim gnjt antiszensz RNS szllal csendestettk. A
poligalakturonz a paradicsom rsekor a sejtfalban lv pektint bontja le, gy a paradicsom rs kzben
puhul, amitl azonban srlkenyebb lesz, s jobban kitett a fertzseknek. Ezrt a hagyomnyos
paradicsomot retlenl szedik le, mivel addig szllthat, amg kemny s kevsb srlkeny. Ez a
gnmdostott paradicsom azonban nem hozta meg a vrt eredmnyeket. Eltarthatsga megnvekedett
ugyan, de retten mgsem volt elg kemny a szlltshoz, gy ugyangy zlden kellett leszedni, mint a
hagyomnyosat, ezrt vissza is vontk a forgalombl. Szintn egy plda a fogyaszti ignyek kielgtsre a
nem-barnul alma, mely jelenleg piacra kerls alatt ll Kanadban s az Egyeslt llamokban. Ez a
gnmdostott alma a barnulst okoz polifenol-oxidz enzimet csak kis mrtkben termeli.
Szmos egyb transzgenikus nvnyt hoztak forgalomba (paradicsom, krumpli, dohny, kukorica, bza,
szja, papaja, citrusflk, gyapot, repce), melyek ellenllnak a bromoxinil vagy glifozt tartalm
gyomirtknak, klnbz rovarirtknak, vrusrezisztensek vagy rovarl hatsuk van.
2000-ben lltottk el az els olyan transzgenikus nvnyt, az aranyrizst, melynek a tprtkt sikerlt
javtani [13]. Nevt srgs sznrl kapta, mely -karotin termelsnek ksznhet. A cl a fleg Afrikt,
Indit s zsia dli rszt rint A-vitamin hiny miatti nagyfok elhallozs (s vaksg) visszaszortsa
volt. Habr humanitrius clokat szolglt, erteljes negatv visszhangot vltott ki krnyezetvdk s anti-
globalizcis aktivistk krben, elssorban transzgenikus volta miatt. A -karotin ellltshoz, ami az A-
vitamin prekurzora, kt enzim hinyzik a rizs termsbl (azonban a leveleiben megvan, gy az termel is -
karotint): a fiton-szintz s a fiton-deszaturz (ld. 15.4. bra).
Az elbbi gnjt (psy) a Narcissus pseudonarcissus nvnybl, az utbbit (crtl) az Erwinia uredovora
talajbaktriumbl izolltk. A kt transzgnt egy plazmidba klnoztk, egy konstitutv, s a magban
expresszld glutein promter mg. A plazmidot higromicin antibiotikum rezisztencia markergnnel
trtn szelekci utn Agrobacteriumba transzformltk, gy juttattk a transzgneket rizs embrikba.
Kutatsok igazoltk, hogy az emberi szervezet kpes a rizzsel bevitt -karotinbl az A-vitamin hatkony
ellltsra. Pr vvel ksbb egy j fajtjt lltottk el, az aranyrizs 2-t, ami 23-szor annyi -karotint
termelt, mint eldje. Ebben a vltozatban az eredeti aranyrizs Narcissus psy gnjt a kukorica psy gnjre
cserltk, mely enzimaktivitsa jval hatkonyabbnak bizonyult. Mindezeket mg egy sor aranyrizs vltozat
kvette, melyek E vitamint, vas-, cink-iont tartalmaztak. Annak ellenre, hogy jelenlegi kutatsok szerint
nem okoz semmilyen allergit, nem hozhat kapcsolatba betegsgekkel, s egy bgre rizs fedezi a napi A-
vitamin szksglet 50%-t, mg nem engedlyezett a piacra kerlse. Egyes kutatk szerint azonban
224
agglyos, hogy nem teszteltk llatokon, gy nem jsolhat hossz tv hatsa a szervezet egszre, mivel a
-karotinbl (amit a rizs tltermel) szrmaz retinoidok bizonytottan krosak az egszsgre. -karotin
azonban termszetes A-vitamin forrsknt szmos ms lelmiszerben is van.
15.4. bra: Az aranyrizs ellltsa. A rizs endospermiumban a bta-karotin szintzis tvonala a geranil-geranil-
pirofoszftnl megll. A pirossal jellt kt enzim bevitele azonban biztostja a teljes bioszintetikus t lefolyst a -
karotinig. A transzgn konstrukci: RB (right border): T-DNS szekvencia; Glu: rizs endospermium specifikus glutein
promter; SSUcrtI: bors ribulz bisz-foszft-karboxilz kis alegysg tranzitpeptid, a kloroplasztiszban val
lokalizci biztostsra; nos: nopalin-szintz termintor; Psy: fiton-szintz; Ubi1: kukorica poliubiquitin promter;
hpt: szelekcis marker gn; LB (left border): T-DNS szekvencia. Az bra als rszn a vad tpus, az els s msodik
genercis aranyrizs fotja (az als brarsz forrsa: www.goldenrice.org/Content2-How/how1_sci.php)
15.1.2.3. Transzgenikus nvnyek a gygyszeriparban, vegyiparban, a krnyezeti
iparban
A transzgenikus nvnyek szerepe a gygyszerkutatsban is nvekv tendencit mutat. Gntechnolgiai
eszkzkkel olyan bannt lltottak el, melyben hepatitisz-B antignt lehet termelni, illetve olyan dohnyt,
mely monoklonlis ellenanyagot termel HIV ellen. Egyik termk sincs mg forgalomban, de a GMO
nvnyekben ellltott rekombinns fehrjegygyszereknek szerepe lehet a jv szemlyre szabott
gygyszatban.
225
Ezen kvl a szerves vegyipar is nagy potencilt lt a transzgenikus nvnyekben. Sok esetben hatkonyabb
a termels, illetve a nvnyek ltal ellltott anyagoknak kedvezbbek lehetnek a tulajdonsgai, mint a
kmiai szintzissel ellltottnak. Szmos laboratrium foglalkozik azzal, hogy nvnyekkel biopolimereket
termeltessen, amilyenek klnbz manyagok, a termszetes gumi vagy a poliaminok. Szintn hasznos
lehet a kmiai szintzisekhez szksges prekurzorok ellltsa nvnyekkel. A rostfehrjk (selyem,
kollagn, elasztin, keratin, glutenin vagy rezilin) repetitv DNS szakaszainak kombincijval, vagy akr
szintetikus szekvencikkal vgtelen sokfle, klnbz tulajdonsg biopolimer llthat el.
A bioremediciban is fontos szerepk van a fleg bakterilis transzgneket tartalmaz nvnyeknek. Az
Arabidopsis thaliana olyan transzgenikus vltozatt lltottk el, amely bakterilis enzimjei segtsgvel a
robbananyagokbl szrmaz talajszennyezst kpes lebontani. A TNT (2,4,6-trinitrotolun) vagy RDX
(hexahidro-1,3,5-trinitro-1,3,5-triazin) olyan mrgez xenobiotikumok, melyek a nem tkletes robbantsok
utn nagy mennyisgben, hossz ideig jelen vannak a talajban, bejutva az ivvizekbe is. Az Egyeslt
llamokban ez a tpus szennyezs igen nagy problma. Nem transzgenikus nvnyek is kpesek a
fitoremedicira, flvve a szennyezanyagot, vakulumokban vagy a sejtfalukban troljk azt (Vicia faba,
Zea mays, Catharanthus roseus), m lebontani nem kpesek. Bioremedici mikrobkkal is mkdhet,
azonban szmos esetben egy adott vegylet lebontshoz szksgesek a nvnyi enzimek, gy a kt
szervezet tvzse bizonyult eddig a leghatkonyabbnak.
15.1.3. Transzgenikus llatok az alapkutatsban s a gygyszatban
Az llatok genetikai mdostsa egy viszonylag lass, aprlkos s drga folyamat, azonban az jabb s
jabb mdszerek megjelense egyre egyszerbb s pontosabb teszi a technolgit. A genetikailag
mdostott llatok egy rszt kutatsi clokbl hozzk ltre, hogy a specifikusan megvltoztatott gnek
fenotpusra kifejtett hatst elemezzk. gy mg ismeretlen gnek funkcija, vagy azok mutciinak hatsa,
gninterakcik, vagy a gnexpresszi helyei feltrkpezhetek. Genetikai mdostssal olyan llnyeket is
ltrehozhatunk, melyek rzkenyebbek bizonyos vegyletekre, ezt hasznljk ki a gygyszerkutatsban,
hatanyagok tesztelsnl. Transzgenikus llatok kivlan alkalmazhatak modellrendszerknt emberi
betegsgek, illetve azok gygytsnak kutatsra is. Ms llatokat gy mdostottak, hogy bizonyos
tulajdonsgaikat a gygyszat vagy az ipar hasznosthassa.
Az els transzgenikus llatot Brinster s Palmiter 1982-ben lltottk el, amikor is egy egr
megtermkenytett petesejtjnek pronukleuszba mikroinjektlssal patkny nvekedsi hormon (GH)
transzgnt juttattak (ld. 1.5.2. fejezet). A hres egr ikerpr a Nature folyirat cmlapjra is rkerlt (ld.
15.5. bra).
15.5. bra: A Patkny nvekedsi hormon transzgnt tartalmaz egr (bal) s vad tpus testvre (jobb) a Nature
folyirat cmlapjn (Vol. 300,1982. december 16 ; a Nature Publishing Group engedlyvel)
1985-re nyl, brny illetve serts megtermkenytett petesejtjbe is sikerlt mikroinjektlssal transzgnt
bevinni. Megjegyzend, hogy a patkny GH transzgnt tartalmaz egr nem azrt lett nagyobb, mert a
patkny GH az llat mrett szabja meg, hanem az n. dzishats miatt, azaz tbb patkny transzgn plt
226
be vletlenszeren az egr genomba. A transzgnt a nehzfmekkel szablyozott metallotionein gn
promtere mg ptettk be a rekombinns DNS konstrukciba.
A ksbbiekben, a szomatikus nukleris gntranszfer alkalmazsval tbb, mint 10 transzgenikus fajt
lltottak el (ld. 15.6. bra). Ezzel a mdszerrel szletett 1996-ban az els olyan brnykln is (Dolly),
amely felntt szomatikus sejt genomjt rklte, habr transzgnt nem tartalmazott. Ezzel bizonytst nyert,
hogy brmely testi sejtnk genetikai anyagbl a teljes szervezet klnozhat.
15.6. bra: Szomatikus nukleris gntranszfer. A mdszer segtsgvel mdostott genetikai anyag donorsejtek
szaporthatak. (Forrs: wikipedia.org, GNU Free Documentation License, szerz: Quelle).
15.1.3.1. Xenotranszplantci s xenogn sejtterpia a gygyszatban
A szervtranszplantcira vrk szma tbbszrse a felhasznlhat humn szerveknek, s szomor tny,
hogy minden vben tbb ezer beteg hal meg megfelel szervek hinyban. Ezt az ignyt prblja kielgteni
a xenotranszplantci, amikor egy nem humn llny szervt ltetik be a betegbe. A serts j
vlasztsnak tnt a kutatk szmra, mivel szerveinek mrete hasonlt az emberhez, az anatmija s
fiziolgija sem tl klnbz, hatkonyan s egyszeren szaporthat s fenntarthat, illetve a technolgia
adott az immungenetikjnak a megvltoztatsra. Transzgenikus sertsek ellltsval a beltetett szerv
azonnali kilkdst (HAR: hyperacute rejection response) s a napokkal ksbbi akut vaszkulris
kilkdst (AVR: acute vascular rejection) szeretnk elkerlni. A hossztv kilkds elkerlsre
egyenlre csupn az egsz leten t tart immunszupressznsok szedse jelent megoldst. Bztat
eredmnyeket mutat a HAR folyamn aktivldott humn komplement rendszert szablyoz fehrjk
termelse az tltetett serts szervben. Az ember ltal termelt antitestek felismerik a serts antigneket, s az
ellenanyag-antign komplex aktivlja a komplement kaszkdot, ami a membrnkrost komplex (MAC:
membrane attack complex) ltrejtthez vezet. Azonban a komplement kaszkdot szablyoz fehrjk, mint
a CD55 (DAF: decay accelerating factor) vagy CD46 (MCP: membrane cofactor protein) meggtoljk a
MAC kialakulst. Embrik mikroinjektlsval ellltottak DAF s MCP fehrjket expresszl
transzgenikus sertst, mely sikeresen meggtolta az tltetett sertsvese kilkdst femlskben (15.7.
bra). A kilkds megakadlyozsra egy msik stratgia, hogy meggtoljk a sejtfelszni antignek
kifejezdst. Az antignek fleg az 1,3--galaktoziltranszferz aktivitsa rvn ltrejv 1,3--gal-
epitpok. Az -gal alllt homolg rekombincival tttk ki serts embrionlis fibroblaszt sejtekbl, ami
aztn nukleris transzferrel kerlt embrisejtekbe, s erre a gnre nzve egszsges KO (knock-out)
malacokat eredmnyezett.
227
15.7. bra: Xenotranszplantcira hasznlt transzgenikus serts ellltsa. A CD55 fehrjt termel gnszakasz
eltt egy citomegalovrus promtere ll (P
CMV
), ami biztostja a gn transzkripcijt mr az let korai szakaszban. A
poliadenilcis szakasz (PA) utn, s a promter szakasz eltt tallhatak a restrikcis enzimek hasthelyei (Pvu I,
Asp 1). (a mdostott bra forrsa: Niemann & Kues, 2003, Application of transgenesis in livestock for agriculture
and biomedicine. Animal Reproduction Science, 79(3), 291-317)
A szervtranszplantci mellett a xenogn sejtterpia is biztat eredmnyekkel szolgl a gygyszat tern.
A xenotranszplantcinl megismert, megfelel transzgenikus llatokbl (serts, marha) trtn sejtizolls
s beltets megoldst nyjthat a humn ssejtterpia mellett a klnbz betegsgek, rendellenessgek
vagy srlsek miatti elhalt szvetek regenercijra. A xenogn sejtterpia egyes betegsgek esetben mr
klinikai tesztels eltti fzisban van. Transzgenikus serts embrionlis idegsejteket Parkinson illetve
Huntington krban szenved betegek agyba transzplantltak, ahol azok dopaminerg neuronokk s glia
sejtekk alakultak. A serts eredet neuronok a beltets helyrl kiindulva kiterjedt axonhlzatot
alaktottak ki a pciens agyban. Szmos ms plda ltezik arra, hogy idegen eredet sejtek kpesek
visszaadni a gazdaszervezet egyes szveteinek funkcijt. Transzgenikus serts mjsejtek transzplantci
utn a mj szveteibe vndoroltak, s ott integrldva mkd LDL receptorokat expresszltak, ezzel
cskkentve egy magas koleszterinszint nyltrzsben a szrum koleszterinszintjt 30-60%-kal. A hasznlt
nyltrzs a homozigta rklds hiperkoleszterinmia llati modelljeknt szolgl. Ezzel el is rkeztnk a
transzgenikus llatok kvetkez rendkvl fontos felhasznlshoz, az emberi betegsgek llati
modelleken keresztl trtn kutatshoz. A donorsejtek sikeres genetikai mdostsa, a xenogn sejtterpia
alkalmazsa emberi betegsgeket modellez llattrzseken sikeres terpis megoldsokhoz vezethet a
humn gygyszatban.
15.1.3.2. Emberi betegsgek llatmodelljei: KO (knock-out) egerek
Knock-out (KO, gnkittt) egerek ellltsa mra mr ltalnos mdszerr vlt, mellyel egy gn
rszt/egszt tvoltjk el vagy helyettestik egyb DNS szekvencival (ld. 14.5.3. fejezet) A gn
kitsvel vizsglni lehet annak funkcijt, fenotpust, illetve utnozni lehet funkcivesztses
mutcikon alapul emberi betegsgeket. Az ember s egr gnjei kztt nagyfok a hasonlsg, ezrt a
klnbz KO egerek jellegzetessgeit vizsglva, illetve a kialakult tnetegyttesre kezelseket kidolgozva
kzelebb kerlhetnk szmos genetikai htter betegsg gygytshoz. A legklnbzbb rktpusok,
tlslyossg, szvelgtelensg, cukorbetegsg, kszvny, Parkinson kr, drogfggsg, regeds mind olyan
terletek, ahol a klnbz KO egerek nagy szolglatot tettek a kutatknak. Az els KO egeret 1989-ben
lltottk el Capecchi, Evans s Smithies (ld. 1.5.2. fejezet). Mra mr tbb ezer KO vagy transzgenikus
egrtrzs ltezik (MKMD: Mouse Knock-out and Mutation Database), s vente tbb milli egeret
hasznlnak fel klnbz kutatsokhoz.
228
A clzott gnkits, mint gn targeting mdszer alapjait a 0. fejezetben rszleteztk. Ebben a fejezetben a
KO egerek ltrehozsnak a lpseit foglaljuk ssze (15.8. bra):
a. A kitni kvnt gnt (clgn) gnknyvtrbl izolljk, majd a gnt mdostjk (delci, inszerci,
specifikus/random mutagenezis). A gnszakaszhoz egy markergnt is fuzionltatnak, ami ltalban egy
antibiotikum vagy toxin rezisztencia gnje, de lehet egyb detektlhat vltozssal jr gntermk is
(szn, fluoreszcencia). A legegyszerbb, ha homolg rekombincival kicserlik a markergnt a kitni
kvnt gnnel.
b. Egr (fehr) blasztocitbl ssejtet (ESC: embyonic stem cell) izollnak, amit in vitro tenysztenek.
c. A mdostott gnszakaszt elektroporcival juttatjk be az ssejtekbe, ami homolg rekombincival
pl be a sejtek genomjba. A sikeres rekombincis esemny igen ritka, ezrt annak az eslye, hogy az
ssejt anyai s apai kromoszmja is tartalmazza a mdostott gnt, igen csekly. gy a legtbb sejt,
ahol a rekombinci megtrtnt, heterozigta lesz erre a gnre nzve.
d. Azokra a sejtekre, amelyek genomja tartalmazza a mdostott gnt, markergnnel szelektlnak
antibiotikum/toxin jelenltben, illetve a fluoreszcens jel alapjn klnbztetik meg ket.
e. A KO gnt tartalmaz sejteket egy msik egr (fekete) blasztocitjba visszajuttatjk. gy a
blasztocita ktfle sejtet tartalmaz: a mdostott fehr egrbl szrmazt, s a nem mdostott fekete
egr eredett. A blasztocitt ezutn beltetik egy lvemhes egr ptanya uterusba, ahol kifejldhet a
kimra utd. Az utd bundjn valban lthat, hogy kimra, a fehr egr eredet sejtek utdai fehr
bundt eredmnyeznek, mg a feket fekett.
f. Nhny kimra gondja is lehet fehr egr leszrmazott, gy az azok ltal termelt ivarsejtek
tartalmazzk a KO gnt. Ezrt ha a kimra egereket proztatjk vad tpussal, lesz olyan utd, ahol
egy kpiban ugyan, de meglesz a KO gn. Ezek az egerek fehrek, de heterozigtk a KO gnre nzve.
g. Mr csak keresztezni kell a heterozigta egyedeket egyms kztt, hogy kapjunk homozigta
egereket a KO gnre nzve, ahol egyltaln nincs funkcionlis gntermk.
Ezzel a mdszerrel kszlt egy rkletes trpesggel jr betegsg, a Laron szindrma llatmodellje is. A
Laron szindrma htterben a nvekedsi hormon receptornak (GHR: growth hormone receptor) defektusa
ll, aminek kvetkeztben a nvekedsi hormonokra nem reagl a pciens. A GHR funkcivesztsnek okt
emberben nehz vizsglni, aminek etikai s gyakorlati okai is vannak. Homolg rekombincin alapul
clzott gnkitssel ezrt ltrehoztk a Laron egereket, melyekben a GHR s GHR-kt fehrje gnjt
tttk ki. Az egerek fenotpusa tipikus Laron szindrma jellegzetessgeket produklt (szlets utni
nvekedsi hibk, majd trpesg, a GHR s ktfehrjjnek hinya, cskkent koncentrcij inzulin-szer
nvekedsi faktor I s megnvekedett GH szint). Ezt a modellllatot azta az regeds kutatshoz is
hasznljk, mivel azt figyeltk meg, hogy a GH rezisztens llatok letideje meghosszabbodott.
Egy gn kitse nem minden esetben eredmnyez letkpes utdokat, a KO egrgnek 15%-a letlis, ezrt
legjobb esetben is csak embrionlis korban tanulmnyozhat a hats. Elfordulhat az is, hogy hiba nagyon
hasonl az egr genomja az emberhez, egy gn funkcivesztse ms fenotpust eredmnyez. Szmos
betegsg modelljt egr helyett patknyra dolgoztk ki, mely szaports tern lnyegben azonos
tulajdonsgokkal rendelkezik, azonban jval nagyobb, ami miatt knnyebb operlni vagy vrt venni tle.
Fontos megjegyezni, hogy fiziolgiai szempontbl is idelisabb vlaszts a patkny. Pulzusa pldul
csaknem a minkkel azonos, mg az egr szve 5-10-szer gyorsabban ver. Detoxifikl enzimjei is jval
kzelebb llnak hozznk, ezrt a potencilis gygyszerek farmakolgiai hatst s toxikussgt jobb
patknyon vizsglni. Mindezek ellenre az egrmodellek is rendkvl fontosak, hisz tbb rgcsl
modelltrzs birtokban jobban meg tudjuk becslni, hogy az szlelt fenotpus rgcsl-specifikus, vagy
ltalnos az emlskben.
229
15.8. bra: Knock-out egerek ellltsa. (Forrs: wikipedia.org. GNU Free licence; szerz: Kjaergaard)
230
Az els transzgenikus patknyt azonban csak 2008-ban sikerlt ltrehozni, melynek f oka, hogy a KO
egerek ellltshoz hasznlt technolgia patknynl nem mkdtt. Mivel a rekombincis esemnyek
gyakorisga igen kicsi, a kutatk egyszeren nem talltak olyan embrionlis ssejteket, ahol ez megtrtnt
volna. Mivel a szomatikus nukleris transzfer mdszer sem eredmnyezett KO patknyokat, maradt a kmiai
mutagenezis, amikoris N-etil-N-nitrozourea (ENU) injektlsval random mutcikat indukltak. Az ENU
etil-csoportja csoporttranszfer reakcival a DNS oxign s nitrogn gykeire kerl, ami mismatch
bzisprosodst eredmnyez. Az ENU-val injektlt hmet vad tpus nstnnyel proztattk, hogy mutns
utdokat kapjanak. Az ENU mutagenezis krlbell egy mutcit okoz brmely gnre nzve minden 200-
700-adik ivarsejtben. Annak ellenre, hogy az ENU mutagenetikus hatsa nagy, mivel kicsi a penetrancija,
gy csupn krlbell 500 gn mutldik el egy hmben, s az sszmutcik csak nagyon kis hnyadnak
van fenotpusos hatsa. AZ ENU mdszerrel ellltott mutcik feltrkpezse igen nehzkes, pnz- s
idignyes, ezrt ma mr nem nagyon hasznljk. Az ttrst a transzgenikus patknyok ellltsban a Zn-
ujj nuklezok (ZFN: zinc finger nucleases) s a transzkripcis aktivtor-szer effektor nuklezok (TALEN:
transcription activator-like effector nucleases) jelentettk, amik a DNS ketts szln szekvenciaspecifikus
hastsra kpesek, gy segtik a genom clzott mdostst (ld. 14.5.2. fejezet). A hastssal aktivljk a
DNS-javt mechanizmusokat, a homolg rekombincit s a trtt vgek kzvetlen sszeragasztst. A
nem homolgin alapul kzvetlen ligls a trtt vgeknl ltalban mutcikhoz vezet.
A mobilis genetikai elemekkel (retrotranszpozonok, transzpozonok) ellltott mutagenezis br random s
nem clzott, mgis alapvet eszkze a transzgenikus emlsk ellltsnak. Elnye, hogy a gnek teljes
kiesst eredmnyez mutagenezis egyenesen az ivarsejtekben trtnik, a bevitt mutci pedig stabilan
fenntarthat. A mutcik tovbb knnyen feltrkpezhetek, gy a KO patknyokbl trtn knyvtrak
ltrehozsa viszonylag egyszer feladat. KO vonalak s szvetspecifikus CRE-rekombinzt expresszl
patknyok proztatsval feltteles (kondicionlis) mutcikat is ltre lehet hozni (tovbbi rszleteket ld.
14.5.4. fejezet).
A rgcslk fiziolgija, anatmija, letideje sok esetben jelentsen eltr az embertl, ami miatt szmos
betegsg modellezshez nem megfelelek. Lass lefolys rktpusokhoz, illetve neurodegeneratv
betegsgekhez a serts, brny vagy marha jobb modell, mivel velk a betegsgek hosszabb ideig
tanulmnyozhatk.
Egy ritka szembetegsg (PR: retinitis pigmentosa) sertsmodelljt, melyre a fotoreceptorok korai elhalsa
jellemz, mikroinjektlssal hoztk ltre. A transzgenikus sertsmodell mutns rodopszint expresszl, ami
hasonl fenotpust eredmnyez az embernl megfigyelthez. A ltrehozott modelltrzs segtsgvel lehetv
vlt a betegsg kezelsnek folyamatos fejlesztse.
Mg a transzgenikus sertsek igen elterjedtek az egyes humn betegsgek modellezsben, addig a
transzgenikus kutya, macska vagy femlsk ellltsa csak nemrgiben vlt lehetv. Az els
transzgenikus kutya 2009-ben szletett, retrovrus-medilt gntranszferrel. A transzgn egy tengeri
szellrzsa piros fluoreszcens fehrjje volt, mely random integrldott a kutya fibroblaszt sejtjeibe. Ezutn
a fibroblaszt sejtekbl szomatikus nukleris transzferrel a transzgnt petesejtbe juttattk, amit osztds utn
ltettek be ptanykba. A kutatk most azon dolgoznak, hogy a kvnt inszercit specifikus helyre lehessen
bevinni. Ha ez sikerl, akkor kvetkez lpsknt sztrogn receptor KO kutykon tanulmnyoznk a
hormon termkenysgre gyakorolt hatst. Ugyanebben az vben, mikor az els transzgenikus kutya is
szletett, japn kutatk bejelentettk, hogy vrus-kzvettett gntranszferrel ellltottk az els stabil
transzgenikus femls trzset. A transzgenikus vonal sikeresen szaporodik, s utdai is tartalmazzk a
transzgnt, ami egy zld fluoreszcens fehrje (GFP: green fluorescent protein). Az jonnan ellltott
femlskben az egren nem tanulmnyozhat betegsgeket szeretnk vizsglni, mint amilyen a Huntington
kr vagy az infarktus. 2011-ben amerikai-japn kutatk sikeresen hoztak ltre GFP transzgnt tartalmaz
macskt, mely a ksbbiekben modellje lehet az emberi HIV okozta AIDS betegsgnek, mivel a macska
immundeficiencia vrus (FIV: feline immunodeficiency virus) a HIV rokona.
231
15.1.3.3. Transzgenikus llatok az lelmiszeriparban
Annak ellenre, hogy a transzgenikus nvnyek jval elterjedtebbek az lelmiszeriparban, szmos pldt
tallunk a GM llatok felhasznlsra is. Az ilyen, gntechnolgiai mdszerekkel mdostott llati termkek
egy rsze arra szolgl, hogy az adott termk emberi egszsgre gyakorolt pozitv hatst fokozzk. Ilyen a
cskkentett koleszterin tartalom, magas vrnyomst cskkent angiotenzin-konvertl enzim inhibitorok
vagy immunrendszert stimull peptidek jelenlte az telben. A hsipar nagy felfedezettje egy olyan
transzgenikus sertsvonal, ami nagyobb arnyban termel teltetlen zsrsavakat, mint teltetteket, gy hsa
egszsgesebb, s fogyasztsval cskkenthet az infarktus vagy a szvproblmk veszlye. Transzgenikus
marhval a tejtermkek legklnbzbb vltozatait lehet ellltani: zsrszegny tej (lipidanyagcsere enzim
modulcijval), hipoallergn tej (-laktalbumin gn kitsvel), laktzmentes tej (-laktalbumin gn
kitsvel), vagy csecsemtej (laktoferrin tltermelssel). A tejben tallhat egyik fontos sszetev, a
kazein klnbz tpusai hatrozzk meg a tej fizikokmiai tulajdonsgait. Ezrt a kazein a tejminsg
javtsnak az egyik f clpontja. Az egyes sszetevk vltoztatsnak hatsa, illetve mellkhatsainak
mrtke egrmodelleken jl kvethet.
15.1.3.4. Transzgenikus llatok a gygyszeriparban: humn fehrjk ellltsa
A terpira hasznlt humn fehrjk emberi vrbl vagy szvetekbl trtn ellltsa kis hatkonysg,
drga, idignyes s magban rejti a humn krokozk terjesztsnek veszlyt. Rekombinns baktrium
vagy sejtkultrk felhasznlsval egyszerbb a gygyszerfehrjk termelse. Htrnyuk, hogy a
baktriumok csak viszonylag egyszer fehrjk termelsre kpesek, a poszt-transzlcis mdostsokra
alkalmas mechanizmusok pedig limitltak. Megfelelnek bizonyul erre a clra tbbfle transzgenikus llat, a
brny, kecske, marha, serts, st a nyl emlmirigye, mellyel sok fehrje elllthat. A rekombinns
fehrje az llatbl a tejjel tvozik, gy tiszttsa sem jelent klnsebb problmt. Ezen llatokban a
glikozilcis mintzatok s a poszt-transzlcis mdostsok is megfelelek. Rekombinns fehrjk
szekrcijra a tej mellett a vrt, a vizeletet illetve egyb testnedveket is felhasznlnak. gretes lehetsg
gyengn immunogn antignek elleni ellenanyag termeltetsre neonatlis Fc-receptorra transzgenikus
llatok (egr, nyl) ltrehozsa (az ImmunoGenes cg fejlesztse).
Szmos rekombinns fehrjt termelnek emlmirigy specifikus promterrel rendelkez gnkonstrukcikkal.
Az gy termelt -antitripszin, antitrombin-III vagy szveti plazminogn aktivtor (TPA) jelenleg klinikai
kiprbls alatt ll. Transzgenikus nyulak emlmirigye ltal termelt -glkozidzt sikeresen alkalmaztk a
Pompe-kr kezelsre. Ez a betegsg a glikognraktrozs rendellenessgeihez vezet s hallos kt ves kor
alatt, amennyiben a beteg nem kap -glkozidzt. Egy msik esetben biolgiailag aktv laktoferrint lltottak
el transzgenikus szarvasmarha tejben, amivel profilaxist illetve szmos fertz betegsget lehet kezelni. A
gntechnolgia ton (baktriumban, lesztben, nvnyi s llati sejtekben) ellltott terpis cl fehrjk
szma gyorsan nvekszik. A 15.1. tblzatban sszefoglaltuk a legfontosabbakat (rszben az FDA ltal
jvhagyott, rszben klinikai kiprbls, rszben mg ksrleti stdiumban vannak)
A klnbz baktriumok nvekv antibiotikum rezisztencijval prhuzamosan egyre n az jfajta
antimikrobilis anyagok irnti igny. A kationos antimikrobilis peptidek (AMP) tulajdonsgai igen sok
elvrsnak megfelelnek: szles hatsspektrummal brnak, mind a Gram+, mind a Gram- baktriumokat
gyorsan elpuszttjk, a klasszikus rezisztencia gnek nem hatnak rjuk, illetve klnbz llatmodellekben
is aktvnak bizonyultak. Az AMP specifikusan a bakterilis sejtmembrnnal kerl kzvetlen kapcsolatba,
amirt a rengeteg anionos foszfolipid s az alacsony membrnpotencil a felels. gy gondoljk, hogy az
AMP a membrnt fizikailag roncsolja, illetve intracellulris molekulkkal is kapcsolatba lp. Az lvilgban
sokfle AMP-t fedeztek mr fel, azonban ezek emberre akr toxikusak is lehetnek (pl. rovar AMP).
A bemutatott sikerek ellenre azt is fontos megjegyezni, hogy jelenleg nem minden fehrjt lehet
transzgenikus llatok felhasznlsval elllttatni. Az eritropoetin termeltetsre irnyul erfesztsek
pldul mind szarvasmarhban, mind nylban kudarcot vallottak, utbbi esetben a gntermk toxicitsa
miatt. A pldbl ltszik, hogy a technolginak jelenleg mg vannak korltai.
232
15.1. tblzat: Rekombinns fehrjk terpis hasznlatra
Egy rdekes j fejleszts a transzkromoszomlis llatok ltrehozsa. A humn immunglobulin teljes nehz
s knnylnc szekvencijt tartalmaz humn mestersges kromoszmt (HAC: human artificial
chromosome) marha fibroblaszt sejtekbe juttattk, amely sejteket ezutn nukleris transzferre hasznltak. A
transzkromoszomlis utdok a vrkben humn immunglobulint termeltek. Egy ilyen rendszer nagy
elrelps lehetne a humn poliklonlis ellenanyagok termelsben. Szintn gretes gnterpis ksrletek
folynak a Duchanne izomdisztfia (MDM) HAC-vektorral trtn gnjavtsra. Az mg a jv krdse,
hogy az extra kromoszma mennyire marad fenn a kvetkez genercikban, s mennyire stabil a rla
trtn expresszi.
15.1.3.5. Transzgenikus llatok a krnyezetvdelem szolglatban
Az Enviropig nven elhreslt transzgenikus sertst krnyezetvdelmi okokbl hoztk ltre. A
gabonaflkben tallhat foszfort a serts nem kpes lebontani, gy az nagy mennyisgben jut a talajba,
illetve ivvizekbe az rlkkel egytt tvozva. A gazdk eddig foszfort bont fitz enzimet is tartalmaz
takarmny vsrlsra voltak ktelezve, hogy cskkentsk krnyezetk foszft szennyezst. Az Enviropig
tartalmazza a fitz gnt, ami az llat nylban termeldik. Az eredetileg E. coli baktriumbl szrmaz fitz
gnt egy egrbl szrmaz konstitutv promter mg klnoztk be, amit a serts kromoszmjba
mikroinjektlssal juttattak be. A mdszerhez nem volt szksg virlis gntranszferre vagy marker gnre, a
transzgn a genom egy specifikus helyre plt be, ahol stabilan fennmaradt.
15.2. Gnterpia
A gnterpia clja, hogy genetikailag hibs testi sejtek genomjt mdostsa emberben, a helyes gn
bevitelvel hozva helyre az elromlott gn szerept. Az emberi zigta, vagy az ivarsejtek genetikai
mdostsa etikai normkat srt, ezrt a gnterpia kifejezetten a nem rkld, szomatikus sejtek genetikai
llomnyt clozza meg. Ktfle szomatikus sejttpust hasznlhat a gnterpia: ssejteket s differencilt,
nem osztd sejteket. Az ssejtek esetben a transzgnt hordoz vektor RNS vrus (retro- vagy lentivrus)
az, ami bepl az ssejt genomjba, gy osztdst kveten is jelen van az utdsejtekben. Gnterpira
jelenleg ktfle forrsbl szrmaz ssejtet hasznlnak, az egyik a csontvelbl szrmaz hematopoetikus
ssejt, a msik egy, a br als rtegben tallhat ssejttpus. Ezek az ssejtek viszonylag knnyen
hozzfrhetek, s ex vivo is fenntarthatk. A gnterpia msik clpontja - differencilt, nem osztd sejtek
- esetben, a vektor nem kell, hogy bepljn a genomba, gy itt DNS vrusokat hasznlnak (adenovrus
vagy adeno-asszocilt vrus) transzgn hordozknt. A legjabb irnyzat, hogy vrus-alap gnbejuttats
233
helyett a transzgnt egy halak genomjban megtallt s fellesztett transzpozon (ugrl gn) viszi be a
gazdasejt genomjba (ld. 14.5.5. fejezet). Egy alv hal transzpozonbl kszlt a Sleeping Beauty
(Csipkerzsika) nvre hallgat, humn sejtek genomjban ugrl transzpozon, amivel transzgnek vihetk
be humn sejtekbe (kt magyar kutat, Izsvk Zsuzsa s Ivics Zoltn eredmnyei).
A gnterpia alkalmazhatsga sok akadlyba tkzik. A technolgia meg kell, hogy kzdjn a transzgn
bejuttatsnak gyenge hatkonysgval, az alacsony szint fehrje expresszival, az integrcival jr
mutagenezis veszlyvel s a vektor vagy a fehrje ltal induklt immunvlasszal. A virlis vektorok
hasznlata is veszlyt rejthet magban. Br a vektor nem tartalmaz patogenitsi faktorokat, egy l
szervezetbe kerlve mindig fennllhat annak a lehetsge, hogy a betegsget okoz tulajdonsgok
visszatrnek.
Az els gnterpis ksrletet 1990-ben vgeztk az Egyeslt llamokban, egy adenozin-deaminz- s
slyos kombinlt immundeficiencia (SCID: severe combined immunodeficiency) betegsgekben szenved
pciens esetben. Azta szerte a vilgon pr ezer gnterpit alkalmaz klinikai tesztrl szmoltak be,
klnbz betegsgek sikeres gygytsval kapcsolatban (X kromoszma kapcsolt SCID,
adrenoleukodisztrfia, krnikus limfoid leukmia, Parkinson kr). 2012-ben az Eurpai Bizottsg elfogadta
az els gnterpin alapul kezelst hivatalos gygymdknt, mely 2013 vgtl mr szleskren
alkalmazhat lesz az Eurpai Uniban s az Egyeslt llamokban egyarnt. A Glybera mrkanven
forgalomba kerl gnterpis szer a slyos hasnylmirigy gyulladst okoz lipoprotein-lipz deficienciban
szenvedknek nyjt gygyulst. A humn lipoprotein-lipz (LPL) gnjt szllt vektor az adeno-asszocilt
vrus 1-es szerotpusa (AAV1), amely a vzizom sejteket clozza meg (ld. 15.9. bra). A vzizom sejtek az
LPL f termelsi helyei. A kezelst kvet 3-12 htben a vrben lv zsrok koncentrcija jelentsen
lecskken. Az AVV1 alkalmazsnak nagy elnye, hogy hinyoznak a patogenitsi faktorai s nem pl be
a genomba, gy nem okoz random mutagenezist, ami a rk kockzatt nveln. Az AVV1 nagyon alacsony
immunvlaszt indukl, ami ltalban semlegest antitestek termelsben merl ki, s alacsony a
citotoxikussgot okoz vlaszreakci is.
15.9. bra: Adenovrus-kzvettett gnterpia. A vrusvektor specifikusan felismeri az izomsejteket, amikbe
receptor medilt endocitzissal jut be. A sejt belsejben az endicitotikus vezikulum lebomlik, majd a vrusvektor
kiszabadulsa utn a sejtmag prusaihoz asszocildik. A sejtmagba a transzgn a vrus DNS-sel egytt jut be.
(Forrs: US National Library of Medicine).
A mai normk szerint a humn gnterpia nem rintheti az ivarsejteket, illetve a transzgn genercirl
genercira nem rkldhet. A gnterpia hasznlatakor alkalmazott alapvet gondolkodsmd, a
Weismann-elv rtelmben az informci mindig az ivarsejtek fell ramlik a bellk kialakult szomatikus
sejtek fel, s soha nem fordtva. Azonban ez nem mindig trtnik gy. Az RNS alap retrovrusok reverz
transzkriptz segtsgvel plnek be a genomba, s aktivitsuk rvn gyakran szlltanak gneket egyik
234
sejtbl a msikba, vagy akr egyik fajbl a msikba (horizontlis gntranszfer). Ha egy szomatikus gnt
szllt retrovrus egy ivarsejtet fertz meg, a szomatikus gnnel egytt beplhet annak genomjba. Fontos
megjegyezni, hogy az emberi szervezetben szmos endogn retrovrus ltezik, mely igen fontos lehet a
gnterpia jvje szempontjbl.
15.3. A transzgenikus llnyek felhasznlsnak tudomnyetikai
s krnyezetbiztonsgi krdsei
A gntechnolgiai mdszerekkel trtn transzgenikus llnyek ellltsa szigor szablyozs alatt ll,
mely kiterjed a ksrletes munkt megelz engedlyeztetsi eljrsra, a laboratriumban felhasznlsra
kerl protokollokra illetve a transzgenikus llny ksbbi sorsra. Ezek a szablyok orszgrl orszgra
vltozhatnak, kivltkpp az emberi fogyasztsra sznt transzgenikus lelmiszerek felhasznlsnak s piacra
kerlsnek tekintetben, ahol a legszigorbb szablyozs az Eurpai Uniban van. Az EU-ban les
ellenttben pldul a GMO-t sokkal inkbb tmogat Egyeslt llamokkal minden genetikailag
mdostott lelmiszer j lelmiszernek minsl, ebbl addan egyedi engedlyeztetsi eljrsra ktelezett.
Magyarorszgon az alkotmny tiltja a GM nvnyek szabadtri termesztst.
A transzgenikus lelmiszerek termesztsnek s fogyasztsnak a krdse les vitkat vlt ki vilgszerte,
ahol a tudomnyos rvek mellett sokszor az rzelmek s a politika is jelents szerephez jut. A vilg nvekv
emberi populcijnak az lelmezse komoly problma, melyet az egyre szlssgesebb s
kiszmthatatlanabb idjrs tovbb slyosbt. Fontos tovbb, hogy ha fizikai rtelemben kpesek is
vagyunk az emberisg szmra szksges mennyisg lelmiszer megtermelsre, azt olyan kltsggel s
hatkonysggal kell tennnk, hogy az mindenki szmra hozzfrhet s megfizethet legyen. Amg egy
tlagos szak-amerikai lakos a jvedelmnek 12%-t klti csupn lelmiszerre, addig ez a szm
Magyarorszgon 27%, de Afrikban s zsiban akr 60-80% is lehet. Ha az lelmiszer rak tovbb nnek a
fejld orszgok emberei egsz egyszeren nem lesznek kpesek lelmet vsrolni. Ilyen krlmnyek
kztt a GM-nvnyek elnyei, mint a magasabb termshozam vagy a kiszmthatbb termels
felrtkeldnek.
Nem szabad azonban megfeledkezni a GM lelmiszerek termesztsnek s fogyasztsnak krnyezeti s
egszsggyi kockzatairl sem. A GM-lelmiszerek fogyasztsval kapcsolatosan nincs olyan dokumentlt
eset, ami azt bizonytan, hogy a gnmdosts, mint technolgia brmifle egszsggyi kockzatot
jelentene. Ettl fggetlenl a transzgn ltal kdolt fehrje kivlthat allergis reakcikat az arra rzkeny
emberekben, amivel szmolni kell.
A transzgenikus emlsk, kivltkpp a femlsk ksrleti illetve gygyszeripari felhasznlsa is szmos
vita forrsa, melyben az ellenzk az llatok felesleges knzsa ellen tiltakoznak. Nem szabad azonban
megfeledkeznnk arrl, hogy az llatksrletek mssal nem helyettesthetk, gy szksgesek. Az llati
ldozatok minimalizlsa illetve a velk val kmletes bnsmd minden kutat trvnyi s erklcsi
ktelessge.
A humn gnterpia korunk nagy lehetsgekkel kecsegtet gygyszati alkalmazsa br mg
gyerekcipben jr, mgis rengeteg etikai krdst vet fel. Hogyan lehet klnbsget tenni a gnterpia j s
rossz felhasznlsa kztt? Ki dnti el, hogy mely tulajdonsgok normlisak, s mik a rendellenesek?
Megengedhet-e az alapvet kpessgeink gnterpival val fokozsa, gymint fizikai teljest kpessg
vagy intelligencia? Br a jelenlegi szablyozs szerint a humn gnterpia nem rintheti az ivarsejteket,
illetve a transzgn genercirl genercira nem rkldhet, nem tudhatjuk, hogy e tekintetben mit hoz a
holnap.
15.4. Tovbbi olvasnival a fejezethez
235
Fraley, RT, et al. (1983) Expression of bacterial genes in plant cells. Proceedings of the National Academy
of Sciences 80: 4803-4807.
Walsh, G (2005) Therapeutic insulins and their large-scale manufacture. Applied microbiology and
biotechnology 67: 151-159.
Kues, WA., and Niemann, H (2004) The contribution of farm animals to human health. TRENDS in
Biotechnology 22: 286-294.
Yang, Y-G, and Sykes, M (2007) Xenotransplantation: current status and a perspective on the future. Nature
Reviews Immunology 7: 519-531.
Sheridan, C. (2011). Gene therapy finds its niche. Nature Biotechnology 29: 121128.
Prickett M, Jain M. (2013) Gene therapy in cystic fibrosis. Transl Res. 161:255-64.
Kay MA (2011) State-of-the-art gene-based therapies: the road ahead. Nat Rev Genet. 12(5):316-28.
236
16. Irnytott evolcis technikk
A molekulris biolgiai mdszerek fejldse lehetv tette a gnek klnozst s az irnytott mutagenezist,
azaz egyes aminosavak clzott kicserlst, minek ksznheten ma mr a fehrjk aminosav sorrendje
szabadon vltoztathat. A kutatk mutagenezisen alapul technikk sort fejlesztettk ki. A fehrjk
vizsglatnak klasszikus, fehrjemrnki megkzeltse egyedi fehrje-mutnsok vizsglatn alapul.
Az ilyen vizsglatok sorn a fehrje egy vagy nhny pozcijban megvltoztatjk az eredeti aminosavat,
majd ezeknek a mutns fehrjknek a tulajdonsgait hasonltjk ssze a termszetben is elfordul,
gynevezett vad tpus fehrjvel. A mutcik szerkezetre s funkcira gyakorolt hatsn keresztl
igyekeznek a vad tpus aminosavak szerept feltrni. Hamar kiderlt azonban, hogy a lehetsges vltozatok
nagy szma miatt az sszes varinst nem lehet ellltani. A fehrje minden pozcit rint teljes
feltrkpezsnek gyakorlati akadlyai vannak, mr egyedi mutnsok vizsglata esetn is, a mutcik
kombincijrl nem is beszlve. A sok egyenknti mutns ellltsa, tiszttsa s vizsglata igen id- s
kltsgignyes. A vizsglatok eredmnyei alapjn felmerl jabb krdseket megvlaszolni, a
hipotziseket altmasztani csak egy, de ltalban tbb jabb mutns ellltsval s vizsglatval van
md.
ttrst jelentett az irnytott evolcis mdszerek megjelense. Ezek a mdszerek olyan esetekben
alkalmazhatk egyszeren, amikor a vizsglat trgya valamely adott molekulhoz szelektven ktd
fehrje. Az evolci mkdsbe lpsnek mindssze nhny alapvet felttele van: a szaporods
kpessge, az rklds (az utd hasonlt a szl(k)re) s a vltozatossg (az utd nem tkletes msolata a
szl(k)nek). Abban a rendszerben, amelyben a felttelek teljeslnek, evolcis folyamatok indulnak be
abban az esetben, ha a tagok eltr tulajdonsgai befolysoljk azok szaporodsi sikert, azaz a
rtermettsget. Egy ilyen rendszerben az adott krnyezeti felttelek kztt legjobban teljestk szaporodnak
a legnagyobb mrtkben, utdaik arnya a kvetkez generciban nagyobb lesz (ld. 16.1. bra). Az brn
bemutatott rendszerben a kiindul helyzethez kpest az A egyedek arnya megntt, s B mutcijval
megjelent a C tpus.
16.1. bra: Az evolvld rendszerek ltalnos brzolsa
A folyamat, ha hossz id (illetve elegenden sok szaporodsi ciklus) ll rendelkezsre, a vltozatok
bmulatos sokflesgt kpes ltrehozni, mely vltozatok rendelkeznek az adott krnyezetben val
fennmaradshoz s a tovbb szaporodshoz szksges adaptcikkal. Erre a fldi llnyek diverzitsa a
ltvnyos bizonytk. Az irnytott evolcis mdszerek az evolcihoz hasonlan mkdnek, s a
termszetben elfordul folyamatokat utnozva segtik a kutatt. Mkdsk a fehrje nagyszm egyedi
mutnsnak, a vltozatossgnak (varinsok knyvtra) ellltsn s az gy ltrehozott sokasgbl a
szelektv ktsen alapul szelekcin nyugszanak. A kutat dnti el, hogy a fehrje mely rszeinek mekkora
vltozatossgt hozza ltre, s, hogy milyen tulajdonsgra szelektl, innen az irnytott jelz.
16.1. Az irnytott evolcis megkzeltsrl ltalban
Az irnytott evolcis technikk nagy elnye, hogy a mutnsokat nem kell egyenknt ellltani, tiszttani
s vizsglni. A gnknyvtrat klnbz, PCR-en s/vagy degenerlt szintetikus oligonukleotidok
hasznlatn alapul mdszerek segtsgvel, egy reakciban lltjk el. A gnknyvtrat gy fejezik ki
fehrjk formjban, hogy azok a gnjeikkel fizikai kapcsolatban maradnak. A szelekci sorn a
237
ktpartnerrel sszehozva kivlaszthatk a sokasgbl azok a fehrje vltozatok, melyek teljestik a
szelekcis feltteleket. Egyedi mutnsok vizsglata helyett ezen, funkcira szelektlt gnek szekvencijnak
analzisvel derthet ki, hogy a vizsglt fehrjn milyen aminosavak szksgesek vagy alkalmasak a
funkci elltsra. A knyvtrkszts s a szelekci sorn tulajdonkppen egy trben zajlik sok milli
egyedi ksrlet, melyeket egyenknt kptelensg volna elvgezni. gy sokkal tbb mutns megvizsglsra
van lehetsg, mint egyedi vltozatok ellltsa esetn. A mdszer ltalnos smjt a 16.2. bra ismerteti.
A knyvtrkszts sorn a mutcik arnya s tpusa bizonyos hatrok kztt szabadon, illetve a cloknak
megfelelen vlaszthat meg. A szelekcis feltteleket, a szelekci krlmnyeit szintn a vizsglat cljtl
fggen lehet belltani. Ennek ksznheten lehetsg van nagyobb affinits klcsnhat partnerek, vagy
enzimek esetn nagyobb katalitikus aktivits vltozatok ellltsra ppgy, mint az eredetitl eltr
partner ktsre, illetve talaktsra kpes fehrjk kifejlesztsre. Az gy ellltott, korbban nem ltez
fehrjk, illetve enzimek egy rszt ipari folyamatokban vagy terpis clokkal hasznljk, ami a
megkzelts risi gyakorlati jelentsgt is mutatja.
Az irnytott evolcis mdszereknek is vannak ugyanakkor korltai. A knyvtrksztsi s szelekcis
eljrsok csak bizonyos variancij knyvtrak teresztsre kpesek, nagyobb knyvtr alkalmazsa esetn
knnyen elveszhetnek vletlenszeren olyan vltozatok is, melyek teljesthetnk a szelekcis feltteleket.
Olyan knyvtr ltrehozsnak, ami egy adott hosszsg polipeptid sszes lehetsges varinst
tartalmazza, mr elvi akadlyai is lehetnek a lehetsges varinsok szmnak exponencilis nvekedse
miatt. Egy 60 aminosavbl ll polipeptid esetben a lehetsges varinsok szma 20
60
, ami meghaladja az
univerzumban ltez elemi rszecskk szmt. Ezrt ezen mdszerek alkalmazsakor sincs lehetsg a
fehrje sszes aminosav pozcijnak teljes kr vizsglatra. Vagy az egyes pozcikban elfordul
aminosavak szmt, vagy a vizsglt pozcik szmt korltok kz kell szortani. A mdszerek
alkalmazhatsgt korltozza az is, hogy segtsgkkel csak ms molekulhoz szelektven kt fehrjk
vizsglhatk, melyeknek a ktpartnere is ismert.
16.2. bra: Az irnytott evolcis eljrsok ltalnos brzolsa
238
16.2. Knyvtrksztsi technikk
16.2.1. PCR alap knyvtrksztsi eljrsok
16.2.1.1. Hibt ejt (error-prone) PCR
A PCR alap knyvtrkszts legegyszerbb mdja az gynevezett hibt ejt (error prone) PCR
alkalmazsa, amelyet rszletesen ismertettnk a 11.1.2. fejezetben. A hibt ejt PCR olyan eljrs, melynek
sorn gyakrabban hibz DNS-polimerz enzim hasznlatval, a reakcikrlmnyek szuboptimlis,
hibra hajlamost belltsval, vagy ppen egyenltlen arnyban adagolt nukleotidokkal a vizsglni kvnt
fehrje gnjnek PCR-rel trtn felszaportsa sorn vletlenszer pontmutcikat tartalmaz kpikat
tartalmaz gnknyvtrat lltanak el. Ezt kveten a mutnsokat is tartalmaz knyvtrat fehrje
formban kifejezik, s egy megfelel szelekcis mdszerrel kivlaszthatjk a sokasgbl a megvltozott
funkcij fehrjket. A kivlasztott fehrjk ezutn tovbb vizsglhatk. Megllapthat a mutci vagy
mutcik pontos helye s tpusa, valamint a funkcira gyakorolt hatsa. A mdszer alkalmazsban
nehzsget okoz pldul a helyes mutcis rta megvlasztsa, ugyanis a mutcik kztt a kros, pldul
teljes funkcivesztst okoz mutcik sokkal gyakoribbak, mint a hasznosak, amelyek a funkci
kimutathat megvltozsval jrnak. Magas mutcis rta esetn a sok kros, pldul a trszerkezetet torzt
mutci elfedheti a vizsglat szempontjbl hasznos, megvltozott funkcit eredmnyez mutcik hatst,
mg tl alacsony mutcis rta esetn a vadtpus dominancija miatt nehezebb a mutnsokat megtallni. A
pontmutcin alapul technika elnysen megvltozott specifits fehrjk ellltsra kevss alkalmas,
ugyanis a mutcik vletlenszeren jelennek meg, s egy lnyeges funkcionlis ugrs elrshez
valsznleg tbb aminosav egyttes megvltozsra van szksg.
Br nem PCR technika hasznlatn alapul, de szintn random mutcikat tartalmaz knyvtr ellltsra
alkalmas mdszer a hibra hajlamostott E. coli sejtek hasznlata (ld. 11.1.1. fejezet). Ezek a sejtek a DNS
hibajavts bizonyos fehrji, vagy proofreading aktivitssal rendelkez DNS-polimerzok mutns
vltozatait hordozzk, ezrt ezekben a sejtekben a DNS replikci sok hibval zajlik.
16.2.1.2. Szexulis PCR
A fejlettebb PCR alap eljrsok a knyvtrkszts sorn a homolg rekombincival analg folyamatokat
hasznlnak ki. Szmtgpes szimulcik igazoljk, hogy a rekombinci kpessgvel rendelkez
rendszerek gyorsabban evolvldnak s robosztusabbak, vagyis kls behatsokra (esetnkben kros
mutcikra) ellenllbbak, mint azok, melyek rekombincira kptelenek. A rekombinci biztostja a
klnbz egyedekben ltrejtt mutcik keverst. A rekombinci s szelekci egyttes megvalsulsa
lehetv teszi a kedvez mutci kombincik kialakulst, valamint megakadlyozza a kros mutcik
elszaporodst. A fent lert hibra hajlamos PCR, valamint a ksbb bemutatsra kerl helyspecifikus
mutagenezisen alapul technikk nem rendelkeznek a rekombinci kpessgvel, ellenttben a
kvetkezkben ismertetett szexulis PCR mdszerrel (ld. 16.3. bra).
A szexulis PCR vagy DNS kevers technika a termszetes vagy mestersges vltozatossg homolg
rekombincival trtn keverst imitl in vitro mdszer, ami kombinlhat az gy ltrejv vltozatok
szelekcijval. A vizsglt fehrje gnjnek a termszetben elfordul vagy pldul hibra hajlamos PCR
segtsgvel ellltott klnbz vltozatait DN-z I enzim segtsgvel vletlenszeren fragmentumokra
hastjk, majd az gy kapott DNS tredkeket tartalmaz mintn hozzadott primerek nlkl PCR-t
vgeznek. A PCR sorn a gn klnbz vltozataibl szrmaz tredkek a komplementer szekvencij
szakaszoknl prosodhatnak egymssal, gy kvzi primerknt szolglva a msolshoz. Az eredetivel
megegyez hosszsg szekvencik plnek fel a PCR reakci sorn, amelyek tbb kiindulsi szekvencira
jellemz szakaszbl llnak. Az jra felplt szekvencik a vltozatok olyan kombinciit hordozzk, melyek
a szli szekvencik kztt nem fordultak el, azaz a vltozatok kztt rekombinci kvetkezik be. A
rekombincinak ksznheten a mdszer alkalmas a kezdeti varici kombinatorikus keversre,
239
segtsgvel kombinatorikus knyvtr llthat el. A rekombinci elnye teht a tbbi mutagenezis
technikval szemben, hogy tbb cikluson keresztl zajl molekulris evolcira ad lehetsget.
16.3. bra: Szexulis PCR
A mdszer msik nagy elnye a rugalmassgban rejlik, ugyanis a krlmnyek belltsval a
vletlenszeren jelentkez pontmutcik gyakorisga a varici tovbbi nvelse rdekben vltoztathat. A
szli szekvencik hozzadsval mintegy visszakeresztezst (back cross) is el lehet vgezni, amivel a
kros, illetve az esetleges csendes, a funkcit nem befolysol mutcik mennyisge alacsonyan tarthat. A
szexulis PCR alkalmazhat pldul enzimek fejlesztsre is egy olyan eljrsban, ami hasonlt az
ellenanyagok kpzdsre a szervezetben. A kutatk ngy klnbz |-laktamz enzim gnjt kevertk
ssze, majd tbb cikluson keresztl engedtek tovbbi rekombincit s pontmutcit. A ciklusok kztt a
knyvtrat hordoz sejteket moxolaktm rezisztencira szelektltk. A leghatkonyabb ellltott kimra
enzim mind a 4 kiindulsi fehrjtl legalbb 100 aminosav pozciban klnbztt, s szmos jonnan
megjelent pontmutcit is tartalmazott.
16.2.2. Helyspecifikus mutagenezisen alapul eljrsok
A DNS szintetizls mdszereinek fejldse lehetv teszi degenerlt oligonukleotidok szintzist, melyek
segtsgvel oligonukleotiddal irnytott helyspecifikus mutagenezis technikkkal kombinatorikus
knyvtrak llthatk el. A degenerlt oligonukleotidok gy kszlnek, hogy a szintzis sorn a
meghatrozott pozciknl a reakcihoz tbbfle nukleotidot adagolnak. A tbbfle nukleotid
vletlenszeren bepl az oligonukleotidokba. gy az oligonukleotidoknak egy olyan keverke keletkezik,
melyek az sszes lehetsges kombinciban tartalmazzk a tervezett mutcikat (ld. 16.4. bra). A
degenerlt oligonukleotidokkal vgzett helyspecifikus mutagenezis segtsgvel kombinatorikus, azaz a
tervezett mutcikat az oligonukleotidokhoz hasonlan minden lehetsges kombinciban tartalmaz
fehrjeknyvtr llthat el. Az egyes mutcik gyakorisga a degenerlt oligonukleotid szintzise sorn a
klnbz nukleotidok adagolsakor, azok arnynak helyes megvlasztsval llthat be. A helyspecifikus
mutagenezis technikkon alapul knyvtrksztsi eljrsok elnye, hogy a mutcik pozcija s az egyes
pozcikban ltrejv vltozatossg pontosan tervezhet.
240
16.4. bra: Degenerlt oligonukleotid szintzis
16.2.2.1. Teltsi mutagenezis
Teltsi mutagenezis sorn a vizsglt pozcikban mind a 20 aminosav elfordulsa megengedett. Ilyen
knyvtrak esetben a randomizland pozcikban a degenerlt oligonukleotidok ltalban NNK vagy
NNS kodonokat tartalmaznak, ahol N a ngyfle bzist jelenti, K = G/T s S = G/C (ld. 16.4. bra s 16.1.
tblzat). Az NNK s NNS kodonok 32 kodon keverkt eredmnyezik. A 32 lehetsges kodon kdolja
mind a 20 aminosavat, s mindssze egyfle stop kodon megjelenst teszi lehetv. Ezzel elrhet, hogy a
knyvtrban az egyes aminosavak kiindulsi arnya egyenletesebb legyen, mint NNN kodonok alkalmazsa
esetn, valamint a stop kodon elfordulsi gyakorisga is kisebb.
16.1. tblzat: IUB nukleotid szimblumok
241
Teltsi mutagenezissel egyszerre kevs pozci vizsglhat, mert a knyvtr elmleti mrete, azaz a
lehetsges vltozatok szma 6-7 pozci vizsglata esetn elri a leggyakrabban alkalmazott szelekcis
technikk ltal vizsglhat maximlis mretet. Az ezzel a mdszerrel ksztett knyvtrak legfontosabb
alkalmazsi terletei ltalban lokalizlt rgik feltrst clozzk meg. Ilyen feladatok pl. lineris peptid
motvumot felismer fehrjk preferenciinak feltrsra random peptid knyvtrak alkalmazsval, vagy az
ellenanyag varibilis hurok rgik vizsglata. A teltsi mutagenezis a legjobb vlaszts akkor is, ha rvid
sszefgg szakasz irnytott evolcis vizsglatt clozzuk meg.
16.2.2.2. Mutcikkal tzdelt (spiked) oligonukleotidok hasznlata
Az egy knyvtrban vizsglt pozcik szmnak kiterjesztsre alkalmas mdszer a mutcikkal tzdelt
(spiked) oligonukleotidok hasznlata. Ilyen knyvtrak esetn a degenerlt oligonukleotid sereg tagjai
alapveten az sszes pozciban a vad tpusnak megfelel nukleotidot tartalmazzk. A szintzis sorn
clzottan, a megvltoztatni kvnt pozcikban adnak a vad tpus mellett kis mennyisgben ms nukleotidot
vagy nukleotidokat is. A mutagenezis sorn ltrejv knyvtr a legtbb pozciban vad tpus gneket fog
tartalmazni, amelyek a vad tpustl eltr nukleotidok adagolsnak fggvnyben fognak mutcikat
hordozni. Ezt a mdszert hasznljk pldul, ha egy klcsnhats paramterein szeretnnek javtani.
16.2.2.3. Megszabott kodonokat hordoz (tailored) oligonukleotidok hasznlata
Ez a stratgia gy terjeszti ki a vizsglatba bevonhat pozcik szmt, hogy az egyes pozcikban csak a
lehetsges 20 aminosav egy rsznek megjelenst engedi meg (ld. 16.2. tblzat).
Ahhoz, hogy ezt a stratgit eredmnyesen lehessen alkalmazni, szksgesek elzetes ismeretek a vizsglt
interakcirl. Ezek alapjn lehet kivlasztani, hogy az egyes pozcikban milyen aminosavak
fordulhassanak el. A tervezsben segthet, ha tbb homolg fehrje szekvencija ismert, ha mr vannak
elzetes irnytott evolcis eredmnyek, azaz lehet tudni, hogy milyen karakter aminosavak kpesek
elltni az interakci ltal megkvetelt funkcit, vagy rendelkezsre ll a vizsglt molekula hromdimenzis
szerkezete.
16.2. tblzat: Gyakran hasznlt aminosav kszletek kdolsa degenerlt kodonokkal az IUB nevezktan szerint
242
16.3. Szelekcis eljrsok
16.3.1. I n vitro szelekcis mdszerek
In vitro knyvtrksztsi s szelekcis mdszerek alkalmazsval van lehetsg a legnagyobb, akr 10
13
klnbz vltozatot tartalmaz knyvtrak ellltsra. Ennek az oka az, hogy a folyamat sorn a DNS
knyvtrat in vitro transzlcis technikkkal fejezik ki fehrje formban. Ennek ksznheten nem kell
alacsony hatkonysg mdszerekkel a DNS-t sejtekbe juttatni, gy a diverzitst csak az in vitro transzlci
sorn a rendszerben jelen lv riboszmk s informcihordoz molekulk mennyisge korltozza.
16.3.1.1. Riboszma-bemutats
A riboszma bemutatssal szelektlhat knyvtrat alkot gnek egy T7 transzkripcis promterbl, egy
riboszma-kthelybl, a knyvtrfehrje gnjbl s egy polipeptid linkert kdol szakaszbl llnak (ld.
16.5. bra). A gn nem tartalmaz stop kodont. A transzkripcit in vitro vgzik T7 RNS-polimerz
segtsgvel, riboszmk s aminoacil-tRNS-ek, GTP valamint a szksges inicicis s elongcis faktorok
jelenltben. A knyvtrfehrje s az azt kvet linker trdik, a riboszma az mRNS vgre r, de a stop
kodon hinya miatt a disszocici nem kvetkezik be. Az trdott peptid linkernek ksznheten a
knyvtrfehrje el tud tvolodni annyira a riboszmtl, hogy a feltekeredse zavartalanul vgbemehessen
s a szelekci sorn a ktpartner hozzfrjen.
A reakci sorn keletkez, a riboszmbl, az mRNS-bl s a knyvtrfehrjbl ll hrmas komplex 4C-
on stabil. Az gy ltrehozott fehrje knyvtrbl a vizsglt fehrje ktpartnervel kivlaszthatak azok a
klnok, amelyek a mutcik ellenre megriztk a partner ktsnek kpessgt, vagy a mutcik
kvetkeztben a vadtpusnl ersebben ktik azt. A szelekcis kvetelmnyeket teljest fehrjket kdol
mRNS-eket reverz transzkripci utn fel lehet szaportani, ezltal lehetsg nylik egyrszt ismtelt
szelekcira, msrszt a gnek szekvenlsra is.
16.5. bra: Riboszma bemutats
16.3.1.2. mRNS-bemutats
Az mRNS-bemutats a riboszma-bemutats tovbbfejlesztett vltozata. A fehrjt kdol mRNS 3
vghez puromicin molekult kapcsolnak kovalensen, egy rvid DNS linkeren keresztl. Az in vitro
transzlci sorn a riboszma megll az RNS-DNS hatron. Ekkor a puromicin belp a riboszma peptidil-
transzferz helyre, s stabil amid ktst alakt ki a keletkez fehrje C-terminlisval. A keletkez komplex
stabil, a kifejezett knyvtr a riboszma-bemutatshoz hasonlan szelektlhat.
243
16.3.2. A fg-bemutats
A fg-bemutats az irnytott evolcis mdszerek legkorbban kifejlesztett kpviselje. Egyszersgnek,
rugalmassgnak s hatkonysgnak ksznheten mindmig a fg-bemutats a leggyakrabban
alkalmazott irnytott evolcis eljrs (ld. 16.6. bra).
16.6. bra: A fg bemutats alapvonsai
A fg-bemutats sorn az evolvlni kvnt fehrje gnjt egy bakteriofg egyik burokfehrjje gnjhez
illesztik. A gn termke fzis fehrje, ami a burokfehrjbl s a knyvtrfehrjbl ll, melyeket ltalban
flexibilis peptid linker kt ssze. A fzis fehrje bepl a bakteriofg burkba, gy a vizsglt fehrje
megjelenik a fg felsznn. A keletkez fgok a ktpartner szmra hozzfrhet formban fejezik ki a
vizsglt fehrje egy varinst, s hordozzk annak gnjt, azaz megvalsul a funkcirt felels fenotpus s
az azt kdol genotpus fizikai kapcsolata. A knyvtrat ltalban helyspecifikus mutagenezisen alapul
eljrssal hozzk ltre, de van lehetsg pl. szexulis PCR alkalmazsra is. A bakteriofg felsznn
kifejezett knyvtrbl kivlaszthatk a szelektv kts kpessgvel rendelkez vltozatok pl. szilrd
felsznhez kttt vagy affinits oszlophoz kttt specifikus ktpartner segtsgvel.
Els bemutatsa ta a fg-bemutats a nagyszm egyedi vltozatot tartalmaz kombinatorikus peptid ill.
fehrje knyvtrak szelekcijnak leghatkonyabb mdszerv vlt. Leggyakrabban a biolgiailag jl
feltrkpezett, nem-litikus fonalas M13 fg felsznn fejezik ki a knyvtrat, de litikus fgokon (, T4, T7)
megjelentett knyvtrak is hasznlatosak.
T7-bemutats esetn lrikus, ktszl DNS-t hordoz, E. coli-t fertz T7 vrus felsznn jelentik meg a
fzis fehrjket. A DNS az ikozader formj fejbe pakoldik. A fejet a 10-es gn kt, eltr mret
termke alkotja hatszg s tszg lapokba rendezdve. A kis peptideket tartalmaz knyvtrakat a
nagyobb burokfehrje C-terminlishoz kapcsolva fejezik ki nagy kpiaszmban. Nagyobb fehrjk
kifejezsre csak kisebb kpiaszmban van lehetsg. A lrikus fg hasznlatnak egyik htrnya az, hogy a
fgok elszaporodsa sorn egy sejtet tbb fg is megfertzhet, gy ltrejhet olyan vrus is, ami tbb
knyvtrtagot is kifejez, de kzlk csak az egyik gnjt hordozza.
Az M13 fg hasznlatn alapul knyvtrak elterjedtebbek az egyszerbb kezelhetsg, valamint a
genotpus s a fenotpus kzti fizikai kapcsolat knny biztosthatsga miatt. A fonalas fgok kb. 10 gnt
tartalmaz vrusok, amelyek Gram-negatv baktriumokat fertznek. A virion egy 6,5 nm tmrj, 800-
2000 nm hossz flexibilis plca, melynek hossza a virionba pakolt DNS mennyisgtl, mrettl fgg. A
244
virion 5-fle fehrjbl ll. A f burokfehrje (protein 8, P8) tbb ezer pldnya alkotja a fg burkt. A
virion lezrsrt a sejtbl elsknt tvoz vgn kt burokfehrje (P7, P9) t-t pldnya, mg a msik
vgn kt msik burokfehrje (P3, P6) szintn t-t pldnya felel. A burok belsejben tallhat a fg
genomja, egy, a trzstl fggen 5-8000 bzis mret, cirkulris, egyszl DNS (ssDNS) molekula. Az M13
bakteriofg F-faktort hordoz, azaz konjugatv F-pilussal rendelkez E. coli sejteket fertz. A fertzs sorn
a vrus ssDNS-e bejut a baktrium sejtbe s a sejt klnbz fehrji s enzimei ltal ktszl, replikatv
dsDNS-s alakul. A ktszl formrl trdnak a vrus fehrji. Ha a virlis fehrjk koncentrcija
meghalad egy kszbt, akkor kezdett veszi a vrus genom n. grdl kr (rolling-circle) mechanizmus
szerint trtn replikcija, amelynek sorn a genom virionba pakold szla sokszorozdik meg. A virion
sszeszereldshez szksges fehrjk a baktrium sejt bels membrnjba kerlnek, s integrns
membrnfehrjeknt jtszanak szerepet az sszeszereldsben.
Az M13 bakteriofg felsznn megjelentett knyvtrak ltalban a P3, a P6 vagy a P8 fehrjhez
kapcsoltan fejezik ki a knyvtrfehrjt. A fg-bemutats sorn alkalmazhat vektorok tpusokba oszthatk,
az alapjn, hogy a fziban rintett burokfehrje gnjt milyen formban s hny kpiban hordozzk.
Az n (itt az n az rintett burokfehrje gn szma) tpus fg-genom vektorok a fg sszes gnjnek, gy a
knyvtrfehrjt bemutat fehrje gnjnek (n) is egyetlen kpijt hordozzk. A knyvtrfehrjt kdol
szekvencit az n gnhez illesztik. Az ilyen vektorrl termeld fgok virionja az n gn termknek kizrlag
fzis pldnyt tartalmazza. A 3-tpus vektorral ltrehozott fg csak fzis P3-at kdol s virionja
elvileg csak fzis P3-at tartalmaz, de bakterilis enzimek a knyvtrfehrjt lehasthatjk. A 8-tpus
vektor a f burokfehrje minden pldnyn hordozza a knyvtrfehrjt, ami ebben az esetben nem fehrje,
hanem legfeljebb 8-10 aminosavbl ll peptid, ugyanis hosszabb peptid kifejezse a virion
sszeszereldst akadlyozn. A knyvtrfehrjk tbb, 8-as tpus esetben tbb ezer pldnyban
fejezdnek ki. Ez jelents aviditst okoz: az egy fgon bemutatott fehrje tbb pldnya egyszerre
kapcsoldhat egy-egy ktpartner molekulhoz, gy a fg ltszlagos affinitsa a ktpartnerhez az nll
knyvtrtag affinitsnak sokszorosa is lehet. Az n tpus knyvtrak esetben nem szablyozhat a
bemutats valencija, azaz az, hogy a fg hny pldnyban mutatja be a fzis peptidet (ld. 16.7. bra).
16.7. bra: A fg-bemutatshoz hasznlhat vektor rendszerek
245
Az nn-tpus fg-genom vektorok az egyik burokfehrje gnjnek kt pldnyt tartalmazzk, egy vad
tpust s egy fzisat. Az ilyen vektorrl termeld fgok mozaikosak, az egyik burokfehrjbl fzisat s
vad tpust is tartalmaznak. A fzis gn el szablyozhat promtert helyezve lehetsg van a
fzis/vadtpus arnyt, azaz a bemutats valencijt szablyozni. Az ilyen vektorok alkalmasak nagyobb
peptidek vagy akr egsz fehrjk kifejezsre is. Vgl az n+n-tpus vektorok fgmid konstrukcik
hasznlatn alapulnak.
A fg-bemutats fontos eleme az, hogy a ktpartnerhez kapcsoldni kpes varinsok kpesek
baktriumokban szaporodni. Ennek ksznheten rvid id alatt tbb szelekcis kr alkalmazhat, melyek
vgre a szelektlt knyvtr feldsul a funkcionlisan hatkony klnokban. A fg-bemutats nagy sikerrel
alkalmazhat ktfelsznek energetikai viszonyainak feldertst s biolgiai folyamatokban fontos szerepet
jtsz ktfelsznek kismolekulj, specifikus ligandumai fejlesztst clz kutatsokban.
16.3.3. Rekombinns fehrje knyvtr bemutatsa s szelekcija l sejtek
felsznn
A fg-bemutats egyik gyakran alkalmazott alternatvja a sejt felsznn val bemutats. Ezekkel a
technolgikkal a rekombinns fehrje knyvtr egyes tagjait l sejtek felsznn jelentik meg. A
knyvtrat bemutat sejtek kzl kivlasztjk a partnerhez ktd varinsokat bemutat sejteket, ezeket a
tbbitl elvlasztjk, majd az ltaluk hordozott gneket elemzik. Bizonyos fehrjket nem lehet ms
irnytott evolcis eljrsokkal vizsglni vagy fejleszteni, ezrt klnsen fontos, hogy ma mr lehetsg
van sejtfelsznen trtn bemutatst alkalmazni. Az vek sorn a kutatk kifejlesztettek bakterilis, s
leszt alap rendszereket is.
16.3.3.1. Fehrjk irnytott evolcija baktrium sejtek felsznn
A baktrium sejtek felsznn trtn irnytott evolcit lehetv tev rendszerek a legtbb ponton
hasonltanak a fg-bemutats rendszerekre. A sejtek egyetlen knyvtrtag gnjt tartalmazzk, ezltal csak
ez a fehrje jelenik meg a felsznkn, azaz megvalsul a genotpus s a fenotpus klonlis fizikai
kapcsolata. Fontos eltrs viszont, hogy a rendszerben lv rszecskk, azaz maguk a sejtek sokkal
nagyobbak a fgoknl, valamint a bemutatott fehrje minden esetben sok pldnyban megjelenik a sejt
felsznn. Eltrs az eddig bemutatott rendszerektl az is, hogy a rekombinns fehrje knyvtrat
megjelent sejtek szelekcijt ltalban nem affinits kromatogrfis mdszerrel, hanem
fluoreszcencival aktivlt sejtszortroz berendezs (FACS) segtsgvel vgzik el.
A knyvtrbl val szelekcinak legegyszerbb mdja a fluoreszcensen jellt partnerrel val inkubls oldat
fzisban, majd a jellt sejtek elvlasztsa a jelletlenektl FACS rendszerben. A knyvtrtagokat bemutat
sejteket a knyvtrban vizsglt fehrje fluoreszcensen jellt ktpartnervel inkubljk oldat fzisban. A
partnert ktni kpes vltozatokat bemutat sejtek gy fluoreszcensen jelltt vlnak. A multivalens
bemutatsnak ksznheten a funkcikpes vltozatokat bemutat sejtek elegend fluoreszcensen jellt
partner molekult ktnek meg ahhoz, hogy a FACS berendezs segtsgvel el lehessen vlasztani a jellt s
a jelletlen sejteket egymstl. A FACS kszlken be lehet lltani, hogy milyen intenzits fluoreszcens
jelet ad sejteket gyjtsn kln a tbbitl. A sejtek ltal megkttt jellt fehrjk mennyisge, azaz a jel
intenzitsa arnyos a bemutatott vltozat affinitsval, azaz az n. kszbrtk helyes megvlasztsval
kivlaszthatak a knyvtrbl a legnagyobb affinits vltozatok.
Ezzel a mdszerrel lehetsg van bizonyos antignekre specifikus ellenanyagok fejlesztsre is. Erre a
fg-bemutats is alkalmas, viszont a sejt felsznn val bemutats s FACS rendszerrel trtn szelekcinak
j lehetsgeket is biztost. Az ellenanyagok fontos tulajdonsga a kereszt-reaktivits, azaz az, hogy a
clponthoz hasonl antigneket felismer-e az ellenanyag. A sejt felsznn trtn bemutatssal megoldhat
akr kereszt-reaktv, akr nagyon specifikus ellenanyagok kifejlesztse. Ilyen esetekben a szelekci sorn
tbbfle antignt alkalmaznak, amelyeket klnbz jellssel ltnak el. Ha kereszt-reaktv ellenanyag
246
kifejlesztse a cl, akkor a FACS kszlket gy programozzk, hogy azokat a sejteket gyjtse kln,
amelyek tbbfle fluoreszcens jellst is hordoznak. Ha specifikus ellenanyagot keresnek a knyvtrban,
akkor a sejtek vlogatsa sorn kizrjk a gyjttt mintbl a tbbfle fluorofrral jellt sejteket.
Az elmlt vekben sikeres irnytott evolcis vizsglatokat vgeztek klnbz ellenanyag fragmentumok,
teljes ellenanyagok, rvid peptidek s ms globulris fehrjk baktrium sejtek felsznn bemutatott s
szelektlt knyvtrakkal.
16.3.3.2. Fehrjk irnytott evolcija leszt sejtek felsznn
A rekombinns fehrje knyvtrak leszt sejtek felsznn val megjelentse s szelekcija dinamikusan
fejld terlet. Az leszt felszni bemutats egyedlll lehetsget knl szmos olyan fehrje
vizsglatra, amelyeket ms irnytott evolcis rendszerben nem lehet kifejezni. Az leszt felszni
bemutats rendszerekben olyan fzis gnt hoznak ltre, amelyrl a knyvtr fehrje az leszt
sejtfalba gyazott fehrjk egyikvel sszekapcsoltan termeldik, s ezltal megjelenik az leszt sejt
felsznn. Ezekben a rendszerekben a knyvtrfehrjt glikozil-foszfatidil-inozitol (GPI) horgonnyal elltott
fehrjkkel, vagy azok megfelel rszletvel fziban lltjk el. Ezek a fehrjk a sejten kvl a sejtfal
komponenseivel vagy ms membrnfehrjkkel kovalens ktssel is kapcsoldnak.
Lehetsg van a knyvtrfehrje nem-kovalens bemutatsra is. Ilyen rendszerekben a fzis partner olyan
leszt fehrje, ami a sejtbl kijutva a sejtfal mannn lncaihoz ktdik msodlagos klcsnhatsokon
keresztl. Eukarita transzmembrn fehrjk horgonyknt szolgl fzis partner alkalmazsa nlkl is
kifejezhetek leszt felsznn.
Az leszt felsznn megjelentett knyvtrak szelekcija a baktrium sejt felsznen kifejezett
knyvtrakhoz hasonlan trtnhet szilrd felsznhez rgztett partner molekulkhoz val ktds
alapjn, vagy fluoreszcensen jellt partner s FACS alkalmazsval.
Az leszt felszni bemutatst leggyakrabban ms molekulkhoz ktni kpes fehrjk ktfelsznnek
feltrkpezsre, vagy a vad tpus molekulnl nagyobb affinits, esetleg megvltozott specifits
vltozatok kifejlesztsre hasznljk. Ezzel a mdszerrel szmos specifikus s nagy affinits ellenanyagot
sikerl kifejleszteni klnbz antignekkel szemben.
16.4. Tovbbi olvasnival a fejezethez
Sidhu S. S. (2005) (szerk) Phage display in biotechnology and drug discovery. Taylor&Francis
Smith G. P. s Petrenko V. A. (1997) Phage Display. Chemical Reviews 97, 391410.
Minshull J. s Stemmer W. P. (1999) Protein Evolution by Molecular Breeding. Current Opinion in
Chemical Biology 3, 284290.
Diaz J. E. s mtsai. (2003) Exploring Biochemistry and Cellular Biology with Protein Libraries. Current
Issues in Molecular Biology 5, 129145.
Pepper, L. R. s mtsai. (2008) A Decade of Yeast Surface Display Technology: Where Are We Now?
Combinatorial Chemistry & High Throughput Screening 11, 127134.
Lfblom, J. Bacterial Display in Combinatorial Protein Engineering. Biotechnology Journal 6, 11151129.
247
17. Klcsnhatsok kimutatsa gntechnolgiai
mdszerekkel
A fehrjk klcsnhatsainak kimutatsa az 1990-es vek elejig gyakran nehezen lekzdhet akadlyokat
grdtett a kutatk tjba. A gntechnolgia eszkztrnak fejldse s a biolgiai folyamatok molekulris
szinten val egyre rszletesebb megismerse egytt tette lehetv a klcsnhatsok kimutatsra szolgl
technikk kifejlesztst az 1980-as vek msodik feltl. A fehrjk ms fehrjkkel, DNS-sel vagy kis
molekulkkal az l sejtben kialaktott klcsnhatsainak kimutatsra alkalmas in vivo mdszerekre nagy
igny mutatkozott az alap- s az alkalmazott kutatsban egyarnt. Az leszt kt-hibrid (yeast two-hybrid)
eljrs volt az egyik els, erre alkalmas eljrs.
17.1. Az leszt kt-hibrid rendszer bemutatsa
Az leszt kt-hibrid rendszer s annak klnbz vltozatai a fehrjk ms molekulkkal kialaktott
interakciinak kimutatsra szolgl, teljes egszben in vivo rendszerek. A mdszercsald klnbz
vltozatainak alkalmazsval lehetsg van fehrje-fehrje, fehrje-DNS, fehrje-kismolekula
klcsnhatsok kimutatsra. A mdszerek alkalmasak az irnytott evolcis technikknl alkalmazott
knyvtrakbl trtn szelekcira is. Ezekben az esetekben egy fehrje rengeteg vltozata kzl vlasztjk
ki azokat, amelyek kpesek ktni a vizsglatban alkalmazott partnerhez. Az leszt kt-hibrid mdszert
azonban gyakrabban alkalmazzk arra is, hogy nagyszm klnbz fehrjt tartalmaz knyvtrbl
kimutassk azokat a fehrjket, amelyek ktnek az alkalmazott partnerhez vagy partnerekhez. A fentiek
rtelmben az leszt kt-hibrid rendszer alkalmazsa sorn nem egyetlen interakci rszletes
feltrkpezst vgzik el, hanem a sejten bell ltrejv, fiziolgis vagy patolgis folyamatokban relevns
klcsnhatsokat keresnek.
Az elsknt lert leszt kt-hibrid technika elnevezse arra utal, hogy ebben a rendszerben ktfle hibrid,
azaz fzis fehrjt alkalmaznak a klcsnhats kimutatsra. Az eljrs azon alapul, hogy a gntrst
serkent transzkripcis faktorok modulris felpts, tbb domnbl ll fehrjk. Bizonyos domnek
felelsek a megfelel DNS szakaszok (upstream szablyoz elemek) specifikus megktsrt (DKD: DNS-
kt domn). Ms domnek a transzkripci inicicijrt felels fehrjkkel alaktanak ki klcsnhatst s
a klcsnhatsokon keresztl serkentik a gn transzkripcijt (transzkripcit aktivl domn, TAD). A
gntrs serkentshez a kt domnnek egy idben kell jelen lennie a gn promternl, de nem felttlenl
kell egyetlen polipeptidlncon bell, kovalensen sszektve lennik, a klcsnhatsuk lehet kzvetett. A kt
nll fehrjeknt ellltott DKD s TAD domnek nem ismerik fel egymst, nem lpnek egymssal
klcsnhatsba. Azonban ha az egyiket egy A fehrjhez, a msikat pedig egy B fehrjhez fuzionljuk,
akkor amennyiben az A s B fehrjk egymst felismerik, gy a ktdsk miatt megvalsul a DKD s
TAD domnek trbeni kzelsge. A DKD rvn a komplex a megfelel helyen lokalizldik s a TAD
kpes serkenteni azoknak a gneknek a kifejezdst, amelyek szablyoz rgija tartalmazza az
alkalmazott DKD ltal felismert szekvencit. Az leszt kt-hibrid rendszerekben az A sB fehrjk
klcsnhatsa egy riporter gn trdst eredmnyezi. A riporter gn kifejezdse alapjn vlasztjk ki
azokat a klnokat, amelyekben kialakult az A s B fehrje kzti kapcsolat.
Az eredeti leszt kt-hibrid rendszerben a S. cerevisiae Gal4 transzkripcis faktor DKD s TAD
domnjt hasznltk. A Gal4 transzkripcis faktor szksges a LacZ riporter gn aktivlshoz. A LacZ
gn termke, a -galaktozidz enzim. Azok a sejtek kk sznek lesznek X-Gal kromogn szubsztrt
analgot tartalmaz kzegben, amelyekben a riporter gn kifejezdik. A vizsglatok sorn olyan leszt
trzseket alkalmaznak, amelyekben nem termeldik a riporter gn termke. Ennek ksznheten a riporter
fehrje csak akkor jelenhet meg, ha az A s B fehrje klcsnhatsba lp egymssal (ld. 17.1. bra)
248
17.1. bra: Az leszt kt-hibrid rendszer smja
Az leszt kt-hibrid rendszerben a DKD domnhez fzionljk az gynevezett csali fehrjt (bait). Egy
vizsglatban egyfle csali fehrjt alkalmaznak, a vizsglat clja a csali fehrje ktpartnereinek
azonostsa. A TAD domnhez fuzionljk az gynevezett prda fehrjt (pray) vagy fehrjket. A prda
lehet egyetlen fehrje knyvtra, de gyakrabban alkalmaznak sok ismert vagy ismeretlen fehrjt tartalmaz
cDNS knyvtrakat. A ktfle plazmiddal ezutn leszt sejteket transzformlnak, majd kivlasztjk a
rendszerbl azokat a sejteket, amelyekben kifejezdtt a riporter gn a csali s a prda fehrje
klcsnhatsnak kvetkeztben. A sejtek szelekcijra tbbfle lehetsg van. A fent bemutatott LacZ
riporter gn hasznlata sorn azok a sejtek kk sznek lesznek X-Gal jelenltben, amelyekben a riporter
gn kifejezdik. Ebben az esetben azok a sejtek is letkpesek, amelyekben nincs klcsnhats a csali s a
prda fehrje kztt. A szelekcis eljrsok msik tpusa sorn a 13.1.2. fejezetben bemutatott auxotrf
trzset hasznlnak, a riporter gn pedig az, amelynek mutcija a trzset auxotrff teszi. HIS3 szelekcis
marker esetn az egyik plazmid tartalmazza a hisztidin bioszintzishez szksges, az alkalmazott trzsben
hibs enzim gnjnek j kpijt. A gn olyan promterrel van elltva, amirl csak akkor rdhat t a
fehrje, ha a csali-prda interakci biztostja a TAD jelenltt a promteren szervezd fehrje komplexben.
A csali plazmidot s a prda-knyvtr egy tagjt tartalmaz sejteket ezutn hisztidin mentes tpkzegben
nvesztik. Csak azok a sejtek lnek tl s kpesek nvekedni, amelyekben a csali s a prda klcsnhatsba
lp egymssal s trdik a hisztdin bioszintzishez nlklzhetetlen fehrje.
17.2. Az leszt kt-hibrid rendszer gyengesgei
Az leszt kt-hibrid rendszer vitathatatlan elnye, hogy l sejteken bell, in vivo lehet a segtsgvel
fehrjk klcsnhatsait kimutatni. Sajnos azonban a rendszernek szmos olyan korltja is van, amelyek
ismeretben az leszt kt-hibrid vizsglatok sorn szerzett informcikat, az azonostott klcsnhat
partnereket fenntartsokkal kell kezelni, illetve tovbbi tesztekben igazolni kell azok valdisgt.
Az leszt kt-hibrid vizsglatok nagy arnyban eredmnyeznek hamis pozitv tallatokat, azaz az
azonostott ktpartner az l rendszerben nem partnere a csali fehrjnek. Elmondhat az is, hogy az
leszt kt-hibrid ksrletek nem mutatnak ki szmos olyan klcsnhatst, amelyek egybknt
megvalsulnak s relevnsak, azaz a hamis negatv eredmnyek arnya is jelents. Hamis pozitv
tallatokat eredmnyez a fzis fehrjk intenzv expresszija. Ennek ksznheten azok nagy
koncentrciban vannak jelen, ezrt gyenge, a fehrjk normlis koncentrcija mellett ki sem alakul
klcsnhatsok is ltrejhetnek. Amikor az leszt sejtben egyszerre expresszldnak, akkor olyan fehrjk
kztt is kialakulhat klcsnhats, amelyek a valsgban soha nem fordulnak el egy idben ugyanannak a
sejtnek ugyanabban a kompertimentumban. Hamis negatv tallatokat, azaz relevns interakcik
kimutatsnak elmaradst okozhatja, ha a fehrjk interakcis felszne a fzis fehrjben nem
hozzfrhet, mert azt a fzis partner eltakarja. Ms llnybl szrmaz fehrjk helyes feltekeredse
vagy a mkdshez szksges poszttranszlcis mdostsa nem biztos, hogy megfelelen vgbemegy az
leszt sejtben, ami szintn azt eredmnyezi, hogy nem alakul ki a klcsnhats a fehrjk kztt. Az
leszt kt-hibrid rendszerben a klcsnhats helye a sejtmag. Elkpzelhet, hogy kt, ms
249
kompartimentumban klcsnhat fehrje a sejtmagban uralkod krlmnyek kztt nem ismeri fel
egymst.
A fentiek miatt az leszt kt-hibrid ksrletek sorn azonostott interakcis partnereket minden esetben
igazolni kell ms, megbzhatbb mdszerrel is. A mdszer korltait ellenslyozza az egyszersge s
gyorsasga. A mai napig szles krben hasznljk a vizsglt fehrjk potencilis partnereinek gyors
azonostsra.
17.3. Hasonl alapokon mkd technikk
Az leszt kt-hibrid rendszerhez hasonl technikk sort fejlesztettk ki az elmlt kt vtizedben. Ezek
egyrszt olyan klcsnhatsok vizsglatra alkalmasak, amelyekre az eredeti rendszer alkalmazsval nincs
lehetsg, msrszt az eredeti rendszer hinyossgainak kikszblsre knlnak megoldst. A
kvetkezkben bemutatott technikk az irnytott evolcis rendszerekhez hasonlan egy adott klcsnhats
feltrkpezsre, vagy j klcsnhat molekulk kifejlesztsre alkalmazhatak.
17.3.1. Fordtott kt-hibrid rendszerek
A fordtott (reverz) kt-hibrid rendszerek alkalmasak egy adott klcsnhats kialakulsa szempontjbl
kritikus aminosavak feltrkpezsre. Ezek a rendszerek olyan riporter gneket alkalmaznak, amelyek
termke a sejt szmra toxikus. Ennek kvetkeztben azok a sejtek maradnak letben, amelyekben a csali s
a prda interakcija a csali fehrje mutcija kvetkeztben nem jn ltre. A tll sejtek ltal kifejezett
csali fehrjk gnjeinek vizsglatval megllapthat, hogy milyen mutci vagy mutcik voltak felelsek
a kt fehrje kzti klcsnhats kialakulsnak megakadlyozsrt (ld. 17.2. bra).
17.2. bra: Reverz leszt kt-hibrid rendszer
17.3.2. Egy-hibrid rendszerek
Az egy-hibrid rendszerekben egyetlen fzis fehrjt alkalmaznak. A leggyakrabban adott DNS
szekvencit felismer DKD kifejlesztsre, vagy adott DKD ltal felismert DNS szekvencia megkeressre
hasznljk. Elbbi esetben a riporter fehrje gnjnek szablyoz rgijba ptik az adott DNS szekvencit.
A ksrlet sorn alkalmazott fzis fehrje egy DKD-hez fzionlt TAD konstrukci. A DKD DNS ktsrt
felels aminosav pozciit randomizljk, gy DKD knyvtrat hoznak ltre. A szelekci sorn azokban a
sejtekben fejezdik ki a riporter fehrje, amelyekben a DKD varins felismeri a riporter gn szablyoz
rgijba ptett DNS szekvencit. Az utbbi esetben a riporter gn szablyoz rgijba nem egy konkrt
DNS szekvencit ptenek be, hanem DNS knyvtrat hoznak ltre. A knyvtrbl aztn egy DKD-TAD
fzis fehrjvel kivlasztjk azokat a vltozatokat, amelyekhez a DKD ktni kpes (ld. 17.3. bra).
250
17.3. bra: Az leszt egy-hibrid rendszer. Az leszt egy-hibrid rendszer alkalmazhat egy adott DKD ltal
felismert DNS szekvencia megkeressre vagy adott DNS szekvencit felismer DKD kifejlesztsre.
17.3.3. Hrom-hibrid rendszerek
A hrom-hibrid rendszerek hrom fzis fehrje vagy hibrid molekula alkalmazsval mutatjk ki a
keresett interakcit. Klnbz vltozatai alkalmasak fehrje-RNS s fehrje-kismolekula
klcsnhatsok, valamint enzimatikus aktivits kimutatsra is.
A fehrje-kismolekula interakci kimutatsra szolgl vizsglatok sorn ltalban kismolekula
knyvtrakbl vlogatjk ki azokat a gygyszer hatanyag jellt molekulkat, amelyek ktnek egy adott
gygyszer clpont fehrjhez. Az ilyen vizsglatok sorn a DKD domnhez egy olyan fehrjt fuzinlnak,
amelynek ismerik ers s specifikus kismolekula partnert. A TAD domnhez fzionljk a gygyszer
clpont fehrjt. A vizsglat sorn olyan hibrid kismolekula knyvtrat hasznlnak, amelynek tagjai a
tesztelt gygyszer hatanyag jellt csoportok mellett tartalmazzk a DKD domnhez kapcsolt fehrje
kismolekula ligandumt is. A kismolekula knyvtr tagjai az ismert ligandumon keresztl kapcsoldnak a
DKD fzis fehrjhez. A vizsglat sorn sejttenyszt lemezek mintahelyein leszt sejteket nvesztenek,
s minden mintahelyhez hozzadjk a hibrid kismolekula knyvtr egy tagjt. Ha az adott knyvtr tag
gygyszer hatanyag jellt csoportja kapcsoldik a gygyszerclpont fehrjhez, akkor kifejezdik a
riporter fehrje. A riporter gn kifejezdse alapjn felttelezheten a gygyszer clpont fehrjhez kt
kismolekulkat ksbb megbzhatbb mdszerekkel is tesztelik (ld. 17.4. bra).
17.4. bra: Gygyszer hatanyag jellt molekulk kivlasztsa kismolekula knyvtrbl leszt hrom-hibrid
mdszerrel
251
17.3.4. Tovbbi olvasnival a fejezethez
Fields S. and Song O. (1989) A Novel Genetic System to Detect Protein-protein Interactions. Nature 340
(6230): 245246.
Fields S. (2009) Interactive Learning: Lessons from Two Hybrids over Two Decades. Proteomics 9 (23):
52095213.
Hamdi A. and Colas P. (2012) Yeast Two-hybrid Methods and Their Applications in Drug Discovery.
Trends in Pharmacological Sciences 33 (2): 109118.
Stynen B. Tournu H. Tavernier J. and Van Dijck P. (2012). Diversity in Genetic in Vivo Methods for
Protein-protein Interaction Studies: From the Yeast Two-hybrid System to the Mammalian Split-luciferase
System. Microbiology and Molecular Biology Reviews 76 (2): 331382.
252
18. Fggelk
Nhny gntechnolgiai mdszer animcija:
Hibridizci (forrs: http://www.youtube.com/watch?v=76eKnmCtCTU)
18.1. animci: Hibridizci
Fluorescens in situ hibridizci (FISH; forrs: http://www.youtube.com/watch?v=BBQWWi6cFXU)
18.2. animci: Fluoreszcens in situ hibridizci
DNS-chip (microarray; forrs: http://www.youtube.com/watch?v=3jX_08zdYCE)
18.3. animci: DNS-chip (microarray)
253
DNS szekvenls lnctermincis mdszerrel (forrs: http://www.youtube.com/watch?v=oYpllbI0qF8)
18.4. animci: DNS szekvenls lnctermincis mdszerrel
Polimerz lncreakci (PCR; forrs: http://www.youtube.com/watch?v=QaWLJVGEFi8)
18.5. animci: Polimerz lncreakci
You might also like
- TételDocument5 pagesTételViki100% (2)
- A Kvantumkémia AlapjaiDocument404 pagesA Kvantumkémia Alapjaipollinctor100% (1)
- 4 - TételDocument4 pages4 - TételViki100% (1)
- Taplalkozas-Es Elelmiszertudomanyi Doktori Iskola Kepzesi Terv 2022 0Document76 pagesTaplalkozas-Es Elelmiszertudomanyi Doktori Iskola Kepzesi Terv 2022 0Bence KlusóczkiNo ratings yet
- Utam A CsucsraDocument245 pagesUtam A CsucsraCsaba AlbertNo ratings yet
- Az Élet Keletkezése És FejlődéseDocument46 pagesAz Élet Keletkezése És FejlődéseMaria MillerNo ratings yet
- Növényi Nyersanyagok Feldolgozástechnológiai MűveleteiDocument248 pagesNövényi Nyersanyagok Feldolgozástechnológiai MűveleteiVeres ZsuzsiNo ratings yet
- Tej És Tejtermékek TáplálkozásbanDocument463 pagesTej És Tejtermékek Táplálkozásbanpollinctor100% (1)
- A Növényi Alapú Alternatív Tej Egészségügyi Kérdései És Technológiai SzempontjaiDocument17 pagesA Növényi Alapú Alternatív Tej Egészségügyi Kérdései És Technológiai SzempontjaiNikolett NagyNo ratings yet
- Mihail Bulgakov: Mester Es MargaritaDocument281 pagesMihail Bulgakov: Mester Es MargaritaTunde Kiss80% (5)
- TételDocument5 pagesTételVikiNo ratings yet
- Oeti Magyarorszag Nemzeti Taplalkozaspolitikaja 2004Document32 pagesOeti Magyarorszag Nemzeti Taplalkozaspolitikaja 2004..No ratings yet
- Az ImmunrendszerDocument66 pagesAz ImmunrendszerRenáta FerencziNo ratings yet
- Muszeres Es BioanalitikaDocument134 pagesMuszeres Es BioanalitikaKatalinNo ratings yet
- Ipari Mikrobiologia II IIIDocument232 pagesIpari Mikrobiologia II IIISzabó TamásNo ratings yet
- Szövettani És Sejtbiológiai VizsgálómódszerekDocument273 pagesSzövettani És Sejtbiológiai VizsgálómódszerekÁdámszki SzabolcsNo ratings yet
- GyogyszKemia 2Document212 pagesGyogyszKemia 2KatalinNo ratings yet
- A Sport TorteneteDocument7 pagesA Sport TorteneteLészai IldikóNo ratings yet
- LC Kromatográfia - Oktatási SegédanyagDocument7 pagesLC Kromatográfia - Oktatási SegédanyagÉva Nikolett MelegNo ratings yet
- 09.01.A SejtDocument8 pages09.01.A SejtMolnár GyulaNo ratings yet
- Gyogyszermetabolizmus Es GyogyszertoxicitasDocument146 pagesGyogyszermetabolizmus Es GyogyszertoxicitascsavassNo ratings yet
- Biokemia KérdésekDocument6 pagesBiokemia Kérdésekelisabeth_pepperNo ratings yet
- Az Információkezelés Elmélete És Gyakorlata Az EgészségügybenDocument192 pagesAz Információkezelés Elmélete És Gyakorlata Az Egészségügybenkom1No ratings yet
- Etelallergiak-Dr-Fajcsak-Zsuzsanna - Lúgosítás A Kor-Talanság Útja I-II - KötetDocument9 pagesEtelallergiak-Dr-Fajcsak-Zsuzsanna - Lúgosítás A Kor-Talanság Útja I-II - KötetAnonymous 0uBSrduoNo ratings yet
- Dr. KERTÉSZ Pál: Építészeti Geológia, Tankönyvkiadó, Budapest, 1972Document158 pagesDr. KERTÉSZ Pál: Építészeti Geológia, Tankönyvkiadó, Budapest, 1972klanyimNo ratings yet
- Gyógyszerészi Kémia Jegyzet - Általános - RészekDocument44 pagesGyógyszerészi Kémia Jegyzet - Általános - RészekZelei ÁgostonNo ratings yet
- Elemit PDFDocument175 pagesElemit PDFKlaudia VidákNo ratings yet
- Immunrendszer KórélettanaDocument23 pagesImmunrendszer KórélettanaNikolett NagyNo ratings yet
- TételDocument4 pagesTételViki100% (1)
- Gyógyszerkémiai AlapfolyamatokDocument238 pagesGyógyszerkémiai AlapfolyamatokAmaziszNo ratings yet
- Nemeth Aron Ipari MikrobiologiaDocument140 pagesNemeth Aron Ipari MikrobiologiaBaloghAndrastuNo ratings yet
- Utmutato Zsiregeteshez PDFDocument64 pagesUtmutato Zsiregeteshez PDFViktória HosszúNo ratings yet
- Komsa Fruzsina Tóth Miklós - Szervetlen Kémia. Összefoglalás Orvostanhallgatók Számára WWW - Semmelweiskiado.hu (Trid:44031)Document28 pagesKomsa Fruzsina Tóth Miklós - Szervetlen Kémia. Összefoglalás Orvostanhallgatók Számára WWW - Semmelweiskiado.hu (Trid:44031)Fruzsina Eniko KomsaNo ratings yet
- Rextra 2014 OnlineDocument148 pagesRextra 2014 OnlineTamásKureczNo ratings yet
- Nanotechnológia Eszközei 2 - Top-Down MódszerekDocument162 pagesNanotechnológia Eszközei 2 - Top-Down MódszerekErik Szilard AcsNo ratings yet
- Sejtalkotok JDocument50 pagesSejtalkotok Jangelika6ill6s100% (1)
- Török Tamás - Korszerű FelületkezelésDocument762 pagesTörök Tamás - Korszerű FelületkezelésBelaba100% (2)
- Cserkeszet Fiuknak 1 PDFDocument182 pagesCserkeszet Fiuknak 1 PDFTamasgall100% (1)
- Hemosztazis SzabalyozasDocument45 pagesHemosztazis SzabalyozasDan DNo ratings yet
- Elelmiszertechnologia Alapjai II LevelezoDocument155 pagesElelmiszertechnologia Alapjai II LevelezoÁdám Rónai0% (1)
- Elelmiszeripari-Kezikonyv Alapfogalmak1 165x230 OnlineDocument149 pagesElelmiszeripari-Kezikonyv Alapfogalmak1 165x230 OnlineGyurmoooNo ratings yet
- 8 Előadás-05052017bDocument53 pages8 Előadás-05052017bkereklovagNo ratings yet
- Nemzetközi Fejlesztés Az ÉghajlatvédelemértDocument50 pagesNemzetközi Fejlesztés Az ÉghajlatvédelemértKataNo ratings yet
- Endokrin4 Szteroidok MVK NemiDocument87 pagesEndokrin4 Szteroidok MVK NemiThomas ChurchNo ratings yet
- 3 KotetDocument222 pages3 KotetCsilla BustyaNo ratings yet
- Graceborley Rovid Sebeszeti DiagnosztikaDocument170 pagesGraceborley Rovid Sebeszeti DiagnosztikacedruspluszNo ratings yet
- Biológia IIIDocument140 pagesBiológia IIIMazel TovNo ratings yet
- 0028 Szilagyi Fizikai Kemia LabgyakDocument25 pages0028 Szilagyi Fizikai Kemia LabgyakFehér MercédeszNo ratings yet
- Eszes Ferenc - Húsipari Technológia - 2010Document206 pagesEszes Ferenc - Húsipari Technológia - 2010Szekrényi KrisztaNo ratings yet
- Baktérium Lista - KockiDocument9 pagesBaktérium Lista - KockiKincsőNo ratings yet
- Az Öregedés ÉlettanaDocument18 pagesAz Öregedés ÉlettanabolcsbekaNo ratings yet
- Táplálkozási BetegségekDocument52 pagesTáplálkozási BetegségekLevente BalázsNo ratings yet
- 2011-0028 NovenytanDocument392 pages2011-0028 NovenytanAndrea Farkas100% (1)
- Fulop Emoke Szovettan MDI LMDocument434 pagesFulop Emoke Szovettan MDI LMAdriana VillarrealNo ratings yet
- SejtbiológiaDocument45 pagesSejtbiológiakereklovagNo ratings yet
- 0028 MoczoGy MuanyagokDocument100 pages0028 MoczoGy MuanyagokNorbert VolkNo ratings yet
- Altalanos KemiaDocument5 pagesAltalanos KemiaArany GittaNo ratings yet
- Neparaczki PHDDocument110 pagesNeparaczki PHDHőgyes KárolyNo ratings yet
- 05 Genomika 2Document19 pages05 Genomika 2Sandor VargaNo ratings yet
- Sejtbiológia Alapkövetelmény TételekjsjdksDocument42 pagesSejtbiológia Alapkövetelmény Tételekjsjdksnayana grey100% (1)
- Rozsa Csilla TezisfuzetDocument28 pagesRozsa Csilla TezisfuzetNagy DóraNo ratings yet
- Emmre 2021Document12 pagesEmmre 2021Nagy DóraNo ratings yet
- Állat 2. KidolgozásDocument100 pagesÁllat 2. KidolgozásNagy Dóra100% (2)