Professional Documents
Culture Documents
Prigusivanje
Prigusivanje
Uploaded by
mferi92Original Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Prigusivanje
Prigusivanje
Uploaded by
mferi92Copyright:
Available Formats
Priguivanje
se javlja
pri
strujanju
fluida
kroz
cevovode. Zapravo, ono
je
vezano
za
pad
pritiska
tokom
strujanja. Kao posledica
priguivanja
menja
se temperatura
fluida.
Temperatura
moe da
se smanji
ili
povea, u zavisnosti
od
konkretnih
uslova.
Sa TD aspekta
posmatrano, priguivanje
je
proces
pri
h=const
PRIGUIVANJE
P1,v1,T1 P2,v2,T2
P1>P2
Priguivanje
su
eksperimentalno
pratili
Joule i Thomson na
jednostavnoj
aparaturi.
Provoenjem
gasa
kroz
epove
razliite
gustine, menjali
su
otpor
i merili
promenu
temperature
Porozni
ep
kao
otpor
Zakljuak:
za
isto
ulazno
stanje
ima
toliko
izlaznih
stanja
koliko
je
otpora
primenjeno.
(tj. izlaznih
pritisaka)
u
i
5
i
3
i
2
i
1
i
4
Niz
moguih
izlaznih
stanja,
pri
emu
su
temperature na
izlazu
vie, jednake
ili
nie
od
ulazne.
STANJA NAKON
PRIGUIVANJA
h
P
T
|
|
.
|
\
|
c
c
=
Kvantifikacija
promene
temperature sa
promenom
(smanjenjem) pritiska
gasa
pri
strujanju, postie se uvodjenjemJoule-Thomsonovog
koeficijenta:
U sluaju
idealnog
gasa m=0, ali
i realan
gas moe se nai u izlaznim
stanjima
tako
da
mu
je
t1=t2.
Imajui u vidu
da
je
DP<0, vai:
1.
m<0 gas se greje
2.
m=0 ne
menja t
3.
m>0 gas se hladi
Priguivanje idealnog gasa
Ovaj
zakon priguivanja vredi
za
sve
fluide, realne
i idealne. Posebno, za
idealne gasove entalpija
zavisi samo
od
temperature:
i zakljuujemo
da
e pri
priguivanju
temperatura idealnih gasova
ostati
nepromenjena:
Na osnovi
ovog
zakljucka
ne
sme
se priguivanje (neravnoteni
proces) poistovetiti
s
izotermnom
(ravnotenom) promjenom! Ipak, u grafikim
prikazima
za
idealne
gasove priguivanje
i linija
izoterme
se poklapaju, ali
se priguivanje
prikazuje
s isprekidanom
linijom.
Nije politropski puna linija
nego isprekidana
0 =
|
|
.
|
\
|
c
c
h
P
T
Na bazi
merenja
mogu
se
formirati
dijagrami
na
slici:
Oblasti grejanja i hlaenja (azot)
( )
i l u
mh z zmh mh + = 1
l g
u i
l i
u i
h
h h
h h
h h
z
=
Ako
se priguivanje
ponavlja
sukcesivno, mogu
se postii vrlo
niske
temperature, tako
da
se gasovi
prevedu
u teno stanje. Taj
postupak
predloio
je
Linde.
ENERGETSKI BILANS
Priguivanje i likvefakcija gasova
You might also like
- Tekst ZadatakaDocument14 pagesTekst Zadatakamferi92No ratings yet
- Tekst ZadatakaDocument272 pagesTekst Zadatakamferi92No ratings yet
- 12 Treci ZakonDocument4 pages12 Treci Zakonmferi92No ratings yet
- 22 Predavanje-AminokiselineDocument10 pages22 Predavanje-Aminokiselinemferi92No ratings yet
- 8 - Drugi ZakonDocument15 pages8 - Drugi Zakonmferi92No ratings yet
- 11 Max RadDocument13 pages11 Max Radmferi92No ratings yet
- 9 - Konverzija Energije - TD SkalaDocument21 pages9 - Konverzija Energije - TD Skalamferi92No ratings yet
- 3 - Nulti ZakonDocument11 pages3 - Nulti Zakonmferi92No ratings yet
- 2 - Osnovni PojmoviDocument8 pages2 - Osnovni Pojmovimferi92No ratings yet
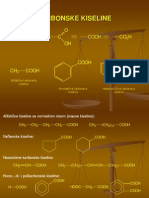
- 18.Predavanje-Karbonske KiselineDocument18 pages18.Predavanje-Karbonske Kiselinemferi92100% (1)
- 21.Predavanje-Supstituisane KiselineDocument17 pages21.Predavanje-Supstituisane Kiselinemferi92No ratings yet
- 23.Predavanje-Heterocikli, Metaloorganska Jed. I Slobodni RadikaliDocument25 pages23.Predavanje-Heterocikli, Metaloorganska Jed. I Slobodni Radikalimferi92No ratings yet
- 19.Predavanje-Karbonske Kiseline-Nezasicene I DikarbonskeDocument14 pages19.Predavanje-Karbonske Kiseline-Nezasicene I Dikarbonskemferi92No ratings yet
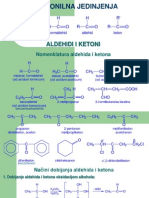
- 17.predavanje - Karbonilna JedinjenjaDocument18 pages17.predavanje - Karbonilna Jedinjenjamferi92No ratings yet
- 23.Predavanje-Heterocikli, Metaloorganska Jed. I Slobodni RadikaliDocument25 pages23.Predavanje-Heterocikli, Metaloorganska Jed. I Slobodni Radikalimferi92No ratings yet