Professional Documents
Culture Documents
Rozróżnianie Anionów
Rozróżnianie Anionów
Uploaded by
Andżelika LorencOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Rozróżnianie Anionów
Rozróżnianie Anionów
Uploaded by
Andżelika LorencCopyright:
Available Formats
Analiza nieorganiczna jakociowa.
Analiza anionw W odrnieniu od kationw, aniony analizuje si bez systematycznego rozdziau (nie ma grup analitycznych anionw). Korzystamy jednak z pewnych wsplnych wasnoci chemicznych, za analiz prowadzi si metod eliminacji. Stwierdza si obecno anionw: lotnych; strcanych przez Ag+; strcanych przez Ba2+; utleniajcych; redukujcych. Reakcje wstpne. Roztwr lub sta prbk zakwaszamy rozcieczonym HCl lub H2SO4: Jeeli nie ma zapachu ani widocznego wydzielania si gazu, tzn. e nie ma S2-, CO32-, SO32-, S2O32-, CN-, ClO-, NO2-, CH3COOClO- : knie, ostry zapach BrO3- (w obecn. Br- lub I-): Br2 lub I2 IO3- (w obecn. Br- lub I-): I2 S2-: zapach, bibua nasyc. Pb(CH3COO)2 czernieje SO32-: zapach (ale nie ma pcherzykw gazu) S2O32-: zapach SO2, mtnieje (S) NO2-: brunatne opary, zapach CO32-: pcherzyki gazu, woda barytowa mtnieje CH3COO-: zapach octu (po podgrzaniu) CN-: zapach migdaw Sta prbk zadajemy stonym H2SO4: F-: ostry zapach HF; krople spywaj po szkle Cl-: HCl, biae dymy z NH4OH, kropla AgNO3 mtnieje Br-: HBr + Br2 I-: ju na zimno utleniaj si do I2 ClO3-: ty gazowy ClO2 (wybuchowy rozkad!) BrO3-: wolny Br2: 4HBrO32Br2+5O2+2H2O IO3-: I2 (po ogrzaniu) NO2-: brunatne NO + NO2 S2-: SO2 NO3-: brunatne NO + NO2 SO32-: SO2 C2O42-: CO + CO2 S2O32-: SO2 + S Obojtny roztwr zadajemy 2% AgNO3:
J. Gliski, w. 4, p. 1
Osady nierozpuszczalne w HNO3: Cl-: biay, fioletowieje na wietle, rozp. w NH4OH Br-: tawy, zielenieje na wietle, rozp. w NH4OH I-: ty, nierozp. w NH4OH, rozp. w KCN CN-: biay, rozp. w NH4OH i nadmiarze CNSCN-: biay, rozp. w NH4OH i nadmiarze SCNS2-: czarny, nierozp. w NH4OH Osady rozpuszczalne w HNO3: PO43-: ty, rozp. w rozc. NH4OH NO2-: biay, rozp w gorcej wodzie CO32-: biay, rozp. w rozc. NH4OH C2O42-: biay, rozp. w rozc. NH4OH CrO42-: czerwonobrunatny, rozp. w rozc. NH4OH AsO33-: brunatny, rozp. w rozc. NH4OH AsO43-: ty, rozp. w rozc. NH4OH [Fe(CN)6]4-: biay, le rozpuszcz. w NH4OH i HNO3 [Fe(CN)6]3-: pomaraczowy, rozp. w NH4OH i HNO3 Obojtny roztwr zadajemy 5% BaCl2: SO42-: biay, nierozp. w rozc. i st. HCl F-: biay, rozp. w st. HCl SO32-, S2O32-, CO32-, C2O42-, PO43-, AsO33-, AsO43-: biae, rozpuszcz. w HCl CrO42-: ty, rozpuszcz. w HCl Lekko zakwaszony H2SO4 roztwr zadajemy 2% KI i dodajemy skrobi: ClO-, ClO3-, BrO3-, IO3-, NO2-, Cr2O72-, AsO43-, MnO4-, [Fe(CN)6]3- : wydziela si I2 Reakcja z I2: roztwr zadajemy roztworem I2 w 10% KI z dodatkiem skrobi: S2-, SO32-, S2O32-, CN- : roztwr si odbarwia
J. Gliski, w. 4, p. 2
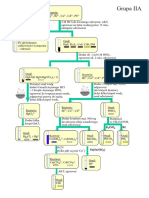
Reakcja z MnO4-: lekko zakwaszony H2SO4 roztwr zadajemy 0.1 M roztworem KMnO4: S2-, SO32-, S2O32-, CN-, SCN-, Br-, I-, NO2-, AsO33-: roztwr si odbarwia Analiza anionw - grupy analityczne wg Bunsena grupa 1 2 3 reakcja grupowa Ag+ wytrca osad rozpuszczalny w rozciecz. HNO Ba2+ nie wytrca osadu Ag+ wytrca osad rozpuszczalny w HNO3 Ba2+ nie wytrca osadu Ag+ wytrca biay osad rozpuszczalny w HNO aniony Cl-, Br-, CN-, NCS-, ClO-, [Fe(CN)6]4-, [Fe(CN)6]3S2-, CH3COO-, NO2SO32-, CO32-, C2O42-, C4H4O62-, BO2S2O32-, CrO42-, Cr2O72-, AsO33-, AsO43-, PO43NO3-, ClO3-, ClO4-, MnO4SO42-, F-, SiF62SiO32(Przy odparowywaniu ze st. HCl tworzy si nierozpuszczalny osad)
3 2+ Ba wytrca biay osad rozpuszczalny w HNO3 Ag+ wytrca barwny osad rozpuszcz. w HNO3 Ba2+ wytrca osad rozpuszczalny w HNO3 Ag+ nie wytrca osadu Ba2+ nie wytrca osadu Ag+ nie wytrca osadu Ba2+ wytrca osad Ag+ wytrca ty osad rozpuszcz. w HNO3 Ba2+ wytrca biay osad rozpuszcz. w HNO3
5 6 7
J. Gliski, w. 4, p. 3
You might also like
- 16 IloczynDocument4 pages16 IloczynAnna BielenicaNo ratings yet
- Test.A.Systematyka Związków Nieorganicznych PDFDocument8 pagesTest.A.Systematyka Związków Nieorganicznych PDFBogdan ArkadiuszNo ratings yet
- SoleDocument6 pagesSoleJulia WarcholNo ratings yet
- Reakcje Charakterystyczne Dla Chemii OrganicznejDocument5 pagesReakcje Charakterystyczne Dla Chemii OrganicznejTomekNo ratings yet
- Reakcje Charakterystyczne AnionoDocument19 pagesReakcje Charakterystyczne AnionoKarolyn 123No ratings yet
- Analiza Jakościowa Anion I KationDocument17 pagesAnaliza Jakościowa Anion I KationTania HoncharukNo ratings yet
- Httpzd2.chem - Uni.wroc - Plfilesinstrukcje01c Kat PDFDocument4 pagesHttpzd2.chem - Uni.wroc - Plfilesinstrukcje01c Kat PDFpilak.pilak1234No ratings yet
- Analiza JakosciowaDocument34 pagesAnaliza JakosciowaNinja698No ratings yet
- Podstawy Technik Laboratoryjnych Wydanie 1Document28 pagesPodstawy Technik Laboratoryjnych Wydanie 1youretoasstNo ratings yet
- Chemia Obs.Document12 pagesChemia Obs.Arkadiusz SkalskiNo ratings yet
- Reakcje AnionówDocument5 pagesReakcje AnionówHugh MayaNo ratings yet
- Chan 05 (Aniony2)Document35 pagesChan 05 (Aniony2)vee.fortesqueNo ratings yet
- Instrukcja - Analiza Jakościowa JonówDocument9 pagesInstrukcja - Analiza Jakościowa JonówOlaf AntczakNo ratings yet
- JONYDocument9 pagesJONYMarta JNo ratings yet
- Chan 02 (Kationy1)Document74 pagesChan 02 (Kationy1)vee.fortesqueNo ratings yet
- ĆW 1 PierwiastkiDocument6 pagesĆW 1 PierwiastkiOlaNo ratings yet
- Chemia Analityczna Czesc2Document11 pagesChemia Analityczna Czesc2mremwuNo ratings yet
- Reakcje CharakterystyczneDocument11 pagesReakcje CharakterystyczneKacperNo ratings yet
- 69 IilDocument8 pages69 IiljakasnazwaxddNo ratings yet
- II-właściwości kwasów-PRDocument16 pagesII-właściwości kwasów-PRAneta WilczewskaNo ratings yet
- Chemia Zbior Zadan Fau M Odpowiedzi Chemia Zeszyt NR 7 OdpowiedziDocument45 pagesChemia Zbior Zadan Fau M Odpowiedzi Chemia Zeszyt NR 7 OdpowiedziKatarzyna WojtczakNo ratings yet
- Chemia Zbior Zadan Fau Odpowiedzi Zeszyt NR 7Document46 pagesChemia Zbior Zadan Fau Odpowiedzi Zeszyt NR 7oliwiagoorka77No ratings yet
- Reakcje CharakterystyczneDocument11 pagesReakcje CharakterystyczneSebastian_Baku_5359No ratings yet
- Cel ĆwiczeniaDocument11 pagesCel ĆwiczeniaNikola WójcikNo ratings yet
- Chemia Kationy GR 1, 2, 4 I 5Document2 pagesChemia Kationy GR 1, 2, 4 I 5OlaNo ratings yet
- AzotowceDocument56 pagesAzotowceKrowaNo ratings yet
- Aniony Reakcje CharakterystyczneDocument2 pagesAniony Reakcje CharakterystycznetenczowybananeksweetNo ratings yet
- SOLEDocument3 pagesSOLEAnna WantuchNo ratings yet
- Rozdział Przez StrącanieDocument3 pagesRozdział Przez StrącanieKinga KucharskaNo ratings yet
- Etody Wydzielania I Zatężania Zagęszczania AnalitówDocument50 pagesEtody Wydzielania I Zatężania Zagęszczania AnalitówGrabie OgrodoweNo ratings yet
- Otrzymywanie Soli W Wyniku ReakcDocument21 pagesOtrzymywanie Soli W Wyniku ReakcMichalina SiwikNo ratings yet
- Laboratorium 2Document24 pagesLaboratorium 2auri blaszczakNo ratings yet
- Sciaga ChemiaDocument2 pagesSciaga Chemiakasiq91No ratings yet
- Azotowce 4Document3 pagesAzotowce 4Gosia KolasaNo ratings yet
- Praca Domowa Reakcje Redox Kasia GDocument8 pagesPraca Domowa Reakcje Redox Kasia GMonika Stępień0% (1)
- Zadania - Blok PDocument6 pagesZadania - Blok Pdoxer123123No ratings yet
- Jakościowa Analiza Kationów: WstępDocument4 pagesJakościowa Analiza Kationów: WstępKarolyn 123No ratings yet
- SoleDocument6 pagesSoleKacper FijołNo ratings yet
- SoleDocument6 pagesSoleRenata TrzepańskaNo ratings yet
- SoleDocument6 pagesSoleZofia WarzechaNo ratings yet
- Kolokwium IDocument1 pageKolokwium INataliaNo ratings yet
- Zestaw Zadań Powtórzeniowych - Sole - Nazewnictwo I OtrzymywanieDocument3 pagesZestaw Zadań Powtórzeniowych - Sole - Nazewnictwo I OtrzymywanieHUS4KYNo ratings yet
- Grupy AnalityczneDocument7 pagesGrupy AnalityczneFast GanNo ratings yet
- Analiza Jakosciowa EcoPrint AM AnionyDocument13 pagesAnaliza Jakosciowa EcoPrint AM AnionyOliwia StasiakNo ratings yet
- Analiza AnionówDocument2 pagesAnaliza AnionówBasia ŻelazkoNo ratings yet
- Kationy 2aDocument1 pageKationy 2ahttpagaNo ratings yet
- KationyDocument3 pagesKationywaffelek.560No ratings yet
- Jakim Reakcjom Chemicznym Ulega OlowDocument24 pagesJakim Reakcjom Chemicznym Ulega Olowpiosob294No ratings yet
- 7 3 RDocument2 pages7 3 Rmaciej.majchrowski.szczecinNo ratings yet
- Związki Koordynacyjne P1 P2Document13 pagesZwiązki Koordynacyjne P1 P2Emilka LasońNo ratings yet
- Kolory ChemiaDocument5 pagesKolory ChemiaDominika CzortekNo ratings yet
- Azotowce 3Document3 pagesAzotowce 3Gosia KolasaNo ratings yet
- Lekcja 30 Praca DomowaDocument4 pagesLekcja 30 Praca Domowaweronika.dachwitzNo ratings yet
- ZCHB Materialy 01Document14 pagesZCHB Materialy 01Iza GłuchowskaNo ratings yet
- Badanie Zachowania Wybranych Tlenkow Wobec ZasadDocument20 pagesBadanie Zachowania Wybranych Tlenkow Wobec ZasadWhite WhiteeNo ratings yet
- Peta Grupa PSEDocument12 pagesPeta Grupa PSELela SNo ratings yet
- AnionyDocument1 pageAnionygasweb19No ratings yet
- Stężenie Procentowe CPDocument4 pagesStężenie Procentowe CPMikołaj KwiecińskiNo ratings yet
- Rozróżnianie AnionówDocument3 pagesRozróżnianie AnionówAndżelika LorencNo ratings yet
- WODA Jako Rozpuszczalnik-1Document16 pagesWODA Jako Rozpuszczalnik-1Edward ZNo ratings yet
- Warta GlassDocument5 pagesWarta GlassMateusz KowalowiczNo ratings yet
- Instrukcja Azul Witraze SintryDocument6 pagesInstrukcja Azul Witraze SintryAleksandra BrodaNo ratings yet
- Kwasy BeztlenoweDocument2 pagesKwasy BeztlenoweKamil100% (1)
- Rozpuszczalnosc Substancji W WodzieDocument16 pagesRozpuszczalnosc Substancji W WodzieMala MalaNo ratings yet
- Chemia !!! ROZTWORYDocument8 pagesChemia !!! ROZTWORYkudkolaNo ratings yet
- Rozpuszczalnosc kl7 1 Marzec 2020Document5 pagesRozpuszczalnosc kl7 1 Marzec 2020Agnieszka FlisNo ratings yet
- Cz. Rozcienczanie I Zatezanie RoztworowDocument3 pagesCz. Rozcienczanie I Zatezanie RoztworowK100% (1)
- Dział. v. Woda I Roztwory Wodne. Klucz OdpowiedziDocument7 pagesDział. v. Woda I Roztwory Wodne. Klucz OdpowiedziMarzena Pakosz-Białasik0% (2)
- Czynniki Wplywajace Na SzybkoscDocument16 pagesCzynniki Wplywajace Na SzybkoscQUIKNo ratings yet
- Woda I Roztwory Wodne Sprawdzian Grupa A OdpowiedziDocument2 pagesWoda I Roztwory Wodne Sprawdzian Grupa A Odpowiedzisupergamer xNo ratings yet