Professional Documents
Culture Documents
Biochemie I Alle Lessen
Biochemie I Alle Lessen
Uploaded by
Janey BeljaarsOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Biochemie I Alle Lessen
Biochemie I Alle Lessen
Uploaded by
Janey BeljaarsCopyright:
Available Formats
Biochemie I: Hoorcollege 1
H1: Inleiding
Biochemie:hoelevenlozemoleculenwaaruitlevendeorganismenbestaanmetelkaar
interageren.
H2: Koolhydraten
Koolhydraatkoolstofwater(CH
2
O)
n
.
Voedsel,energie,omopteslaan(verschillendeopslagvormen).
Aangemaaktviafotosynthese:CO
2
enH
2
O.
Indelingopbasisvangrootte:mono(n),oligo(enkele)enpolysacchariden(veel).
Mono:vb.1polyhydroxyaldehyde.
Oligo:korteketensvanmonosacchariden.
Poly:meerdan20monosacchariden(cellulose,glycogeen).
Monosacchariden
Aldehydeofketon:aldoseofketose.
Meerdan1hydroxylgroep.
3Cs(triose),4Cs(tetrose),5Cs(pentose),6Cs(hexose),7Cs(heptose).
Hetkoolstofskeletisonvertaktenerzijnaltijdenkelvoudigebindingentussende
Catomen.
Dubbelebindingmetzuurstof:carbonyl.
Asymmetrischecentra,dusallemonosaccharidenbehalvedihydroxyacetonhebben
chiralecentraendusoptischeisomeren.
Glyceraldehydeheeft1chiraalcentrumdustweestereoisomeren,hetzijn
enantiomerenvanelkaar.
Chiraal:nooitsuperponeerbaaropzijnspiegelbeeld.Erzitten4verschillende
functionelegroepenophetCatoom.
nisomeerishetDisomeer,hetanderehetLisomeer.
DOHgroepophetchiralecentrumhetverstvandecarbonylgroepzitrechts
indefisherprojectie.
LOHgroepophetchiralecentrumhetverstvandecarbonylgroepzitlinksin
defisherprojectie.
Hetaantalmogelijkestereoisomeren:2
aantalchiralecentra
,waarvandehelfteenDsuikerisen
dehelfteenLsuiker.DesuikersdieindenatuurvoorkomenzijnmeestalDsuikers.
AlsjevaneenDsuikernaareenLsuikerwilgaan,moetjeelkchiraalcentrum
nemenenelkeOHgroepspiegelen!
Dihydroxyacetonisdeenigezonderchiralecentra.
1
Biochemie I: Hoorcollege 2
Epimeer:deconfiguratieverschiltmaaropnchiraalcentrum,bijvoorbeeldDglucose
enDgalactose.
Demeestemonosaccharidenhebbeneenringstructuur.Dehemiacetaal/hemiketaal
wordtgevormdalsdemoleculeeenringwordt.
Hemiacetaal:aldehyde+alcohol.
Hemiketaal:keton+alcohol.
Allesuikersmetmeerdan5Catomenkunneneenringsluitingvormen,aldotetrosenook.
Ermoeteenbepaaldehoeveelheidruimteinzitten.
Deringsluitingbevindtzichtussentweekoolstofatomenenerwordteenextra
chiraalcentrumgevormd.
Alfaenbeta:hetverschilhiertussenisdepositievandeOHgroepophetanomere
koolstofatoom:bovenofonderdering.
Alfaenbetavanhetzelfdesuikerhebbenalleenophetanomerekoolstofatoom
eenverschilinconfiguratie,hetzijnanomerenvanelkaar.
HetanomerereferentieatoomishetchiraleCatoomdathetverstverwijderdis
vanhetanomereCatoom.Danmoetjekijkennaardepositievandegroepdieop
hetreferentieatoomstaat.
Alfasuiker:deOHgroepzitaandetegenovergesteldekantvandegroep
ophetreferentieatoom.
Betasuiker:deOHgroependegroepophetreferentieatoomstaan
allebeinaarbovenofallebeinaarbeneden.
JemoetaltijdkijkennaardehydroxylgroepopC1.
Pyranosenzijnzesringen,furanosenzijnvijfringen.
Hexosenkomenhetmeestvoorindenatuur,verhoudingenvanvormenhangenafvan
welksuikerhetis.
Haworthprojectie:suikergetekendineen3Dringstructuur.
Reducerendeennietreducerendesuikers:monosaccharidenzijnreducerend.
Reducerend:hetkangeoxideerdworden,decarbonylgroepkangeoxideerd
wordentotcarboxylgroep.Ditisbijallesuikerswaarvanderingopenkangaan.
Fischer naar Haworth
TekendeFischerprojectieentekendejuisteringstructuur,leeg.
HetanomerekoolstofatoomC1zitrechts,vervolgensmoetjewijzerzindeandere
koolstofatomennummeren.
Dsuiker:CH
2
OHomhoog.Lsuiker:CH
2
OHomlaag.
Alfasuiker:anomereOHtegenovergesteldaanCH
2
OH.Betasuiker:anomereOHaan
dezelfdekantalsCH
2
OH.
DeandereOHgroependierechtsstaaninFischer,staanomlaaginHaworth.De
OHgroependielinksstaaninFischer,staanomhooginHaworth.
Disacchariden
Tweemonosaccharidenmeteenglycosidischebinding.
Reactievaneenhemiacetaalmeteenalchol,vormingvaneenacetaal.
Oglycosidisch:bindingmetzuurstof.
Nglycosidisch:bindingmetstikstof.
2
MaltoseisalfaDglucoseviaeenalfa1,4glycosidischebindinggekoppeldaan
betaDglucose.Hetheefteenalfaeneenbetavorm.
Mutarotatie:alseenringzichsluit,ontstaatereenautomatischevenwichttussenalfaen
beta,ditmoetjeweergevenmeteengekronkeldlijntjemetOHenHeraan,alserniet
genoemdisofjealfaofbetamoettekenen.
Lactose:beta1,4glycosidischebindingtussenbetagalactoseenglucose,duserisalfa
enbetalactose.
Sucrose:fructoseenglucoseinglycosidischebindingwaarbijdetweeanomerechirale
centraverbondenzijn.
Ofeensuikerreducerendisofniet,hangtafvanhetaantalanomereCatomenbetrokken
bijdeglycosidischebinding.
Tweebetrokken:nietreducerendglycosylglycoside.
Eenbetrokken:reducerendglycosylglycose.
Polysacchariden
Langeketensvanmonosacchariden.
Onderscheidopbasisvan:
Typemonosaccharide:1soorthomo, 2soortenheteropolysaccharide.
Ketenlengte.
Typeglycosidischebinding.
Matevanvertakking.
Functieshomopolysacchariden:opslagvormvankoolhydraten(brandstofglycogeen,
zetmeel),structuurelementindecelwandvanplantenenhetexoskeletvandieren
(cellulose,chitine).
Functiesheteropolysacchariden:extracellulaireondersteuningvanorganismenvanalle
rijken.
Verschilmeteiwitten(polymerenvanaminozuren):DNA/RNA/eiwittenhebbeneen
welbepaaldesamenstellingenlengteeneenbepaaldmoleculairgewicht.Bij
polysaccharidenisergeentemplate,dusgeenvoorafbepaaldelengte/grootte.
Zetmeel:amyloseenamylopectine.
Amyloseislineair,onvertaktDglucosemeteenalfa14glycosidischebinding.
Hetispolymaltose.
AmylopectineissterkvertaktDglucoseeniszeergroot.Deketenbestaatuitalfa
14glycosidischebindingen,devertakkingenzijnalfa16van2430residuen.
Zetmeelwordtaandenietreducerendeuiteindenafgebroken.
Hetbiologischevoordeelvanvertaktemoleculenisdaterzeersnelveelglucose
vrijgesteldkanworden.
3
Biochemie I: Hoorcollege 3
H3: Aminozuren
Bouwstenenvaneiwitten.Eiwittenzijnuiterstdiversinstructuurenfunctie,maartoch
opgebouwduit20aminozurendiecovalentgebondenzijntoteenlineairesequentie,
gebaseerdopdeDNAsequentie.
Eiwittenzijndiversinstructuurenfunctie:enzymen,hormonen,antilichamen,
transporters,
Structuur:centraalkoolstofatoom,eenaminogroep,eencarboxylgroep.
Alfakoolstofatoom:chiraalcentrum(behalveglycine),2mogelijke
stereoisomeren:enantiomeren(spiegelbeeld).
Enantiomeren:D/Lnomenclatuur.AlleaminozurenineiwittenzijnLaminozuren.
Erzijntweesystemenvoorhetnummerenvandekoolstofatomen:vanafde
carboxylgroep,ofmetGriekselettersvanafhetalfakoolstofatoom.
ClassificatiegebeurtopbasisvandeRgroep,opbasisvanpolariseiten
waterolosbaarheid.
Nietpolair,alifatisch:hydrofobezijketens.
Aromatisch:absorberenUVlicht.
Polair,ongeladen:zijketensvormenHbindingen.
Positiefgeladen:basischezijketen.
Negatiefgeladen:zurezijketen.
Zuur-base eigenschappen
NeutralepH:aminozuurkomtvooralszwitterion.Kanreagerenalszuurofalsbase.Amfolyt:
amfotereelektrolyt.
Eenmonoamine,monocarboxylaminozuur,iseendiprotischzuurwanneerhetvolledig
geprotoneerdisenheefteenkarakteristieketitratiecurve.
Biochemie I: Hoorcollege 4
H4: Peptiden
Depeptidebindingmaakteenpolymeervanaminozuren.
Peptiden:kleinecondensatieproductenvanaminozuren.Eiwitten
bestaanuitveelaminozuren.Degrenstussendezetweeisvaag.
Links/bovenvandepeptidebindingzitdeaminoterminaalen
rechts/onderdecarboxylterminaal.Bijvormingvandepeptidebinding
ontstaatH
2
O.Enzymenzorgendatdezebindingengevormdworden.
Zekunnenookweergebrokenworden.
Residu:individueelaminozuurineenpeptide.
Dipeptide:2aminozuren.
Tripeptide:3aminozuren.
Functies:hormonen(insuline(suiker),oxytocine(geboorte)),neuropeptiden
(neuropeptideY(energiemetabolisme)),bescherming(vb.toxines(amanitine,
chlorotoxine).
Eiwitten
Polypeptiden:covalentgebondenalfaaminozurenmeteventueelcofactoren,conzymen
ofprostetischegroepen:geconjugeerdeeiwitten,alseiwittendefunctienietalleenuit
kunnenvoeren.
Degroottekanheelveelvariren,netalso.a.vormensamenstelling.
Eiwittenkunnenookaanietsgekoppeldzijn,bijvoorbeeldaanvetten:lipoprotenen.
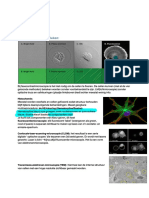
Werkenmeteiwitten
Scheidenvaneiwittenuiteenmengselkanopverschillendemanieren.
Kolomchromatografie:opbasisvanionen,grootteofaffiniteit.Glazenbuisjemet
bepaaldematrixerin,daarboveneenstaalaanbengenvanwatjewilscheidenmetboven
hetbuisjeeenreservoir.Dematrixisdestationairefasewaardemobielefase/staal
doorheenbeweegt.Deverschillendeeiwittenbewegenmetverschillendesnelheiddoor
dematrix,waardoorjeverschillendefractiesvanhetmengselkrijgt.
Ionenuitwisselingschromatografie:destationairefaseisopgebouwduitiets
metnegatievelading.BijeenbepaaldepHverschillendeverschillendeeiwittenin
lading.Denegatiefstgeladeneiwittenwordenhetsterkstafgestotendoorde
stationairefaseengaanerdushetsnelstdoorheen.Groottespeelthierbijgeen
rol.
Sizeexclusionchromatography:dematrixbestaatuitbolletjesporeus
materiaal.Groteeiwittenkunnennietdoordematrixdusgaanerlangs,kleine
passenweldoordematrixmaarondervindenweerstandduszijnlaterbeneden.
Affinitychromatography:meestspecifiek,interesseomeenspecifiekeiwitte
scheidenvanderest.Dematrixiszodathetgekozeneiwiteengroteaffiniteit
heefteneraanblijftplakken,derestgaatwelnaarbeneden.Daarnawordtde
kolomgespoeldmetdestofvandestationairefasezodatercompetitietussen
mobielenstationairkomt.
5
Elektroforese:elektrischveldtrekteiwittenaandoorhunlading.Gelmatrixverhindert
mobiliteitvaneiwitten,vooraldievandegrotezodatdielangzamerzijn.Demobiliteitis
afhankelijkvanderatiolading/massa.Meernegatieveenkleinegaansneller.Somsowrdt
ereenmolecuultoegevoegdzodatdeladingvanheteiwitwordtafgeschermdener
alleennogmaaropbasisvangroottewordtgescheidenalsdegrootte/massagekend
moetzijn.Erwordendaneiwittenmeteenbekendemassaalsreferentietoegevoegd.
Isoelectricfocusing:meesthogeresolutie.Scheidenopbasisvanhetisoelektrisch
punt:depHwaarbijdeladingvanheteiwitnulis.HeteiwitwordtindepHgradint
gebrachtwaarbijdepHgradieelafneemt.Erwordteenelektrischveldtoegevoegdzodat
deeiwittennaarbenedenmigreren.Opeenbepaaldpuntisheteiwitopzijnisoelektrisch
puntenwordthetnietmeeraangetrokkentoteen+ofladingdusbeweegthetnietmeer.
2Dgelelektroforese:scheidingintweestappen.
Isoelectricfocusingzodatjegroepjeseiwittenkrijgtmeteengelijkaardig
isoelektrischpunt.
Resultaatvandatwordtnuingelgescheiden,dankunjeeeneiwituitdegel
snijdenenverderonderzoeken.
Zekunnenookgesequencedworden:bepalenvandeaminozuursequentie.
H5: Eiwitstructuur
Enzymenzijndebelangrijkstefamilie.
Erzijnvierniveaus:primair,secundair,tertiair,quaternair.Erisnietaltijdeenquaternair
niveau.
Deruimtelijkestructuurbepaaltdefunctie.
Primaire structuur
Aminozuursequentie,beschrijvenvanallecovalentebindingenineeneiwit
aminozuursequentie,disulfidebindingen,peptidenverbondendoordisulfidebindingen.
Bepaalthetvouwpatroomendefunctie.Deaminozuursequentieisredelijk
geconserveerdomdefunctietebehouden.
2030%vandeeiwittenispolymorf:verschillendevarianten.Isovorm:devariantvaneen
eiwitmetdezelfdefunctie,deefficintievanisovormenkanverschillen.
Kunnenontstaandoorverwantegenenofverschillendegenenvanhetzelfdegen,
ofdooralternativesplicing.
Isovormenzijnvaakweefselspecifiek:bijvoorbeeldeenvooreenspier,eenvoor
delever.Somszijnzeookspecifiekvoorverschillendecelcompartimenten.
Secundaire structuur
Elkeiwitheefteenspecifiekeeigenstructuur,directgerelateerdaandefunctie.Gedicteerddoor
deaminozuursequentieeninteractiestussenaminozuren.Destructuurwordtdeelsbepaald
doordeeigenschappenvandepeptidebinding,dieiseenresonantiehybridewaardoordebinding
rigideenplanairis.Erkannietomheengeroteerdwordenenhijvertoonteendipoolmoment.
Erisalleenrotatiemogelijkrondbindingenaan
C
alfa
,viahoek enhoek .Ineenvolledig
uitgestrektpolypeptidezijndiehoeken180
graden.0gradenisdemeestopgevouwen
positie.DehoekenwordenbekekenvanuitC
alfa
,
6
derotatiewordtbekekenvanuithetdistaleatoom.
Ramachandrangrafiek:allecombinatiesphienpsidieineenbepaaldeiwitvoorkomen.
Sommigekunnennietvoorkomendoorsterischeeffecten.
Desecundairestructuurisregelmatigofonregelmatig.Regelmatig:alfahelixen
betaconformatiekomenhetmeestevoor.
Alfahelix:spiraal,zeerstabieldoorwaterstofbruggentussendepeptidebindingen.
Compact:0
o
<psi<70
o
.Depeptidebindingenstaanparallelaandeasvande
helix,dezijketensstaanloodrechtopdeasvandehelix.Linkshandigof
rechtshandig:indenatuuraltijdrechts.25%vandeaminozurenkomtvoorals
alfahelix.Nietalleaminozurenzijnsterkealfahelixvormers.Bovenaan
+
en
onderaan
indehelix:negatieveaminozurenkomenvaakvooraanhetpositief
geladenuiteinde.
Betaconformatieissterkuitgerekt:90
o
<psi<180
o
.Erzijngeen
waterstofbruggenbinnendeketen,weltussendeketenszodatzeeen
betasheet/gevouwenbladvormen.
Betaturns:bochtenvan180gradenovervieraminozuren,opdeplaatsenwaar
betasheetsvanrichtingveranderen.
7
Biochemie I: Hoorcollege 5
Tertiaire structuur
Nietalleeiwittenhebbenverschillendetypenvansecundairestructuren.Detertiairestructuuris
dealgemeneruimtelijkeordeningvanatomenineenvolledigpolypeptideofeiwit.Erzijntwee
groteklassen:
Vezelachtigeeiwitten:onoplosbaarennenkelesecundairestructuur
Alfakeratine:haar,wol,nagels,hoorns,huid,klauwen,vanzoogdieren.Twee
helicesdieparallelopgewondenzijnineenspoel,deaminouiteindenzittenaan
dezelfdekant.Aanhetoppervlakzittenhydrofobeaminozuren.Disulfidebindingen
versterkenhet.
Permanentje:disulfidebindingenwordenverbrokenennahetveranderen
vanhethaarweergevormd.
Collageen:zeersterkmaarflexibel.Inpezen,kraakbeen,hoornvlies,De
structuurlijktopdievanalfakeratinemaardanmetalfaketensinplaatsvan
alfahelix(compacter).Erzijndriealfaketensomelkaargewonden.Erzijngeen
disulfidebruggenmaarbruggentussenlysineenhydroxylysine.
Fibrone/zijde:vandezijderups,spinnenwebben.Sterk,kannietuitgerektworden:
betasheets,zijnalzovermogelijkuitgerekt.Hetiswelflexibeldoornietcovalente
interactiestussendebetasheets,zekunneneenbeetjeoverelkaarschuiven.
Globulaireeiwitten:bolvormig,hebbenmeersecundairestructuren.Erzijn
wateroplosbare(incytosol,bloed,)envetoplosbare(vb.inmembranen).De
3Dstructuurkancomplexzijnmaarisaltijdgerelateerdaandefunctie.
Myoglobine:zuurstofbindendeiwitinspiercellen,bestaatuit153aminozuren.De
structuurisgelinktaandefunctie:alsdestructuurwijzigt,bijvoorbeelddoor
mutatie,wijzigtdefunctieook(vb.sikkelcelanemie).Myoglobineheefteen
haemgroepenbestaatuit8alfahelicesverbondendoorbetaturnsenandere
structuren.
DemeestehydrofobeRgroepenzittenaandebinnenkant,demeeste
hydrofieleaandebuitenkant.Ditzorgtvoordeoplosbaarheid.
DehaemgroepzitineenbeschermendepocketomdeoxidatievanFe
2+
naarFe
3+
teverhinderen.Fe
3+
isdegeoxideerdevormvanFe
2+
enkan
geenzuurstofbinden.Hetijzeratoommoetdusbeschermdwordentegen
oxidatie.
Quaternaire structuur
Heteiwitbestaatuitsubunitstertiairestructurendiealleeneenbiologischefunctieuitkunnen
voerenalszeopeenbepaaldemaniertoteenquaternairestructuurzijngeassocierd.Subunits
kunnendezelfdefunctiehebbenmetverschillendegevoeligheid,zekunnenookcoperatie
realiserenofanderefunctieshebbendiecomplementairzijn.
Erzijntweesoortensymmetrie:rotationelesymmetrieiscyclisch,dihedraalof
icosahedraal.Helicalesymmetrieishelixvormig.
Somsisdequaternairestructuureenhelixdiebestaatuitsubunitsdieopzichzelfaleen
completetertiairestructuurhebben.Ditisgeenalfahelixwantdiebestaatuit
aminozuren.
8
Myoglobineheeftgeenquaternairestructuur,maarnvandesubunitsvanhemoglobine
lijktopmyoglobine.Inhemoglobinezijnvierbindingspositiesvoorzuurstof.
Eiwitdenaturatie:hetverliesvanstructurele
integriteitmetdaarmeesamenhangendhet
verliesvandefunctie.Eiwittenkunnen
gedenatureerdwordendoor:warmte(eikoken:
wordtwit),koude,pH,organischesolventen,
chaotropischestoffenzoalsureum
(chaotropisch=verstorenvanHbindingen).
Denaturatiecurve:T
m
=T
melting
.AlsdeT
m
lageris,denatureertheteiwit
sneller/bijeenlageretemperatuur.De
waardebij50%geefteenideevande
gevoeligheid.Opdeyasstaathet
percentagedenaturatie,opdexas
hetgeendatvoordenaturatiezorgt,in
ditgevaldetemperatuur.
Somsisdenaturatieomkeerbaar:
renaturatie.Ditgebeurtalsdedenaturatieveroorzakendecomponentopgehevenwordt.
H6: Eiwitfunctie
Defunctieisafhankelijkvandebindingaanhetmolecuul.Vaakisdefunctiebindenaan
eenmolecuul,erietsmeedoenzoalstransporterenofwijzigenendanweerloslaten.
Zonmoleculeiseenligand,dieeenligandbindingvormtmeteeneiwit.Debindingis
transint.
Eiwittenzijnnietstatisch,alseenliganderaanbindt,kandestructuurvanheteiwit
lichtjesveranderen.Doorinteractiemetdemoleculenverandertdefunctie.
Erzijntweemodellendiedeligandeiwitbindingbeschrijven.Dewerkelijkheidiseen
combinatievandietwee:
Keylock:ligandpastpreciesopheteiwit.
Inducedfit:deligandbindingveroorzaakteenconformatiewijzigingdieeenbinding
toelaat.Somskaneenbindingdeaffiniteitvooreentweedebindingverhogen:
indirecteinducedfit.
Enzymen
Bindenentransformerenanderemoleculenenstellenzedanweervrij.
Enzymenkunnengestuurdworden.
Hetzijnkatalysatoren:zevergemakkelijkenreactiesmaarwordenzelfnietgebruiktof
gewijzigd.
Fysicochemischeomstandighedenindecelzorgendatreactiesnietspontaanverlopen,
doorenzymenkunnenzetochdoorgaan.
Haemgroep
Zuurstofbindingvoortransportenopslag.
Rgroepenvaneiwittenhebbeneenlageaffiniteitvoorzuurstofduseriseenbijkomende
groepnodig:dehaemgroepdieijzerbevatdatzuurstofkanbinden.IJzerkomtvooronder
9
devormvanFe
2+
,watmakkelijkgeoxideerdwordttotFe
3+
datgeenzuurstofkanbinden.
Fe
2+
wordtdaaromdoordepocketendehaemgroepbeschermd.
IJzerheeft6bindingsplaatsen:
4voordebindingaandehaemgroep.
1voorbindingaanheteiwit.
1voorbindingaanzuurstof.
DevierNatomenzijndeessentievanhettweede
beschermingsmechanismetegenoxidatie:zezijnerg
elektronegatiefenwillendusgraagelektronen
bijhouden.HierdoorisdekanskleindatFe
2+
een
elektronverliest.
Myoglobine
Bindtzuurstofinspierweefsel.
8helices,verbondendoorbetaturnsenanderestructuren.
Bindingvaneenligand:evenwichtsreactie.P(protene)+L(ligand) PL.Inditgeval:P
=myoglobine,L=zuurstof.
Evenwichtsconstante/associatieconstante:K
a
=[PL]/[P][L].
Dissociatieconstante:K
d
=1/K
a
=[P][L]/[PL].
isdegraadvanverzadiging:bezettebindingsplaatsen/mogelijke
bindingsplaatsen
[PL]/[PL]+[P].
Decurvesteltdebinding
vanhetligandaanheteiwit
voor.K
d
isdeconcentratie
liganddieaanleidinggeeft
tot50%vandesaturatie.
EenhogereK
d
betekent
eenlagere
bindingsaffiniteit.Erisdan
eenhogereconcentratie
ligandnodigomheteiwit
50%tesatureren.
Biochemie I: Hoorcollege 6
Bindingscurvemyoglobine:demaximaalrealiseerbaresaturatiegraadwordtsnelbereikt:
DecurveligtvernaarlinksendeK
d
hierp
50
)iszeerklein.Myoglobineheefteenhoge
bindingsaffiniteitvoorzuurstofenbindthetdussnelenmakkelijk:efficintomde
zuurstofvoorraadoppeiltehouden.
Destructuurvanheteiwitbepaalthoeligandenbinden(ruimtelijkepositie):invrijhaem
bindtCO20.000xbeterdanO
2
,inmyoglobinebindthetnogmaar200xbeter
sterischehinder.
DeplaatswaarO
2
bindtispreciesgemaaktomeenmolecuultebindenindehoekdieO
2
vormt.DaarombindtCOminderefficintdantheoretischhetgevalzouzijn.
DebindingvanO
2
wordtbepaalddoorhetademenvanheteiwit:depocketgaatheelsnel
openenweerdicht,precieslanggenoegvoorO
2
omerintegaan.Haemzitgoed
10
verstoptinheteiwitvoordebeschermingvanFe
2+
tegenoxidatie,maarhierdoorishet
slechttoegankelijkvoorO
2
.
Hemoglobine
MyoglobineslaatO
2
op,hemoglobinetransporteerthet.Myoglobinebindtzoefficintdat
hetgeenzuurstofafkangevenaandeweefsels.
2alfasubunits,2betasubunitsendus4haemgroepen.Desubunitslijkenallemaalop
myoglobine.Eerstassocirendealfasubunitsmetdebetasubunits.Ditisdesterkste
interactie.Jehebtdan2alfabetaprotomerendiesamenhetdimeerhemoglobine
vormen.Hemoglobineisduseendimeervanalfabetaprotomeren.
Erzijn2vormenhemoglobinedoordatdesubunitstenopzichtevanelkaarkunnen
bewegen.Alleeneiwittenmeteenquaternairestructuurkunnendusverschillende
bindingsaffiniteitenhebben.
Tvorm:tensed/gespannen.Lageaffiniteit.Deoxyhemoglobine:geenO
2
.Veel
interactiestussendomeinen.
Rvorm:relaxed/ontspannen,hogeaffiniteit.Oxyhemoglobine:O
2
gebonden.Er
zijnminderinteractiestussendedomeinen.
BindingvanzuurstofveroorzaaktdetransitievanTnaarR:depositievandehaemgroep
t.o.v.histidineverandert.Debindingheefteffectopdeaffiniteitvandeanderesubunits:
dieaffiniteitstijgt.
Omgekeerdgebeurthetook:alsnO
2
loslaat,wordthetvoordereststeeds
makkelijkeromooklostelatencoperatieveligandbinding.
Coperatieve ligandbinding
DepO
2
indelongenis13,3kPa,dieinde
weefsels4kPa.Myoglobinekanditniet
realiseren,hemoglobinelosthetopmetzijn4
subunitsendeT/Rtoestand.
MyoglobinekangoedO
2
bindenmaarmoeilijk
afstaan,hetiseenslechttransporteiwit.
Debindingsplaatseninhemoglobine
interagerenmetelkaar:deeerstebinding
verhoogtdeaffiniteitopdeandereplaatsen.
Ditkanherkendwordenaandesigmodale
curve.
Allosterischeregulatie:bindingvan
eenligandbenvloedtde
eigenschappenvandeandere
bindingsplaatsen.
Erzijntweemodellendiecoperatie
beschrijven:geconcerteerdensequentieel.
Erzijnookanderefactorendiedeaffiniteitbenvloeden:
Hb+O
2
HbO
2
.
pH:protonenhebbeneenanderebindingsplaatsdanO
2.
LagepH(veelprotonen):
lageaffiniteit,doorhetpHverschilindeweefsels.DoorhetpHverschilkaner
zowelgoedeopslagalsgoedtransportgebeuren.
HHb
+
+O
2
HbO
2
+H
+
.
11
2,3bifosfoglyceraat(BPG):hoge[BPG]lagebindingsaffiniteit.BPGwordt
gemaaktopbasisvanglucoseafbraak.BPGverlaagtdeaffiniteitvoorO
2
en
stabiliseertdedeoxyvormvanhemoglobine.
HbBPG+O
2
HbO
2
+BPG.
Mogelijkeexamenvraag:hoogindebergen,waarweinigzuurstofis,ishetdaneen
voordeeldatdeaffiniteitvanhemoglobinevoorzuurstofhogeroflagerisdanop
zeeniveau?ziegrafiek.
H7: Lipiden
Erzijnopslagvetten,lipidenalsstructuurinmembranenenlipidenmetanderefuncties
(vb.bepaaldehormonenopbasisvanvetten).
Eendeelvandeopslagvettenisafkomstigvansuikers.Vetteneneiwittenkunnen
somsnaarelkaargeconverteerdworden.
Zeerheterogenegroeporganischestoffenmetnofmeer(lange)apolairealkylketens.
Zezijnoplosbaarinapolairoplosmiddel,nietinwater.
Erzijnenkelvoudigelipiden(opslag,vettenenolin,wassen),samengesteldelipiden
(fosfo,sfingo,glycolipiden)enlipode/vetachtigestoffen(vetzuren,carotenoden,
steroden).
Biologischefuncties:energievoorraad,brandstof,structuurfunctieinmembranen.
Hormonen,vitaminen,signaalmoleculen,antibiotica,
Vetzuren
Lipidenzijnderivatenvanvetzuur( lipide).Incellengebeurtervetzuursynthese:ze =/
kunnenzelfvetzurenaanmaken.Vetzurenzijncarboxylzurenmetkoolwaterstofketens.
Zezijnsterkgereduceerd.Biologischrelevantevetzurenhebben436Cs.Zezijn
verzadigdofonverzadigd,vertaktofonvertakt.
Basisvetzuurheeft16Cs.
Demeestvoorkomendevetzurenhebbenonvertakteketensvan1224(evenaantal)
koolstofatomen.
Zehebbeneenpolaire,wateroplosbarekopeneenapolaire,vetoplosbarestaart.
Dierlijkevettenzijnvooralverzadigd,plantaardigevooralonverzadigd.Synthesegebeurt
doorhetsteedsverlengenvandeketenmet2Cs,afbraakgebeurtooksteedsper2Cs.
Naamgevinggebeurtaandehandvandeketenlengteenhetaantalendepositievande
dubbelebindingen.
Vb.arachidonzuur:20:4(
5,8,11,14
)betekenteenketenvan20koolstofatomen,4
dubbelebindingenopdeplaatsen5,8,11en14.Jemoettellenvanafhet
carbonylkoolstofatoom.
12
Biochemie I: Hoorcollege 7
Depositievandubbelebindingeninvetzurenismeestal9,12of15.Dedubbele
bindingenzijnbijnanooitgeconjugeerd:meestalzittenerminstens2enkelebindingen
tussentweedubbele.Bijnaallenatuurlijkeonverzadigdevetzurenhebbeneen
cisconfiguratie,waardoorereenknikindeketenkomt.
Fysicochemischeeigenschappenwordenbepaalddoordeketenlengte:hoegroterde
keten,hoegroterhetbelangvandepolairestaartoplosbaarheidneemtaf.
T/meenketenlengtevan4ishetnogoplosbaarinwater.
Vanafeenketenlengtevan12ishetvolledigonoplosbaarinwater.
Eenvetzuurisdusnietoplosbaarinbloed.
Deeigenschappenwordenookbepaalddoordematevanverzadiging:
Verzadigdevetzuren(meestaldierlijk)zijnvastbijkamertemperatuur.
Onverzadigdevetzurenzijnvloeibaarbijkamertemperatuur(meestalplantaardig)
doordeknikdieerinkomt:zekunnenmoeilijkeropgestapeldworden.
Doordatzewateronoplosbaarzijn,zijnvetzurentijdenstransportgebondenaaneeneiwit
(albumineishetbelangrijkst).Vettenwordenverpaktinvesikelsvoortransport.
Vetzurenzijnamfipatisch:zehebbeneenhydrofieleneenhydrofoobdeel.Hierdoorgaan
zezichinwaterigmilieuorganiserenalsmicellen.Doordatdepolairekopaande
buitenkantzit,zijnzebeteroplosbaarinwater.
Alsjededubbelebindingenbenoemtvanafdepuntvandestaart,komtereen voor.
Dezetellingheeftfysiologischerelevantie.Erzijnomega3enomega6vetzuren.De
ratioomega6/omega3moettussende1/1en4/1zitten.Hetgaatnietzozeeromde
hoeveelheidvandietwee,vooralomdeverhouding.
Opslagvetten
Slaanenergieopinvetweefsel.Hetgaatomenergiedienietdirectnodigisenlater
gebruiktkanwordenalshetnodigis.
Triacylglycerolen/TAGzijnestersvanhetalcoholglycerolendrievetzuren.Eenvoudige
bestaanuitdriedezelfdevetzuren,gemengdeuit2ofmeerverschillende.
Opmerkelijk:TAGwordtgemaaktmetglycerol3fosfaati.p.v.glycerol.Het
eindresultaatvanafbraakvanTAGiswelglycerol.TAGwordtafgebrokenalser
energienodigis.
Vetcellen/adipocytenhebbeneenvolumedatbijnavollediguitvetbestaat.Degroottevan
vetcellenneemttoe/afbijdikkerworden/afvallen,niethetaantal.Omdecelgrotertelaten
worden,moetdemembraanookgroterworden.
Energiediebinnenkomt,kanwordenopgeslagenalsvetofalssuiker.
VoordelenTAGvergelekenmetsuikers:sterkergereduceerddusdeafbraak
(oxidatie)levertmeerdan2xmeerenergieop.Zeerhydrofoobduserzitgeen
watertussendemoleculen:lagergewicht,compacter.
NadelenTAG:duurtrelatieflangomhetaftebreken.
Voordelensuikers:snelbeschikbareenergiebron.Oplosbaarinwater,
eenvoudigertransport.
Vetteninvetweefselkomenvanverschillendeplaatsen.Sommigekomenuitvoeding,
anderewordendoorhetorganismegesynthetiseerd.PUFA(polyonverzadigdevetzuren)
kanhetlichaamnietzelfmaken.Eriseencorrelatietussenhartenvaatziektenen
verzadigdevetzuren,eendieetmetveelPUFAisbelangrijk,diezittenvooralin
plantaardigvet.
13
Naastdenatuurlijkecisvettenzijnerooktransvetten.Zewordeninrumengeproduceerd
doorfermentatieenhetlichaamneemtzedusopviazuivelofvlees.Ookwodenze
geproduceerddoorhydrogenatievanplantaardigeolinomdebewaartijdteverlengen.
Dedubbelebindingenwordengereduceerdwaardooralsbijproducttransonverzadigde
vetzurenontstaan.
Wassen
Waterafstotend(bescherminghaar,huid,
vogelveren,planten,).Vb.bijenwas.
ZezijneenvoudigerdanTAG:eenestervan
decarboxylvaneenvetzuurendehydroxyl
vaneenalcohol(langeketenvetzuurvan1436Cseneenlangeketenalcoholvan
1630Cs).
HetsmeltpuntishogerdanvanTAG.
Vetten als structuurelement in membranen
Destructuurvanbiologischemembraneniseenlipidedubbellaag.
Barrirevoorpolairemoleculen(ionen,water).
Membraanlipidenzijnamfipatisch.Dedubbelelaagontstaatdooronderlingeinteracties
tussendelipiden(hydrofoob)enhydrofieleinteractiestussendelipidenenwater.
Debiologischemembraaniseenstructuurdiepreciespastineenwaterigmilieu.De
diametervandekopisongeveergelijkaandievandetweestaartensamen,waardoorde
structuurrelatiefrechtis.
Erzijnvijfhoofdtypes:glycerofosfolipiden,galactolipidenensulfolipiden,tetratherlipiden,
sfingolipidenensterolen(lipod).
Fosfolipide:fosfaatgroepvormtdepolairekop.
Glycolipide:suikervormtdepolairekop.
Galactolipide:glycerolenhetsuikergalactosevormendepolairekop.
Sulfolipide:galactolipidemeteensulfaatgroepophetsuiker.
Glycerofosfolipiden
Glycerolisdebasis,mettweevetzurenveresterd.Depolairegroepisgebondenviaeen
fosfodisterbinding.Glycerolisprochiraal:hetisnietchiraalmaarbindingvaneen
fosfaatgroepaannuiteindemaakthetwelchiraal.
Debasismoleculeisfosfatidinezuur.Andereglycerofosfolipdenzijnhierderivatenvan:
Fosfatidylethanolamine,fosfatidylcholine,fosfatidylserine,
14
Biochemie I: Hoorcollege 8
Eriseengrootverschilinvetzuursamenstelling.Ditisweefselensoortafhankelijk.
MeestalziteropC1eenverzadigdevettzuurketenvan16of18CsenopC2een
onverzadigdevan1020Cs.
Etherlipidenzijnglycerofosfolipidenmetnetherbinding.Devetzuurketendieverbonden
ismeteenetherbindingkanonverzadigdzijnopC1/C2(plasmalogenen)ofkanverzadigd
zijn(alkyletherlipiden).
Galactolipiden
Debasisisglycerol,met2vetzureneropveresterdeneensuikeralspolairekopwaar
evt.eensulfaatgroepopstaatsulfolipiden.
Hetsuikerheeft1of2galactoseresiduen.Galactolipidenkomenvnl.voorinplanten.
Membranenvanplantenhebbendusminderfosfaatdandierlijke.(Waarschijnlijkomdat
erooiteentekortisgeweestaanfosfaatenplantentoendevoorkeurhaddenomfosfaten
voorDNAsynthesetegebruikenevolutionairetradeoff.)
Tetratherlipiden
Tweelangekoolstofketensvan32Cs,via4etherbindingengebondenaan2
glycerolmoleculen.Erzijn2polairekoppendusnlaagkanaleenmembraanvormen.
KomenvoorinArchaeadievaakinextremeomstandighedenleven.Etherbindingenzijn
resistentertegenafbraakonderzwareomstandigheden.
Sfingolipiden
Polairekopentweeapolairestaarten.Debasismoleculeissfingosine,diezelfnvan
destaartenvormt.Deandereiseenvetzuur.
Samenmetdeglycerofosfolipidenisditdebelangrijkstesoortmembraanlipideninde
dierlijkecel.
Depolairekopiseenfosfodisterbindingofeenglycosidischebinding.
Debasismoleculebestaatuitsfingosine,1vetzuureneenpolairekop.
Driesubklassensfingolipidennaargelangdepolairekopdieeropzit:
Sfingomyelines:deenigemeteenfosfodister.Zehebbenfosfocholineof
fosfoethanolaminealskopgroepenkomenvoorindeplasmamembraanvan
dierlijkecellen,vooralveelinmyelineschedes.
Glycosfingolipiden:ladingslozeglycolipiden.Erzijncerebrosiden(1suiker)en
globosiden(2,3,4suikers).
Gangliosidenzijndemeestcomplexesfingolipiden.Zehebbenoligosacchariden
alspolairegroep,vaakvertakt.BijpH7zijnzenegatiefgeladen.
Afbraakvanfosfolipiden:inlysosomen,voorelkehydrolyseerbarebindingisereenspecifiek
enzym:
FosfolipaseA1kniptdestaartenaf,bijalleenC1.
FosfolipaseA2kniptalleenafbijC2.
FosfolipaseBkanbijzowelC1alsC2destaartknippen.
FosfolipaseCkniptdekopgroepvrhetfosfaat.
FosfolipiaseDkniptdekopgroepnadefosfaatgroep.
15
Sterolen
Structurelelipideninbijnaallemembranenaanwezig.Hetzijnderivatenvancholesterol.
Devierringenzijneraltijd,dekoolstofketenenstructurelegroepenvariren.
H8: Membranen
Celmembraandefinieertdeexternegrensvandecel.Binnendecelzijnerooknog
membranen:celletjesbinnendecelorganellen.
Membranensluiteniets(cel,organel)afvanderest:compartimentalisatie.
Omstandighedeninhetcompartimentkunnenminofmeeronafhankelijkvande
buitenwereldveranderdworden.Membranenlatencommunicatietussende
compartimentenselectieftoedoorregulatievanmoleculairtransportoverdegrenzen.
Demogelijkhedenineencelhangenafvanwaardemembraanoverbeschikt.Deze
bepalenwatdecel/organelwelofnietkanmembranenzijndusnietstatisch!
Membranenhebbenookreceptoren:decelkansignalenvandebuitenwereldoppikken.
Membranenbevattengespecialiseerdeeiwtten:transportersvoormetabolietenenionen,
receptorenvoordetectievanextracellulairesignalenenadhesieeiwitten.
Suikers,vettenneiwittenzijnbelangrijkomeenmembraanzijnfunctionaliteittegeven.
Demembraanisdusmeerdaneendubbelelipidenlaag.
Membranenbinneneencelorganiserencellulaireprocessen:vetsynthese,synthesevan
bepaaldeeiwitten,energietransductieenenergieproductie.
Destructuurvanmembranen:2dunnelagenvanmoleculen,inessentie2D,watsterkdekans
vergrootopinteractietussenmoleculen.Hierdoorkunnenprocessenefficinterdoorgaan.
Belangrijkeprocessenzijndusmeestalgekoppeldaandemembraan(vb.ATPsynthese).
Cytosolischeprocessenzijnminderefficintwantdatisineen3Druimte.
Demembraanbestaatuitpolairelipiden,eiwittenensuikers(alsglycoproteneof
glycolipide).Eriseenzeergrotevariatietussensoortenmembranen,omdat
verschillendecellenverschillendebehoeftenhebben.Desamenstellinghangtdus
volledigafvandefunctiesvandecel.
Membraanarchitectuur
Decelmembraandefinieertdeexternegrensvandecel.Binnendecelzittenook
membranen,dezelijnendeorganellenaf.
Deomstandighedenindecompartimentendiemembranenaflijnen,kunnenminofmeer
onafhankelijkvandebuitenwereldveranderdworden.
Zeregelenmoleculairtransportoverdemembraan:zelatencommunicatietussen
verschillendecompartimentenselectieftoe.
Demogelijkhedenindecelhangenafvanhetgeenwaardemembraanoverbeschikt.Dit
bepaaltwathetcompartimentwelofnietkan.Eenmembraanisnietstatisch!
Zezijnflexibelenzelfsluitend.
Zezijnselectiefdoorlaatbaarvoorpolairestoffen.
Doorlaatbaarvooreenaantalapolairestoffen:sterodeenschildklierhormonen.
Membranenhebbenookreceptorenwaardoorzesignalenvanbuitenafkunnen
opvangen.
Membranenbevattengespecialiseerdeeiwitten.Nietalleeneiwitten,maarooksuikersen
vettenzijnbelangrijkomeenmembraanzijnfunctionaliteittegeven.Deeiwitten:
Transportersvoormetabolietenenionen.
16
Receptorenvoorextracellulairesignalen.
Adhesieeiwitten.
Membranenbinneneencelorganiserencellulaireprocessen:vetsynthese,eiwitsynthese,
energietransductieenproductie.
Membranenbestaanuittweedunnelagenvanmoleculenenzijninessentie2D.Dit
vergrootdekansopinteractietussenmoleculenwantzekunnenelkaarmakkelijker
tegenkomen.Ditheeftimpactopdewerkingvanbijvoorbeeldenzymen.Processen
kunnenhierdoorefficinterdoorgaan.Belangrijkeprocessenzijndusmeestalgekoppeld
aandemembraanvb.ATPsynthese.Cytosolischeprocessenzijnminderefficint
omdatzeineen3Druimtegebeuren.
Samenstellingvanmembranen:polairelipiden,eiwitten(receptoren,transport,
membraangekoppeldeprocessen),suikers(glycoproteneoflipide).
Verschillendecellenhebbenverschillendebehoeftenendusverschillende
samenstellingenquabiomoleculen.Desamenstellingisheelbelangrijkenhangtafvan
defunctiesvandecel.
Membranenzijndoorlaatbaarvoorapolairestoffen,onlaatbaarvoorpolaire.Zezijn
510nmdikenzijntebeschrijvenvolgenshetfluidmosaicmodel,datbeschrijftdatde
membraaneenvloeibarestructuuris:
Fosfolipidenvormeneendubbellaagdiedoorhydrofobereactieswordt
gestabiliseerd.
Indedubbellaagzijneiwitteningebeddieookdoorhydrofobereacties
gestabiliseerdworden.
Hijisvloeibaardoornietcovalentereactiesflexibel.
Deeiwittenhebbeneenfunctioneleasymmetrie:dieaandebuitenkantzijnniet
noodzakelijkhetzelfdealsdieaandebinnenkant.
Glycerofosfolipideninwater:onoplosbaar.Erzijnhydrofobeinteracties.Zevormen
aggregaten:micellen,dubbellaag,liposoom.
Plasmamembraan:ookdelipidenhebbeneenasymmetrie.Dezeisnietabsoluutenkan
wijzigen.Vb.rodebloedcel:debuitenzijdeheeftvooralcholinebevattendelipiden,de
binnenzijdeanderelipiden.
Membraaneiwittenwordenin3typenonderverdeeld:
Integraleeiwitten:zijneenintegraaldeelvandemembraan.Hydrofobereacties
metdemembraan.
Perifereeiwitten:bindenopdeintegraleenzittenindeperiferie(elektrostatische
enHbindingen).
Amfitropeeiwitten:kunnenassocirenmetdemembraanenweerloskomen.
Biologischeregulatiezorgthiervooralshetnodigisenalszeweerlosmoeten.
Hetgeeftcellentijdelijkeennieuwefunctie.Erzijnsubtypesaandehandvande
manierwaaropzegeassocieerdworden:covalentofelektrostatisch.
Sommigeintegraleeiwittenzijnnpolypeptidemetmeerdereapolairestukjesdietot
cilinderzijnopgeroldmetelkaarendepolairelussenhangenindebuisionenkanaal.
Delussenzijneensoortfilterdatbepaaltwelkeionendoorkunnen.
De3Dstructuurvanintegraleeiwittenkanvoorspeldwordena.d.h.v.desequentie.Alser
eenononderbrokensequentievan20hydrofobeaminozurenis,isereen
transmembranairdomein:potentieelomtehechtenindemembraan.
Geladenresiduenzittenaandebinnenofbuitenkant,deapolairezittenindedubbellaag.
17
Biochemie I: Hoorcollege 9
Membraandynamiek
Alsjeeengatmaaktineenmembraan,herstelthetzichzelf:membranenzijndynamisch.
Membraanfosfolipidenkunnenzichbinnendemembraanverplaatsen,tussende
lagen/transbilayerdiffusieofbinnendezelfdelaag/lateralediffusie.
Hulpmechanismen:eiwittendieindemembraanzitten.Hetzijnenzymendiedit
katalyseren:zelatendereactiesnellerenefficinterverlopenmaarblijvenzelf
ongewijzigd(zowelstructuuralsfunctie).Deenigebeperkingvanenzymenishun
levensduur.
Flippase:buitenstelaagnaardebinnenste,erisATPnodig.
Floppase:vandebinnenstelaagnaardebuitenste,erisATPnodig.
Scramblase:uitwisseling.
Hetbeschrijvenvandemogelijkhedenenbeperkingenvaneencel:membraandynamiek.
Detemperatuurbenvloedtdit:
Lagetemperatuur:gelfase.
Hogetemperatuur:vloeibareongeordendetoestand.Detemperatuuriszohoog
daterrandombewegingisendedingendienormaalvoorordezorgenniet
functioneelkunnenzijn.
Fysiologischrelevantetemperatuur:vloeibaregeordendetoestand.
Verzadigdevetzurenzijndebelangrijkstefactor,zezijndichtgestapeldwanterisgeen
knik.Zedragenbijaanderigiditeitenbevoordelendevloeibaregeordendetoestand.
Onverzadigdevetzureninterfererenmetdenormalestapelingenbevoordelende
vloeibareongeordendetoestand.Defluditeitkangeregeldwordendoordeverhouding
verzagdig/onverzadigdvetzuur.Desamenstellingvandemembraanisdusook
dynamisch.
Cholesterol:dwingtnaburigevetzurenindemeestuitgestrektevorm,zevlakkende
knikkenuit.Cholesterolreduceertdusdefluditeit.
Membranerafts:combinatievanglycosfingolipidenencholesterol.Lagefluditeit(cholesterolen
langeverzadigdevetzuren),dikkerdandefosfilipidedubbellaag.Zevormenvlottendiedrijven
tussendelipidenvandemembraan.Devetzureninderaftszijnlangerdaninderestvande
membraanenzezijndikker.
Zeerrijkaantweeklassenamfitropeeiwitten,covalentgebondenaanlipiden.Eiwitten
kunnenlangzaaminenuitraftsbewegen,tot50%vandemembraankunnenraftszijn.
Zedragenbijaandealgemenemembraanstructuurenbrengeneiwittensamen.Ze
houdenenzymenbijelkaarzodatzeelkaarniethoeventezoekenenverhogenzode
efficintie(vb.receptorenensignaaleiwitten).
Membraankrommingenmembraanfusiezijnfundamenteelinveelbiologischeprocessen.De
fusiestartmetlokalekrommingdoorverwijderenvanwatertussenmembranen.Hemifusie:
alleendebuitenstemembraanlagen,ofergebeurtvolledigefusie.Decelmaaktdeeiwittenaan
enbepaaltduszelfdekromming.Dithoortookbijmembraandynamiek:
Eeneiwitdatvanzichzelfkromis,interageertmetdemembraanzodatdieookkrom
wordt.
Verschillendesubunitsassocirenzodatereengroterekrommingkomt.
18
Elementenindemembraanduwendebovenstefosfolipidenuitelkaar,watonderniet
gebeurt.Doorhetspanningsverschilkomtereenkromming.
H9: Nuclenezuren
Metabolefunctiesvannucleotiden:
BouwstenenvanDNAenRNA.
Energieeenheidinmetabolereacties(vb.ATP).
Signaalmoleculen(signaaltransductieproces:uitwendigsignaalverwerkennaar
inwendig).
Componentenvanbelangrijkeconzymen(anderemolecule(nieteiwit)dienodig
isomeenenzymtelatenwerken).
DNA:genen,opslaanenoverbrengenvangenetischeinformatie.
RNA:onderanderetRNA,rRNA,mRNAmaarerzijnveelmeertypes.
miRNA:ombepaaldegenentijdelijkuitteschakelen.Zehebbeneeneffectopde
transcriptiemaaropmRNAnadetranscriptie.Hetisklein:21nucleotiden.
Nucleotidenbevatten3componenten:eenstikstofbevattendebase,eenpentoseeneen
fosfaatgroep.Zonderdefosfaatgroepisheteennucleoside.
Erzijn2familiesvanbasen:pyrimidines(2Ns)enpurines(4Ns).Adenineenguanine
zijnpurines,cytosineenthyminezijnpyrimidines.AstaattegenoverTenCtegenoverG.
InRNAiseruracilinplaatsvanthymine.
Nummeringkoolstofatomenvandepentose:accent.Erzijn2soortenpentosen:
RNA:Dribose,2OH.
DNA:2deoxyDribose,2H.
Opbouwnucleotiden:NbetaglycosidischebindingtussenN1(pyrimidine)ofN9(purine)
en1koolstofatoomvanhetpentose.Eriseenfosfaatestertussendefosfaatgroepen
het5koolstofatoomvanhetpentose.
DNAenRNA:denucleotidenzijnaanelkaargekoppeldviaeenfosfaatgroeptussen5
vandeeneen3vandeandere,watresulteertineen3eindeeneen5einde,duseris
eenrichtingindeketen.Eriseenfosfodisterbinding.
InteractiestussenDNAenRNAstrengengebeurenviawaterstofbindingen.Erzijn
specifiekecombinatiesvanbasenparen:AenT/Umet2Hbruggen,GenCmet3
Hbruggen.
Structuur van nuclenezuren
2helicaleDNAketenszijnomeenasgewonden,rechtsdraaiendenantiparallel.De
ruggengraatishydrofiel(pentosefosfaat).Debasenzittenaandebinnenkant,desuikers
enfosfaataandebuitenkant.StabilisatiegebeurtdoorHbindingen.
Dekleineengrotegroevezijnbelangrijk:anderemoleculenmoetenbindenmetDNA.
Bepaaldeassocirenmetdekleineenanderemetdegrote.
Antiparallel:deorintatieisparallelm.b.t.de5en3uiteinden,watgevolgenheeftvoor
hoehetcellulairsysteemermeeomgaat.
HetverlengingsprocesbijDNAreplicatieheefteenrichting:vanhet5vandenieuwe
strengnaarhet3,dusalleenaan3kunnendingenwordentoegevoegd:deleading
strand.DelaggingstrandwachttotereenstukDNAisvrijgekomenensynthetiseertdan
eenstukjevan5naar3Okazakifragmenten.OmdeOkazakifragmentenaante
sluitenisereenmechanisme.
DNApolymeraseisdekatalysator.
19
Erzijnverschillendesoortenhelices:
ADNAiseencompacterehelix.
BDNAiseenklassiekehelix.
ZDNAiseenlinkshandigehelix.
Andereruimtelijkestructurenzijnhetgevolgvandespecifiekenucleotidensequentieen
zelfcomplementariteitpalindroom,spiegelbeeld,haarspeld,kruisvormig.
DestructuurvanRNAiscomplex:enkelstrengig,lokaaldubbelstrengig,dubbelstrengig,
Eriseenneigingtotrechtshandigehelixvormingeneriscomplexiteitdoor
zelfcomplementariteit.
Nuclenezuurchemie
DNAkangedenatureerdworden:Hbruggenbreken,danwordtheteenenkelestreng
i.p.v.dubbel.DitgebeurtbijextremepHofhogetemperaturen,verstorenvande
Hbindingen,scheikundigestoffen,ontwindendubbelehelix.
Herstelvandeconditiesis
renaturatie:van2enkelenaareen
dubbelstreng.
Onderfysiologischrelevante
omstandighedenisdenaturatieniet
waarschijnlijk,tochishetvoorveel
processennoodzakelijk(vb.voor
duplicatie/mRNA).Enzymenhebben
hierbijeenbelangrijkerol:ditgebeurt
danzeergecontroleerd.
Alsdefactorvoordenaturatie
wegvalt,gebeurterrenaturatie,waar
geenmechanismevoornodigis.
Denaturatiecurve:%denaturatieis
hetpercentageHbruggendat
verbrokenis.Metdezecurvekunnen
hittegevoelighedenvergelekenworden.
G/Cgehalte:hoehogerhetG/Cgehalte,hoehogerT
m
wantdaarzitten3Hbindingenen
bijATmaar2.
Andere functies van nucleotiden
Energiedrager,cofactorvanenzymen,signaalmoleculen.
20
ATPisnietdeenigeenergiedrager,erisookGTP,CTP,UTP.GTPkanalsATPgebruikt
wordenenandersom.
Afsplitsenvandefosfaatgroepgeeft30kJ/molenergie:vanATPnaarADP.
Verbrekenvandeesterbindinggeeft14kJ/molenergie:naarAMP.Deeigenlijke
energiezitdusindebindingvande2laatstefosfaatgroepen.
CoenzymA:cofactorinondermeerhetvetmetabolisme,afgeleidvanadenosineals
nucleoside.
NAD
+
:nicotinamideadeninedinucleotide,cofactorino.a.hetkoolhydraatmetabolisme.
Signaalmoleculen,regulatorvanmetabolisme,vanreproductie,...
21
You might also like
- Biologie Voor Jou VWO Zakboek, VWO3 (2014)Document22 pagesBiologie Voor Jou VWO Zakboek, VWO3 (2014)Daan KulmanNo ratings yet
- ToetsDocument42 pagesToetsBo StruijkNo ratings yet
- 2023 24 THK 114 KoolhydraatmetabolismeDocument19 pages2023 24 THK 114 Koolhydraatmetabolismekorat63749No ratings yet
- Natuurwetenschappen 1Document14 pagesNatuurwetenschappen 1mathijs_clarysseNo ratings yet
- De Chemische Samenstelling Van CellenDocument5 pagesDe Chemische Samenstelling Van CellenBis2n M2diNo ratings yet
- CelbiologieDocument22 pagesCelbiologiev5b9z26rp2No ratings yet
- CelbiologieDocument57 pagesCelbiologieNette de BruijnNo ratings yet
- Moleculair KokenDocument26 pagesMoleculair KokenHana JafaryNo ratings yet
- HC 2.2 Chemische Bindingen en MacromoleculenDocument6 pagesHC 2.2 Chemische Bindingen en MacromoleculenkkstschhhcNo ratings yet
- Hoofdstuk 3 BiomoleculenDocument85 pagesHoofdstuk 3 BiomoleculenStella AlekianNo ratings yet
- Biologie Thema6Document8 pagesBiologie Thema6anoukloykensNo ratings yet
- 3VWOoefentoetsH4H5antw1Document4 pages3VWOoefentoetsH4H5antw1bo op de weeghNo ratings yet
- Vwo StofwisselingDocument49 pagesVwo StofwisselingPooja JaganNo ratings yet
- Biologie Havo 5Document13 pagesBiologie Havo 5Rosanne BurgersNo ratings yet
- Opdracht Bouwen KoolhydratenDocument5 pagesOpdracht Bouwen KoolhydratendflhkjNo ratings yet
- Biologie SamenvattingDocument13 pagesBiologie SamenvattingburnerballerbrandNo ratings yet
- Antwoorden Examenvragen Deel BarelDocument12 pagesAntwoorden Examenvragen Deel BarelcnnTNo ratings yet
- BIOLOGIE: Samenvatting h2: Chemische Stoffen in OrganismenDocument6 pagesBIOLOGIE: Samenvatting h2: Chemische Stoffen in OrganismenlolauytdehaageNo ratings yet
- Thema 2 Chemische StoffenDocument9 pagesThema 2 Chemische StoffenJAtochNo ratings yet
- Samenvatting BiochemieDocument11 pagesSamenvatting BiochemieJulian BakkerNo ratings yet
- Scheikunde Polymeren PODocument16 pagesScheikunde Polymeren POTobias WertheimNo ratings yet
- Samenvatting Q2 MGZDocument73 pagesSamenvatting Q2 MGZggghuhNo ratings yet
- CM Samenvatting ZelfstudieDocument48 pagesCM Samenvatting Zelfstudiealidebalo1No ratings yet
- Voorbeeldexamen Scheikunde Havo 2015 OpgavenDocument15 pagesVoorbeeldexamen Scheikunde Havo 2015 OpgavenMax JansenNo ratings yet
- 4S LP 2-2 1.2 de AtoombindingDocument7 pages4S LP 2-2 1.2 de AtoombindingYash PanchamNo ratings yet
- Scheikunde Samenvatting Hoofdstuk 10 en 11Document5 pagesScheikunde Samenvatting Hoofdstuk 10 en 11brittkoster09No ratings yet
- Bacteriologie SamenvattingDocument51 pagesBacteriologie SamenvattingEvelyne RedeleNo ratings yet
- 7 0 BVJ Havo 4b UitwerkingenDocument101 pages7 0 BVJ Havo 4b UitwerkingenvanluikgijsbertNo ratings yet
- Inspanningsfysiologie CollegesDocument55 pagesInspanningsfysiologie CollegesTamar FoppenNo ratings yet
- Hoofdstuk 1 TM 6 Cell BiologyDocument10 pagesHoofdstuk 1 TM 6 Cell BiologyMaxime PeerenboomNo ratings yet
- VoorbeeldDocument8 pagesVoorbeeldMeander KloostermanNo ratings yet
- Celbiologie CollegesDocument26 pagesCelbiologie CollegesAmanda HolstNo ratings yet
- MMS - Bepaling Van de Effectiviteit Van Chlorine Dioxide in de Behandeling Van COVID 19Document34 pagesMMS - Bepaling Van de Effectiviteit Van Chlorine Dioxide in de Behandeling Van COVID 19Paula de JongeNo ratings yet
- PolymeerchemieDocument108 pagesPolymeerchemieThaVinciNo ratings yet
- Stuvia 1933270 Bgz2021 Uitgebreide Samenvatting Taken CollegesDocument395 pagesStuvia 1933270 Bgz2021 Uitgebreide Samenvatting Taken CollegesCarmen SteynNo ratings yet
- MondDocument2 pagesMondMirtheNo ratings yet
- Samenvatting de Cel dt1Document23 pagesSamenvatting de Cel dt1xiaoyoubergerNo ratings yet
- Biologie Hoofdstuk 11Document9 pagesBiologie Hoofdstuk 11133354No ratings yet
- Lichaam en Mond Deel 1Document50 pagesLichaam en Mond Deel 1yana vercruysseNo ratings yet
- Mindmap Sachariden Deel 1Document1 pageMindmap Sachariden Deel 1viktorhaak2006No ratings yet
- Biologie Samenvatting Thema 3Document3 pagesBiologie Samenvatting Thema 3nesideNo ratings yet
- DE CEL SamenvattiingDocument10 pagesDE CEL Samenvattiingmohaadib03No ratings yet
- 2e - Ba - DGK - Fysiologie - Pathofysiologie - II - Les - 2NIEUWNIEUWNIEUW Kopie PDFDocument10 pages2e - Ba - DGK - Fysiologie - Pathofysiologie - II - Les - 2NIEUWNIEUWNIEUW Kopie PDFBabs MuyldermansNo ratings yet
- BLG 1501 - Basiese BiologieDocument69 pagesBLG 1501 - Basiese BiologieWillenay Jantjies100% (1)
- Celbiologie 1Document28 pagesCelbiologie 1A van der MeulenNo ratings yet
- Mindmap Sachariden Deel 2Document1 pageMindmap Sachariden Deel 2viktorhaak2006No ratings yet
- MK 1.2aDocument11 pagesMK 1.2anoelle02.smitNo ratings yet
- 15 - Februari Kopie PDFDocument39 pages15 - Februari Kopie PDFBabs MuyldermansNo ratings yet
- Polyfunctionele KoolstofverbindingenDocument5 pagesPolyfunctionele Koolstofverbindingenarthur.dewildeNo ratings yet
- Examen Anatomie FinalDocument56 pagesExamen Anatomie FinalinkaNo ratings yet
- CelfysiologyDocument71 pagesCelfysiologyHanne Leysen0% (1)
- Hoorcollege 14 & 15Document4 pagesHoorcollege 14 & 15Meander KloostermanNo ratings yet
- Samenvatting Mgot 2Document40 pagesSamenvatting Mgot 2xiaoyoubergerNo ratings yet
- Practicum 5 en 6Document3 pagesPracticum 5 en 6Meander Kloosterman0% (2)
- Dyslipidemia (Hadeel Hlayel)Document56 pagesDyslipidemia (Hadeel Hlayel)Natsku AE100% (1)
- Biologie SamenvattingDocument4 pagesBiologie SamenvattingLaurens Eeftinck SchattenkerkNo ratings yet