Professional Documents
Culture Documents
Resumen: Practica Nº2 Velocidad de Las Reacciones Químicas
Resumen: Practica Nº2 Velocidad de Las Reacciones Químicas
Uploaded by
Derin BenitesOriginal Description:
Original Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Resumen: Practica Nº2 Velocidad de Las Reacciones Químicas
Resumen: Practica Nº2 Velocidad de Las Reacciones Químicas
Uploaded by
Derin BenitesCopyright:
Available Formats
PRACTICA Nº2 VELOCIDAD DE LAS REACCIONES QUÍMICAS
Resumen
En la presente práctica se tocara el tema de la velocidad de las
reacciones, para ello realizaremos algunos procesos experimentales con
la finalidad de determinar de forma cuantitativa la velocidad, aprender a
realizar las gráficas de velocidad a través de la variación en las
concentraciones en función a los tiempos.
Laboratorio de Química General AII
1
PRACTICA Nº2 VELOCIDAD DE LAS REACCIONES QUÍMICAS
Introducción
En la naturaleza de las reacciones se poder evaluar diversos aspectos,
entre ellos está la velocidad con la que las misma se realiza, la cual
podría servirnos para analizar por ejemplo si se debería agregar mayor
cantidad de reactantes, elevar la temperatura o modificar otros factores
a fin de lograr una reacción eficaz, en esta práctica nos enfocaremos en
demostrar experimentalmente los cálculos
Laboratorio de Química General AII
2
PRACTICA Nº2 VELOCIDAD DE LAS REACCIONES QUÍMICAS
Historia
Antes de 1900, el gran foco de la cinética en las reacciones químicas consistía en
establecer leyes naturales acerca de la rapidez de estas. Existieron diferentes
estudios desde hace más de 200 años,
cuando Wenzel en 1771 notó que la
disolución de zinc y cobre en ácido no era
instantánea, sino que tomaba un tiempo
finito de tiempo. Posteriormente en 1778,
Priestley encontró que la cantidad de
tiempo requerido para transformar el
Laboratorio de Química General AII
3
PRACTICA Nº2 VELOCIDAD DE LAS REACCIONES QUÍMICAS
óxido de mercurio en mercurio elemental era dependiente la cantidad de oxigeno
presente. Así se consideró que las primeras medidas sobre las velocidades de las
reacciones químicas mostraban que existía un tiempo finito para que se llevaran a
cabo, sin embargo, aún no se entendían bien estos fenómenos (Massel, 2001).
En una serie de artículos publicados entre 1860 y 1879, los científicos Hercourt y
Essen mostraron que existía una relación entre la rapidez de las reacciones químicas
y la concentración de los reactivos. Este período histórico es muy importante ya que
químicos como Bernoulli, Joule, Kronig y particularmente Maxwell, permitieron a
través de la teoría cinética de los gases determinar bases conceptuales para
comprender diferentes fenómenos y poder estudiarlos con nuevas teorías, por
ejemplo la Teoría de las Probabilidades (Niaz, 2009). Durante los siguientes años,
en1886 Van´t Hoff propuso la idea para mostrar que la rapidez de las reacciones era
una función de la concentración en el reactor y de la temperatura. Arrhenius
cuantificó el comportamiento sobre la temperatura en la rapidez de una reacción
química y Menschutkin mostró que la rapidez también variaba con la estructura de
las moléculas y la naturaleza de los disolventes (Massel, 2001).
Las primeras teorías de la rapidez de una reacción fueron propuestas entre 1889 y
1930. En 1889 Arrhenius escribió una famosa publicación –Estudios de dinámica
química- donde propuso que las reacciones eran activadas porque sólo las
moléculas “calientes” en realidad pueden reaccionar. Eso condujo a la idea que la
rapidez de una reacción era determinada por la rapidez de colisión de las moléculas
“calientes”. En 1918, Trautz y Lewis cuantificaron la idea mostrando que la rapidez de
una reacción era igual a la rapidez de la colisión, por la probabilidad de que la
colisión conduzca a la reacción. El modelo resultante se llamó Teoría de colisiones,
el cual sigue vigente (Massel, 2001).
Laboratorio de Química General AII
4
PRACTICA Nº2 VELOCIDAD DE LAS REACCIONES QUÍMICAS
Actualmente, la Cinética de las Reacciones Químicas se considera una rama de la
Termodinámica, la cual investiga los estados intermedios (desequilibrios) de las
transformaciones físico-químicas desde la variable tiempo, la cual es
inherentemente dependiente del camino que siguen tales procesos. Así sobre la
base del concepto de reversibilidad en el equilibrio químico, desde un enfoque
macroscópico, es que parámetros como temperatura, presión, concentración,
etc…toman una importancia significativa, los estudios se basan en estados de
equilibrio y procesos reversibles desde un enfoque microscópico por lo que trabaja
sobre parámetros como temperatura, presión, etc. La diferencia entre la Cinética y
la Termodinámica, es que la primera estudia los procesos físicos y químicos
tomando en cuenta la perspectiva temporal.
Laboratorio de Química General AII
5
PRACTICA Nº2 VELOCIDAD DE LAS REACCIONES QUÍMICAS
Fundamentos teóricos
Velocidad de reacción
La velocidad de reacción nos indica lo rápido que se efectúa la reacción, se define como la
cantidad de sustancia que se transforma en la unidad de tiempo. Esta, depende de diversos
factores entre los cuales están la naturaleza de los reactivos, facilidad con que los reactivos
entran en contacto, concentración de los reactivos, temperatura del sistema reaccionante,
presencia de un catalizador.
Teoría de colisiones
Propuesta por Gilbert N. Lewis y otros químicos, afirma que para que ocurra un cambio
químico es necesario que las moléculas de la sustancia o sustancias iniciales entren en
contacto mediante una colisión o choque.
Pero no todos los choques son iguales. El
choque que provoca la reacción se
denomina choque eficaz y debe cumplir
estos dos requisitos:
- Que el choque genere la suficiente
energía para romper los enlaces
entre los átomos (energía de activación).
- Que el choque se realice con la orientación adecuada para formar la nueva molécula.
Los choques que no cumplen estas condiciones y no dan lugar a la reacción, se denominan
choques ineficaces. A veces, el paso de reactivo a producto se realiza mediante la
Laboratorio de Química General AII
6
PRACTICA Nº2 VELOCIDAD DE LAS REACCIONES QUÍMICAS
formación de un compuesto intermedio o complejo activado que se transformará
posteriormente en los productos.
La energía de activación: en química es la energía que necesita un sistema antes de poder
iniciar un determinado proceso. La energía de activación suele utilizarse para denominar la
energía mínima necesaria para que se produzca una reacción química dada. Para que
ocurra una reacción entre dos moléculas, éstas deben colisionar en la orientación correcta y
poseer una cantidad de energía mínima.
Orden de reacción
La ley de velocidad es la relación empírica entre la velocidad y la concentración de reactivos
en cualquier instante. Se determina experimentalmente y es de la forma:
v=k·[A]m · [B]n
Donde k se llama constante de velocidad.
Los exponentes m y n, de la ley de velocidad, se llaman órdenes parciales de la reacción
con respecto a los reactivos A y B, respectivamente. La suma m + n se llama orden total de
la reacción. En general, m y n no coinciden con los coeficientes estequiométricos.
Laboratorio de Química General AII
7
PRACTICA Nº2 VELOCIDAD DE LAS REACCIONES QUÍMICAS
En una reacción cuyo orden de reacción con respecto a A es uno (reacción de primer
orden) hay una relación lineal entre la concentración y la velocidad. Por tanto si la
concentración de A se duplica la velocidad se duplica, si se cuadriplica, la velocidad se
cuadriplica y si la concentración se reduce a la mitad, la velocidad se reduce a la mitad.
Ecuación de Arrhenius
La ecuación de Arrhenius: K = K0 · e-EACT/RT, nos define como varía la constante cinética,
K, con la temperatura, T, determina el factor de frecuencia K0. Recuerda que R tiene un
valor de 8,31·10-3 kJ·mol-1
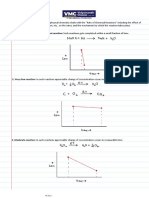
Si tomamos logaritmos neperianos a la ecuación de
Arrhenius, nos queda una ecuación que representará una
recta de pendiente negativa: ln K = ln K0 - (EACT/R) · 1/T.
Si representamos gráficamente para una determinada
reacción el logaritmo neperiano de K frente a 1/T se
obtendrá una recta cuya ordenada en el origen es el factor
de frecuencia K0 y la pendiente - EACT/R, de cuyo valor se
podrá extraer la energía de activación.
Si representamos en un papel milimetrado en el eje de
ordenadas los valores del ln K y en el eje de abcisas los
valores de 1/T. Determinamos la pendiente de la recta
Laboratorio de Química General AII
8
PRACTICA Nº2 VELOCIDAD DE LAS REACCIONES QUÍMICAS
obtenida y multiplícala por el valor de R (8,31•10-3kJ•mol-1) deberías obtener la energía de
activación.
EACT = |pendiente| • R
Ahora de la ordenada en el origen (punto de corte con el eje de ordenadas) podemos
obtener el valor del factor de frecuencia K0, este valor será:
Como la ordenada en el origen = ln K0 ð K0 = e (ordenada origen)
Fundamentos de la reacción:
Se ha seleccionado una reacción cuya cinética es fácil de medir para determinar el avance
de la reacción se emplea la reacción de oxidación de alcoholes con cromo (VI)
El K2Cr2O7 se transforme en HCrO4- , en medio acido (HCl)
C𝑟2 𝑂72− + 𝐻2 𝑂 + 𝐻𝐶𝑙 → 2 𝐻𝐶𝑟𝑂4− Solución “A”
Al reaccionar con la solución A, el etanol se oxida a ácido acético según la siguiente
reacción:
+ 3+
3𝐻2 𝐻5 𝑂𝐻(𝑎𝑐) + 4𝐻𝐶𝑟𝑂4(𝑎𝑐) + 16𝐻(𝑎𝑐) → 3𝐶𝐻3 𝐶𝑂𝑂𝐻(𝑎𝑐) + 4𝐶𝑟(𝑎𝑐) + 13𝐻2 𝑂
NARANJA VERDE
La ley de la velocidad para esta reacción se expresa como:
𝑉 = 𝑘[𝑐2 𝐻5 𝑂𝐻] 𝑋 [𝐻𝐶𝑟𝑂4− ]𝑌 [𝐻]𝑍
Sin embargo si las concentraciones de etanol y de ácido son suficientemente grandes, se
puede considerar que la variación es despreciable durante la reacción, por lo tanto
[𝐶2 𝐻5 𝑂𝐻] y [𝐻 + ] se hacen prácticamente constantes y la ley de la velocidad se puede
reducir a:
𝑉 = 𝑘[𝐻𝐶𝑟𝑂4− ]𝑌
La velocidad de una reacción se expresa en términos de la desaparición de los reactantes y
de la aparición de los productos, en un tiempo dado. Toda reacción química surge del
número de choques eficaces entre las partículas (moléculas, iones...) de las sustancias
reaccionantes. Este número es proporcional a la cantidad de partículas que se encuentran
en la disolución (concentración).
Una medida de la velocidad de reacción es, pues, la relación entre el cambio de la
concentración molar de un reaccionante o de un producto y el tiempo de cambio. Sea la
reacción:
A+B C+D
Laboratorio de Química General AII
9
PRACTICA Nº2 VELOCIDAD DE LAS REACCIONES QUÍMICAS
A y B se gastan, por tanto su concentración decrece en un tiempo t, por el contrario la
concentración de C y D aumenta en el mismo tiempo de reacción.
La velocidad media de la reacción se puede expresar:
Si en la reacción anterior la concentración de la sustancia B es tan alta, respecto a la de A,
que podemos considerarla constante durante toda la reacción, esta velocidad dependerá
en cada instante de la variación de la concentración molar de A.
Por otra parte, un cambio en la temperatura de los reaccionantes se traduce en un
incremento de la velocidad de sus partículas, de su energía cinética, de los choques eficaces
y, en consecuencia de la velocidad de reacción. En muchas reacciones, la velocidad de la
misma se duplica cuando la temperatura aumenta 10ºC.
Ciertas sustancias, llamadas catalizadores, cambian la velocidad de reacción. Su sola
presencia modifica la energía de activación, traduciéndose en una variación del número de
choques eficaces entre las partículas reaccionantes.
En la velocidad de una reacción química influyen varios factores; entre ellos, los más
importantes son la concentración de los reactivos, la presencia de catalizadores y la
temperatura de la reacción.
Aunque todos los factores mencionados pueden afectar las reacciones químicas
simultáneamente, puede plantearse la experiencia de forma que se mantengan constantes
todos los factores excepto uno en cada ensayo.
Para observar estos efectos utilizaremos una reacción cuyo final es fácilmente determinable.
La reacción que utilizaremos es:
a) IO3- + 3 HSO3- I - + 3 SO42- + 3 H+
El I- que se va produciendo, reaccionará con IO3- el dando I2, pero aún así queda HSO3- ;
este yodo molecular, reaccionará otra vez dando I-.
b) I2 + HSO3- 2 I- + SO42- + 3 H+
Tan solo cuando se haya consumido todo el HSO3- (final de la reacción) podrá reaccionar
el yoduro con el yodato:
c) IO3- + 5 I- + 6H+ 3I2 + 3 H2O
Todos los ensayos se van a realizar con exceso de ion yodato, para que una vez consumido
el ion hidrógeno sulfito presente en la disolución, el yodato sobrante oxide al ión yoduro
producido.
Laboratorio de Química General AII
10
PRACTICA Nº2 VELOCIDAD DE LAS REACCIONES QUÍMICAS
La formación de yodo en presencia de almidón, se detecta inmediatamente por la
presencia de color azul en la disolución, significando además que han terminado las
reacciones a) y b) y se inicia la reacción c).
Detalles Experimentales
1. Materiales y reactivos
Laboratorio de Química General AII
11
PRACTICA Nº2 VELOCIDAD DE LAS REACCIONES QUÍMICAS
Materiales: Reactivos:
2 vasos precipitados Solución A: 𝐻𝐶𝑟𝑂4− + 𝐻𝐶𝑙
Bureta de 50 ml Solución B: KI 3%
2 matraces Erlenmeyer 250 ml Solución C: Na2S2O3 0,022M
Pipeta de 2ml y de 5ml Etanol
Probeta de 50 ml Almidón
Soporte universal
Pinza para bureta
Bagueta
2. Proceso Experimental
A. Determinación de [𝐻𝐶𝑟𝑂4− ]0
Se enrasara la bureta de 50 ml con la solución “C”
Usando el vaso C , llenar 50 ml de la solución “C” 𝑁𝑎2 𝑆2 𝑂3 , 0,022𝑀
En un matraz Erlenmeyer agregar 5 ml de la solución “A” con una pipeta de 5ml
Con la pipeta de 2ml agregar 2ml de solución “B” KI al 3%m/m
Agregar 3 gotas del indicador almidón, esto ayudara a identificar la presencia de
yodo
Titular gota a gota hasta que llegue a una coloración verde claro (formación del
complejo yodo-almidon)
En la experiencia se usaron 5,9mL de la solcucion “C”
La ecuación de este proceso será:
− + − 3+
2 𝐻𝐶𝑟𝑂4(𝑎𝑐) + 14 𝐻(𝑐𝑐) + 6 𝐼(𝑐𝑐) → 3𝐼2(𝑎𝑐) + 2 𝐶𝑟(𝑎𝑐) + 8 𝐻2 𝑂(𝑙)
Al agregarle el almidón:
𝐼2(𝑎𝑐) + 2 𝑁𝑎2 𝑠2 𝑜3(𝑎𝑐) → 2 𝑁𝑎 𝐼 (𝑎𝑐) + 𝑁𝑎2 𝑆4 𝑂6(𝑎𝑐)
(+ Almidón) azul
Laboratorio de Química General AII
12
PRACTICA Nº2 VELOCIDAD DE LAS REACCIONES QUÍMICAS
B. Determinación de [HCrO-4]f
En un matraz Erlenmeyer colocar 50mL de la solución A (K2Cr2O7) más 1mL de
etanol , a partir de este momento se contara la velocidad de reacción
Trascurridos 10 min trasvasar una alícuota de 5mL a otro matraz y adicionarle 2mL
de la solución B (kI) y 10 gotas de almidón luego titular con la solución C (Na2S4O6)
hasta obtener un color verde claro, anotar el cambio de volumen en el cuadro N°1
repetir las mediciones cada 10 minutos hasta completar la tabla.
Tiempo (min) Solución “C” (mL) [HCrO-4] (M)
0 5.9
10 4.6
20 3.7
30 2.9
40 2.1
50 1.9
60 1.4
C. Cálculos:
𝑚𝑜𝑙 1
5,9𝑚𝑙 𝑥 0, ,22 𝑥 = 6,38 𝑥 10−4 𝑚𝑜𝑙
𝑙 103 𝑚𝑙
1 𝑚𝑜𝑙 𝐼2 2 𝑚𝑜𝑙 𝐻𝐶𝑟𝑂𝐻 − 𝐻𝐶𝑟𝑂𝐻 −
1,34 𝑥 10−5 𝑚𝑜𝑙 𝑁𝑎2 𝑆𝑂3 𝑋 𝑋 = 4,47 𝑥 10−5 𝑚𝑜𝑙𝑒𝑠 𝑑𝑒
2𝑚𝑜𝑙𝑒𝑠 𝑁𝑎2 𝑆𝑂3 3𝑚𝑜𝑙𝑒𝑠 𝐼2 5𝑚𝐿
200 𝐻𝐶𝑟𝑂𝐻 −
𝑥 (4,47 𝑥 10−5 𝑚𝑜𝑙𝑒𝑠 𝑑𝑒 ) = 8.94𝑥10−3 𝑀
200 5𝑚𝐿
Laboratorio de Química General AII
13
PRACTICA Nº2 VELOCIDAD DE LAS REACCIONES QUÍMICAS
Tabla Nº 1 y 2
Tiempo (min) Solución “C” (mL) [HCrO-4] (M)
0 5.9 8.94x10-3
10 4.6 6.74x10-3
20 3.7 5.42x10-3
30 2.9 4.25x10-3
40 2.1 3.08x10-3
50 1.9 2.19x10-3
60 1.4 2.05x10-3
Laboratorio de Química General AII
14
PRACTICA Nº2 VELOCIDAD DE LAS REACCIONES QUÍMICAS
Tabla Nº 3
∆[𝐻𝐶𝑟𝑂4− ] [𝐻𝐶𝑟𝑂4− ]
∆𝑡
2.2x10-4 6.74x10-3
1.32 x10-4 5.42x10-3
1.17 x10-4 4.25x10-3
1.17 x10-4 3.08x10-3
0.89 x10-4 2.19x10-3
0.14 x10-4 2.05x10-3
Laboratorio de Química General AII
15
PRACTICA Nº2 VELOCIDAD DE LAS REACCIONES QUÍMICAS
Conclusiones
Se dio a conocer que la velocidad de una reacción química se muestra a
través del cambio en las concentraciones con relación con al tiempo.
La ley de la velocidad relaciona la velocidad de la reacción con las
concentraciones de los reactivos, elevadas a las potencias apropiadas.
La vida media de una reacción se puede usar para determinar la constante
de velocidad de una reacción de primer orden.
Laboratorio de Química General AII
16
PRACTICA Nº2 VELOCIDAD DE LAS REACCIONES QUÍMICAS
Recomendaciones
Laboratorio de Química General AII
17
PRACTICA Nº2 VELOCIDAD DE LAS REACCIONES QUÍMICAS
Se recomienda titular gota a gota la solución para evitar gastar demás un
volumen
Se recomienda agitar constantemente la solución para optimizar el proceso
de titulación
Se recomienda sacar los 2 ml de solución en la parte.4.2 ni bien se cumplan
los 10 min
Tener en cuenta que el almidón no forma parte ni de los reactantes ni de los
productos, sino que es un indicador, de igual forma la titulación se podría
hacer sin la presencia del mismo.
Laboratorio de Química General AII
18
PRACTICA Nº2 VELOCIDAD DE LAS REACCIONES QUÍMICAS
Bibliografía
http://es.slideshare.net/FelipeSepulveda2/cintica-qumica-velocidad-de-reaccin
Domingo 13; 11:14 a.m.
https://es.wikipedia.org/wiki/Velocidad_de_reacci%C3%B3n Domingo 13; 11:52 a.m
http://cienciasenbachillerato.blogspot.pe/2011/05/velocidad-de-reaccion-y-
equilibrio.html Domingo 13; 12:25 pm.
http://www.gobiernodecanarias.org/educacion/3/usrn/lentiscal/1-cdquimica-tic/DIR-
Q/Cinneticaquimica/fundamento%20teorico.htm 11-09-15; 4:14 pm
http://fisica.universidadlaboralab.es/wordpress/.../velocidad-de-reaccion1.doc leído 16-
09-15 02:30 pm
https://cineticaquimica2013.wordpress.com/2013/02/20/brevehistoriadelacinetica/ leído 16-09-
15 02:19pm
Laboratorio de Química General AII
19
PRACTICA Nº2 VELOCIDAD DE LAS REACCIONES QUÍMICAS
Apéndice
Cuestionario
1.
2. Expliqué de manera breve, cual es la función del Na2S4O6 y porque su concentración de ser lo
exacta posible
Nos permite determinar cuál es la concentración del ion HCrO4- , el cual reacciona con el yoduro
para formar yodo molecular, su concentración debe ser lo más exacta posible para que al
momento de calcular la concentración del ion HCrO4- nos salgan valores más exactos y no tan
dispersos.
3. Uno de los factores que aumenta la velocidad de reacción es la temperatura. Explique, de
manera sencilla, como se podría demostrar este efecto en la experiencia del laboratorio.
4.
5. En la descomposición del NO2 a 383°C se encontraron los siguientes datos
Tiempo en s 0 5 10 15
[NO2] 0.10 0.017 0.009 0.0062
Demuestre que la descomposición del NO2 obedece a una reacción de segundo orden
Hallando el valor de k:
Laboratorio de Química General AII
20
PRACTICA Nº2 VELOCIDAD DE LAS REACCIONES QUÍMICAS
Tenemos
1 1
− = 𝑘 ∗ (15)𝑠
0.0062 𝑀⁄𝐿 0.10 𝑀⁄𝐿
𝐿
𝑘 = 10.09
𝑀∗𝑠
𝐿
Como k tiene las unidades de 𝑀∗𝑠 se demuestra que es una ecuación de segundo grado
Laboratorio de Química General AII
21
You might also like
- Greek and Roman Jewellery (Art History)Document168 pagesGreek and Roman Jewellery (Art History)MN D King Maker100% (4)
- The First Computers Were PeopleDocument39 pagesThe First Computers Were Peopleskywriter36No ratings yet
- Formal Written Lab Report - Experiment 1 - Group 1 (1st Year - Summer Sem)Document7 pagesFormal Written Lab Report - Experiment 1 - Group 1 (1st Year - Summer Sem)Cheska BiolenaNo ratings yet
- Chemical Rxns 1 Final ReportDocument20 pagesChemical Rxns 1 Final ReportNouran ShedidNo ratings yet
- Chemical KineticsDocument8 pagesChemical KineticsHosam Hasan Abd ElhadyNo ratings yet
- Chemical KineticsDocument3 pagesChemical KineticsSunny RohidaNo ratings yet
- Lecture Notes Chemical EngineeringDocument40 pagesLecture Notes Chemical Engineeringkrishnaswamy9No ratings yet
- Introduction Chemical KineticsDocument4 pagesIntroduction Chemical KineticsDenis PrasetiaNo ratings yet
- Practical Physical Chemistry CourseDocument68 pagesPractical Physical Chemistry CourseMahmoud AbdAllahNo ratings yet
- Rates and Rate Laws: SpectrosDocument6 pagesRates and Rate Laws: Spectrosdharul khairNo ratings yet
- Chem 17 Formal ReportDocument4 pagesChem 17 Formal Reportchemeister111No ratings yet
- Laboration - Biokemi Enzymer KatalasDocument30 pagesLaboration - Biokemi Enzymer KatalasAyla AlijaniNo ratings yet
- Chemical Kinetics FRDocument6 pagesChemical Kinetics FRJo FernandezNo ratings yet
- CHEMISTRYDocument10 pagesCHEMISTRYlifep7417No ratings yet
- 03 Homogeneous ReactorsDocument18 pages03 Homogeneous ReactorssanelisofuturemoyoNo ratings yet
- Introduction To Reaction Kinetics, Hazle CoxDocument83 pagesIntroduction To Reaction Kinetics, Hazle CoxcachorroingenieroNo ratings yet
- Approval SheetDocument25 pagesApproval SheetSelni Sandabunga'No ratings yet
- Chemical Kinetics 1234 FinalDocument22 pagesChemical Kinetics 1234 FinalJayesh SavaliyaNo ratings yet
- CBSE Class 12 Chemistry Notes: Chemical Kinetics: HomepageDocument14 pagesCBSE Class 12 Chemistry Notes: Chemical Kinetics: HomepageBHAVYA BNo ratings yet
- Arrianna Peter - Exp 3Document25 pagesArrianna Peter - Exp 3Arrianna PeterNo ratings yet
- 1 Chemical Kinetics and EquilibriumDocument77 pages1 Chemical Kinetics and EquilibriumApril Mergelle Lapuz100% (1)
- Introduction To Chemical KineticsDocument10 pagesIntroduction To Chemical Kineticsraimasharma024No ratings yet
- Name:Saiful Islam Bin Ahmad HusniDocument11 pagesName:Saiful Islam Bin Ahmad Husninike7No ratings yet
- C117Sec1 Group-4 Expt-1 LabReportDocument7 pagesC117Sec1 Group-4 Expt-1 LabReportJazer John Tacda LirazanNo ratings yet
- Lecture 4a. Chemical Kinetics 2020Document23 pagesLecture 4a. Chemical Kinetics 2020Montassar DridiNo ratings yet
- Justice 3Document27 pagesJustice 3Arierhi JusticeNo ratings yet
- Kinetics Lecture NotesDocument31 pagesKinetics Lecture NoteschweetomahiNo ratings yet
- Reaction KinetcisDocument5 pagesReaction KinetcisIrtizahussainNo ratings yet
- Kinetics DR JagadishDocument37 pagesKinetics DR JagadishVikas KumarNo ratings yet
- Formal Lab Report - Expt 2 Sample2bDocument17 pagesFormal Lab Report - Expt 2 Sample2bkamyar moradiNo ratings yet
- Lab Chem 3 :kinetics-Factor Affecting Rate of ReactionDocument2 pagesLab Chem 3 :kinetics-Factor Affecting Rate of ReactionNadiah Matarsim60% (5)
- Experiment 5 Chemical Kinetics: Rate Reaction: I. Experiment's Date: April, 11 2017 II. ObjectiveDocument17 pagesExperiment 5 Chemical Kinetics: Rate Reaction: I. Experiment's Date: April, 11 2017 II. Objectiveyokehong tanNo ratings yet
- Combustion Part3 WatermarkDocument23 pagesCombustion Part3 Watermark84105851No ratings yet
- SS 2 Week 3Document71 pagesSS 2 Week 3Denzel MusaNo ratings yet
- Chemistry Notes Puspanjali PDFDocument85 pagesChemistry Notes Puspanjali PDFDURGA PRASADNo ratings yet
- Chemical Kinetics-1 NotesDocument14 pagesChemical Kinetics-1 NotesRachit rajputNo ratings yet
- Reporte #11Document10 pagesReporte #11EDWIN PAUL MONTAÑEZ CALACHUANo ratings yet
- CREII-Module-I - Lecture 1Document38 pagesCREII-Module-I - Lecture 1Aditya parasNo ratings yet
- Chapter # 11 Reaction KineticsDocument24 pagesChapter # 11 Reaction KineticsAnoshKhanNo ratings yet
- Melc 130 138 Chemical KineticsDocument36 pagesMelc 130 138 Chemical KineticsAlayna AlejagaNo ratings yet
- Informe 8 Cinetica QuimicanbDocument5 pagesInforme 8 Cinetica QuimicanbKimberly SánchezNo ratings yet
- Chemical Kinetics PDFDocument8 pagesChemical Kinetics PDFAlexandra minNo ratings yet
- Chemical Kinetics Continuation Co4Document26 pagesChemical Kinetics Continuation Co4dexterNo ratings yet
- Chemical EquilibriumDocument34 pagesChemical EquilibriumLala Rifa0% (1)
- Introduction, K Inetics, Therm Odynam IcsDocument13 pagesIntroduction, K Inetics, Therm Odynam IcsJonathan ByamunguNo ratings yet
- Chemical Kinetics ProjectDocument31 pagesChemical Kinetics ProjectArul VNo ratings yet
- Experiment 6 FinalDocument13 pagesExperiment 6 FinalFroileth Pulido100% (1)
- PDF Revised Chemical Kinetics and CatalysisDocument68 pagesPDF Revised Chemical Kinetics and CatalysisTomateGreenNo ratings yet
- Physical Chemistry Chemical KineticsDocument10 pagesPhysical Chemistry Chemical Kineticsبلسم محمود شاكرNo ratings yet
- Chem 1108 Reflection No 4Document3 pagesChem 1108 Reflection No 4Renato BatumbakalNo ratings yet
- Chapter 16.1 Dan 16.2Document11 pagesChapter 16.1 Dan 16.2jihanfazlinaNo ratings yet
- I. Title of Experiment: II. Date of Experiment: Iii. The End of Experiment: IV. Purpose of Experiment: V. Basic Theories A. Reaction RateDocument14 pagesI. Title of Experiment: II. Date of Experiment: Iii. The End of Experiment: IV. Purpose of Experiment: V. Basic Theories A. Reaction RateputriNo ratings yet
- IB HL Chemistry Assessment Statements Topic 6 and 16Document4 pagesIB HL Chemistry Assessment Statements Topic 6 and 16AndrewNo ratings yet
- 3.0 Accounting For The Rate LawsDocument5 pages3.0 Accounting For The Rate LawsomoljavanNo ratings yet
- Chemical KineticsDocument26 pagesChemical KineticsyusrahgoldNo ratings yet
- AssignmentDocument5 pagesAssignmentAnsel MercadejasNo ratings yet
- Chapter 9Document18 pagesChapter 9JeromeNo ratings yet
- Summary of Learnings (Chemical Kinetics)Document3 pagesSummary of Learnings (Chemical Kinetics)Kath PagilaganNo ratings yet
- Reflection Paper 4Document3 pagesReflection Paper 4Paul Winston RegaladoNo ratings yet
- Physico-Chemistry of Solid-Gas Interfaces: Concepts and Methodology for Gas Sensor DevelopmentFrom EverandPhysico-Chemistry of Solid-Gas Interfaces: Concepts and Methodology for Gas Sensor DevelopmentNo ratings yet
- Tank BlanketingDocument27 pagesTank Blanketingkhali54100% (1)
- Project On FacebookDocument12 pagesProject On FacebookKrish ShewaniNo ratings yet
- SMART Objective RubricDocument1 pageSMART Objective RubricKeren HapkhNo ratings yet
- st10f269 DsDocument160 pagesst10f269 DsДрагиша Небитни ТрифуновићNo ratings yet
- E45 Laboratory4Document7 pagesE45 Laboratory4nickNo ratings yet
- Factors Affecting The Tardiness of Selected Senior High Students of Queen Anne School Santa Rosa S.Y. 2010-2020Document11 pagesFactors Affecting The Tardiness of Selected Senior High Students of Queen Anne School Santa Rosa S.Y. 2010-2020Shai Anne Cortez100% (2)
- (LIT) LS90 LS110 LS160 BrochureDocument20 pages(LIT) LS90 LS110 LS160 BrochureJuan Carlos Reinhold Niembro SuchowitzkiNo ratings yet
- Danfoss Vane Tip LUG SylaxDocument18 pagesDanfoss Vane Tip LUG SylaxmaggamNo ratings yet
- Msi MPG b550 Gaming PlusDocument68 pagesMsi MPG b550 Gaming PlusMarvelous WololoNo ratings yet
- 5354 3fl A4 Brochure FADocument6 pages5354 3fl A4 Brochure FAennuar gazabonNo ratings yet
- 10 मानव स्वास्थ्य एवं रोगDocument12 pages10 मानव स्वास्थ्य एवं रोगraghuwanshimahashivNo ratings yet
- Staffing: The Management and Nonmanagerial Human Resources InventoryDocument22 pagesStaffing: The Management and Nonmanagerial Human Resources InventorySophia Pintor0% (1)
- Ca Q&aDocument129 pagesCa Q&aRavi TejaNo ratings yet
- Collaborative Publishing Lecture JOURNALISTS' GROUP 2013Document125 pagesCollaborative Publishing Lecture JOURNALISTS' GROUP 2013Geoffrey Tolentino-Unida94% (48)
- Get All Employee Details From The Employee TableDocument23 pagesGet All Employee Details From The Employee TableSachin KumarNo ratings yet
- Confessions of Some High Ranking 1Document111 pagesConfessions of Some High Ranking 1Habilian AssociationNo ratings yet
- Metaverse Tourism Conceptual Framework and Research PropositionsDocument8 pagesMetaverse Tourism Conceptual Framework and Research PropositionsMarc MonerNo ratings yet
- 6 Key Challenges For Financial Close and ReportingDocument7 pages6 Key Challenges For Financial Close and ReportingGodfrey KakalaNo ratings yet
- CD Account Opening FormDocument2 pagesCD Account Opening FormYeshi WangmoNo ratings yet
- Simatic ManagerDocument19 pagesSimatic ManagerNabilBouabana100% (2)
- Storage Regulations For Petroleum ProductsDocument3 pagesStorage Regulations For Petroleum ProductsSaumyaChandraNo ratings yet
- Hitachi Trouble ShootingDocument18 pagesHitachi Trouble Shootingjacklyn ade putra75% (4)
- Radar Plotting SheetDocument1 pageRadar Plotting SheetAlfathir VarokahNo ratings yet
- (The Logic of Political Survival) .Bruce Bueno de Mesquita, Alastair Smith, Randolph M. Siverson, James D. Morrow PDFDocument551 pages(The Logic of Political Survival) .Bruce Bueno de Mesquita, Alastair Smith, Randolph M. Siverson, James D. Morrow PDFjasonnijmh100% (1)
- ISKCON Desire Tree - Krishna Showing Universal FormDocument29 pagesISKCON Desire Tree - Krishna Showing Universal FormISKCON desire treeNo ratings yet
- Why Critical Thinking Is ImportantDocument3 pagesWhy Critical Thinking Is ImportantMehreen KandaanNo ratings yet
- BiomesDocument23 pagesBiomesdipon deb nathNo ratings yet
- Resume Keerthana PG PDFDocument1 pageResume Keerthana PG PDFVivek GNo ratings yet