Professional Documents
Culture Documents
Sistem Kalkon Flavanon Bahan Turunan Asatofanon Banzaldahld
Sistem Kalkon Flavanon Bahan Turunan Asatofanon Banzaldahld
Uploaded by
Dewi WulandhariOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Sistem Kalkon Flavanon Bahan Turunan Asatofanon Banzaldahld
Sistem Kalkon Flavanon Bahan Turunan Asatofanon Banzaldahld
Uploaded by
Dewi WulandhariCopyright:
Available Formats
Indonesian Journal of Chemistry
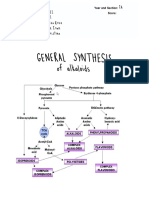
SYNTHESIS OF CHALCONE AND FLAVANONE
COMPOUND USING RAW MATERIAL OF ACETOPHENONE
AND BENZALDEHYDE DERIVATIVE
Sistem Senyawa Kalkon dan Flavanon Menggunakan Bahan Dasar Senyawa
Turunan Asatofanon dan Banzaldahld
ISMIYARTO
Chemistry Dept., Diponegoro University, Semarang
SABIRIN MATSJEH, CHAIRIL ANWAR
Chemistry Dept., Gadjah Mada University, Yogyakarta
ABSTRACT
Synthesis of flavanoid compounds of chalcone and flavanone groups have been conducted.
Flavanoid is one of the group natural products which is mostly found in plants and have been
proved to have physiological activity as drug. In this research, chalcone proup compounds that
being shinthesized are: chalcone, 3,4-dimethoxychalcone, 2'-hldroxy-3,4-dimethoxychalcone
where as compound of flavanone group that being sinthesized is 3’,4'-dlmethoxyflavanone.
The synthesis of chalcone group are carried out based on Claisen-Schmidt reaction by using
raw material of aromatic aldehydes and aromatic ketones. The synthesis in carried out by strirring
at the room temperature using alkali solution as catalyst and ethanol as solvent. The synthesis of
3',4'-dimethoxyflanone is made based on the nucleophilic 1,4 addition of the unsaturated a,p
ketone. The synthesis is made by refluxing 2'-hydroxy-3,4-dimethoxychalcone in alkali condition
for 12 hours. The identification of flavanoid compound is carried out by using spectroscopic IR,
GC-MS and 1H-NMR methods.
The result of each synthesis chalcone group are is follows: chalcone as yellowish solid with
m.p* 50°C and the yield is 83.39%; 3,4-dimethoxychalcone as yellow solid with m.p* 57°C and
the yield is 76.00% ; 2’-hydroxy-3,4-dimethoxychalcone as orange solid with m.p* 90°C and the
yield is 74.29%, for 3’,4'-dimethoxyflavanone as pale yellow solid with m.p* 80°C and the yield Is
72.00%.
Keywords: Claisen-Schmidt, Chalcone, Addition, Flavanone
PENDAHULUAN
Senyawa flavanoid adalah senyawa yang
mempunyai kerangka dasar yang terdiri dari
15 atom karbon, tersusun dari 2 inti fenolat
yang dihubungkan oleh tiga atom karbon [6].
Kerangka isoflavan
Penelitian mengenai senyawa flavanoid telah
Menurut Greissman dan Crout (1969) banyak dilakukan oleh para peneliti, baik, dari
kerangka senyawa flavanoid mempunyai 4 Indonesia maupun dari luar negeri. Sebagian
bentOk. Bentuk kerangka senyawa flavanoid besar topik penelitian tersebut melibatkan
teknik isolasi dan identifikasi senyawa
flavanoid yang terdapat dalam jenis tanaman
tertentu. Sebagai contohnya adalah Puyvelde,
dkk. (1989) telah berhasil mengisolasi
senyawa helikrisetln (2’,4’,4-trihidroksi-6-
metoksikalkon) termasuk senyawa kalkon dari
bunga Helichrysum odoratissimum.
Kerangka kalkon Kerangka flavan Linuma, dkk (1993) telah berhasil mengisolasi
:c£x>-‘
4
Kerangka auron
(±) leakianon G (5,7,2'4’-tetrahidroksi-8-
prenilflavanon) yang termasuk senyawa
flavanon dari tanaman Sophora leachiana.
Sebaliknya sedikit sekali dari penelitian
Ismiyarto, Sabirin Matsjeh, Chairil Anwar
Indonesian Journal of Chemistry 82
tersebut yang melibatkan adanya transformasi lebih lanjut, misalnya dehidrasi
pengembangan sintesis senyawa flavanoid. PI.
Salah satu metode sintesis senyawa Mekanisme reaksi kondensasi aldol
flavanoid telah berhasil dilakukan oleh Baker- menggunakan katalis basa melibatkan
Venkataraman dalam sintesis senyawa pembentukan karbanion pada senyawa
flavon. Sintesis senyawa tersebut melibatkan karbonil yang mempunyai atom Ha, diikuti
reaksi Claisen intramolekuler dengan dengan adisi karbanion tersebut pada
menggunakan bahan dasar benzilklorida dan senyawa karbonil yang sama atau senyawa
orfo-hidroksiasetofenon [1], Bu dan Li (1993) karbonil yang lain [3].
telah berhasil melakukan sintesis senyawa
flavanon yaitu (±) leakinon G dan Tahap adisi
eksiguaflavanon K (5,7,4'-trihidroksi-5'- Pembentukan karbanion
—
metoksi-8-prenilflavanon) dengan meng¬
gunakan bahan dasar turunan asetofenon dan
turunan benzaldehida.
R-CH-C + B® R-CH-CT +BH
Penelitian mengenai senyawa flavanoid tlHa \R.
R XR'
sering kali dikaitkan dengan manfaat senyawa
tersebut untuk kehidupan sehari-hari.
Senyawa flavanoid dapat digunakan sebagai Adisi nukleofilik
obat tradisional dan juga dapat dimanfaatkan
sebagai bahan dasar pembuatan zat warna.
R-CH2-C=0
t
+ R-CH-CT
©
— fi |*
2-C-CH-C=0
R-CH2-'
•U
Senyawa hesperidin yang termasuk senyawa \ ,
flavanon mempunyai aktifitas
memperkuat pembuluh darah kapiler yang
dalam
k
relatif lemah [7], serbuk kayu tanaman
mimosa tenuefolia L yang ternyata PfflinWsn wtQn
mengandung senyawa kalkon telah dikenal R' R' R' R' R'
oleh masyarakat Meksiko sebagai obat luka
bakar [4]. Senyawa flavon dan kalkon R-CH2-C-CH-C■O ♦ H-B
— R-CH2-C-I1 H-C=0 + B
mempunyai warna dominan kuning sehingga
dapat digunakan sebagai bahan dasar
pembuatan zat wama kuning.
.U OH
Berdasarkan uraian di atas maka perlu
adanya pengembangan mengenai sintesis
senyawa flavanoid. Hahlbrock telah Tahap dehidrasi
menyatakan bahwa senyawa-senyawa R'R' R'
flavanoid yang ada di alam ini merupakan
turunan senyawa kalkon melalui alur tertentu r,\
[10]. Hubungan antara senyawa kalkon /
RCH2
\R
dengan senyawa flavanoid tersebut OH
mendorong diadakannya kajian-kajian dari
segi reaksi kimia yang mungkin dilakukan di Reaksi kondensasi aldol silang yang
laboratorium dalam mensintesis senyawa melibatkan penggunaan senyawa aldehida
flavanoid lain dengan menggunakan zat aromatis dan senyawa alkil keton sebagai
antara senyawa kalkon. reaktannya dikenal sebagai reaksi Claisen-
Jenis senyawa flavanoid ditentukan oleh Schmidt. Dalam reaksi ini karbanion dari
bentuk kerangka dan gugus-gugus yang senyawa aldehida aromatis menghasilkan
terikat pada kerangkanya, sehingga untuk senyawa p-hidroksiketon, senyawa ini
mendapatkan jenis senyawa flavanoid yang selanjutnya mengalami dehidrasi
berbeda-beda perlu dilakukan variasi menghasilkan senyawa a,p-keton tak jenuh
terhadap bahan dasar yang digunakan. [3J.
Reaksi kondensasi aldol dapat dilakukan Biasanya ikatan n suatu alkena tidak
dengan menggunakan katalis basa. Syarat diserang oleh suatu nukleofilik tanpa
agar reaksi kondensasi aldol dapat diserang oleh elektrofilik terlebih dahulu.
berlangsung adalah salah satu atau kedua Senyawa karbonil tak jenuh a,p mempunyai
senyawa karbonil yang digunakan sebagai ikatan rangkap yang terkonjugasi dengan
reaktan harus mempunyai atom Ha. pada gugus karbonil sehingga Cp dapat
kondisi tertentu hasil reaksi akan mengalami mengemban muatan positif. Struktur
Ismiyarto, Sabidn Matsjeh, Chairil Anwar
Indonesian Journal of Chemistry 83
resonansi senyawa tersebut adalah sebagai Jalan penelitian
berikut: 0
Sintesis kalkon
CH2 SXIH- CHzÿCH.— ►
CH2-CH=C
Dituangkan 2,2 g (0,055 mol) NaOH
dalam 15 ml air dan 12 mL etanol ke dalam
labu leher tiga yang dilengkapi dengan
pengaduk magnet. Campuran didinginkan
Pada struktur resonansi di atas menunjukkan dengan pecahan es, selanjutnya 0,02 mol
bahwa Cp dapat mengemban muatan positif, asetofenon dituangkan dalam campuran dan
sehingga nukleofil dapat menyerangnya. segera diaduk. Sebanyak 0,02 mol
Berikut adalah adisi 1,4 nukleofilik pada benzaldehida dituangkan ke dalam campuran
senyawa karbonil tak jenuh a,p oleh serangan dan diaduk pada suhu kamar selama 3 jam.
ion sianida dari HCN dalam basa encer. Pada Campuran reaksi yang terjadi didinginkan di
reaksi adisi ini ion sianida dapat menyerang dalam kulkas selama 12 jam, selanjutnya
Cp atau karbon pada gugus karbonilnya. didiamkan pada suhu kamar selama 1 jam.
Mekanisme reaksi adisi nukleofilik pada C* padatan hasil reaksi disaring dengan
penyaring Buchner dan dicuci dengan air
sampai netral. Padatan diambil dan
CHÿCH-CS.—■■ CH2-C-l CH2-CH=C-CH3
ditentukan sifat fisiknya (titik lebur dan
warnanya), selanjutnya dianalisis dengan
\AH Li L, spektrometer IR (pelarut CCI4), UV-Vis
(pelarut metanol) dan 1H NMR (pelarut
/
»
r
■/.
l' HCN
CDCIp).
Sintesis 3,4-dimetoksikalkon
CH2-CH2-CV— CH2-CH=Cÿ + CtT Sintesis 3,4-dimetoksikalkon dilakukan
£N \H3 menggunakan prosedur yang sama seperti
dalam sintesis kalkon dengan bahan dasar
Mekanisme reaksi adisi nukleofilik pada asetofenon dan veratraldehida. Untuk sintesis
karbon auaus karbonil: 3,4-dimetoksikalkon pengadukan dilakukan
9 selama 24 jam pada suhu kamar. Analisis
? padatan hasil sintesis dilakukan dengan
CH2-CH-C7*— CH2-CH-LCH3—
CH2»CH-kcH3 CH2«CH-C-CH3+Ct?
< menggunakan spektrometer IR, UV-Vis
(pelarut metanol) dan 1H NMR (pelarut CCU).
CN Sintesis 2'-hidroksi-3, 4-dimetoksikalkon
Dituangkan larutan 2,2 gram (0,055 mol)
Halangan sterik di sekitar ikatan rangkap NaOH dalam 15 ml air dan 12 ml etanol ke
atom karbon gugus karbonil dapat dalam labu leher tiga yang telah dilengkapi
menyebabkan serangan tertuju pada posisi dengan pengaduk magnet dan termometer.
yang kurang terintangi. Aldehida mempunyai Campuran didinginkan dengan pecahan es,
atom karbon gugus karbonil yang kurang selanjutnya 0,02 mol orto-hidroksiasetofenon
terintangi, sehingga akan lebih mudah dituangkan ke dalam campuran dan segera
diserang suatu nukleofil dibandingkan pada diaduk. Sebanyak 0,02 mol veratraldehida
senyawa keton. dituangkan ke dalam campuran dan diaduk
pada suhu kamar selama 24 jam. Campuran
EKSPERIMEN reaksi diasamkan dengan HCI 5% dan hasil
reaksi pengasaman diekstraksi dua kali
Dalam penelitian ini, bahan-bahan yang masing-masing dengan 15 ml diklorometana.
digunakan adalah asam klorida, Selanjutnya lapisan diklorometana
benzaldehida, veratraldehida, etanol, natrium dikeringkan dengan Na2S04 anhidrat. Setelah
aulfat anhidrous, natrium asetat trihidrat. pelarut diklorometana diuapkan dengan
Diklorometana, akuades, natrium hidroksida, evaporator buchi, residu didinginkan di dalam
asetofenon dan orto-hidroksiasetofenon. kulkas selama 12 jam, selanjutnya didiamkan
Alat-alat yang digunakan meliputi selama 1 jam pada suhu kamar. Padatan
spektrometer infra merah (IR. Shimadzu yang terjadi disaring dengan penyaring
FTIR-8201 PC), spektrometer 1H-resonansi Buchner dan ditentukan sifat fisiknya.
magnetik inti (1H NMR, Jeol JNM-MY 60), Selanjutnya dianalisis dengan menggunakan
spektrometer UV-Vis (UV, Milton Roy- spektrometer IR, UV-Vis (pelarut metanol)
Spectronic 3000). dan 1H NMR (pelarut CCI4).
Ismiyarto, Sabirin Matsjeh, Chairil Anwar
{Indonesian Journal of Chemistry 84
Sintesis 3’,4’-dimetoksiflavanon
Dituangkan 1,272 gram (0,0045 mol) Reaksi tahap kedua adalah dehidrasi
senyawa 2’-hidroksi-3,4-dimetoksikalkon ke senyawa p-hidroksiketon menghasilkan
dalam labu leher tiga yang berisi larutan 2 kalkon. Senyawa p-hidroksiketon mempunyai
gram (0,0150 mol) natrium asetat dalam 10 ml Ha terhadap gugus karbonil, sehingga dalama
etanol dan 3 ml air, selanjutnya campuran suasana basa atom Ha mudah lepas. Hal ini
tersebut direfluks selama 12 jam. Kemudian mempercepat dehidrasi senyawa p-
campuran reaksi yang terjadi diencerkan hidroksiketon menghasilkan produk yang
dengan air dingin sebanyak 20 ml dan stabil karena mempunyai ikatan rangkap
didiamkan pada suhu kamar selama 1 jam. yang terkonjugasi dengan cincin aromatis.
Padatan yang terjadi disaring dengan Reaksi dehidrasi tersebut sebagai berikut:
penyaring Buchner dan ditentukan sifat
fisiknya. Selanjutnya dianaiisls dengan
menggunakan spektrometer IR, UV-Vis
(pelarut metanol) dan 1H NMR (pelarut CCI4).
HASIL DAN PEMBAHASAN
Sintesis kalkon digunakan yaitu benzaldehida yang tidak
Dalam sintesis senyawa kelompok mempunyai atom Ha, maka pada kondisi basa
kalkon ini bahan dasar yang digunakan dimungkinkan terjadi reaksi Cannizzaro.
adalah benzaldehida dan asetofenon. Reaksi ini dapat mengurangi kalkon yang
Asetofenon mempunyai atom Ha terhadap dihasilkan. Reaksi Cannizzaro melibatkan
gugus karbonilnya, sehingga dalam kondisi perpindahan hidrida dari molekul
basa mampu membentuk karbanion dengan benzaldehida yang satu ke molekul
reaksi sebagai berikut: benzaldehida yang lain. Menurt Sykes (1989)
mekanisme reaksi Cannizzaro adalah sebagai
berikut:
Karbanion tersebut relatif stabil karena dapat
berkonjugasi menghasilkan ion enolat.
Sintesis senyawa kelompok kalkon ini
berdasarkan reaksi Claisen-Schmidt yang
melibatkan dua tahap reaksi. Tahap pertama Reaksi Cannizzaro tersebut menghasilkan
adalah tahap reaksi adisi nukleofilik. Pada garam benzoat dan benzil alkohol.
tahap ini karbanion dari asetofenon Menurut Sykes (1989) aldehida yang
menyerang karbon dari gugus karbonil mempunyai Ha dari gugus karbonil akan
benzaldehida dengan reaksi sebagai berikut: mengalami reaksi aldol relatif cepat
dibandingkan dengan reaksi Cannizzaro.
Berdasarkan pendapat Sykes tersebut, maka
untuk mencegah adanya reaksi Cannizzaro,
karbanion terlebih dahulu dibuat dengan
mereaksikan asetofenon dengan larutan
basa. Karbanion yang terbentuk dengan cepat
Hasil reaksi adisi nukleofilik di atas menyerang karbon gugus karbonil
mengalami transfer proton dari molekul air benzaldehida menghasilkan p-hidroksiketon.
Selama percobaan tidak terbentuk endapan
putih dari garam benzoat, sehingga dapat
disimpulkan bahwa dalam reaksi sintesis
kalkon ini reaksi Claisen-Schmidt relatif
Ismiyarto, Sabirin Matsjeh, Chairil Anwar
Indonesian Journal of Chemistn 85
dominan dibandingkan dengan reaksi Sintesis 3,4-dimetoksikalkon
Cannizzaro. Dalam sintesis kalkon ini Dalam sintesis 3,4-dimetoksikalkon,
dihasilkan padatan berwama kuning muda bahan dasar yang digunakan adalah
dengan titik lebur 52 °C, berat 3,47 gram veratraldehida dan asetofenon. Asetofenon
(rendemen 83,39%). Untuk mengetahui dalam kondisi basa dapat menghasilkan
struktur senyawa yang dihasilkan, maka karbanion yang mampu bertindak sebagai
dilakukan analisis padatan tersebut dengan nukleofil dalam reaksi Claisen-Schmidt.
menggunakan spektrometer IR, UV-Vis dan Veratraldehida mempunyai gugus metoksi
1H NMR. pada posisi meta dan para dari gugus
Dari spektrum IR terlihat pita tajam dekat aldehidanya. Harga tetapan substituen gugus
1664 cm*1 yang menunjukkan adanya serapan metoksi pada posisi meta adalah o°=0,1
gugus karbonil (-C=0). Menurunnya harga (gugus penarik elektron), sedangkan untuk
frekuensi vibrasi rentangan gugus karbonil posisi orto adalah o°=-0,12 (gugus pemberi
normal (frekuensi vibrasi rentangan C=0 pada elektron). Gugus metoksi pada posisi orto
2-pentanon 1717 cm*1) tersebut diduga tersebut dapat menambah kerapatan elektron
karena gugus karbonil dari senyawa yang atau karbon gugus karbonil pada
dianalisis terkonjugasi dengan cincin aromatis veratraldehida, sehingga reaksi antara
dan atau ikatan rangkap -C=C-. Adanya cincin asetofenon dan veratraldehida dilakukan
aromatis dapat dilihat pada pita dekat 1557 dalam waktu yang lebih lama (24 jam)
cm'1 dan 1450 cm*1 hasil serapan gugus - dibandingkan reaksi antara asetofenon dan
C=C- aromatis, sedangkan serapan guaus - benzaldehida (3 jam). Pengaruh gugus
C=C- terdapat pada pita dekat 1608 cm'1. Hal metoksi pada posisi para tersebut juga
ini diperkuat adanya pita dekat 3028 cm*1 mempengaruhi hasil yang diperoleh.
hasil serapan gugus =C-H. Rendemen sintesis 3,4-dimetoksikalkon
Hasil analisis menggunakan 76,00%, sedangkan untuk sintesis kalkon
spektrometer UV-Vis menghasilkan spektrum dihasilkan rendemen 83,39%.
dengan dua buah puncak, masing-masing Reaksi sintesis 3,4-dimetoksikalkon
dengan panjang gelombang maksimum 312 adalah sebagai berikut:
dan 224 nm. Puncak dengan panjang
gelombang maksimum 312 nm (puncak I)
menunjukkan adanya serapan sistem sinamoil
kerangka kalkon. Puncak dengan panjang
gelombang maksimum 224 nm (puncak II)
menunjukkan adanya sistem benzoil kerangka
kalkon.
e3
Dari spektrum 1H NMR terlihat adanya
puncak multiplet pada 5= 7,8-8,2 ppm yang
menunjukkan resonansi proton Ha. untuk Sintesis 3,4-dimetoksikalkon ini
puncak multiplet pada 5=7,3-7,8 ppm menghasilkan padatan berwama kuning, titik
menunjukkan adanya resonansi proton selain lebur 57 °C, berat 5,36 gram (rendemen
H, dalam kalkon. 76%). Analisis terhadap padatan tersebut
Berdasarkan spektrum IR dapat dilihat menggunakan spektrometri IR, UV-Vis dan 1H
bahwa padatan yang dianalisis mengandung NMR.
gugus karbonil yang terkonjugasi dengan Hasil analisis padatan menggunakan
cincin aromatis dan atau ikatan rangkap spektrometri IR menghasilkan pita tajam
-C=C-, sedangkan dari spektrum UV-Vis dekat 1662 cm*1 yang menunjukkan serapan
didapatkan informasi bahwa padatan yang gugus karbonil yang terkonjugasi dengan
dianalisis mengandung sistem sinamoil dan cincin aromatis. Adanya cincin aromatis
benzoil kerangka kalkon dan didukung oleh ditunjukkan oleh pita dekat 1577 dan 1512
spektrum 1H NMR, maka dapat disimpulkan cm'1 hasil serapan gugus -C=C- cincin
bahwa padatan yang dianalisis adalah kalkon.
Ismiyarto, Sabirin Matsjeh, Chairil Anwar
Indonesian Journal of Chemistry 86
aromatis. Pita dekat 2837 cm'1 menunjukkan Adanya Ha pada ion fenoksida tersebut
serapan gugus -C-H. mengakibatkan terjadinya pertukaran proton
Analisis padatan menggunakan menghasilkan karbanion yang relatif stabil.
spektrometer UV-Vis menghasilkan spektrum
dengan dua buah puncak , masing-masing
dengan panjang gelombang maksimum 356
dan 260 nm. Puncak I dengan panjang
gelombang maksimum 356 nm menunjukkan
adanya serapan sinamoil kerangka kalkon,
sedangkan puncak II dengan panjang Selanjutnya karbanion dari ion fenoksida
gelombang 260 nm menunjukkan adanya tersebut menyerang karbon karbonil
serapan sistem benzoil kerangka kalkon. veratraldehida dengan reaksi sebagai berikut:
J
Dari spektrum 1H NMR terlihat adanya
puncak singlet pada 5= 7,9-8,1 ppm yang
menunjukkan adanya resonansi proton Ha.
Resonansi proton Hb, Hc, Hd, H„, H, dan He
ditunjukkan adanya puncak multiplet pada 5=
6,6-7,9 ppm. Adanya gugus metil ditunjukkan
oleh adanya puncak singlet pada 5= 3,8-3,9
ppm yang merupakan basil resonansi proton
pada C-H. Dari perbesaran spektrum pada 5= Pengaruh gugus hidroksi pada posisi orto
6,6-7,9 ppm didapatkan bahwa Jte adalah 18 tersebut mempengaruhi jumlah hasil sintesis
Hz, sehingga dapat disimpulkan bahwa 2'-hidroksi-3,4-dimetoksikalkon (rendemen
struktur dan 3,4-dimetoksikalkon adalah Z. 74,29%), sedangkan untuk sintesis 3,4-
Berdasarkan spektrum IR dapat dilihat dimetoksikalkon mempunyai rendemen
bahwa padatan yang dianalisis mengandung 76,00%. Hal ini disebabkan karena karbanion
gugus karbonil yang terkonjugasi dengan tidak langsung terbentuk, tetapi melalui
cincin aromatis dan mempunyai ikatan -C-H, pembentukan ion fenoksida terlebih dahulu.
sedangkan dari spektrum UV-Vis diperoleh Pengasaman terhadap campuran reaksi
informasi bahwa padatan tersebut hasil sintesis 2'-hidroksi-3,4-dimetoksikalkon
mengandung sistem sinamoil dan benzoil dengan HCI 5% bertujuan untuk menetralkan
kerangka kalkon. Spektrum 1H NMR fenoksida yang terbentuk menghasilkan 2'-
memperkuat kesimpulan bahwa padatan yang hidroksi-3,4-dimetoksikalkon.
dianalisis adalah 3,4-dimetoksikalkon.
Sintesis 2’-hidroksi-3,4-dimetokslkalkon
Sintesis 2’-hidroksi-3,4-dimetoksikalkon
ini menggunakan bahan dasar veratraldehida
dan o/to-hidroksiasetofenon. orto-
Hidroksiasetofenon dalam kondisi basa dapat
menghasilkan karbanion yang mampu
bertindak sebagai nukleofil untuk menyerang
karbon gugus karbonil veratraldehida dalam
reaksi Claisen-Schmidt. orto-Hidroksiaseto
fenon dalam suasana basa akan membentuk Ion fenoksida 2'-hidroksi-3,4-
ion fenoksida dengan reaksi sebagai berikut: dimetoksikalkon
Untuk memisahkan hasil reaksi
pengasaman dilakukan dengan ekstraksi
menggunakan diklorometana, 2'-hidroksi-3,4-
dimetoksikalkon larut dalam diklorometana.
Ismiyarto, Sabirin Matsjeh, Chairil Anwar
Indonesian Journal of Chemistry 87
Sintesis 2'-hidroksi-3,4-dimetoksikalkon mengandung sistem sinamoil dan benzoil
ini menghasilkan padatan berwarna oranye, kerangka kalkon. Pada spektrum 1H NMR
titik lebur 95°C, berat 5,68 gram (rendemen teriihat bahwa padatan yang dianalisis
74,29%). Analisis terhadap padatan tersebut mepunyai proton metoksi dan proton OH yang
menggunakan spektrometri IR, UV-Vis dan 1H mengalami ikatan hidrogen intramolekuler, ini
NMR. ditunjukkan puncak pada 5= 13 ppm hasil
Analisis hasil sintesis 2’-hidroksi-3,4- resonansi proton OH. Dari ketiga spektrum
dimetoksikalkon menggunakan spektrometer tersebut dapat disimpulkan bahwa padatan
IR menghasilkan spektrum yang mempunyai tersebut adalah 2'-hidroksi-3,4-
pita dekat 1683 cm’1 yang merupakan hasil dimetoksikalkon
serapan gugus karbonil yang mengalami Sintesis senyawa ksiompok flavanon
konjugasi dengan cincin aromatis dan atau Dalam sintesis senyawa kelompok
ikatan rangkap -C=C-. Adanya cincin aromatis flavanon ini bahan awal yang digunakan
ditunjukkan pada pita dekat 1512 dan 1488 adalah 2’-hidroksi-3,4-dimetoksikalkon, yang
cm*1 hasil serapan gugus C=C cincin mempunyai gugus karbonil yang terkonjugasi
aromatis. Pita dekat 1635 cm*1 adalah hasil dengan ikatan rangkap dua, sehingga Cb
serapan gugus -C=C-., dapat mengemban muatan positif parsial dan
Analisis hasil sintesis 2’-hidroksi-3,4- atom 0 mengemban muatan negatif parsial.
dimetoksikalkon menggunakan spektrometri
UV-Vis menghasilkan spektrum yang
mempunyai dua puncak, masing-masing
dengan panjang gelombang maksimum 372
dan 263 nm. Puncak (I) dengan panjang
gelombang maksimum 372 nm menunjukkan
adanya serapan sistem sinamoil kerangka
kalkon, sedangkan puncak (II) dengan
panjang gelombang maksimum 263 nm Sintesis senyawa kelompok flavanon ini
menunjukkan adanya serapan sistem benzoil dilakukan dengan merefluk campuran pada
kerangka kalkon. suhu 80 °C. Pada suhu ini ikatan hidrogen
intramolekuler 2’-hidroksi-3,4-dimetoksikalkon
dilemahkan sehingga dapat mempunyai
struktur sebagai berikut:
Analisis hasil sintesis 2’-hidroksi-3,4-
dimetoksikalkon menggunakan spektrometri
1H NMR menghasilkan spektrum dengan Senyawa 2’-hidroksi-3,4-dimetoksikalkon
puncak singlet pada 5= 3,8=4,1 ppm yang mempunyai karakter asam, sehingga dalam
menunjukkan resonansi proton Hj (metoksi). suasana basa akan terjadi reaksi asam basa
Resonansi proton Ha1, Htf, H*. H*. Hb, HCH, sebagai berikut:
Hd, Hr, dan Hg ditunjukkan oleh adanya ft
puncak multiplet pada 5=6,5-8,2 ppm .
Adanya puncak singlet pada 5= 13 ppm
menunjukkan adanya resonansi proton pada
Hk (OH). Resonansi proton pada 5= 13 ppm
ini disebabkan karena proton tersebut terlibat
dalam pembentukan ikatan hidrogen
intramolekuler, sehingga protonnya relatif Hasil reaksi asam basa di atas adalah ion
tidak terlindungi. fenoksida. Ion fenoksida tersebut dapat
Berdasarkan spektrum IR dapat dilihat bertindak sebagai nukleofil untuk menyerang
bahwa padatan yang dianalisis mengandung Cp yang parsial positif. Reaksi sintesis 3’,4’-
gugus karbonil yang terkonjugasi dengan dimetoksiflavanon adalah sebagai berikut:
cincin aromatis dan atau ikatan rangkap dua,
sedangkan dari spektrum UV-Vis didapatkan
infbrmasi bahwa padatan yang dianalisis
Ismiyarto, Sabirin Matsjeh, Chairil Anwar
{Indonesian Journal of Chemistry 88
Dari spektrum 1H NMR hasil sintesis
3’,4'-dimetoksifiavanon teriihat adanya puncak
multiplet dengan pada 5= 6,5-8,2 ppm yang
Bentuk enol dapat mengalami kesetimbangan menunjukkan resonansi proton pada cincin
menjadi bentuk keto seperti pada gambar aromatis. Puncak kuartet dengan 5=5,2-5,8
berikut: ppm menunjukkan adanya resonansi dari
OCH, proton Hf dari struktur senyawa 3',4'-
>VÿOCH, dimetoksiflavanon teriihat bahwa H,
OCH, mempunyai sebuah proton tetangga yang
berposisi cis dengannya (Hg1) dan sebuah
proton tetangga yang berposisi trans
•nol ktto
dengannya (Hg2), sehingga puncak hasil
Kedua bentuk ini mempunyai ikatan yang resonansi protonnya adatah kuartet. Puncak
berbeda. Senyawa keto mempunyai ikatan C- doublet pada 5=3,2-3,6 ppm menunjukkan
H, C-C dan C=0, sedangkan senyawa enol adanya resonansi proton Hg resonansi proton
mempunyai ikatan C=C, C-0 dan O-H. Dari gugus metoksi teriihat dengan adanya puncak
jenis ikatan pada masing-masing senyawa singlet pada 6= 3,8-4,2 ppm.
tersebut, senyawa keto mempunyai energi Berdasarkan spektrum IR padatan yang
ikatan yang lebih besar dibandingkan dengan dianalisis mengandung gugus karbonil yang
senyawa enol sebesar 12 kkal/mol, sehingga terkonjugasi dengan cincin aromatis,
senyawa keto reiatif stabil dibandingkan sedangkan dari spektrum UV-Vis didapatkan
dengan senyawa enol. informasi bahwa padatan yang dianalisis
Hasil sintesis 3’,4'-dimetoksiflavanon mempunyai kerangka flavanon. Spektrum 1H
berupa padatan berwama kuning tua dengan NMR memperkuat kesimpulan bahwa
titik lebur 80 °C, berat 0,92 g (rendemen padatan yang dianalisis adalah 3',4’-
72,00%). Analisis padatan dilakukan dengan dimetoksiflavanon.
menggunakan spektrometri IR, UV*Vis dan 1H
NMR. KESIMPULAN
Analisis hasil sintesis 3',4’-
dimetoksifiavanon menggunakan Dari hasil penelitian dan pembahasan
spektrometer IR menghasilkan spektrum yang telah diuraikan, maka kesimpulan dalam
dengan pita dekat 1652 cm'1 yang penelitian ini adalah:
menunjukkan adanya serapan gugus karbonil 1. Kelompok senyawa kalkon dapat disintesis
yang terkonjugasi dengan cincin aromatis. berdasarkan reaksi Claisen-Schmidt
Adanya cincin aromatis dapat teriihat pada dengan menggunakan bahan dasar
pita dekat 1558 dan 1463 cm'1 hasil serapan senyawa turunan asetofenon dan senyawa
gugus -C=C- cincin aromatis. turunan benzaldehida. Senyawa kelompok
Analisis sintesis 3’,4’-dimetoksiflavanon kalkon tersebut adalah:
menggunakan spektrometri UV-Vis a. Benzilidenasetofenon (kalkon) meng¬
menghasilkan spektrum dengan dua puncak, gunakan bahan dasar benzaldehida
masing-masing dengan panjang gelombang dan asetofenon dengan rendemen
maksimum 326 dan 252 nm. Puncak yang 83,39%.
reiatif rendah (I) dengan panjang gelombang b. 3,4-dimetoksikalkon menggunakan
maksimum 326 nm menunjukkan adanya bahan dasar veratraldehida dan
serapan yang melibatkan cincin B pada asetofenon dengan rendemen 76,00%.
kerangka flavanon, sedangkan puncak yang c. 2’-hidroksi-3,4-dimetoksikalkon
reiatif tinggi (II) dengan panjang gelombang menggunakan bahan dasar veratral¬
maksimum 252 nm menunjukkan adanya dehida dan o/fo-hidroksiasetofenon
serapan sistem benzoil kerangka flavanon. dengan rendemen 74,29%.
Ismiyarto, Sabirin Matsjeh, Chairil Anwar
{Indonesian Journal of Chemistr j 89
2. Vanilin tidak dapat bereaksi Claisen Organik, Jilid I, Edisi 4, Penerbit
Schimdt dengan asetofenon menghasilkan Erlangga, Jakarta.
4-hidroksi-5-metoksikalkon, karena 6. Geissman, T.A., dan D.H.G. Crout., 1969,
pengaruh adanya gugus OH pada vanilin. Organic Chemistry of Secondary Plant
3. 3’,4’-dimetoksiflavanon dapat disintesis Metabolism, Freeman, Cooper &
melalui siklisasi 2’-hidroksi-3,4- Company, California.
dimetoksikalkon berdasarkan reaksi adisi 7. Ikan, R., 1991, Natural Product: A
1,4-nukleofilik pada senyawa keton tak Labotarory Guide, edisi 2, Academic
jenuh a,p menggunakan katalis basa Press, Inc., New York.
dengan rendemen 72,00%. 8. linuma, M., M. Ohyama dan T. Tanaka.,
1993, Three New Phenolic Compounds
DAFTAR PUSTAKA From The Roots of Sophora Leachiana,
J. Nat. Prod.. 5§, (12), 2212-2215.
1. Aress, J.J., P.E. Outt., S.V. Kakodkar., 9. Kohler, E.P., dan H.M. Cadwell, 1948,
R.C. Buss dan J.C. Geiger., 1993, A Organic Synthesis Coll, Vol. 1.
Convenient Large Scale Synthetic of 5- 10. Markham, K.R., Techniques of Flavanoid
methoxyflavone and It’s Application to Indentifocation, Diterjemahkan oleh
Analog Preparation, J. Pro. Chem.. 55, Kosasih Padmawinata, 1988, Cara
7903-7905. Mengidentifikasi Flavanoid, Penerbit ITB,
2. Bu, X., dan Y. Li., 1996, Synthesis of Bandung.
Exyguaflavanone K and (±)-Leachianone 11. Puyvelde, I.V., N.D. Kimpe., S. Costa., V.
G, J. Nat. Prod.. 52, 968-969. Munyjabo., S. Nyirankuliza., E.
3. Carrey, F.A., dan R.l. Sundberg., 1990, Hakizamungu., dan N. Schamp., 1989,
Advanced Organic Chemistry Part B: Isolation of Flavanoids and A Chalcone
Reactions and Synthesis, edisi 3, Plenum from Helichrysum Odoratissimum and
Press, New York dan London. Synthesis of Helichrysetin, J. Nat. Prod..
4. Dominguez, X.A., dan S.G. Garcia., 1989, 52, (3), 629-633.
Kukulkanins A and B, New Chalcones 12. Sykes, P., A Guidebook to Mechanism in
from Mimosa Tenuefolia, J. Nat. Prod.. Organic Chemistry, diterjemahkan oleh
52. (4), 864-867. A.J. Hartono, dkk., 1989, Penuntun
5. Fessenden, R.J., dan J.S. Fessenden, Mekanisme Reaksi Kimia Organik, PT.
Organic Chemistry, Diterjemahkan oleh Gramedia, Jakarta.
A. Hadyana Pudjaatmaka, 1995, Kimia
Ismiyarto, Sabirin Matsjeh, Chairll Anwar
You might also like
- UConn Athletics Financial StatementDocument83 pagesUConn Athletics Financial StatementHartford CourantNo ratings yet
- Hagerman, 2002Document116 pagesHagerman, 2002Dini Iga PutriNo ratings yet
- Activity 2 Investments in Equity SecuritiesDocument4 pagesActivity 2 Investments in Equity SecuritiesVi Vid100% (5)
- Privatization and Management Office v. Strategic Alliance Development CorporationDocument2 pagesPrivatization and Management Office v. Strategic Alliance Development CorporationJaypee Ortiz67% (3)
- Venus in Fur - Presskit & Interwiew With Roman PolanskiDocument21 pagesVenus in Fur - Presskit & Interwiew With Roman PolanskiКонстантин НовосадовNo ratings yet
- Stress-Lnduced Phenylpropanoid Metabolism: Richard A. Dixon' and Nancy L. PaivaDocument14 pagesStress-Lnduced Phenylpropanoid Metabolism: Richard A. Dixon' and Nancy L. PaivaSergio mauricio sergioNo ratings yet
- Optimization of Time Reaction and Hydroxide Ion Concentration On Flavonoid Synthesis From Benzaldehyde and Its DerivativesDocument6 pagesOptimization of Time Reaction and Hydroxide Ion Concentration On Flavonoid Synthesis From Benzaldehyde and Its DerivativesAnonymous 3hPHKsFUYNo ratings yet
- TH 14 70 8480Document8 pagesTH 14 70 8480JuanManuelAmaroLuisNo ratings yet
- A Convrnirnt Approach To The Synthesis of Prrny L-, Furo - and Pyrano-Quinolinb Alkaloids of The RutacrarDocument6 pagesA Convrnirnt Approach To The Synthesis of Prrny L-, Furo - and Pyrano-Quinolinb Alkaloids of The RutacrarDavid DelgadoNo ratings yet
- Tannin ChemistryDocument116 pagesTannin ChemistryExaudi EbennezerNo ratings yet
- Synthesis of FlavanoneDocument5 pagesSynthesis of FlavanonefikarisvitaNo ratings yet
- Carr 1969Document6 pagesCarr 1969Liudas SlepikasNo ratings yet
- Mps 02 00070Document8 pagesMps 02 00070mxtyowoNo ratings yet
- (Hevea Brasiliensis) : Processed Products of The Hevein Precursor in The Latex of The Rubber TreeDocument3 pages(Hevea Brasiliensis) : Processed Products of The Hevein Precursor in The Latex of The Rubber TreeGrace ApriliaNo ratings yet
- Methoxy and Hydroxy Derivatives of 3,4-Dihydro-3 - (Di-N-Propylamino) - 2h-1-Benzopyrans - New Synthesis and Dopaminergic ActivityDocument8 pagesMethoxy and Hydroxy Derivatives of 3,4-Dihydro-3 - (Di-N-Propylamino) - 2h-1-Benzopyrans - New Synthesis and Dopaminergic ActivityHamilton MorrisNo ratings yet
- Chalcone Synthesis, Structure DiversityDocument13 pagesChalcone Synthesis, Structure DiversityDini Elsi ANo ratings yet
- The Tannin Handbook HagermanDocument121 pagesThe Tannin Handbook Hagermanqotrin nidaNo ratings yet
- Colorants With Mixt Naphthoquinone-Azomethine Cromophore-Synthesis, Characterization and in Vitro Toxicity AnalysisDocument14 pagesColorants With Mixt Naphthoquinone-Azomethine Cromophore-Synthesis, Characterization and in Vitro Toxicity AnalysisRoxana IonescuNo ratings yet
- Phenolic Compound IIDocument24 pagesPhenolic Compound IIMuhammad Irfan AmiruddinNo ratings yet
- Liu IIIDocument8 pagesLiu IIIaji subaktiNo ratings yet
- Sintesis 2Document9 pagesSintesis 2monicaNo ratings yet
- 223 242 PDFDocument20 pages223 242 PDFRaoul WembeNo ratings yet
- I3Xif: Isolation of Alkaloids From Structure of Balf OurodineDocument6 pagesI3Xif: Isolation of Alkaloids From Structure of Balf OurodinekanensuNo ratings yet
- Full Paper: Anna Rosiak, Wolfgang Frey, and Jens ChristoffersDocument11 pagesFull Paper: Anna Rosiak, Wolfgang Frey, and Jens Christofferstakiq laseNo ratings yet
- Chalcone To Pyrimidine by Urea Indian PaperDocument7 pagesChalcone To Pyrimidine by Urea Indian PaperAnkit Kumar Singh100% (1)
- Naphthoquinone Epoxide Ring OpeningDocument4 pagesNaphthoquinone Epoxide Ring Openingjinzo88No ratings yet
- 3shikimic Sintesis IsotopicDocument4 pages3shikimic Sintesis IsotopicIsmael GuardiaNo ratings yet
- Tetrahedron: Chamseddine Derabli, Raouf Boulcina, Gilbert Kirsch, Abdelmadjid DebacheDocument8 pagesTetrahedron: Chamseddine Derabli, Raouf Boulcina, Gilbert Kirsch, Abdelmadjid DebacheBi LouNo ratings yet
- CCA 77 2004 361 366 Medic Saric2 PDFDocument6 pagesCCA 77 2004 361 366 Medic Saric2 PDFAndra Ch123No ratings yet
- Isolation and Spectrophotometric Characterization o F Photosynthetic Pigments Rodney F BoyerDocument4 pagesIsolation and Spectrophotometric Characterization o F Photosynthetic Pigments Rodney F BoyerLucy ZuluNo ratings yet
- Enzymology: The Reported Presence of A Coenzyme BDocument6 pagesEnzymology: The Reported Presence of A Coenzyme BAndreiNo ratings yet
- Bioorganic & Medicinal ChemistryDocument10 pagesBioorganic & Medicinal ChemistryPaxton FettelNo ratings yet
- Current+Organic+Chemistry +2008, 12,+1116-1183Document96 pagesCurrent+Organic+Chemistry +2008, 12,+1116-1183Murali Venkat NagNo ratings yet
- A Simple and Practical Approach To The Dibenzo (C, F) Thiazolo (3,2-A) Azepines: A Novel Fused Tetracyclic Azepine SystemDocument12 pagesA Simple and Practical Approach To The Dibenzo (C, F) Thiazolo (3,2-A) Azepines: A Novel Fused Tetracyclic Azepine SystemJuanManuelAmaroLuisNo ratings yet
- KC27 1 0214 PDFDocument4 pagesKC27 1 0214 PDFArash AbbasiNo ratings yet
- Importante-Anhidrido CHO Generan Multiheterociclo en CascadaDocument8 pagesImportante-Anhidrido CHO Generan Multiheterociclo en CascadaFernando RSNo ratings yet
- Bioorganic & Medicinal Chemistry Letters: Hanumantharao Paritala, Steven M. FirestineDocument4 pagesBioorganic & Medicinal Chemistry Letters: Hanumantharao Paritala, Steven M. FirestineHadeel Al-SinjilawiNo ratings yet
- Isolation, Biological Activities and Synthesis of Indoloquinoline Alkaloids: Cryptole-Pine, Isocryptolepine and NeocryptolepineDocument22 pagesIsolation, Biological Activities and Synthesis of Indoloquinoline Alkaloids: Cryptole-Pine, Isocryptolepine and NeocryptolepineDayse_sbNo ratings yet
- Gaonkar-Vignesh2017 Article SynthesisAndPharmacologicalProDocument35 pagesGaonkar-Vignesh2017 Article SynthesisAndPharmacologicalProEduardo SilvaNo ratings yet
- Silva Et Al 2011 Diterpene Lactones With Labdane Halimane and Clerodane FrameworksDocument8 pagesSilva Et Al 2011 Diterpene Lactones With Labdane Halimane and Clerodane Frameworkskontiki500No ratings yet
- Methods For The Synthesis of CinnolinesDocument22 pagesMethods For The Synthesis of CinnolinesMohsen Gomaa0% (1)
- Recent Advances in The Chemistry of Oripavine & DerivativesABB - 2014072111275178Document15 pagesRecent Advances in The Chemistry of Oripavine & DerivativesABB - 2014072111275178Ji ChemNo ratings yet
- Interrupted Carbonyl-Olefin Metathesis Via Oxygen Atom TransferDocument8 pagesInterrupted Carbonyl-Olefin Metathesis Via Oxygen Atom TransferFeniletilaminNo ratings yet
- Isolation of PALDocument9 pagesIsolation of PALdarkangel9000No ratings yet
- CR 100258 KDocument35 pagesCR 100258 KzoyudgNo ratings yet
- SLCT 201801951Document4 pagesSLCT 201801951shruti guptaNo ratings yet
- Production of Resveratrol From Tyrosine in Metabolically Engineered Saccharomyces CerevisiaeDocument6 pagesProduction of Resveratrol From Tyrosine in Metabolically Engineered Saccharomyces CerevisiaeMaría Angélica Otálora MartínezNo ratings yet
- Dihydrocoronatine Promising Candidate For A Chemical Probe To Study Coronatine Jasmonoid and Octadecanoid Binding ProteinDocument5 pagesDihydrocoronatine Promising Candidate For A Chemical Probe To Study Coronatine Jasmonoid and Octadecanoid Binding ProteinQuenguan FranklinNo ratings yet
- Separations 09 00087 1Document12 pagesSeparations 09 00087 1Sana AjmalNo ratings yet
- NIH Public Access: A Convenient Preparation of Xanthene DyesDocument19 pagesNIH Public Access: A Convenient Preparation of Xanthene DyesUmar IjazNo ratings yet
- Communications: Discovery, Structure, and Anticancer Activity of An Iridium Complex of DiselenobenzoquinoneDocument4 pagesCommunications: Discovery, Structure, and Anticancer Activity of An Iridium Complex of DiselenobenzoquinonesherajekiNo ratings yet
- Module 04Document60 pagesModule 04shashi vermaNo ratings yet
- Sintesis de CineolDocument4 pagesSintesis de CineolNatalia RuizNo ratings yet
- Group 03 (2A) 2Document8 pagesGroup 03 (2A) 2-No ratings yet
- 18 Vol. 5 Issue 12 December 2014 IJPSR RA 4227 A Paper 18Document6 pages18 Vol. 5 Issue 12 December 2014 IJPSR RA 4227 A Paper 18Md. BadrulNo ratings yet
- Thiophene 1Document18 pagesThiophene 1AYUSH DUBEYNo ratings yet
- Experiment 4 CHM 624Document11 pagesExperiment 4 CHM 624arefeena100% (2)
- Synthesis of Levulinic Acid-Glycerol Ketal-Ester Oligomers and Structural Characterization Using NMR SpectrosDocument7 pagesSynthesis of Levulinic Acid-Glycerol Ketal-Ester Oligomers and Structural Characterization Using NMR SpectrosLucas de MeloNo ratings yet
- Chapter 1 (Philoid-In)Document34 pagesChapter 1 (Philoid-In)Anonymous c8QLG3No ratings yet
- Synthesis of Flavones From 2-Hydroxy Acetophenone and Aromatic Aldehyde Derivatives by Conventional Methods and Green Chemistry ApproachDocument4 pagesSynthesis of Flavones From 2-Hydroxy Acetophenone and Aromatic Aldehyde Derivatives by Conventional Methods and Green Chemistry ApproachQuang Bách HồNo ratings yet
- Synthesis of Regioselectively Functionalized Benzo (B) Thiophenes by Combined ortho-Lithiation-Halocyclization StrategiesDocument4 pagesSynthesis of Regioselectively Functionalized Benzo (B) Thiophenes by Combined ortho-Lithiation-Halocyclization StrategiesDiogomussumNo ratings yet
- Transition Metal Catalyzed Furans Synthesis: Transition Metal Catalyzed Heterocycle Synthesis SeriesFrom EverandTransition Metal Catalyzed Furans Synthesis: Transition Metal Catalyzed Heterocycle Synthesis SeriesNo ratings yet
- Studies in Natural Products Chemistry: Stereoselective SynthesisFrom EverandStudies in Natural Products Chemistry: Stereoselective SynthesisNo ratings yet
- Alkanolamines - Method For The Determination of 11Document26 pagesAlkanolamines - Method For The Determination of 11Dewi WulandhariNo ratings yet
- A Sensitive Method For Determination Glycolic Acid, Mono - and Di-Chloroacetic Acid in Betaine Media Using Amino-Functionalized SBA-15 As A Sorbent and HPLC AssayDocument8 pagesA Sensitive Method For Determination Glycolic Acid, Mono - and Di-Chloroacetic Acid in Betaine Media Using Amino-Functionalized SBA-15 As A Sorbent and HPLC AssayDewi WulandhariNo ratings yet
- AN 259 IC N Methylpyrrolidine Cefepime LPN2586 ENDocument6 pagesAN 259 IC N Methylpyrrolidine Cefepime LPN2586 ENDewi WulandhariNo ratings yet
- Zhou 2019Document8 pagesZhou 2019Dewi WulandhariNo ratings yet
- HyperrezDocument5 pagesHyperrezDewi WulandhariNo ratings yet
- Dionex Easion Ion Chromatography System Operator's Manual: Document No. 155028 Revision 01 August 2020Document126 pagesDionex Easion Ion Chromatography System Operator's Manual: Document No. 155028 Revision 01 August 2020Dewi WulandhariNo ratings yet
- Lactulose-USP MonographDocument2 pagesLactulose-USP MonographDewi WulandhariNo ratings yet
- Natural Gas Analyser: Calorifi C Value / Wobbe Index (ISO 6976) Robust and FL Exible DesignDocument4 pagesNatural Gas Analyser: Calorifi C Value / Wobbe Index (ISO 6976) Robust and FL Exible DesignDewi WulandhariNo ratings yet
- Azithromycin at Low Nanogram LevelsDocument2 pagesAzithromycin at Low Nanogram LevelsDewi WulandhariNo ratings yet
- Determining Inorganic Anions in Drinking WaterDocument4 pagesDetermining Inorganic Anions in Drinking WaterDewi WulandhariNo ratings yet
- Review of Spectrophotometric Methods For Determination of FormaldehydeDocument16 pagesReview of Spectrophotometric Methods For Determination of FormaldehydeDewi WulandhariNo ratings yet
- Pad IcDocument8 pagesPad IcDewi WulandhariNo ratings yet
- Oligo 2Document1 pageOligo 2Dewi WulandhariNo ratings yet
- Principles of Flow Injection Analysis: January 2020Document30 pagesPrinciples of Flow Injection Analysis: January 2020Dewi WulandhariNo ratings yet
- Stability Indicating HPLC-ECD Method For The Analysis of Clarithromycin in Pharmaceutical Dosage Forms: Method Scaling Versus Re-ValidationDocument20 pagesStability Indicating HPLC-ECD Method For The Analysis of Clarithromycin in Pharmaceutical Dosage Forms: Method Scaling Versus Re-ValidationDewi WulandhariNo ratings yet
- Validasi Metode Analisis Kadar Ambroksol Hidroklorida Dalam Sediaan Tablet Cystelis Secara Kromatografi Cair Kinerja TinggiDocument10 pagesValidasi Metode Analisis Kadar Ambroksol Hidroklorida Dalam Sediaan Tablet Cystelis Secara Kromatografi Cair Kinerja TinggiDewi WulandhariNo ratings yet
- 36 1 93 96 Jakovac enDocument4 pages36 1 93 96 Jakovac enDewi WulandhariNo ratings yet
- Designation D2163 - 07 Standard Test Method ForDocument11 pagesDesignation D2163 - 07 Standard Test Method ForDewi WulandhariNo ratings yet
- 2644921LR AssignmentDocument24 pages2644921LR AssignmentPARAKRAM ROY100% (1)
- America & WW - IIDocument5 pagesAmerica & WW - IIalikhanNo ratings yet
- Assigment (1&2) Statistical Methods (1551) PDF - Docx (21-06-2018) PDFDocument6 pagesAssigment (1&2) Statistical Methods (1551) PDF - Docx (21-06-2018) PDFMaria AsgharNo ratings yet
- Nimzo-Indian Defence - WikipediaDocument9 pagesNimzo-Indian Defence - WikipediaMadhu KaushikaNo ratings yet
- Chemicals Brochure (Global)Document2 pagesChemicals Brochure (Global)soumitrabanNo ratings yet
- Using Social Media For CSR Communication and Engaging StakeholdersDocument24 pagesUsing Social Media For CSR Communication and Engaging StakeholdersMeowKhanNo ratings yet
- 1st Rhyming GameDocument6 pages1st Rhyming GameCikgu Pejo50% (2)
- Family Reunion Visa NewDocument2 pagesFamily Reunion Visa NewAli Hyder ZaidiNo ratings yet
- Civil Original Jurisdiction Writ Petition (Civil) No 924 of 2017 (Under Article 32 of The Constitution of India)Document53 pagesCivil Original Jurisdiction Writ Petition (Civil) No 924 of 2017 (Under Article 32 of The Constitution of India)PGurusNo ratings yet
- Reading and Math Online Resources - 2017-18Document3 pagesReading and Math Online Resources - 2017-18api-32237090No ratings yet
- CRRCPro GF45IDocument8 pagesCRRCPro GF45IJulio CesarNo ratings yet
- Train Ticket TK28767782M68Document3 pagesTrain Ticket TK28767782M68Prdeep KumarNo ratings yet
- By: Tenneco EuropeDocument23 pagesBy: Tenneco EuropecmxxiNo ratings yet
- Yoga For The Modern AgeDocument22 pagesYoga For The Modern AgeSubhag SenNo ratings yet
- Random Questions. ZZZZDocument15 pagesRandom Questions. ZZZZMary Ann SagunNo ratings yet
- UCHEOMA's Project StartDocument105 pagesUCHEOMA's Project StartSudheer Kumar NadukuditiNo ratings yet
- Met304 SchemeDocument30 pagesMet304 SchemenikhilasoknNo ratings yet
- Progressive Interest Calculator: Selling Price Interest Rate (%) Tenure (Years) Deposit (%) Total Deposit Loan AmountDocument1 pageProgressive Interest Calculator: Selling Price Interest Rate (%) Tenure (Years) Deposit (%) Total Deposit Loan AmountNajib MohamedNo ratings yet
- SCRIPT - Advantages For Authentic and Created MaterialsDocument3 pagesSCRIPT - Advantages For Authentic and Created MaterialsChristian Joy Elandag JacobeNo ratings yet
- Vol 1 CLUP (2013-2022)Document188 pagesVol 1 CLUP (2013-2022)Kristine PiaNo ratings yet
- Catamco. A InfographDocument1 pageCatamco. A InfographAvian Henna CatamcoNo ratings yet
- Kazuo Ohno 'S Dance and His Methodology: From Analyzing His Butoh-FuDocument8 pagesKazuo Ohno 'S Dance and His Methodology: From Analyzing His Butoh-FudNo ratings yet
- Criticism For Max WeberDocument18 pagesCriticism For Max WeberAisha KhanNo ratings yet
- Course Outline - MATH 204 (Fall 2023)Document4 pagesCourse Outline - MATH 204 (Fall 2023)Gonzalo AlvarezNo ratings yet
- Pattern of IR in IndiaDocument3 pagesPattern of IR in IndiaMeenakshi ChoudharyNo ratings yet
- 10 Eng ExerDocument17 pages10 Eng ExerGuruNo ratings yet