Professional Documents
Culture Documents
Exercicis Selectivitat Model Actual
Exercicis Selectivitat Model Actual
Uploaded by
Liv Giron0 ratings0% found this document useful (0 votes)
35 views2 pagesOriginal Title
EXERCICIS SELECTIVITAT MODEL ACTUAL
Copyright
© © All Rights Reserved
Available Formats
DOCX, PDF, TXT or read online from Scribd
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
© All Rights Reserved
Available Formats
Download as DOCX, PDF, TXT or read online from Scribd
Download as docx, pdf, or txt
0 ratings0% found this document useful (0 votes)
35 views2 pagesExercicis Selectivitat Model Actual
Exercicis Selectivitat Model Actual
Uploaded by
Liv GironCopyright:
© All Rights Reserved
Available Formats
Download as DOCX, PDF, TXT or read online from Scribd
Download as docx, pdf, or txt
You are on page 1of 2
1.
El bromometà (o bromur de metil) es va utilitzar com a plaguicida fins que es va
començar a prohibir en molts països, a partir de l’any 2000, pel fet que genera radicals
de brom (Br) que participen en el procés de reducció de la capa d’ozó a l’estratosfera.
En aquesta capa de l’atmosfera pot tenir lloc la reacció de fotodissociació següent:
CH 3 Br hν CH 3+ Br
→
a. Calculeu la freqüència i la longitud d’ona de la radiació electromagnètica capaç de
trencar l’enllaç C-Br en una molècula de bromometà.
b. Definiu el terme orbital atòmic segons el model ondulatori de l’àtom. Escriviu la
configuració electrònica de l’àtom de brom i indiqueu els nombres quàntics de
l’electró més extern d’aquest àtom.
DADES: Energia de l’enllaç C-Br: 276 kJ mol -1
Nombre d’Avogadro: NA = 6,02·1023.
Velocitat de la llum en el buit: c=3,00 ·10 8 m s-1.
Constant de Planck: h=6,63·10-34 J s.
Nombre atòmic: Z(Br) = 35.
2. La descomposició de l’ozó a l’estratosfera s’esdevé mitjançant una cadena de
reaccions. La primera consisteix en el trencament d’una molècula d’oxigen en dos
àtoms d’oxigen:
O2 (g) 2 O (g) ∆Ho = 495 kJ mol-1
a. Calculeu l’energia de la radiació electromagnètica capaç de produir aquesta
reacció. Expliqueu raonadament si la radiació infraroja podria provocar el
trencament de la molècula d’oxigen.
b. Definiu el terme orbital atòmica segons el model ondulatori de l’àtom. Escriviu la
configuració electrònica en estat fonamental de l’àtom d’oxigen i indiqueu els
nombres quàntics de l’electró més intern d’aquest àtom.
DADES: Nombre atòmic (Z): Z(O) = 8
Nombre d’Avogadro: NA = 6,02·1023
Constant de Planck: h=6,63·10-34 J s
3. La primera vegada que es va identificar l’heli va ser quan es va poder observar una línia
groga lluent en l’espectre d’emissió d’un eclipsi solar. Posteriorment, es va aïllar l’heli
a la Terra tractant un mineral, la cleveïta, i es va identificar l’emissió d’una línia groga
amb una energia de 3,37 x 10 -19 J, que es corresponia amb la línia observada en
l’espectre solar.
a) Calculeu la freqüència i la longitud d’ona d’un fotó de la línia d’emissió identificada
per a l’heli.
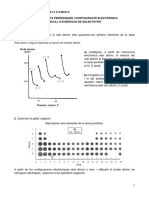
b) La figura següent representa el diagrama d’energies dels orbitals atòmics de l’heli;
les fletxes indiquen unes quantes transicions electròniques d’emissió permeses
segons l’espectroscòpia.
Identifiqueu la transició electrònica corresponent a la línia groga d’emissió de l’heli
i indiqueu a quin salt electrònic correspon. Definiu el terme orbital atòmic segons
el model ondulatori de l’àtom i escriviu la configuració electrònica de l’heli abans i
després del salt electrònic.
DADES: Velocitat de la llum en el buit: c =3,00 ·108 m s-1.
Constant de Planck: h=6,63·10-34 J s.
Nombre atòmic: Z(He) = 2.
You might also like
- Ejercicos Propiedades PeriodicasDocument2 pagesEjercicos Propiedades PeriodicaschematenaNo ratings yet
- Exercicis Química SelectivitatDocument6 pagesExercicis Química SelectivitataalbassNo ratings yet
- Problemes FEiODocument11 pagesProblemes FEiOsthebemitaNo ratings yet
- Sol - 01 - Ud02 - Quim1 - Batxcien - Batx 3Document3 pagesSol - 01 - Ud02 - Quim1 - Batxcien - Batx 3Isabella Castaño GonzálezNo ratings yet
- L'àtomDocument2 pagesL'àtomFaniMilletNo ratings yet
- Exercicis Interacció Radiació-MatèriaDocument6 pagesExercicis Interacció Radiació-MatèriaJaime Carrero FernándezNo ratings yet
- Exercicis de Selectivitat de Propietats PeriòdiquesDocument4 pagesExercicis de Selectivitat de Propietats Periòdiquesbruna dedesNo ratings yet
- 002 Estructuraatomica Parte1 5488Document29 pages002 Estructuraatomica Parte1 5488MarceloSerranoVigoNo ratings yet
- Tema 2. Exercicis I Qüestions Estructura Atòmica I S. Periòdic PDFDocument9 pagesTema 2. Exercicis I Qüestions Estructura Atòmica I S. Periòdic PDFLuisa Rubio VillarrealNo ratings yet
- Tema 1 Exercicis MilloraDocument10 pagesTema 1 Exercicis MilloraClaudia RodríguezNo ratings yet
- Física 2023jDocument32 pagesFísica 2023jMaRTY AlcalàNo ratings yet
- Examen Fisica Selectivitat 2023 070623Document16 pagesExamen Fisica Selectivitat 2023 070623Pere Egolatra AlterNo ratings yet
- Tema 8 - Enllaç Químic Problemes SolucionsDocument10 pagesTema 8 - Enllaç Químic Problemes SolucionsOriol CostaNo ratings yet
- Física ModernaDocument10 pagesFísica ModernaFederico EspindolaNo ratings yet
- FQ Pau QüestionsDocument4 pagesFQ Pau QüestionsWinter MonoNo ratings yet
- Tema 8 - Enllaç Químic ProblemesDocument15 pagesTema 8 - Enllaç Químic ProblemesOriol CostaNo ratings yet
- Problemes de Fisica QuànticaDocument3 pagesProblemes de Fisica QuànticaMònica Cabanillas DiéguezNo ratings yet
- Tema 1 - Àtoms I Molècules. - SolucionsDocument44 pagesTema 1 - Àtoms I Molècules. - SolucionsOriol CostaNo ratings yet
- Exercicis Propietats Periã DiquesDocument3 pagesExercicis Propietats Periã DiquesPAU YI RAMOSNo ratings yet
- Pau Fisi17slDocument4 pagesPau Fisi17slTecnidonNo ratings yet
- FISICADocument8 pagesFISICAtamylemor2002No ratings yet
- Pau Fisi2Document3 pagesPau Fisi2Xavier SoléNo ratings yet
- Exercicis Q1 U7 Models AtomicsDocument4 pagesExercicis Q1 U7 Models AtomicsPaula Raga RoperoNo ratings yet
- Unitat 2 Estructura Atòmica I Sistema PeriòdicDocument23 pagesUnitat 2 Estructura Atòmica I Sistema PeriòdicVentas RP TecnologíaNo ratings yet
- Problemes de Estructura AtòmicaDocument5 pagesProblemes de Estructura AtòmicajawadmanoutNo ratings yet
- TEMA 4valDocument3 pagesTEMA 4valJuanNo ratings yet
- fq4 Exer DossierDocument39 pagesfq4 Exer Dossiermireia coleNo ratings yet
- Annex 8.30 Problemes. SolucionsDocument3 pagesAnnex 8.30 Problemes. Solucionsmarquitussm3No ratings yet
- TEMA1 - Estructura Atòmica - BoDocument20 pagesTEMA1 - Estructura Atòmica - BoIZAN JHNo ratings yet
- Enunciat FISICA JUNY 2017Document2 pagesEnunciat FISICA JUNY 2017Claudia PlanasNo ratings yet
- 1-0 Model Atomic Actual Exercicis 2324Document8 pages1-0 Model Atomic Actual Exercicis 2324aromuncalNo ratings yet
- Recull PAU 15-19Document60 pagesRecull PAU 15-19marti.miroNo ratings yet
- U7 PDFDocument6 pagesU7 PDFCarles Alcaide BlayaNo ratings yet
- 1BATQ UD2-5 Prop Periodiques I Config Electronica Recull Exercicis PAU Fins2022 2324 ALUMNATDocument5 pages1BATQ UD2-5 Prop Periodiques I Config Electronica Recull Exercicis PAU Fins2022 2324 ALUMNATaromuncalNo ratings yet
- Problemes Naturalesa de La Llum4Document4 pagesProblemes Naturalesa de La Llum4Sergi Caicedo GarciaNo ratings yet
- Pau Fisi16jlDocument8 pagesPau Fisi16jlIman Eljabri AdsouliNo ratings yet
- Exercicis Q1 Models Atòmics 20-21Document14 pagesExercicis Q1 Models Atòmics 20-21bruixettaNo ratings yet
- Solucionari Estructura de LaDocument15 pagesSolucionari Estructura de Laabril.geladaNo ratings yet
- Model Examen (V)Document2 pagesModel Examen (V)LauraNo ratings yet
- Examen Fisica Selectivitat 2022 SetembreDocument16 pagesExamen Fisica Selectivitat 2022 Setembreguerrera tousNo ratings yet
- Física Con Hojas ExtraDocument96 pagesFísica Con Hojas ExtraSara Juan NuñoNo ratings yet
- Exercicis Estructura Atòmica FinalsDocument2 pagesExercicis Estructura Atòmica FinalsBy ÁlexNo ratings yet
- Estructura de La MatèriaDocument19 pagesEstructura de La MatèriaFaniMilletNo ratings yet
- Exercicis Estructura AtòmicaDocument2 pagesExercicis Estructura Atòmicalaia.gavaldaNo ratings yet
- Ions I IsotopsDocument3 pagesIons I IsotopsAnaNo ratings yet
- Models Atòmics Fitxa 1Document5 pagesModels Atòmics Fitxa 1Gemma Paredes OlivellaNo ratings yet
- REFORÇ 1a AVALUACIÓ 1r BATXDocument5 pagesREFORÇ 1a AVALUACIÓ 1r BATXtexida7864No ratings yet
- Selectivitat Fisica ModernaDocument12 pagesSelectivitat Fisica ModernaToni Vives SuredaNo ratings yet
- Exercicis de RepàsDocument4 pagesExercicis de Repàslucarebenaque2No ratings yet
- Electricitat I Magnetisme PREGUNTES TIPUS PROVA ESCRITADocument4 pagesElectricitat I Magnetisme PREGUNTES TIPUS PROVA ESCRITAxaviperez304No ratings yet
- Control Q1 Models Atomics 2015-16Document3 pagesControl Q1 Models Atomics 2015-16PokeLink 10No ratings yet
- Examen Física de Baleares (Extraordinaria de 2013)Document2 pagesExamen Física de Baleares (Extraordinaria de 2013)Soler InstiNo ratings yet
- Full Repàs 1a Avlauació SOLUCIONSDocument11 pagesFull Repàs 1a Avlauació SOLUCIONSnachapalNo ratings yet
- Còpia de ACTIVITATS Diversitat D'àtomsDocument5 pagesCòpia de ACTIVITATS Diversitat D'àtomsAya ElKhayat El KhayatNo ratings yet
- Problemes Sistema PeriòdicDocument5 pagesProblemes Sistema PeriòdicjawadmanoutNo ratings yet
- Examen Fisica Selectivitat 2024Document16 pagesExamen Fisica Selectivitat 2024winterjuanluNo ratings yet
- Dossier Recuperació 4t Av 1-2Document11 pagesDossier Recuperació 4t Av 1-2Naruto UzumaquiNo ratings yet
- Apunts UNITAT 6 (4ESO)Document17 pagesApunts UNITAT 6 (4ESO)tjvmh4s6rfNo ratings yet