Professional Documents
Culture Documents
Przewodnictwo
Przewodnictwo
Uploaded by
adamOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Przewodnictwo
Przewodnictwo
Uploaded by
adamCopyright:
Available Formats
18.03.
08’
Marcin Zgrys (gr.3)
Karolina Kotra (gr.2)
Zespół 2
Ćwiczenie nr 2
Nazwa ćwiczenia: Przewodnictwo elektryczne roztworów.
1. Wstęp teoretyczny
Celem ćwiczenia było wyznaczenie średnich współczynników aktywności oraz termodynamicznej
stałej dysocjacji kwasu octowego.
2. Spis użytych symboli
c - stężenie [N]
k - stała naczynka [m-1]
к - przewodnictwo właściwe [s·m-1]
λ - przewodnictwo równoważnikowe [s·m2 ·(kgrównoważnik)-1]
λ∞- graniczne przewodnictwo równoważnikowe [s·m2 ·(kgrównoważnik)-1]
α - stopień dysocjacji
Kc - stała dysocjacji
Kac - termodynamiczna stała dysocjacji
γ± - średni współczynnik aktywności
3. Dane dotyczące użytych symboli
к0,01M KCl = 0,1413 [s·m-1]
cKCl = 0,01
λ∞ CH3COOH = 39,071 [s·m2 ·(kgrównoważnik)-1]
4. Obliczenia
Przewodnictwo 0,01M KCl: 2,9 [mS]
Przewodnictwo wody redestylowanej: 3 [μS]
Schemat obliczeń jest następujący:
1. Obliczenie stałej naczynka konduktometrycznego:
[m-1]
2. Obliczenie przewodnictwa właściwego na podstawie przewodnictw kwasu octowego
uzyskanych za pomocą pomiarów (od otrzymanych przewodnictw odejmujemy
przewodnictwo wody redestylowanej):
[s·m-1]
3. Obliczenie przewodnictwa równoważnikowego:
[s·m2 ·(kgrównoważnik)-1]
4. Obliczenie stopnia dysocjacji:
5. Obliczenie stałej dysocjacji:
6. Obliczenie termodynamicznej stałej równowagi (na podstawie ekstrapolacji wykresu)
7. Obliczenie średnich współczynników aktywności:
Wyniki pomiarów i obliczeń zostały zestawione w poniższych tabelach:
Przewodnictwo
Zmierzone
c po odjęciu к λ α Kc γ±
przewodnictwo
H2Ored
0.05 0.0008 0.000797 0.0388 0.7767 0.0199 2.016·10-5 0.9608
0.02 0.0005 0.000497 0.0242 1.2108 0.0309 1.982·10-5 0.9689
0.01 0.0004 0.000397 0.0193 1.9343 0.0495 2.579·10-5 0.8495
0.005 0.0003 0.000297 0.0145 2.8942 0.0741 2.963·10-5 0.7925
0.0025 0.000225 0.000222 0.0108 4.3267 0.1107 3.448·10-5 0.7347
0.001 0.00015 0.000147 0.0072 7.1624 0.1833 4.115·10-5 0.6725
0.0005 0.00014 0.000137 0.0067 13.3504 0.3417 8.868·10-5 0.4581
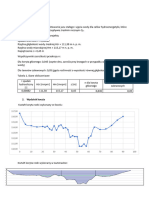
Na podstawie powyższej tabeli uzyskaliśmy wykres logK c = f(√c·α) [wykres 1] oraz wykres γ± = f(c)
[wykres 2] załączone do pracy.
You might also like
- 20a SPRDocument8 pages20a SPRLuke Koltun100% (1)
- Komin StalowyDocument23 pagesKomin Stalowy邱立伟No ratings yet
- Sprawozdanie 4 FizykaDocument7 pagesSprawozdanie 4 FizykaoliwiaskaNo ratings yet
- 03 - Ugięcie - Metoda Dokładna - Przykład PDFDocument5 pages03 - Ugięcie - Metoda Dokładna - Przykład PDFIgor PeregudNo ratings yet
- CW 12 Pomiar Temperatury Orazsprawdzenie TermometrówDocument11 pagesCW 12 Pomiar Temperatury Orazsprawdzenie TermometrówDariusz KotykNo ratings yet
- Metrologia Sprawozdanie 6Document8 pagesMetrologia Sprawozdanie 6Sebastian ZawistowskiNo ratings yet
- Zalacznik 10 Metodyka Szacowania Zmniejszenia Strat Ciepla-SieciDocument9 pagesZalacznik 10 Metodyka Szacowania Zmniejszenia Strat Ciepla-SieciPaweł SattlerNo ratings yet
- Projektowanie Przekładni ŁańcuchowejDocument4 pagesProjektowanie Przekładni Łańcuchowejpiotrek8324No ratings yet
- Przewodnictwo Cześć IDocument5 pagesPrzewodnictwo Cześć IadamNo ratings yet
- 4wykres PiezometrycznyDocument6 pages4wykres PiezometrycznyBartosz AugusewiczNo ratings yet
- Budo Wodne Cz. 1Document15 pagesBudo Wodne Cz. 1kborowska2406No ratings yet
- Sprawozdanie 3 FizykaDocument6 pagesSprawozdanie 3 FizykaoliwiaskaNo ratings yet
- Uwaga! Przykładowe Sprawozdanie Z Laboratorium FizykiDocument8 pagesUwaga! Przykładowe Sprawozdanie Z Laboratorium FizykiminissNo ratings yet
- ĆwzeroDocument5 pagesĆwzeroopyka514No ratings yet
- DiodyDocument6 pagesDiodyOktawianNo ratings yet
- WprowadzenieDocument6 pagesWprowadzenieOktawianNo ratings yet
- 64 - Wyznaczanie Składowej Poziomej Natężenia Ziemskiego Pola Magnetycznego PDFDocument5 pages64 - Wyznaczanie Składowej Poziomej Natężenia Ziemskiego Pola Magnetycznego PDFJakub .BarańskiNo ratings yet
- Sprawko - Cewka Helmholtza - KopiaDocument5 pagesSprawko - Cewka Helmholtza - KopiasewerynbanasiakNo ratings yet
- Pspice 1Document11 pagesPspice 1OleksandrNo ratings yet
- Fizyka. Cwiczenie 422222224aDocument6 pagesFizyka. Cwiczenie 422222224atrcwk16No ratings yet
- CW 45 Pomiar Strumienia Przepływajacego Gazu I Jego ParametrówDocument14 pagesCW 45 Pomiar Strumienia Przepływajacego Gazu I Jego ParametrówDariusz KotykNo ratings yet
- KisielewaDocument3 pagesKisielewajaneckihNo ratings yet
- Arkadiusz Rozmus - Badanie Pompy WirowejDocument4 pagesArkadiusz Rozmus - Badanie Pompy WirowejArkadiusz RozmusNo ratings yet
- Zad 0 1 PogladoweDocument2 pagesZad 0 1 PogladoweRadek PaśNo ratings yet
- Perhitungan Alinyemen Horizontal FC SCS SSDocument16 pagesPerhitungan Alinyemen Horizontal FC SCS SSHanafiahHamzahNo ratings yet
- Moj ProjektDocument13 pagesMoj Projektkamilek69No ratings yet
- Sprawozdanie - Reakcja HydrodynamicznaDocument5 pagesSprawozdanie - Reakcja Hydrodynamicznahenry003No ratings yet
- Projekt Lekkiej Kątowej Ścianki OporowejDocument15 pagesProjekt Lekkiej Kątowej Ścianki OporowejJa WaNo ratings yet
- 44A - Pomiar Zależności Oporności Metali I Półprzewodników Od TemperaturyDocument8 pages44A - Pomiar Zależności Oporności Metali I Półprzewodników Od TemperaturyJakub .BarańskiNo ratings yet
- Strugarka GleasonaDocument10 pagesStrugarka GleasonasensacjeNo ratings yet
- Lab 1 - Wyznaczanie Współczynnika Lepkości Dynamicznej, Zależność Lepkości Od TemperaturyDocument5 pagesLab 1 - Wyznaczanie Współczynnika Lepkości Dynamicznej, Zależność Lepkości Od TemperaturyJarek IbrahimowicNo ratings yet
- Hydro 1Document6 pagesHydro 1jaqb0208No ratings yet
- Cwiczenie 4-2Document9 pagesCwiczenie 4-2bofek39656No ratings yet
- Preparation For School ExamDocument7 pagesPreparation For School Exammaxb85852No ratings yet
- cw1 SPR PDFDocument7 pagescw1 SPR PDFSylwesterNowakNo ratings yet
- Projekt 2 SkarpaDocument7 pagesProjekt 2 SkarpaHubert UrbanekNo ratings yet
- Statyka Budowli Projekt 2 - Metoda PrzemieszczeńDocument25 pagesStatyka Budowli Projekt 2 - Metoda PrzemieszczeńSara NooitgedagtNo ratings yet
- Politechnika Poznańska: Badanie Przekaźnika Ritx 21 O Charakterystyce NiezależnejDocument4 pagesPolitechnika Poznańska: Badanie Przekaźnika Ritx 21 O Charakterystyce NiezależnejNot MeNo ratings yet
- Przykladowe SprawozdanieDocument5 pagesPrzykladowe SprawozdaniejanNo ratings yet
- Czwiczenie 204 Maksym LutvynchukDocument7 pagesCzwiczenie 204 Maksym LutvynchukdragonhardNo ratings yet
- Ficha Selección Baltimore VXC (6554)Document8 pagesFicha Selección Baltimore VXC (6554)Vladimir Santos Mariano OrtegaNo ratings yet
- Obl 8 Konstr NosnaDocument7 pagesObl 8 Konstr NosnatechspawNo ratings yet
- Grochowska Konstrukcje 9 2014Document5 pagesGrochowska Konstrukcje 9 2014Jacek MarusaNo ratings yet
- Obliczenia 95Document13 pagesObliczenia 95Michał GolańskiNo ratings yet
- No Nie WyszłoDocument3 pagesNo Nie WyszłoStarsza KrewNo ratings yet
- UHuP Lab 1Document7 pagesUHuP Lab 1matpisarzewski4No ratings yet
- Projekt BWDocument3 pagesProjekt BWNatalia BielNo ratings yet
- LPF WPPT 44Document5 pagesLPF WPPT 44Katarzyna MiodyńskaNo ratings yet
- CW 3 GR 2 Sprawozdanie IBMDocument6 pagesCW 3 GR 2 Sprawozdanie IBMRebelandarrowNo ratings yet
- Mechanika Gruntów, ProjektDocument11 pagesMechanika Gruntów, ProjektKrzysztof StankiewiczNo ratings yet
- Projekt 6b - 2Document17 pagesProjekt 6b - 2Szymon PenczekNo ratings yet
- 44 WeraDocument7 pages44 WeraAndziaNo ratings yet
- Sprawozdanie Zginanie PrętaDocument6 pagesSprawozdanie Zginanie PrętamiketencikNo ratings yet
- Przerwa EnergetycznaDocument11 pagesPrzerwa EnergetycznaAlicja HanulakNo ratings yet
- LPF WPPT PWR 48Document4 pagesLPF WPPT PWR 48Katarzyna MiodyńskaNo ratings yet
- ĆW NR 2 - Strona Tytułowa - Wprowadzenie I Wytyczne WykonaniaDocument6 pagesĆW NR 2 - Strona Tytułowa - Wprowadzenie I Wytyczne Wykonaniaxyp8jd5dkcNo ratings yet
- Maszyny Transportowe (Suwnica Czaja)Document11 pagesMaszyny Transportowe (Suwnica Czaja)kamilek69100% (1)
- Oblczenie Slupa Żelbetowego WG EC2 - WprowadzenieDocument29 pagesOblczenie Slupa Żelbetowego WG EC2 - Wprowadzeniepiotr_buk100% (2)
- IX Badanie Równowagi Fazowej Ciecz-Ciecz W Układzie AdwuskładnikowymDocument3 pagesIX Badanie Równowagi Fazowej Ciecz-Ciecz W Układzie AdwuskładnikowymadamNo ratings yet
- CH FLab Ciecz CieczDocument2 pagesCH FLab Ciecz CieczadamNo ratings yet
- PrzewodnictwoDocument5 pagesPrzewodnictwoadamNo ratings yet
- LepkośćDocument2 pagesLepkośćadamNo ratings yet
- PrzewodnictwoDocument2 pagesPrzewodnictwoadamNo ratings yet
- Równowaga Ciecz paraDocument3 pagesRównowaga Ciecz paraadamNo ratings yet
- Przewodnictwo Cześć IDocument5 pagesPrzewodnictwo Cześć IadamNo ratings yet
- Przewodnictwo Częsc IIDocument1 pagePrzewodnictwo Częsc IIadamNo ratings yet
- Przewodnictwo NaszeDocument6 pagesPrzewodnictwo NaszeadamNo ratings yet