Professional Documents
Culture Documents
Chapter 4
Chapter 4
Uploaded by
nhatlong.superboy0 ratings0% found this document useful (0 votes)
2 views22 pagesCopyright
© © All Rights Reserved
Available Formats
PDF, TXT or read online from Scribd
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
© All Rights Reserved
Available Formats
Download as PDF, TXT or read online from Scribd
Download as pdf or txt
0 ratings0% found this document useful (0 votes)
2 views22 pagesChapter 4
Chapter 4
Uploaded by
nhatlong.superboyCopyright:
© All Rights Reserved
Available Formats
Download as PDF, TXT or read online from Scribd
Download as pdf or txt
You are on page 1of 22
Chăm sóc răng miệng cho các bệnh khu trú và bệnh toàn thân
Viêm lợi miệng Herpes nguyên phát (Primary Herpetic Gingivostomatitis):
Virus Herpes Simplex (Herpes đơn dạng) tuýp 1 (HSV-1) là một virus DNA lớn, gây ra
các bệnh lý: Viêm lợi miệng Herpes nguyên phát (VLMHNP – PHG), bệnh về niêm mạc da vùng
miệng mặt, bệnh lý mắt, bệnh Herpes Gladiatorum (xuất hiện ở các vận động viên thể thao có “va
chạm” – contact sport), bệnh chàm bội nhiễm (Eczema Herpeticum), viêm nang lông herpes
(Herpetic sycosis) vùng râu mọc; và bệnh Herpes sinh dục (Herpes Genitalis) ít gặp hơn, đa số do
nhiễm Virus Herpes Simplex tuýp 2 (HSV-2) gây nên. HSV là nguyên nhân phổ biến nhất gây
bệnh hồng ban đa dạng (Erythema multiforme). Mặc dù VLMHNP (PHG) là bệnh truyền nhiễm
có khả năng lây nhiễm cao, chỉ 5-10% bệnh nhân lây nhiễm lần đầu có triệu chứng, tổn thương
lâm sàng. Bệnh VLMHNP chủ yếu lây truyền qua tiếp xúc trực tiếp với da hoặc dịch cơ thể; bệnh
lây lan nhanh chóng trong môi trường kín như nhà trẻ hoặc trại mồ côi. Khởi phát bệnh bất ngờ
với các biểu hiện lâm sàng từ nhẹ đến nặng cần được nhập viện. Bệnh có các triệu chứng không
đặc hiệu bao gồm: Phì đại hạch bạch huyết cổ (Cervical Lymphadenopathy), khó chịu, bức bối,
kích thích, viêm đường hô hấp trên, sốt nhẹ. Bệnh VLMHNP (PHG) gây ra các tổn thương trong
và ngoài miệng, sưng và chảy máu mô nướu. Tổn thương miệng có thể bắt đầu từ những mụn nước
trên lưỡi, niêm mạc má, nướu. Các mụn nước vỡ nhanh chóng tạo thành các vết loét có kích thước
1-3mm, từ đó hình thành các vùng lở loét lớn được bao phủ bởi lớp màng xám vàng. Bệnh nhiễm
trùng sẽ tự khỏi sau 10-14 ngày, quá trình lành thương không để lại sẹo. Trẻ em nhiễm bệnh có
thể có sự xuất hiện của cơn đau khu trú dữ dội, khiến việc ăn uống trở nên khó khăn, nguy cơ mất
nước. Các triệu chứng thường gặp là chảy nước dãi, hơi thở hôi, đau họng. Các biến chứng hiếm
gặp, lây qua tiếp xúc trực tiếp có thể dẫn tới viêm kết mạc giác mạc (Keratoconjunctivitis), và mụn
rộp trắng (Herpetic whitlow) (Ví dụ như viêm da đầu gối, ngón tay/chân, bàn tay). Các biến chứng
này là bệnh nghề nghiệp cổ điển của các chuyên gia chăm sóc sức khỏe. Sau lần nhiễm trùng ban
đầu, virus có thể trở về trạng thái ngủ đông, song dễ dàng được tái kích hoạt và phát bệnh trở lại
với các triệu chứng giảm nhẹ.
Điều trị VLMHNP (PHG) hướng đến phục hồi tổn thương, chăm sóc tại nhà, cung cấp đủ
nước và chất dinh dưỡng; phòng ngừa nguy cơ lây nhiễm như tránh tiếp xúc trực tiếp với người
bệnh, xài chung dụng cụ cá nhân như muỗng, nĩa, thức ăn, khăn tắm, bàn chải, bình nước, núm
bình sữa, ly, đồ chơi. Cần tránh tiêu thụ thức ăn, nước uống có nồng độ acid cao hoặc nhiều gia
vị. Tiêu thụ các sản phẩm lạnh như kem, đá bào có tác dụng giảm đau và bổ sung nước. Thuốc
giảm đau, thuốc tê tại chỗ, đắp thuốc giúp xoa dịu cơn đau, hỗ trợ cho việc ăn uống và bổ sung
chất dinh dưỡng cần thiết. Thuốc tê tại chỗ cần được sử dụng thận trọng vì chúng được hấp thụ
nhanh chóng bởi các vết loét; bệnh nhân được khuyến cáo nhổ thuốc tê ra sau khi sử dụng. Nuốt
hoặc súc miệng với thuốc tê có thể gây ức chế phản xạ nôn (Gag reflex), dẫn đến nguy cơ hít thuốc
tê vào phổi. Sử dụng nước súc miệng kháng khuẩn không cồn có thể giúp giảm nguy cơ nhiễm
trùng thứ cấp ở bệnh nhân có tình trạng bệnh nướu đáng chú ý và vệ sinh răng miệng kém.
Chẩn đoán bệnh được dựa vào các biểu hiện lâm sàng và tiền sử bệnh. Tuy nhiên, tiêu
chuẩn vàng để chẩn đoán là kết quả dương tính của xét nghiệm nuôi cấy virus. Quá trình nuôi cấy
virus bắt đầu bằng việc lấy tăm bông thấm đẫm dịch và cạo phần đế của mụn nước. Tăm bông sau
đó sẽ được đặt vào môi trường vận chuyển virus (transport media) đặc biệt và gửi đến phòng thí
nghiệm. Thông thường, virus được nuôi cấy phân lập sẽ phát triển trong 5 ngày. Chẩn đoán phân
biệt bao gồm: Viêm họng mụn nước (Herpangina), loét áp-tơ miệng (Aphthous stomatitis), bệnh
tay-chân-miệng (Hand-foot-and-mouth disease), hội chứng Stevens-Johnson, bệnh bọng nước tự
miễn (Pemphigus), nhiễm Zoster miệng, viêm nướu hoại tử lở loét (Necrotizing ulcerative
gingivitis), và hội chứng Behcet. Thuốc Acyclovir (ACY) được cho rằng có khả năng làm thuyên
giảm một số triệu chứng của VLMHNP và giảm tỉ lệ nhập viện cho trẻ em dưới 6 tuổi. Liều dùng
ACY qua đường miệng là 15 mg/kg, tối đa 80 mg/kg hằng ngày: sử dụng mỗi 3 tiếng khi tỉnh táo
hoặc 5 lần/ngày trong vòng 10 ngày. Hạn chế của thuốc ACY là khả năng hấp thu qua đường tiêu
hóa kém và sinh khả dụng thấp. Valacyclovir và famciclovir được phát triển để tăng sinh khả dụng
của thuốc, song hiện tại hai loại thuốc này không thể dùng cho trẻ em.
Nhiễm Herpes Simplex tái phát (Recurrent Herpes Simplex Infection):
Nhiễm HSV vẫn là một vấn đề sức khỏe toàn cầu nghiêm trọng mặc cho sự thành công
trong việc điều trị với ACY và các thuốc liên quan. HSV là nguyên nhân hàng đầu dẫn đến các
bệnh như viêm não (encephalitis) và bệnh loét bộ phận sinh dục, và nó còn là nguyên nhân chính
gây lây nhiễm HIV. Sau giai đoạn nhiễm trùng nguyên phát, HSV rơi vào trạng thái ngủ đông tại
Hạch Gasser (Trigeminal ganglion – Hạch thân kinh tam thoa). Trong thời kì ngủ đông, quá trình
sao chép của virus giảm. Khi có các tác nhân kích thích (ví dụ: bệnh tật, ánh nắng mặt trời, stress,
căng thẳng, giai đoạn hành kinh, điều trị nha khoa, tăng thân nhiệt ác tính, v.v.), virus tái hoạt
động, sao chép tại hạch thần kinh, sau đó di chuyển đến vùng da và niêm mạc. Sự phát tán virus ở
bệnh nhân không triệu chứng thường xảy ra, và là yếu tố nguy cơ chính góp phần lây lan bệnh. Có
3 dạng nhiễm HSV sau đây: Herpes môi tái phát (Recurrent herpes labialis – RHL), nhiễm trùng
miệng tái phát (Intraoral recurrence), tái phát có triệu chứng như nhiễm trùng nguyên phát. Các
tổn thương của bệnh tái phát ở bệnh nhân suy yếu miễn dịch thường xảy ra ở vùng da quanh miệng,
vùng cánh mũi, và tại vùng tiếp xúc giữa ranh giới đỏ son (Vermilion Border) và da môi
(Cutaneous lip) dưới dạng Herpes môi tái phát (RHL). Các tổn thương Herpes tái phát trong miệng
được tìm thấy hầu như riêng biệt ở niêm mạc sừng hóa của khẩu cái cứng, nướu dính và đôi khi
trên lưng lưỡi (Dorsum of the tongue). Ở bệnh nhân suy giảm hệ miễn dịch, nhiễm HSV tái phát
có thể gây nên các vết loét lớn, tiến triển, dai dẳng kéo dài. Chẩn đoán thường gặp trở ngại do các
triệu chứng không điển hình, đôi khi tổn thương miệng có thể lan tới các vùng niêm mạc không
sừng hóa.
Bệnh nhân Herpes môi tái phát (RHL/Cold sore – vết loét lạnh) thường trải qua các giai
đoạn ngứa ran và tê, đau rát, nổi rộp, mụn nước trong vài giờ; sau đó tạo thành các vết loét, rỉ
nước, đóng vảy trong vòng 72-96 tiếng. Thời điểm lây nhiễm, phát tán mạnh nhất là trong 24 giờ
đầu, khi xuất hiện các tổn thương. Đa số các cơn tái phát thường tự miễn (từ 7-14 ngày), triệu
chứng nhẹ và ngắn hạn ở bệnh nhân khỏe mạnh, cửa sổ điều trị hẹp. Bệnh tái phát đa dạng. Bệnh
nhân bị Herpes môi tái phát do mặt trời kích thích cần sử dụng son dưỡng và lotion bảo vệ môi.
Trẻ em bị nhiễm Herpes tái phát có triệu chứng giống với VLMHNP, và được điều trị tại nhà tương
tự như VLMHNP. Thuốc kìm virus cần được sử dụng trước khi tải lượng virus chạm ngưỡng, do
các tổn thương lên các tế bào biểu mô sẽ không thể tái tạo lại được. Việc sử dụng thuốc kháng
virus dự phòng cho người bị tái phát 1-2 lần/năm không được khuyến cáo vì nguy cơ kháng thuốc
và nguy cơ lợi-hại. ACY là thuốc đặc hiệu cao cho tế bào nhiễm virus và ít độc tính cho tế bào
(mô) khỏe mạnh. Tuy nhiên khuyết điểm lớn nhất của ACY là sinh khả dụng thuốc qua đường
miệng thấp. Các bằng chứng khoa học chỉ ra rằng dầu bôi chứa 5-10% ACY không có tác dụng
hiệu quả trong việc điều trị Herpes môi tái phát ở bệnh nhân khỏe mạnh, nguyên nhân do độ thẩm
thấu thấp. Kem bôi chứa 5% ACY có thể làm giảm thời gian tổn thương tồn tại nếu được sử dụng
sớm trong giai đoạn tiền triệu chứng, nhưng không có hiệu quả giảm đau. Song, người bệnh với
các cơn tái phát dài và đau dữ dội được điều trị hiệu quả với thuốc bôi tại chỗ; thuốc kháng viêm
có thể được thêm vào để tăng hiệu quả của ACY. Liều dùng của ACY qua đường miệng (toàn
thân) là 200-400 mg (cho người lớn) 5 lần/ngày trong 5 ngày cho người bệnh Herpes môi tái phát
(RHL) có chức năng giảm đau, lành thương, giảm lây lan trong 1-1.5 ngày (đặc biệt khi điều trị
sớm). Kem chống nắng (SPF 15 hoặc tốt hơn) giúp giảm tỷ lệ tái phát bệnh RHL. Acyclovir tác
dụng toàn thân (200 mg mỗi 3 giờ khi tỉnh táo trong 5 ngày) được chỉ định cho trẻ có hoặc nhiều
hơn 6 cơn tái phát RHL/năm. Các thuốc kháng virus khác bao gồm: valacyclovir, ganciclovir,
valganciclovir, penciclovir, famciclovir, foscarnet, và cidofovir. Độ an toàn và hiệu quả điều trị
của các thuốc này trên trẻ em chưa được xác nhận. Docosanol, là thuốc không kê đơn duy nhất
được FDA (Food and Drug Administration - Cục quản lý Thực phẩm và Dược phẩm Hoa Kỳ) công
nhận dùng để điều trị RHL cho trẻ em trên 12 tuổi. Thuốc được sử dụng 5 lần/ngày để thoa lên các
tổn thương (vùng bị ảnh hưởng) ở môi và mặt. Thuốc cần được sử dụng sớm nhất có thể khi vừa
có triệu chứng để đạt được hiệu quả tối đa. Các loại thuốc kháng virus và vaccine đang được thử
nghiệm và kiểm nghiệm bao gồm imiquimod, resiquimod, undecylenic acid, thymopentin, và
thuốc kháng vi sinh dùng cho niêm mạc.
Bệnh nhân đang điều trị ung thư có nguy cơ cao đối với nhiễm HSV tái phát, do đó cần
được điều trị phòng ngừa. Nhóm bệnh nhân này khi có tổn thương không tự lành sau 7-10 ngày
cần được xét nghiệm sinh thiết, nuôi cấy vi sinh, và test độ nhạy với thuốc ACY. Các cá thể bệnh
nhân được ghép tế bào gốc tạo máu có tỉ lệ kháng ACY cao nhất và được điều trị bằng foscarnet.
Bệnh nhân có bệnh lý suy giảm chắc năng thận được điều trị giảm liều ACY xuống 50%. Trong
trường hợp bệnh nhân vừa mắc VLMHNP và nhiễm Herpes tái phát, chuyên gia nha khoa cần đảm
bảo dinh dưỡng, cung cấp đủ nước cho người bệnh, giữ vệ sinh răng miệng tốt, sạch sẽ, kiểm soát
quá trình phát triển và ngăn ngừa sự lây lan của bệnh lý. Các điều trị nha khoa cần được hoãn lại
đến khi diễn ra sự lành thương.
Nhiễm nấm Candida hầu- họng (Oropharyngeal Candidiasis):
Nhiễm nấm Candida là một loại nhiễm trùng cơ hội, nguyên nhân gây bệnh là do sự phát
triển của chủng nấm Candida dưới các tác nhân như sử dụng thuốc kháng sinh/corticosteroid, tình
trạng khô miệng (xerostomia), đái tháo đường (diabetes mellitus), khí cụ chỉnh nha che phủ khẩu
cái, hút thuốc, hệ miễn dịch chưa hoàn thiện hoặc bị suy giảm. Nhiễm nấm Candida phổ biến nhất
ở trẻ em là dạng màng giả và dạng ban đỏ. Nhiễm nấm Candida dạng màng giả có các mụn sẩn và
dát lớn màu trắng-vàng, di động, kích thước và hình dáng đa dạng, tỏa tròn, che phủ ban đỏ
(Erythema) phía dưới. Nhiễm nấm Candida dạng màng giả thường xuất hiện ở niêm mạc má, vết
gấp niêm mạc má, hai bên lưng lưỡi, và hầu họng. Nhiễm nấm Candida dạng ban đỏ hoặc dạng
teo có các mẩn đỏ lan tỏa hoặc thành từng dát, chủ yếu tập trung ở khẩu cái và lưng lưỡi. Sự tích
tụ nước bọt tại các nếp gấp sâu vùng mép miệng tạo điều kiện cho sự xâm lấn của nấm và vi khuẩn
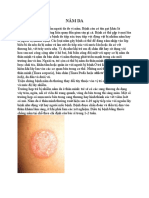
(gây bệnh chốc mép – angular cheilitis). Bệnh chốc mép có màu đỏ, đôi khi tạo thành vết loét và
đóng vảy, thường đau rát, xuất hiện nhiều ở trẻ em có thói quen mím môi (có thể lây sang vùng da
quanh miệng). Bệnh nhân nhiễm nấm Candida miệng trải qua các cơn đau miệng, bỏng rát niêm
mạc và lưỡi, khó nuốt, ăn uống khó khăn. Chẩn đoán bệnh được dựa vào nhân khẩu học, các yếu
tố sức khỏe của người bệnh, các dấu hiệu, triệu chứng lâm sàng, cũng như các tiêu chí trong phòng
thí nghiệm. Đánh giá kỹ lưỡng sức khỏe và các loại thuốc bệnh nhân đang sử dụng rất quan trọng
trong việc đưa ra phương pháp điều trị nấm hiệu quả và giảm thiểu tỉ lệ tái phát. Nuôi cấy vi sinh
rất hữu ích trong việc chẩn đoán và điều trị các tổn thương không đáp ứng phép trị liệu.
Việc cải thiện vệ sinh răng miệng, kiểm soát sâu răng, làm sạch núm vú giả và khí cụ chỉnh
nha, thay bàn chải mới rất quan trọng trong việc kiểm soát căn bệnh (nhiễm nấm). Đa số các thuốc
kháng nấm hiện nay có phổ rộng để chống lại Candida albicans cũng như các chủng Candida khác
(chúng thường được phân lập nhiều hơn). Các yếu tố tiềm ẩn cần được đánh giá khi nhiễm nấm
tái phát thường xuyên và không rõ nguyên nhân, ví dụ như bệnh toàn thân, tình trạng sức khỏe dẫn
đến suy giảm miễn dịch, bầu ngực người mẹ đang cho con bú. Sự kháng thuốc của nấm Candida
thường được thấy trong các trường hợp sử dụng thuốc kháng nấm trong thời gian dài. Thuốc kháng
nấm tại chỗ là hỗn dịch thuốc clotrimazole (10 mg/ml) và nystatin đường miệng (100,000 U/ml);
bệnh nhân súc miệng trong 2 phút rồi nuốt hoặc nhổ ra, 4 lần/ngày trong vòng 2 tuần; sau đó, việc
đánh giá lại khoang miệng sẽ được thực hiện. Người bệnh không nên ăn hoặc uống sau 30 phút
đầu. Trẻ vị thành niên có thể dùng 1-2 viên thuốc ngậm (200,000 U) để tan dần trong miệng 5
lần/ngày. Hỗn dịch Nystatin có chứa 30-50% sucrose, vì vậy cần tăng cường vệ sinh răng miệng.
Thuốc ngậm Clotrimazole (10mg) cũng có thành phần chứa nhiều sucrose, được ngậm tan dần
trong miệng mỗi 3 tiếng khi tỉnh táo (5 lần/ngày) trong vòng 14 ngày. Thuốc kháng nấm toàn thân
sẽ điều trị hiệu quả hơn khi được kết hợp bổ sung với thuốc kháng nấm tại chỗ. Các loại thuốc này
bao gồm fluconazole 6 mg/kg đường miệng mỗi 12 hoặc 24 giờ, trong 5-7 ngày; trẻ vị thành niên
có thể sử dụng 200-mg liều nạp (loading dose) cùng 100-200 mg liều thường mỗi ngày trong vòng
1 tuần. Ketoconazole có thể được sử dụng cho trẻ em với liều dùng 5-10 mg/kg mỗi 12 hoặc 24
giờ, cho trẻ vị thành niên 200-400 mg mỗi 24 giờ trong vòng 5-7 ngày. Thuốc có hiệu quả tốt kèm
theo sự tuân thủ tốt của bệnh nhân. Các tác dụng phụ thường thấy khi dùng thuốc toàn thân gồm:
buồn nôn, ói, ngứa ngáy, nổi ban, đầy hơi, đau bụng, nhức đầu, bất thường trong kết quả test chức
năng gan, viêm gan do thuốc. Chlorhexidine gluconate 0.12% có thể được dùng làm nước súc
miệng chống vi sinh, có chức năng duy trì vệ sinh hơn là chống nấm như các loại thuốc kháng nấm
đầu tay. Các thuốc bôi, kem kháng nấm bao gồm nystatin, clotrimazole, miconazole, và
ketoconazole. Trong các trường hợp bệnh nhân chốc mép mạn tính, kem bôi nystatin và
triamcinolone acetonide (Mycolog-II) là lựa chọn điều trị tốt nhất, được dùng để thoa vào mép
miệng 3 lần/ngày trong vòng 5 ngày.
Nhiễm nấm xâm lấn ở trẻ em đang gia tăng do số lượng suy giảm miễn dịch nguyên phát
và thứ phát ở trẻ gia tăng. Các trường hợp nhiễm nấm thường diễn ra trong môi trường bệnh viện,
đa số do các chủng nấm Candida, tiếp sau là nhiễm các chủng nấm Aspergillus (gây ra bệnh nhiễm
nấm mốc phổ biến). Nhiễm nấm Candida máu (nhiễm nấm huyết - Candidemia) ở trẻ em có tỉ lệ
mặc bệnh và tử vong cao, kéo dài thời gian nhập viện, gia tăng chi phí chăm sóc điều trị. Nhiễm
trùng nấm có thể lan tỏa đến các cơ quan đích như não, phổi, gan, thận, mắt và lá lách. Các yếu tố
nguy cơ gây ra nhiễm nấm huyết gồm: thời gian dài điều trị trong ICU (Đơn vị điều trị tích cực),
ức chế miễn dịch, nhiễm khuẩn từ trước, sau phẫu thuật, đặt ống thông (catheter) tĩnh mạch trung
tâm, sử dụng thiết bị trợ thở (thông khí cơ học), chạy thận nhân tạo (dialysis), sử dụng vancomycin
kéo dài, đái tháo đường, chấn thương, dinh dưỡng tĩnh mạch hoàn toàn (total parenteral nutrition-
TPN). Nhiễm nấm huyết có thể được điều trị bằng fluconazole hoặc echinocandin theo liệu pháp
thực nghiệm (Empirical therapy, chữa trị theo kinh nghiệm). Caspofungin là thuốc thuộc nhóm
echinocandin duy nhất được FDA công nhận dùng để điều trị cho trẻ em, tuy nhiên thời gian bán
thải của thuốc ở trẻ chỉ bằng 1/3 so với người lớn. Trẻ em, đặc biệt là trẻ sơ sinh dung nạp thuốc
amphotericin b thông thường tốt hơn người lớn. Tuy nhiên trẻ nhiễm nấm cần được tăng liều dùng
đối với thuốc voriconazole để đặt được ngưỡng điều trị cần thiết so với người lớn (voriconazole
được dùng để điều trị nhiễm nấm mốc Aspergillus xâm lấn (Aspergillosis)). Thuốc voriconazole
cũng là liệu pháp hiệu quả để điều trị nhiễm nấm Candida. Vẫn còn ít dữ liệu về việc sử dụng
nhóm thuốc triazole thế hệ hai (posaconazole, isavuconazole, ravuconazole, và albaconazole) cũng
như nhóm thuốc echinocandin (anidulafungin, micafungin) cho nhóm bệnh trẻ em. Itraconazole
có thể được dùng để điều trị cho bệnh nhi, song việc giám sát theo dõi và sử dụng thuốc này khó
hơn việc sử dụng fluconazole. Mặc cho sự ra đời của các loại thuốc kháng nấm mới, nhiễm nấm
xâm lấn (bao gồm cả nhiễm nấm candida) vẫn đang là vấn đề sức khỏe nghiêm trọng do các hạn
chế về độc tính, giá điều trị cao, và khả năng kháng thuốc.
Lợi ích của điều trị dự phòng để giảm thiểu các bệnh lý xâm lấn (invasive diseases) ở trẻ
em vẫn chưa có biểu hiểu rõ trong các trường hợp: trẻ mắc bệnh ung thư máu (ung thư hệ tạo
huyết), trẻ được cấy ghép tủy xương, nội tạng, trẻ mắc bệnh suy giảm miễn dịch nguyên phát.
Nguyên nhân là do vẫn chưa có thử nghiệm lâm sàng nào đủ độ ngẫu nhiên và số lượng mẫu chuẩn
để đánh giá việc điều trị kháng nấm dự phòng trong các trường hợp trên. Việc sử dụng thuốc dự
phòng không được khuyến cáo cho trẻ, ngoại trừ việc sử dụng itraconazole dự phòng cho bệnh nhi
u hạt mạn tính (Chronic granulomatous disease).
Bệnh hồng cầu hình liềm (Sickle Cell Disease):
Bệnh thiếu máu hồng cầu hình liềm (Sickle cell anemia – SCA) là bệnh di truyền thường
gặp, nhất là ở người Châu Phi, người gốc Phi-Carribean, người Trung Đông, Ấn Độ, Trung và
Nam Mỹ, người gốc Địa Trung Hải. Bệnh thiếu máu hồng cầu hình liềm (SCA) gồm các hồng cầu
hình liềm đặc trưng (lành tính); cùng với các bệnh lý bất thường liên quan đến hồng cầu hình liềm
(Sickle Cell Disease - SCD): tan máu bất thường (tán huyết – hemolysis), tổn thương cơ quan, nội
tạng mạn tính, các biến chứng cấp tính đe dọa đến tính mạng. Nguyên nhân bệnh là do đột biến
gene B-globin, tạo thành HbS (Hemoglobin hình liềm), liên quan đến việc vận chuyển oxy trong
máu. Cơ chế phân tử của bệnh hồng cầu hình liềm là do sự thay thế tại amino acid thứ 6 trong
protein B-globin (Valine thay cho Glutamic acid), Valine khiến cho HbS bị khử (deoxygenated)
polymer hóa. Tại Mỹ, SCA là bệnh phổ biến nhất được phát hiện qua xét nghiệm sàng lọc sơ sinh
(neonatal screening).
Quá trình polymer hóa (Polymerization) của HbS (bị khử) là sự kiện chính gây bệnh SCD,
sự trùng hợp (polymer hóa) của HbS phụ thuộc vào nồng độ HbS trong máu, mức độ nhả oxy của
tế bào, độ pH và nồng độ hemoglobin thai nhi (Fetal hemoglobin – HbF) nội bào (HbF có chức
năng bảo vệ khỏi biến dạng hình liềm). Cần trải qua một khoảng thời gian nhất định để quá trình
polymer hóa nội bào diễn ra đủ và biến đổi hình dạng tế bào. Các polymer được tạo ra có dạng
những bó sợi hình ống quánh đặc, làm biến dạng tế bào hồng cầu thành hình liềm. Các tế bào hình
liềm thường mắc kẹt trong dòng chảy chậm của các tiểu tĩnh mạch trong hệ thống vi tuần hoàn,
khiến các tế bào này tăng cường bám dính vào nội mạc mạch máu, tạo thành các cụm tế bào dị
loại (heterocellular aggregate) dẫn đến giảm oxy máu tại chỗ (local hypoxia), tăng sự trùng hợp
của HbS, và làm tắc nghẽn mạch máu liền kề. HbS không chỉ làm biến dạng tế bào hồng cầu hình
liềm mà còn khiến chúng kết dính, dẫn đến tổn thương nội mạc mạn tính. Một biến thể lâm sàng
đáng chú ý là bệnh lý viêm mạch máu mạn tính, tiến triển thành các tổn thương cơ quan nội tạng
đặc trưng bởi các giai đoạn đau dữ dội và biến chứng bệnh phổi. Thiếu máu và bệnh lý mạch máu
là những đặc trưng tiêu biểu của bệnh SCD, các triệu chứng bệnh lý xuất hiện trong 6 tháng đầu
đời. Tuổi thọ trung bình của tế bào hồng cầu hình liềm giảm từ 120 ngày xuống còn 12-17 ngày,
lượng huyết sắc tố (Hemoglobin – Hb) 6-9 g/dl (ở người khỏe mạnh: 12-18 g/dl), số lượng hồng
cầu lưới (reticulocyte counts) chiếm 5-15% (ở người khỏe mạnh: 0.5-1.5%).
Cơn bệnh đau đớn những năm đầu đời là bệnh lý viêm ngón (Dactylitis) (Tình trạng ngón
chân ngón tay xúc xích) gây ra bởi tình trạng nhiễm trùng, mất nước, nhiệt độ khắc nghiệt, giảm
oxy máu (hypoxia), các căng thẳng thể chất và tinh thần, giai đoạn hành kinh. Cơn đau nhức xương
thường dữ dội, tương xứng, tại nhiều vị trí, kéo dài từ vài phút đến vài ngày. Hội chứng giam hãm
tiểu cầu trong lách (Splenic sequestration crises) xảy ra do lượng lớn tế bào hồng cầu mắc kẹt tại
lá lách, và là nguyên nhân gây ra tình trạng thiếu máu đột ngột và nghiêm trọng, chứng giảm tiểu
cầu (Thrombocytopenia), chứng tăng hồng cầu dạng lưới (Reticulocytosis). Hội chứng nhiễm
trùng huyết sau cắt lách (Postsplenectomy sepsis) là bệnh lý đe dọa tính mạng chủ yếu gây ra bởi
vi khuẩn có vỏ bọc polysaccharide, đặc trưng là phế cầu khuẩn Streptoccocus Pneumoniae (Là
nguyên nhân tử vong hàng đầu ở trẻ mắc SCD). Các biểu hiện toàn thân khác bao gồm: Các vấn
đề tim mạch (cardiovascular problems), viêm tủy xương (osteomyelitis), loãng xương
(Osteoporosis), rối loạn phát triển (growth disturbances), hoại tử xương (osteonecrosis), hội chứng
ngực cấp (acute chest syndrome), tai biến mạch máu não (CerebroVascular Accident – CVA), suy
thận mạn tính (chronic renal failure), Chứng cương dương (Hội chứng Priapism – cương đau
dương vật kéo dài). Các biến chứng về tâm lý xã hội (Psychosocial complications) thông thường
gồm có suy giảm chức năng tâm lý (impaired psychosocial functioning) và giảm chất lượng cuộc
sống.
Điều trị can thiệp quan trọng nhất cho bệnh nhân SCD là sử dụng thuốc penicillin V
potassium 125mg đường miệng, 2 lần/ngày bắt đầu từ 2 tháng tuổi để phòng ngừa nhiễm phế cầu
khuẩn (Pneumococcus). Liều thuốc được tăng gấp đôi khi bệnh nhân đủ 3 tuổi, và được kéo dài
điều trị đến 5 tuổi. Ngoài ra, thuốc này cũng được dùng để điều trị, theo dõi hậu phẫu cắt lách
trong 2 năm. Có nhiều nghiên cứu, thí nghiệm đang được tiến hành để tìm ra loại thuốc điều trị
hiệu quả, lí tưởng cho bệnh nhân SCD. Hydroxyurea (HU) có ứng dụng ban đầu là chất chống ung
thư, song có khả năng làm tăng lượng HbF, góp phần giảm thiểu các biến dạng hình liềm cũng như
các di chứng dài hạn của bệnh. Độc tính của HU nhẹ và thoáng qua bao gồm: tình trạng thiếu máu,
buồn nôn, giảm bạch cầu trung tính (neutropenia), giảm tiểu cầu. Cấy ghép tế bào gốc tạo máu là
liệu pháp duy nhất điều trị bệnh hoàn toàn, và cần được tiến hành sớm, trước khi tình trạng rối
loạn chức năng tạng (organ dysfunctions) hình thành. Nhìn tổng quan, tỷ lệ tử vong do SCD đã
giảm, tuổi thọ trung bình người bệnh ở Mỹ đã tăng lên (42 tuổi ở đàn ông và 48 tuổi ở phụ nữ có
đồng hợp tử gene HbS), số người tử vong do nhiễm trùng đã giảm.
Các biểu hiện và triệu chứng răng miệng (của SCD):
Các triệu chứng răng miệng ở bệnh nhân SCD không có tính đặc hiệu, có thể tìm thấy ở
những người khỏe mạnh, cũng như ở những người có bệnh lý toàn thân. Niêm mạc có thể bị vàng
(jaundice) vì tình trạng tan máu (hemolysis) và trở nên xanh xao (pallor) do dung tích hồng cầu
(hematocrit) thấp. Viêm lưỡi (Glossitis) và chậm mọc răng cũng một trong số các triệu chứng
bệnh. Phim X-quang cho thấy mật độ bức xạ (radiodensity) xương giảm, cấu trúc xương xốp thô
(coarse trabecular pattern), giới hạn dưới của xương hàm dưới mỏng, tiêu chiều cao xương ổ răng,
lamina dura hiện rõ, kém khoáng hóa ngà (dentin hypomineralization), khuyết czermak
(interglobular dentin) ở vùng quanh chóp răng, canxi hóa buồng tủy, quá sản cement
(hypercementosis). Dị tật sọ mặt (craniofacial abnormalities) bao gồm hội chứng hô hai hàm
BIMAX (Bimaxillary protrusion) và vẩu răng cửa, xương đỉnh và xương gò má nhô lên (prominent
parietal and zygomatic bones) (Hội chứng sọ hình tháp – “tower skull”), mở rộng khoang tủy
xương sọ (widening of the diploic space) bằng việc làm giảm độ dày lớp ngoài vòm sọ (thinning
of the table of the calvarium) và tăng sinh bè tủy xương dọc (vertical trabeculation) (hình dạng
“Hair-on-end”: X-quang sọ: các nét dựng đứng vuông góc với bề mặt xương. Dấu hiệu này nhìn
giống những sợi tóc đang dựng đứng), và các tổn thương xơ cứng vòm sọ (fibrotic calvarial lesions)
với hình vòng tròn (tổn thương dạng doughnut).
Biến dạng hình liềm diễn ra ở hệ vi tuần hoàn của xương mặt và tủy răng gây nên cơn đau
mặt (không do bệnh lý của răng). Các cơn tắc nghẽn mạch máu gần lỗ thần kinh cằm có thể gây
nên dị cảm môi dưới kéo dài dai dẳng. Bệnh nhân SCD không có xu hướng mắc bệnh nha chu
nhiều hơn người bình thường. Việc sử dụng kháng sinh penicillin dự phòng trong thời gian dài có
thể đã chống lại sự xâm nhiễm của khuẩn mutans streptococcus, giúp giảm tỉ lệ sâu răng một cách
đáng kể ở bộ răng sữa. Tuy nhiên khi đủ 8 tuổi, liệu trình kháng sinh dự phòng được dừng lại, trẻ
em mắc SCD có tỉ lệ sâu răng ngang bằng với trẻ đồng trang lứa khỏe mạnh.
Các lưu ý trong điều trị răng miệng (cho bệnh nhân SCD):
Các cá thể mang kiểu hình (tính trạng) này không gặp trở ngại gì trong việc điều trị răng
miệng. Đối với bệnh nhân bị ảnh hưởng bởi SCD, tiền sử bệnh cần được khai thác chi tiết, bao
gồm các biến chứng liên quan, các dấu hiệu đặc trưng khi lên cơn đau, chăm sóc y tế trong quá
khứ và hiện tại, sự hiện diện của bộ phận nhân tạo thay thế cho bộ phận cơ thể bị mất, mang mầm
bệnh virus trong máu, các vấn đề về tăng trưởng và phát triển, thuốc men (bao gồm cả việc sử
dụng bisphosphonates), dị ứng, và hồ sơ tóm tắt tâm lý. Tiền sử răng miệng của bệnh nhân cần
được xem xét, gia đình người bệnh cần được giáo dục về việc chăm sóc sức khỏe răng miệng tốt
góp phần cải thiện chất lượng cuộc sống. Những phàn nàn về cơn đau ở những răng khỏe mạnh
cần được đánh giá kĩ lưỡng, nghiêm túc vì ở bệnh nhân SCD có khả năng bị sung huyết và hoại tử
tủy. Không có giải pháp tiếp cận nào là hoàn hảo trong các tình huống này. Mọi nhiễm trùng miệng
cần được tích cực điều trị, cần tránh điều trị phẫu thuật không bắt buộc. Khi lập kế hoạch điều trị
chỉnh hình răng hàm mặt cần khảo sát, đánh giá cấu trúc xương và sinh lý. Nếu bệnh nhân đã hoặc
đang sử dụng bisphosphonates, gia đình người bệnh cần được thông báo về nguy cơ hoại tử xương
hàm liên quan đến bisphosphonates sau khi điều trị nha khoa xâm lấn. Mọi điều trị chăm sóc nha
khoa đều an toàn tại phòng khám trong thời kì không phát bệnh. Bệnh nhân đeo bộ phận giả có thể
phải uống kháng sinh dự phòng trước khi điều trị nha khoa xâm lấn. Đối với bệnh nhân đang sử
dụng HU, cần phải thực hiện bộ công thức máu hoàn chỉnh vì họ mang các nguy cơ giảm bạch cầu
trung tính, giảm tiểu cầu. Không có bằng chứng khoa học nào ủng hộ việc sử dụng thuốc tê không
chứa thuốc co mạch cho bệnh nhân SCD. Việc sử dụng nitrous oxide (N2O) là an toàn, song cần
cẩn thận khi sử dụng, đề phòng giảm oxy huyết. Thuốc an thần đường miệng có thể được sử dụng
sau khi tham khảo kiến bác sĩ huyết học của bệnh nhân, thuốc phải được lựa chọn cẩn thận, tránh
gây ra tình trạng suy hô hấp. Cần phải xin ý kiến của bác sĩ gây mê hồi sức dày kinh nghiệm, trước
khi điều trị nha khoa dưới hình thức gây mê toàn diện để xác định nguy cơ biến chứng và ngăn
ngừa các trở ngại có thể xảy ra trong lúc phẫu thuật. Bệnh nhân có nguy cơ thấp có thể được điều
trị ở trung tâm phẫu thuật ngoại trú, bệnh nhân có nguy cơ cao hơn cần được điều trị trong phòng
mổ bệnh viện, với các thiết bị hỗ trợ y tế. Viện y tế quốc gia (The National Institutes of Health -
NIH) không khuyến cáo việc truyền máu đơn giản trong qui trình điều trị nha khoa hay phẫu thuật
miệng.
Bệnh lý máu khó đông Hemophilia A:
Bệnh máu khó đông Hemophilia A là một rối loạn di truyền do gene lặn trên nhiễm sắc thể
X, dẫn đến thiếu hụt yếu tố đông máu VIII, với tỉ lệ 1/5000 ở nam giới. Hemophilia A có tần suất
chiếm 85% trong tất cả các bệnh lý máu khó đông hemophilia, và được phân loại theo mức độ như
sau: Nặng (Không có yếu tố VIII nào trong máu được phát hiện), trung bình (yếu tố VIII khỏe
mạnh chiếm 1-4%), nhẹ (yếu tố VIII khỏe mạnh chiếm 5-25%). Trong trường hợp bệnh nhẹ, bệnh
nhân có thể không có tiền sử chảy máu, chỉ có thế phát hiện bệnh khi điều trị phẫu thuật hoặc chấn
thương. Cần nghi ngờ tình trạng máu khó đông ở bệnh nhân nam khi có dấu hiệu chảy máu bất
thường, trong đó, các chỉ số tiểu cầu (PLT count), thời gian máu chảy, thời gian thrombin, thời
gian prothrombin đều bình thường, nhưng thời gian thromboplastin một phần hoạt hóa bị kéo dài.
Các xét nghiệm đặc trưng yếu tố đông máu được dùng để phân biệt giữa bệnh lý máu khó đông
Hemophilia A và Hemophilia B (thiếu hụt yếu tố IX), chiếm 10-15% bệnh lý hemophilia.
Dấu hiệu lâm sàng của bệnh Hemophilia A là xuất huyết khớp và cơ, dễ thâm tím, chảy
máu kéo dài có khả năng gây tử vỏng sau chấn thương hoặc phẫu thuật, tuy nhiên các vết cắt, vết
xước nhỏ không gây chảy máu nhiều. Chứng tụ máu khớp (Hemarthroses) được phát hiện lần đầu
tiên khi trẻ bắt đầu tập đi. Nếu xuất huyết khớp không được chữa trị, việc vận động sẽ bị hạn chế
nghiêm trọng và có thể dẫn tới tàn tật vĩnh viễn. Khối tụ máu trong bắp có thể đè nén các cấu trúc
quan trọng và gây liệt thần kinh, cũng như làm tắc nghẽn mạch máu hoặc đường thở. Việc điều trị
Hemophilia A được thực hiện dựa theo phân loại mức độ nghiêm trọng của bệnh, dạng chảy máu
hiện tại hoặc dự đoán, sự hiện diện của các chất ức chế. Việc truyền dịch yếu tố VIII thường xuyên
được sử dụng để điều trị chảy máu nhiều trong các cuộc đại phẫu, đe dọa đến tính mạng.
Vasopressin (desmopressin) có khả năng làm tăng yếu tố VIII và yếu tố von Willebrand trong máu,
được dùng để điều trị hemophilia dạng nhẹ và trung bình (khi bệnh nhân đáp ứng tốt với liều thuốc
thử do bác sĩ huyết học thực hiện vài ngày trước cuộc phẫu thuật). Hiệu quả thuốc đạt đỉnh sau 20-
60 phút sử dụng, với thời lượng 4 giờ. Phương pháp điều trị ít được dùng hơn là việc sử dụng huyết
tương tươi đông lạnh (Fresh frozen plasma – FFP), tủa lạnh giàu yếu tố VIII đông khô. Một tình
huống thách thức xảy ra khi cơ thể bệnh nhân tạo nên kháng thể chống lại yếu tố VIII (hiện diện
ở 15% bệnh nhân hemophilia dạng nặng). Liệu pháp gene đang được nghiên cứu để kiểm soát và
điều trị bệnh máu khó đông hemophilia.
Các lưu ý khi điều trị răng miệng (cho bệnh nhân hemophilia):
Nha sĩ cần lưu ý bệnh sử và các biểu hiện lâm sàng của bệnh nhân; tuân theo pháp đồ và
hướng dẫn điều trị. Việc xem xét, đánh giá kĩ lượng tiển sử bệnh, kết quả xét nghiệm máu gần nhất
là tối quan trọng để khôi phục cơ chế đông máu về lại các chỉ số đông máu có hiệu quả, hỗ trợ cầm
máu bằng thuốc và biện pháp cục bộ. Việc xem xét tiền sử nha khoa cũng vô cùng quan trọng, đặc
biệt là các giai đoạn chảy máu khoang miệng, chế độ ăn, vệ sinh răng miệng, bởi vì việc chăm sóc
phòng ngừa và duy trì sức khỏe răng miệng rất cần thiết đối với bệnh nhân bị rối loạn chảy máu
(bleeding dyscrasia). Không cần điều trị sơ bộ trước khi cạo vôi trên nướu đối với bệnh nhân
hemophilia dạng nhẹ và trung bình. Tuy nhiên, một số điều trị sơ bộ cần được thực hiện trước khi
cạo vôi dưới nướu. Trong trường hợp bệnh nhân mắc hemophilia dạng nặng, không được gây tê
vùng hay sử dụng các phương pháp chích tê khác trước khi xử lí chảy máu thành công, bởi vì chích
tê có thể làm chảy máu ở mô sâu, có nguy cơ cao làm tắc nghẽn đường thở. Bệnh nhân mắc
hemophilia dạng nhẹ và trung bình có nguy cơ thấp. Sử dụng đê cao su và kẹp đê chắc chắn là việc
làm quan trọng để bảo vệ mô mềm. Chêm và khuôn trám có thể được đặt vào nhẹ nhàng, cẩn thận,
khí cụ có thể được gắn nếu không gây tổn thương đến các mô. Lấy tủy toàn phần, bán phần, điều
trị nội nha có thể được thực hiện mà không gây ra chảy máu đáng kể, tránh đưa dụng cụ và chất
trám vượt quá chóp. Điều trị nội nha có thể là lựa chọn duy nhất để kiểm soát áp xe răng cho bệnh
nhân kháng thuốc điều trị. Kĩ thuật phẫu thuật phải không gây tổn thương, các mảnh xương và mô
hạt cần được loại bỏ, vết thương được khâu đóng kín để bảo vệ, giữ cục máu đông. Thuốc kháng
sinh cần được sử dụng khi dùng chất cầm máu có thể hấp thụ, nếu không sẽ nhiễm trùng. Điều trị
chỉnh hình răng mặt không bị chống chỉ định, tuy nhiên cần lưu ý khi sửa dụng dây cung có đầu
nhọn và đặt khâu chỉnh nha có cạnh bén.
Bệnh nhân mắc hemophilia dạng trung bình và nặng cần được truyền yếu tố VIII trước khi
trải qua quá trình điều trị phẫu thuật miệng. Yếu tố đông máu có thể được truyền qua đường tĩnh
mạch, đạt ngưỡng trị liệu sau vài phút, và đạt ngưỡng 100% sau khi truyền. Một phương pháp khác
là truyền 50% liều lượng trước phẫu thuật, và 50% còn lại sau 12 giờ, được bổ sung bằng các
phương pháp cầm máu tại chỗ (đè ép vết thương, khâu đóng, dùng gelatin sponge, vật liệu
cellulose, thrombin, vi sợi collagen, keo dán fibrin, v.v.), thuốc chống tiêu sợi huyết đường miệng
(nước súc miệng tranexamic acid). Thời gian bán phân hủy của yếu tố VIII là 12 giờ. Vasopressin,
ε-aminocaproic acid, và tranexamic acid có thể được dùng theo đường toàn thân sau khi nhổ răng.
Bệnh nhân được chỉ định đại phẫu và sử dụng thuốc ức chế cần được nhập viện điều trị, vì bệnh
viện có môi trường hậu phẫu kín, có thể giám sát và truyền yếu tố đông máu tích cực.
Loãng xương ở trẻ em (Pediatric Osteoporosis):
Mật độ xương thấp đang có xu hướng gia tăng ở trẻ em. Gãy xương là nguyên nhân chính
khiến trẻ nhập viện từ độ tuổi 10-14 tuổi, số lượng gãy xương ở trẻ đang gia tăng qua 3 thập kỉ trôi
qua. Các yếu tố thời thơ ấu như lối sống, chế độ ăn, bệnh mạn tính, thuốc men có ảnh hưởng ngắn
hạn đến sức khỏe xương; ảnh hưởng dài hạn đến việc đạt khối lượng xương đỉnh (peak bone mass),
và tiềm năng mắc bệnh ở tuổi trưởng thành. Các yếu tố nội tại không thể thay đổi (ví dụ: chủng
tộc, bộ gene, giới tính) chịu trách nhiệm quyết định từ 75% đến 80% khối lượng xương đỉnh của
từng cá thể; trong khi đó, các yếu tố ngoại lai có khả năng biến đổi (ví dụ: chế độ ăn, hormones,
bệnh tập, thể dục thể thao) có nhiều ảnh hưởng đáng kể đến khối lượng xương sau cùng (ultimate
bone mass). Việc dung nạp đủ lượng canxi và vitamin D, và việc hoạt động thể dục thể thao thường
xuyên là một trong những yếu tố ngoại lai quan trọng nhất để đạt được mật độ xương và khối
lượng khoáng chất trong xương tối ưu.
Loãng xương (Osteroporosis) là bệnh lý xương toàn thân, với các đặc điểm sau: khối lượng
xương thấp, có sự thay đổi chất lượng siêu cấu trúc (ultrastructural quality) của xương, sự suy
giảm cấu trúc xương xốp, tăng độ xốp (porosity) ở xương vỏ, giảm độ dày xương vỏ, giảm chiều
rộng của xương, tăng nguy cơ gãy xương của người bệnh. Các dạng loãng xương nguyên phát là
các tình trạng di truyền hiếm gặp, trong khi đó, các dạng loãng xương thứ phát ngày càng phổ biến
do tình trạng trẻ em mắc bệnh mạn tính có thể sống lâu hơn. Cơ chế hoạt động của sinh lý của
bệnh loãng xương thứ phát là do chế độ dinh dưỡng nghèo nàn, ít hoạt động thể dục thể thao, dậy
thì trễ, ảnh hưởng của thuốc men lên cơ thể, dẫn đến ức chế sự hình thành của xương, tăng tiêu
xương, giảm khả năng đáp ứng kích thích cơ học của xương.
Tốc độ gia tăng khối lượng xương có xu hướng tỉ lệ thuận với việc phát triển chiều cao;
vào cuối thời kì dậy thì, con người đạt được 90% khối lượng xương đỉnh. Các bé gái bước vào thời
kì phát triển, biến đổi mạnh mẽ tuổi dậy thì sớm hơn các bé trai, song nam giới có thời kì phát
triển tuổi dậy thì lâu hơn và đạt đỉnh phát triển cao hơn nữ giới. Thất bại trong việc đạt khối lượng
xương đỉnh sẽ dẫn tới tăng nguy cơ loãng xương, gãy xương ở người trưởng thành. Dư hoặc thiếu
các hormone sinh trưởng, hormone tuyến giáp (thyroid hormone), hormone tuyến cận giáp
(parathyroid hormone), nội tiết tố sinh dục (sex steroids) cũng có thể dẫn đến giảm mật độ khoáng
chất của xương (mật độ xương – Bone mineral density – BMD).
Việc xác định và miêu tả loãng xương ở trẻ em là một thách thức, nguyên nhân là do trị số
mật độ xương (BMD) ở trẻ em luôn thay đổi theo độ tuổi, giới tính, kích thước cơ thể, thời kì dậy
thì, độ trưởng thành của khung xương, các hoạt động nội tiết tố (hormone action), kích thước
xương, và chủng tộc. Vấn đề trở nên phức tạp hơn, trong nhiều trường hợp bệnh nhi có BMD thấp
là kết quả (thứ phát) của nhiều bệnh trạng và bất thường khác nhau, ảnh hưởng đến chiều cao, cân
năng, phát triển tuổi dậy thì, và có mức ảnh hưởng khác nhau lên từng vùng của khung xương.
BMD ở trẻ em được đánh giá bằng chỉ số Z-score; trong đó quần thể tham chiếu có cùng chủng
tộc, giới tính, độ tuổi mẫu chuẩn, tuy nhiên thật không may là cơ sở dữ liệu vẫn còn bị hạn chế.
Chỉ số Z-score là sự khác biệt giữa trị số BMD đo được và trị số chuẩn (reference value), được thể
hiện qua độ lệch chuẩn (Standard Deviation – SD unit). Chỉ số Z-score không tính đến các biến số
được nêu trên (giới tính, kích thước cơ thể, giai đoạn dậy thì, sự trưởng thành của khung xương,
hoạt động nội tiết tố, kích thước xương, và chủng tộc), từ đó hình thành vấn đề về độ chính xác
của chẩn đoán, nguyên nhân là do việc giải nghĩa các chỉ số đo hàng loạt (serial measurements)
của một đứa trẻ là vô cùng khó khăn. Vì vậy, chẩn đoán bệnh loãng xương ở bệnh nhi không chỉ
duy nhất dựa vào việc đo mật độ xương. Chỉ số Z-score dưới -2 thường được cho là cảnh báo
nghiêm trọng đối với nguy cơ loãng xương, tuy nhiên các chuyên gia sẽ không đưa ra bất cứ chẩn
đoán nào tới khi xuất hiện ít nhất một tình trạng gãy xương do vấp ngã/ va chạm nhẹ (fragility
fracture). Cơn đau xương mạn tính và/hoặc các dấu hiệu xương loãng (rarefied bone) trên phim
X-quang làm dấy lên nghi ngờ về sự hiện diện của bệnh loãng xương. Thuật ngữ “Mật độ xương
thấp theo tuổi thời gian” (low bone mass for chronologic age) được sử dụng khi chỉ số Z-score
thấp hơn hoặc bằng -2; thuật ngữ “suy giảm mật độ xương” (osteopenia), không được sử dụng cho
hồ sơ bệnh xương ở trẻ em. Vì việc gãy xương do vấp ngã/ va chạm nhẹ (fragility fracture) là dấu
hiệu lâm sàng đặc trưng của bệnh lý loãng xương, tiêu điểm đánh giá bệnh đã được chuyển từ chỉ
số BMD thấp sang suy giảm độ cứng chắc của xương (compromised bone strength), nhấn mạnh
rằng nguy cơ gãy xương liên quan đến nhiều yếu tố phức tạp hơn chứ không chỉ dựa vào một chỉ
số đo lường định lượng. Một cách tiếp cận để xác định bệnh lý loãng xương ở trẻ em là dựa vào
mối quan hệ giữa chỉ số mật độ xương (BMD) hay chỉ số khối lượng xương (BMC- Bone Mineral
Content) của trẻ với khối lượng cơ, nguyên nhân là do các hoạt động cơ bắp tác động lên xương
sẽ tăng độ cứng chắc của xương. Chỉ số mật độ xương (BMD) tiếp tục được dùng làm thông số
chẩn đoán bệnh loãng xương ở trẻ em.
Hiện nay có nhiều phương pháp đo chỉ số BMD, trong đó phương pháp hấp thu tia X năng
lượng kép (Dual Energy X-ray Absorptiometry – DEXA) là công cụ cơ bản, và được ứng dụng
rộng rãi nhất cho việc chẩn đoán và kiểm soát bệnh lý loãng xương ở người trưởng thành. Phương
pháp DEXA cung cấp độ chính xác cao, độ tái lập (reproducibility) tốt, liều bức xạ thấp, song
phương pháp này không đo được thể tích mật độ xương (Volumetric bone density) cũng như không
phân biệt được xương vỏ hay xương xốp. Phương pháp DEXA có thể đưa ra kết quả sai khi dùng
trên chủ thể đang phát triển, nó có thể hạ thấp chỉ số mật độ thật của xương nhỏ, và nâng cao chỉ
số của xương lớn. Vì vậy, chỉ số thật của mật độ khoáng xương BMAD (Bone Mineral Apparent
Density) biểu hiện chính xác nhất mật độ xương trong quần thể nhi khoa, nhờ vào khả năng đưa
ra được kết quả thể tích mật độ xương; tuy nhiên, DEXA vẫn là phương pháp được ưa chuộng hơn
để đánh BMC (chỉ số khối lượng xương) và BMD (chỉ số mật độ xương) theo diện tích (areal).
Vùng trước/sau xương sống và vùng toàn thân trừ đầu (total body less head) là các khu vực tái
hiện phù hợp nhất cho việc đo mật độ xương (densitometry). Một số phương pháp khác để đo chỉ
số mật độ xương BMD gồm có: Chụp cắt lớp vi tính định lương (Quantitative Computerized
Tomography – QCT), siêu âm định lương (Quantitative ultrasound), và chụp cộng hưởng từ MRI
(Magnetic Resonance Imaging).
Hướng dẫn phòng ngừa (Anticipatory guidance- cho cha mẹ, người giám hộ để giúp trẻ
tránh các vấn đề sức khỏe, sự cố, tai nạn trong tương lai của trẻ) về lối sống lành mạnh, thường
xuyên tập thể dục thể thao, có chế độ ăn cân bằng, tránh sử dụng rượu bia, thuốc lá, thuốc cấm, là
rất quan trọng để phòng ngừa tiêu xương, cần được phổ cập vào thời kì đầu của trẻ. Đây là lĩnh
vực mà các chuyên gia nha khoa có thể tạo nên ảnh hưởng lớn tới sức khỏe người bệnh, và cần
được bàn đến trong tất cả các cuộc tái khám. Trong các trường hợp giảm BMD ít nghiêm trọng,
việc điều chỉnh chế độ dinh dưỡng kém, cung cấp thêm canxi và vitamin D, đi đôi với việc tập tạ
giúp ích tốt với nguy cơ rủi ro thấp. Tính chất, số lượng, và loại hình hoạt động thể dục thể thao
cần được điều chỉnh phù hợp với giới tính, lứa tuổi, và tình trạng sức khỏe của bệnh nhân; lý do là
vì nếu hoạt động quá sức sẽ đem lại ảnh hưởng xấu cho xương. Một ví dụ cụ thể là rối loạn biếng
ăn tâm lý (chán ăn tâm thần – anorexia nervosa). Vitamin D ở mức thấp có thể gây tăng giải phóng
nội tiết tố tuyến cận giáp (parathyroid hormone), dẫn đến việc kích thích hủy cốt bào tái hấp thu
xương. Tiêu thụ nước uống có gas gây ảnh hưởng tiêu cực đến việc tích lũy khoáng của xương ở
lứa tuổi dậy thì (ảnh hưởng các bé gái nhiều hơn các bé trai). Bệnh chậm phát triển, dậy thì chậm,
suy tuyến sinh dục (hypogonadism) cần được chữa trị bằng liệu pháp nội tiết tố (hormonal therapy).
Các chất chống tiêu xương (Anti-resorptive agents) như là bisphosphonates, làm chậm quá trình
tái hấp thu xương, trong khi đó quá trình tạo xương vẫn tiếp diễn bình thường. Thuốc chống tiêu
xương chỉ được dùng cho bệnh nhi có chỉ số Z-score thấp hơn -2, đặc biệt là khi các tình trạng gãy
xương xảy ra sau chấn thương nhẹ (tối thiểu), và các biện pháp dự phòng (ví dụ như chế độ ăn, thể
dục thể thao) thất bại trong việc đảo ngược sự tiêu xương. Thuốc bám chặt vào tinh thể
hydroxyapatite, làm giảm sự tái hấp thu xương bằng việc ức chế hoạt động chức năng tế bào và
đẩy nhanh cái chết của hủy cốt bào, đặc biệt là ở xương xốp và xương có tỉ lệ thay mới cao (high
turnover rate). Mặc dù cần có thêm nhiều nghiên cứu đánh giá độ an toàn và hiệu quả của thuốc
trên bệnh nhi, ứng dụng lâm sàng của thuốc ngày càng được chấp nhận, phổ biến rộng. Chưa có
sự nhất trí về liều lượng, thời gian trị liệu cũng như loại chất bisphosphonate nào tối ưu nhất trong
việc điều trị cho bệnh nhi. Các tác dụng phụ nghiêm trọng ở người lớn như viêm màng bồ đào
(uveitis), chứng giảm tiểu cầu (thrombocytopenia), lở loét miệng và thực quản hiếm xảy ra ở trẻ
em. Đến thời điểm hiện tại, các bằng chứng khoa học không ủng hộ việc sử dụng bisphosphonates
như là liệu pháp tiêu chuẩn để điều trị loãng xương thứ phát ở bệnh nhi.
Các lưu ý trong điều trị răng miệng (cho bệnh nhân loãng xương):
Bệnh nhi được chẩn đoán có chỉ số BMD thấp và loãng xương, được điều trị đang gia tăng,
bằng các thuốc đòi hỏi phải có sự lưu ý đặc biệt (special care) khi điều trị chăm sóc răng miệng.
Các chuyên gia nha khoa phải kỹ lưỡng, tỉ mỉ trong việc thu thập tiền sử bệnh của trẻ em và trẻ vị
thành niên có nhu cầu chăm sóc y tế đặc biệt; nguyên nhân là do nhiều trường hợp có tiền sử loãng
xương và có chỉ số BMD thấp. Các thông tin quan trọng cần thu thập là:
1. Chỉ số BMD thấp như thế nào? Việc chuyển bệnh nhi từ xe lăn lên ghế nha, tác động
vật lí để giữ trẻ yên một chỗ (physical restraint), và việc nhổ răng (đặc biệt là răng vĩnh
viễn) có thể gây gãy xương nếu không được tiến hành cẩn thận.
2. Nguyên nhân của chỉ số BMD thấp hay bệnh lý loãng xương là gì?
3. Điều trị nào sẽ được thực hiện đối với tình trạng xương người bệnh để đề phòng các
vấn đề, trở ngại như hoại tử xương hàm liên quan đến bisphosphonate (Bisphosphonate-
Related OsteoNecrosis of the Jaws – BRONJ)? Việc sử dụng bisphosphonate có thể là
mỗi tuần, mỗi tháng nên bệnh nhân và người chăm sóc không nhớ được họ có dùng
hay không nếu không được hỏi rõ. Đặt thêm câu hỏi cụ thể về việc sử dụng thuốc vào
tờ khai tiền sử bệnh và nhận thức được tiềm năng gây nên biến chứng miệng dài hạn
của thuốc là việc làm quan trọng (Vì thời gian bán đào thải của thuốc là nhiều năm).
Việc giáo dục cho bệnh nhi và người chăm sóc về tầm quan trọng của sức khỏe răng miệng, các
tác dụng phụ dài hạn của thuốc khi điều trị nha khoa xâm lấn là điều cần thiết. Các tác nhân tiềm
năng gây nhiễm trùng niêm mạc và nhiễm trùng do răng cần được loại bỏ trước khi bệnh nhân bắt
đầu điều trị thuốc bisphosphonate. Việc tránh các điều trị phẫu thuật miệng, đặc biệt đối với bệnh
nhân được truyền tĩnh mạch (IV) bisphosphonates (BIS), là vô cùng quan trọng để giảm nguy cơ
BRONJ (hoại tử xương hàm liên quan đến bisphosphonate). Nguy cơ BRONJ ở những bệnh nhân
dùng bisphosphonate đường miệng giảm đáng kể so với những người truyền tĩnh mạch (IV) BIS.
Chưa có đủ bằng chứng khoa học đề nghị người bệnh sử dụng BIS đường miệng tránh tiếp nhận
thường xuyên các điều trị phẫu thuật như cấy ghép implant, nhổ răng, v.v., mặc dù thời gian điều
trị BIS đường miệng (nhiều hơn 3 năm) có liên quan đến sự phát triển và mức độ nghiêm trọng
của BRONJ. Nhiều người suy đoán rằng việc nhổ răng sữa không gây ra nguy cơ phát triển
BRONJ, với lý do là vết thương nhỏ, xương hàm của người trẻ xốp hơn và có nhiều mạch máu
hơn người trưởng thành. Một lý do khác là do bệnh nhi dùng liều BIS thấp hơn người trưởng thành.
Các nghiên cứu khoa học được công bố nói về việc BRONJ không tồn tại ở bệnh nhi có nhiều sai
sót trong quá trình thiết kế thí nghiệm (ví dụ: số lượng bệnh nhân ít, không có sự ngẫu nhiên, thời
gian theo dõi ngắn, thuốc và liều lượng được dùng khác nhau), các sai sót này phải được xem xét
khi diễn giải các kết quả. Tuy nhiên, số lượng thanh thiếu niên được điều trị nhổ răng để chỉnh
nha, nhổ răng mọc kẹt, răng khôn, phẫu thuật nha chu, lấy mô sinh thiết ngày càng nhiều khiến
cho nguy cơ BRONJ có thể gia tăng. Trước khi tiến hành có qui trình điều trị xâm lấn đối với quần
thể này, nha sĩ nhi khoa cần phải hội chẩn với bác sĩ điều trị (BIS) và thu được giấy chấp nhận có
hiểu biết (informed consent/ ~ giấy cam đoan chấp nhận phẫu thuật, thủ thuật và gây mê hồi sức)
chi tiết và nêu rõ các khả năng biến chứng từ người chăm sóc bệnh nhân. Sinh lý bệnh, chẩn đoán
và điều trị cho BRONJ đã được mô tả chi tiết nhiều nơi.
Bisphosphonate có thể cản trở sự di chuyển của răng, gây khó khăn cho việc điều trị chỉnh
hình răng mặt (dựa vào hoạt động của hủy cốt bào để di chuyển răng). Bệnh nhân có nguy cơ/mức
độ cao về ức chế hoạt động của hủy cốt bào ví dụ như các bệnh nhân đã/đang truyền BIS tĩnh mạch
được đề nghị tránh tiến hành điều trị chỉnh hình răng mặt. Thuốc bisphosphonate cũng có liên quan
đến quá trình chậm mọc răng ở bệnh nhi mắc chứng xương thủy tinh (Osteogenesis imperfecta –
OI).
Rối loạn phổ rượu ở thai nhi (Fetal Alcohol Spectrum Disorders – FASDs):
Rối loạn phổ rượu ở thai nhi (FASD) là thuật ngữ chung (umbrella term) không chẩn đoán,
bao gồm một phổ lớn các bất thường cấu trúc (structural anomalies), và các khuyết tật về hành vi,
nhận thức; FASD là hậu quả của việc phơi nhiễm rượu (alcohol) ở thai nhi đang phát triển. Hội
chứng rượu bào thai (Fetal Alcohol Syndrome- FAS) là dạng nặng nhất của Rối loạn phổ rượu ở
thai nhi (FASD) trong các hậu quả gây dị tật bẩm sinh, quái thai của rượu. Tiêu chuẩn chẩn đoán
bao gồm tiền sử tiêu thụ rượu bia của người mẹ, cùng với một số thành phần nằm trong cả ba phạm
trù sau đây: dị dạng sọ mặt (craniofacial dysmorphism), chậm phát triển (growth retardation) ở
thời kì trước (prenatal) và sau khi sinh (postnatal), rối loạn chức năng hệ thần kinh trung ương
(Central Nervous System – CNS dysfunction) (ví dụ như: thiểu năng trí tuệ, khuyết tật học tập, rối
loạn khó khăn làm chủ hành vi). Viện Hàn Lâm Nhi Khoa Hoa Kì (The American Academy of
Pediatrics) khuyến cáo phụ nữ cai rượu khi đang mang thai hoặc có dự định mang thai, nguyên
nhân là do tiêu thụ rượu bia dù ít hay nhiều cũng có hại khi mang thai. Nguy cơ suy giảm chức
năng (functional impairment) ở người con tăng từ 2-5 lần khi có bà mẹ uống ít nhất 5 li mỗi dịp, 1
tuần 1 lần, có độ tuổi 30 trở lên.
Hội chứng rượu bào thai là nguyên nhân hàng đầu dẫn đến thiểu năng trí tuệ ở Mỹ. Các
đứa trẻ bị bệnh thường đến từ các gia đình bất ổn, và biểu hiện ra các khó khăn về tâm lý xã hội
và có vấn đề về điều chỉnh tâm lý hành vi cả đời. Khả năng học tập (school functioning) bị suy
giảm, đặc biệt là sự thiếu hụt về suy luận toán học (arithmetic), điều này được thể hiện qua việc
bệnh nhân gặp trở ngại lớn về sự trù tượng, ví dụ như thời gian và không gian, mối quan hệ nhân
quả. Người bệnh cũng gặp khó khăn trong việc quan sát, học tập rút kinh nghiệm từ tình huống
này để ứng dụng xử lý tình huống khác. Điều này có vẻ là cản trở lớn nhất trong việc sống tự lập
của bệnh nhân, kỹ năng phán đoán kém, và rối loạn chức năng toàn diện (general dysfunction).
Biểu hiện lâm sàng ở sọ mặt và các lưu ý trong điều trị nha khoa:
Các đặc điểm thường gặp của FAS (Hội chứng rượu bào thai) gồm có tật mắt nhỏ
(microphthalmia), khe mi ngắn, nhân trung kém phát triển, bờ đỏ son (vermilion border) mỏng,
dẹt mặt (flattening of the maxillary area).
Triệu chứng đặc trưng (Discriminating features):
- Khe mi ngắn
- Mặt giữa phẳng
- Mũi ngắn
- Nhân trung không rõ ràng (kém phát triển)
- Môi trên mỏng
Triệu chứng liên quan (Associated features):
- Sóng mũi ngắn
- Nếp mí rẻ quạt (Epicanthal fold)
- Dị tật tai nhỏ
- Cằm nhỏ (Micrognathia)
Người mắc FAS (Hội chứng rượu bào thai) có thể được phân biệt từ nhóm mẫu chính xác
100% chỉ bằng hai số đo sọ mặt: Chu vi vòng đầu (Head circumference) và bề ngang hai điểm
gonia (hai điểm góc hàm – bigonial breadth). Chụp hình mặt kỹ thuật số (Digital facial
imaging) được ứng dụng ngày càng nhiều để mô tả (delineation) hội chứng. Trẻ em mắc FAS
còn có thể biểu hiện sứt môi cô lập (isolated cleft lip) có hoặc không có hở hàm ếch (cleft
palate). Tạng người thấp, tật đầu nhỏ (microcephaly) là khiếm khuyết tăng trưởng (growth
deficiency) nổi bất nhất khi trẻ lớn lên. Tuy nhiên, các thay đổi về kiểu hình (phenotype) vật
lý, cũng như khuôn mặt trở về trạng thái bình thường trong giai đoạn dậy thì, do nhân trung
phát triển, mũi và cằm tăng trưởng. Đến thời điểm này, vẫn chưa có dữ liệu nào bàn luận về tỉ
lệ sâu răng ở quần thể này. Trở ngại lớn nhất trong việc điều trị cho bệnh nhi mắc hội chứng
rượu bào thai (FAS) tại phòng mạch là kiểm soát hành vi của bệnh nhi.
Ung thư trong nhi khoa (Pediatric cancer):
Ung thư là nguyên nhân tử vong phổ biến thứ nhì ở trẻ em tại Mỹ, đứng sau tai nạn. Tỷ lệ
mắc bệnh ung thư thời thơ ấu đỉnh điểm là trong năm đầu đời, với đỉnh chóp thứ nhì là vào
năm 2-3 tuổi. Tỷ lệ ung thư thời thơ ấu ở Mỹ vẫn không thay đổi, hằng năm có khoảng 7300
trẻ em từ độ tuổi 0-14 tuổi được chẩn đoán mắc bệnh ung thư. Các bệnh ung thư bạch cầu cấp
tính (leukemia), ung thư hạch bạch huyết/u lympho (lymphoma), u não, u phần mềm (soft
tissue tumor), u thận là các khối u ác tính thường gặp ở trẻ em. Việc chẩn đoán sớm và các tiến
bộ y khoa đã góp phần cải thiện kết quả điều trị, tăng tỉ lệ sống sót của người bệnh. Tuy nhiên,
đi cùng sự tiến triển này là sự gia tăng của các tác dụng phụ không mong muốn do các chiến
lược điều trị ung thư xâm lấn mạnh hơn được sử dụng.
Phương pháp điều trị đa mô thức (multimodal treatment approach) ứng dụng phẫu thuật và
xạ trị (radiotherapy) để kiểm soát bệnh khu trú, hóa trị (chemotherapy) được dùng để loại bỏ
bệnh toàn thân. Hóa trị can thiệp quá trình tổng hợp hoặc chức năng của các nucleic acid quan
trọng trong tất cả tế bào, trong khi đó, xạ trị gây tổn thương DNA ở các tế bào ung thư, hạn
chế gây hại tối thiểu đến các tế bào liền kề (quan trọng trong bệnh nhi). Các tế bào sinh sôi
nhanh chóng nhạy cảm hơn, chết nhanh hơn khi xạ trị so với các tế bệnh phân chia bình thường,
cũng như với các tế bào không phân chia vô cảm với xạ trị. Việc xạ trị được tiến hành trong
nhiều tuần trong các khoảng thời gian bằng nhau, các giai đoạn (khoảng thời gian) thường cách
nhau 24 giờ để hỗ trợ cho việc sửa chữa ở các tế bào khỏe mạnh, và tăng ảnh hưởng đến các
tế bào ung thư. Mặc dù sự tiến bộ trong hóa trị và xạ trị ion hóa (ionizing radation) đã giúp
giảm bớt bức xạ cũng như các thủ thuật phẫu thuật cắt xén, việc phẫu thuật vẫn có thể cần thiết
cho việc điều trị khối u ở gian đoạn đầu, lấy sinh thiết, cắt bỏ u, phẫu thuật kiểm tra theo dõi
khối lần thứ 2, lần thứ 3 (second/third looks). Liệu pháp miễn dịch (Immunotherapy) dùng tế
bào bạch cầu, kháng thể đơn dòng (monoclonal antibody), và cytokine cho việc phá hủy khối
u; chúng có độ đặc hiệu cho tế bào ung thư, có thể giúp bảo vệ bệnh nhân khỏi các tác dụng
phụ thường gặp khi điều trị với các liệu pháp thông thường. Bệnh bạch cầu nguyên bào lympho
cấp tính (Acute Lymphoid Leukemia – ALL) chiếm 75% các ca bệnh bạch cầu leukemia ở trẻ
em, với tỷ lệ mắc bệnh cao nhất ở độ 4 tuổi, tỷ lệ chữa khỏi hoàn toàn là 90%. Các dấu hiệu
và triệu chứng thường gặp nhất là: chứng biếng ăn (anorexia), bức rức, khó chịu, ngủ lịm, uể
oải (lethargy), thiếu máu, chảy máu, chấm xuất huyệt (petechiae), sốt, phì đại hạch bạch huyết,
cường lách (splenomegaly), phì đại gan (hepatomegaly). Đau xương khớp có thể do các nguyên
nhân như sự thâm nhiễm của tế bào bạch cầu vào xương màng sụn, khớp xương, cũng có thể
là do bạch cầu leukeamia lan rộng (leukemic expansion) trong khoang tủy xương, khiến bệnh
nhi đi khập khiễng hoặc từ chối đi lại. Các biểu hiện ở đầu và cổ, trong miệng phổ biến nhất
của ALL (Bệnh bạch cầu nguyên bào lympho cấp tính) tại thời điểm chẩn đoán là phì đại hạch
bạch huyết, đau họng, đau thanh quản, chảy máu nướu, lở loét miệng. Bệnh nhân tái phát được
điều trị bằng hóa trị tích cực, và điều trị nối tiếp bằng liệu pháp ghép tế bào gốc tạo máu
(Hematopoietic Stem Cell Transplantation – HSCT). Việc kiểm soát, điều trị bệnh ALL được
dựa vào nguy cơ lâm sàng, và thường được chia thành 4 giai đoạn:
1. Pha dẫn nhập để đẩy lui bệnh (Remission induction): Thường kéo dài 28 ngày, điều trị
bằng 3-4 loại thuốc (ví dụ: vincristine, prednisone, và L-asparaginase), có tỉ lệ thành
công đạt 95%. Việc đẩy lui bệnh là điều kiện tiên quyết (prerequisite) cho việc kéo dài
sự sống.
2. Liệu pháp cho dự phòng thâm nhiễm thần kinh trung ương (CNS preventive
therapy/prophylaxis): Hệ thần kinh trung ương có thể trở thành nơi trú ẩn cho các tế
bào bạch cầu thâm nhiễm leukemia (leukemic infiltrates), điều này là do thuốc sử dụng
trong liệu pháp hóa trị thông thường không thể vượt qua hàng rào máu não (BBB –
Blood-Brain Barrier). Việc chiếu xạ sọ não, hoặc tiêm tủy sống (intrathecal injection)
bằng thuốc hóa trị hàng tuần (thường là methotrexate), có thể được sử dụng. Việc điều
trị trước khi xuất hiện triệu chứng có thể được tiến hành ở mỗi giai đoạn.
3. Pha tăng cường hoặc củng cố (Consolidation or Intensification): Nhằm mục đích giảm
thiểu sự phát triển của đề kháng thuốc chéo (drug cross-resistance) bằng cách tăng
cường điều trị tích cực với mục đích tiêu diệt toàn bộ các tế bào leukemia còn sót lại.
4. Liệu pháp duy trì kéo dài (Maintenance): Hướng tới việc ức chế sự phát triển của bệnh
ung thư máu leukemia thông qua việc tiếp tục sử dụng methotrexate và 6-
mercaptopurine. Thời gian tối ưu cho giai đoạn này vẫn chưa được xác định chính xác,
nhưng hường kéo dài từ 2.5-3 năm.
Số lượng tế bào máu của bệnh nhân thường bắt đầu giảm sau 5-7 ngày kể từ khi bắt đầu
mỗi chu kỳ điệu trị, chúng giữ ở mức thấp trong khoảng 14-21 ngày, sau đó tăng lên trở lại.
Các lưu ý khi chăm sóc răng miệng (Cho bệnh nhân ung thư):
Việc điều trị bằng hóa trị và/hoặc xạ trị gây ra nhiều biến chứng cấp tính và dài hạn cho
khoang miệng. Nhiễm trùng răng miệng có thể làm phức tạp hóa và trì hoãn quá trình điều trị ung
thư, dẫn đến tình trạng bệnh tật và dẫn đến chất lượng cuộc sống kém cho trẻ. Các biến chứng
khoang miệng cấp tính thường xuyên xảy ra ở trẻ em. Can thiệp nha khoa sớm và tích cực sẽ giảm
thiểu các vấn đề rủi ro biến chứng trong miệng, cũng như các biến chứng toàn thân. Các chấn
thương liên quan đến chức năng miệng, và làm tổn thương niêm mạc, như trong trường hợp nhiễm
herpes, tăng nguy cơ chảy máu ở người bệnh. Do đó, việc thăm khám nha khoa cần được thực hiện
ít nhất một lần cho bệnh nhân mới được chẩn đoán (ung thư) để hoàn thành quá trình điều trị, chăm
sóc răng miệng trước khi bắt đầu quá trình điều trị ung thư. Mỗi bệnh nhân đều được điều trị theo
nhu cầu cá nhân, và có được ý kiến tư vấn từ bác sĩ và các chuyên gia nha khoa khác trước khi tiến
hành chăm sóc nha khoa.
Các biến chứng răng miệng và sọ mặt trong điều trị ung thư:
Các biến chứng cấp tính từ việc điều trị bằng hóa trị và xạ trị:
Viêm niêm mạc (Mucositis)
Bệnh lý rối loạn chức năng tuyến nước bọt (Salivary gland dysfunction)
Viêm tuyến nước bọt (chỉ có ở xạ trị - Sialadenitis)
Tình trạng khô miệng (Xerostomia)
Nhiễm độc thần kinh (Neurotoxicity)
Rối loạn vị giác (Taste dysfunction)
Quá cảm ngà (Dentinal hypersensitivity)
Rối loạn khớp thái dương hàm (TemporoMandibular Dysfunction – TMD)
Chảy máu miệng (oral bleeding_
Nhiễm trùng cơ hội (ví dụ: virus, nấm, vi khuẩn)
Các biến chứng dài hạn trong việc điều trị bằng chiếu xạ vùng mặt:
Niêm mạc xơ hóa và teo nhỏ (Mucosal fibrosis and atrophy)
Tình trạng khô miệng
Sâu răng
Hoại tử xương sau xạ trị
Rối loạn vị giác
Sẹo niêm mạc (Mucosal fibrosis)
Xơ hóa cơ/da (Muscular/cutaneous fibrosis)
Nhiễm trùng nấm và vi khuẩn
Các vấn đề cản trở sự phát triển của răng và sọ mặt (Dental and craniofacial development
problems) (cũng được tìm thấy trong việc điều trị bằng hóa trị)
Tiền sử bệnh và tình trạng huyết học của bệnh nhân:
Một đánh giá kỹ lưỡng cần bao gồm thông tin về bệnh nền (underlying diseases), thời điểm
chẩn đoán, các phương pháp điều trị bệnh nhân đã trải qua kể từ lúc chẩn đoán (hóa trị, xạ trị, phẫu
thuật, v.v.), các biến chứng, bao gồm cả các lần tái phát. Việc ghi chú các lần nhập viện, nhập
phòng cấp cứu, nhiễm trùng (cả trong miệng và toàn thân), hiện trạng huyết học, dị ứng, các loại
thuốc đang sử dụng, và bảng đánh giá các hệ thống cơ quan (tim, phổi, thận, v.v.) là quan trọng.
Đa số các bệnh nhân sẽ được đặt ống thông tĩnh mạch trung tâm (central line catheter) vào
tâm nhĩ phải của tim, ống thông này hỗ trợ cho việc lấy mẫu máu cũng như truyền các chất hóa trị
để chữa bệnh. Ống thông trung tâm có thể được đặt một phần (ví dụ: catheter Broviac, Hickman)
hoặc đặt dưới da (ví dụ: Mediport, BardPort, Port-a-Cath). Chưa có bằng chứng khoa học nào ủng
hộ việc sử dụng kháng sinh dự phòng trước khi tiến hành điều trị nha khoa xâm lấn cho các bệnh
nhân được đặt ống thông trung tâm.
Chảy máu lâu cầm ở bệnh nhi ung thư có thể là do các nguyên nhân sau: suy tủy do hóa trị
(Chemotherapy-induced myelosuppression), một số loại thuốc đang sử dụng, và các rối loạn đông
máu và tiểu cầu liên quan đến các bệnh nền (baseline disease). Chảy máu có ý nghĩa lâm sàng
thường khó xảy ra khi lượng tiểu cầu (PLT count) lớn hơn 20,000/mm3 trong trường hợp không
có các yếu tố phức tạp (complicating factors). Các thủ thuật nha khoa có thể được thực hiện khi số
lượng tiểu cầu lớn hơn 40,000/mm3, và có sự lưu ý đặc biệt đến biện pháp kiểm soát chảy máu lâu
cầm. Các xét nghiệm đông máu khác có thể được thực thiện cho bệnh nhân có bệnh lý gan và rối
loạn đông máu (liver involvement and coagulopathies).
Tế bào bạch cầu trung tính (neutrophil) là hàng rào phòng ngự đầu tiên (first line of defense)
của cơ thể; vì vậy tỷ lệ và mức độ nghiêm trọng của nhiễm trùng tỷ lệ nghịch với số lượng của
chúng. Khi số lượng bạch cầu trung tính tuyệt đối (Absolute Neutrophil Count – ANC) dưới
1000/mm3, các điều trị nha khoa tự chọn (elective dental work) cần được hoãn lại vì nguy cơ nhiễm
trùng tăng lên đáng kể. Tuy nhiên, một số bác sĩ điều trị ung thư cho phép thực hiện điều trị nha
khoa xâm lấn tự chọn nếu chỉ số ANC trên 500/mm3.
Vệ sinh răng miệng, chế độ ăn, và phòng ngừa sâu răng:
Bất kể tình trạng huyết học của bệnh nhi, duy trì vệ sinh răng mặt tích cực trong suốt quá
trình điều trị ung thư là việc làm quan trọng để giảm thiểu các biến chứng răng miệng. Suy giảm
tiểu cầu không là yếu tố quyết định duy nhất cho việc duy trì vệ sinh răng miệng, bệnh nhân có thể
đánh răng mà không lo chảy máu ở các mức độ tiểu cầu khác nhau. Khoa học chứng minh rằng,
bệnh nhân chăm sóc răng miệng tích cực sẽ giảm thiểu nguy cơ phát triển bệnh lý viêm niêm mạc
trung bình/nặng, mà không làm tăng nguy cơ nhiễm trùng máu hay nhiễm trùng khoang miệng.
Chải răng bàng bàn chải thông thường lông mềm hay bản chải điện ít nhất hai lần mỗi ngày là
phương pháp hiệu quả nhất trong việc giảm thiểu nguy cơ nhiễm trùng và chảy máu nhiều ở nướu.
Miếng bọt biển vệ sinh răng miệng (sponge), bàn chải siêu mềm không thể giúp làm sạch cơ học
hiệu quả do độ mềm của chúng; vì vậy chúng chỉ được sử dụng trong trường hợp viêm niêm mạc
nặng, khi bệnh nhân không chịu được bàn chải thông thường. Bàn chải cần được phơi khô trong
không khí giữa có lần sử dụng, kem đánh răng không chứa nhiều các chất tạo mùi vì các chất này
có thể gây kích thích mô. Người bệnh trong tình trạng suy giảm bạch cầu trung tính,cần tránh việc
sử dụng tăm xỉa răng hay tăm nước, vì chúng có thể phá vỡ các liên kết mô, tạo thành các lối xâm
nhập cho vi sinh vật và gây chảy máu. Bàn chải điện ultrasonic (siêu âm) và chỉ nha khoa có thể
được sử dụng đối với bệnh nhân đã được hướng dẫn đúng cách. Người bệnh có vệ sinh răng miệng
kém, bệnh lý nha chu cần phải súc miệng chlorhexidine mỗi ngày cho đến khi sức khỏe nướu được
phục hồi hoặc cho đến khi xuất hiện các dấu hiện đầu tiên của bệnh lý viêm niêm mạc. Tại thời
điểm đó, cần tránh sử dụng nước súc miệng chứa cồn (alcohol) và các chất tạo mùi hương, nguyên
nhân là do các chất này có thể làm khô và kích thích niêm mạc. Nhiễm trùng nha chu là một mối
lo ngại lớn vì các sinh vật xâm chiếm có thể gây ra nhiễm khuẩn huyết (bacteremia).
Chế độ ăn uống là nguyên nhân khiến cho bệnh nhi ung thư có nguy cơ sâu răng cao hơn
trẻ khỏe mạnh. Ngoài ra, nhiều thuốc điều trị răng miệng cho trẻ em chứa sucrose lượng lớn; do
đó, chúng nên được sử dụng một cách hiểu quả để giảm thiểu nguy cơ sâu răng. Ví dụ, trẻ em
không được phép ngậm thuốc viên clotrimazole hay dung dịch nystatin chứa đường khi đi ngủ.
Mặc dù thường được kê toa, nhưng nystatin không có hiệu quả phòng ngừa nhiễm nấm Candida ở
bệnh nhân bị suy giảm miễn dịch, và không nên được khuyến cáo sử dụng. Nôn mửa là một tác
dụng phụ thường thấy khi điều trị ung thư, do đó, bệnh nhân cần súc miệng sau các đợt nôn mửa
bằng nước vòi hoặc nước trắng để loại bỏ acid dạ dày, acid này có thể gây kích thích mô miệng và
mất khoáng hóa ở men răng. Việc cung cấp fluoride và việc sử dụng fluoride dạng nước súc miệng
trung hòa hay dạng gel được chỉ định cho bệnh nhân có nguy cơ mắc bệnh sâu răng.
Các lưu ý trong điều trị răng miệng (cho bệnh nhân ung thư):
Bệnh nhân cần được xem xét, đánh giá tiền sử nha khoa, tiến hành kiểm tra, thăm khám kỹ
lưỡng vùng đầu, mặt, cổ, mô mềm và mô cứng trong miệng, đồng thời bổ sung chụp phim x-quang
khi được chỉ định. Một số bệnh nhân có thể phàn nàn về tình trạng dị cảm do các tế bào bạch cầu
ung thư leukemia thâm nhiễm vào dây thần kinh ngoại biên. Một số khác có thể than phiền về cơn
đau răng giống với đặc trưng của viêm tủy không hồi phục mà không bất kì nhiễm trùng răng/nha
chu. Đây có thể là tác dụng phụ của thuốc vincristine và vinblastine (hai loại thuốc hóa trị được sử
dụng phổ biến). Trong trường hợp này, người bệnh nên tránh những tình huống làm cảm giác
không thoải mái (ví dụ: đồ ngọt, đá, v.v.), và sử dụng thuốc giảm đau theo toa để kiếm soát cơn
đau. Cơn đau thường sẽ chấm dứt sau vài ngày hoặc vài tuần sau khi ngưng liệu pháp hóa trị gây
đau. Bệnh nhân cũng có thể phàn nàn về tình trạng răng nhạy cảm. Cơ chế của nhạy cảm răng vẫn
chưa được hiểu rõ, và có thể được kiểm soát bằng fluoride tại chỗ hoặc kem đánh răng ngăn ngừa
ê buốt.
Số lượng tế bào máu của bệnh nhân trở về mức bình thường giữa các chu kì hóa trị. Vì thời
gian dành cho việc chăm sóc nha khoa trước khi bắt đầu điều trị ung thư có hạn, nên việc điều trị
các nhiễm trùng, nhổ răng, điều trị nha chu, và các tác nhân gây kích thích cần được ưu tiên hơn
so với việc điều trị răng sâu, chữa tủy cho răng vĩnh viễn, và thay thế các phục hình cũ, bị lỗi.
Nguy cơ nhiễm trùng tủy răng, gây đau sẽ quyết định tổn thương sâu răng nào cần được điều trị
trước, nguyên nhân là do nhiễm trùng tủy răng ở bệnh nhân ức chế miễn dịch có thể dẫn đến tình
huống nguy kịch, đe dọa đến tính mạng. Phục hình tạm thời có thể được đặt vào, các điều trị nha
khoa không cấp tính có thể được trì hoãn đến khi sức khỏe bệnh nhân ổn định trở lại. Cần xem xét
việc truyền tiểu cầu trước phẫu thuật và 24 giờ sau phẫu thuật khi lượng tiểu cầu nằm trong mức
40,000-75,000/mm3. Khi lượng tiểu cầu dưới mức 40,000/mm3, việc điều trị chăm sóc nha khoa
cần được hoãn lại. Trong giai đoạn ức chế miễn dịch, mọi qui trình điều trị nha khoa tự chọn cần
được bãi bỏ. Trong trường hợp khẩn cấp, phải liên với bác sĩ trước khi tiến hành bất kỳ điều trị
nha khoa nào, nguyên nhân là do việc truyền tiểu cầu, và kháng sinh dự phòng là không đủ để
phòng ngừa bệnh viêm nội tâm mạc (endorcarditis), việc nhập viện có thể là cần thiết để tiến hành
điều trị nha khoa.
Trong thời gian trước khi bắt đầu điều trị ung thư, cần tiến thành cạo vôi răng và thực hiện
các điều trị dự phòng, sửa và làm mới các phục hình cũ bị lỗi, đánh bóng, loại bỏ các cạnh sắc
nhọn của răng. Cho đến thời điểm hiện tại, mặc dù vẫn chưa có một nghiên cứu nào đánh giá độ
an toàn của việc điều trị nội nha răng sữa trước khi bắt đầu tiến hành hóa trị và/hay xạ trị, chọn
nhổ răng làm điều trị triệt để giảm thiểu các nguy cơ biến chứng về răng miệng và toàn thân do
chữa tủy thất bại trong giai đoạn ức chế miễn dịch, là một quyết định sáng suốt; sự lựa chọn này
có ảnh hưởng đáng kể đến quá trình điều trị ung thư. Các răng đã được điều trị nội nha và có dấu
hiệu lâm sàng, hình ảnh x-quang lành mạnh không gây nguy hiểm. Các răng vĩnh viễn chết tủy
biểu hiện triệu chứng cần được điều trị nội nha ít nhất 1 tuần trước khi bắt đầu trị liệu ung thư.
Nếu không thể chữa tủy, răng được chỉ định nhổ và điều trị kháng sinh theo dõi trong khoảng 1
tuần. Điều trị nội nha cho răng vĩnh viễn có vẫn đề quanh chóp răng không triệu chứng có thể được
trì hoãn nếu bệnh nhân bị suy giảm bạch cầu trung tính. Trong giai đoạn ức chế miễn dịch, việc
sưng và chảy mủ không hiện diện, làm che đi các dấu hiệu kinh điển của nhiễm trùng do răng,
khiến chúng không được phát hiện trên lâm sàng. Trong trường hợp này, chụp phim x-quang là
việc làm quan trọng để đánh giá tình trạng bệnh lý quanh chóp/giữa chẻ răng.
Khí cụ chỉnh nha cố định và hàm giữ khoảng (space maintainer) cần được tháo bỏ đối với
bệnh nhân có vệ sinh răng miệng kém, hoặc là khi qui trình điều trị có nguy cơ gây viêm niêm mạc
trung bình đến nặng. Biện pháp phòng ngừa này không áp dụng cho các khí cụ có bề mặt phẳng,
lắng ví dụ như là khâu chỉnh nha (band), dây cung và thanh duy trì mặt lưỡi hàm dưới cố định
(fixed lower lingual arch). Các khí cụ có thể giữ lại các mảnh thức ăn, gây hại cho vệ sinh miệng,
vừa đóng vai trò là một kích thích cơ học, làm tăng nguy cơ nhiễm trùng thứ phát. Khí cụ và hàm
duy trì tháo lắp (Removable appliances and retainers) vừa vặn, khít tốt có thể được đeo sử dụng
nếu bệnh nhân chấp nhận được và duy trì vệ sinh răng miệng tốt. Nếu việc tháo band chỉnh nha là
bắt khả thi, thì có thể sử dụng máng bảo vệ miệng (mouth guard) hoặc sáp chỉnh nha để giảm các
chấn thương mô miệng.
Nướu che phủ một phần răng (các răng hàm mọc thấp/bán phần) có thể trở thành nguồn
nhiễm trùng do tiến triển thành bệnh lý viêm lợi trùm (periocoronitis – viêm quanh thân răng), vì
vậy phần nướu che phủ cần được cắt lọc nếu nha sĩ xem đó là một nguy cơ tiềm tàng. Răng sữa
lung lay cần được để rụng tự nhiên, và để phòng ngừa nhiễm khuẩn máu, bệnh nhi được dặn dò là
không chơi đùa với chúng. Nếu bệnh nhi không tuân thủ yêu cầu này, răng sữa lung lay cần được
nhổ bỏ. Răng mọc kẹt, mảnh chân răng, răng khôn bị nướu lấp một phần, răng có túi nha chu trên
6 mm, răng có nhiễm trùng cấp, răng không thể khôi phục cần được nhổ bỏ ít nhất từ 4 đến 7 ngày
(lý tưởng là 2 tuần) để có đủ thời gian lành thương, trước khi bắt đầu liệu trình điều trị ung thư.
Nếu như răng vĩnh viễn không thể nhổ bỏ vì lý do sức khỏe y khoa tại thời điểm đó, nha sĩ nhi
khoa có thể xem xét, lựa chọn phương án cắt bỏ phần thân răng trên nướu, sau đó điều trị tủy răng
và đặt thuốc kháng sinh vào ống và buồng tủy bịt kín. Cần kê toa thuốc kháng sinh từ 7 đến 10
ngày sau đó, tiếp đó là điều trị nhổ răng khi tình trạng huyết học bệnh nhân đạt mức chấp nhận
được. Nhổ răng vĩnh viễn ở những bệnh nhân đã và sẽ điều trị chiếu xạ vùng mặt cần được chú ý
đặc biệt vì có nguy cơ mắc hoại tự xương hàm do tia xạ (Osteoradionecrosis). Các thủ thuật phẫu
thuật phải được thực hiện một cách không sang chấn nhất có thể, không để lại các mép xương sắc
nhọn và đảm bảo khép kín mép vết thương tốt. Các phương pháp cầm máu tại chỗ khả dụng bao
gồm đè ép vết thương, khâu đóng vết thương, sử dụng bông cầm máu (gelatin sponges – spongel),
thrombin cầm máu tại chỗ, collagen vi sợi. Nếu cầm máu tại chỗ thất bại, cần liên hệ bác sĩ điều
trị ngay lập tức.
Khi bệnh nhân đang trong giai đoạn liệu pháp duy trì kéo dài, tiên lượng tổng thể tốt, tình
trạng huyết học gần ngang mức bình thường. Các điều trị nha khoa có thể được tiến hành theo lịch
trình thông thường, nhưng trước đó cần phải kiểm tra, xác định mức độ, số lượng tế bào máu. Có
thể tiến hành bắt đầu hoặc tiếp tục điều trị chỉnh hình răng mặt sau khi hoàn hành tất cả các trị liệu,
và ít nhất là sau 2 năm không mắc bệnh. Vào thời điểm đó, nguy cơ tái phát đã thuyên giảm, bệnh
nhân không còn sử dụng thuốc ức chế miễn dịch. Tuy nhiên, bác sĩ điều trị cần đánh giá bất kỳ rối
loạn phát triển răng (dental developmental disturbances) nào gây ra bởi quá trình trị liệu ung thư,
đặc biệt là ở bệnh nhi được điều trị trước 6 tuổi. Dahllof và các đồng nghiệp đã đưa ra chiến lược
điều trị chỉnh hình răng mặt cho các biến chứng nha khoa (do quá trình điều trị ung thư) như sau:
(1) sử dụng các khí cụ chỉnh nha giảm thiểu nguy cơ tiêu chân răng, (2) dùng lực nhẹ hơn trong
quá trình điều trị chỉnh hình răng mặt, (3) kết thúc quá trình điều trị sớm hơn thời gian thông
thường, (4) chọn phương pháp đơn giản nhất để giải quyết nhu cầu điều trị, (5) tránh điều trị hàm
dưới. Tuy nhiên, các hướng dẫn đặc trưng cho điều trị chỉnh hình răng mặt bao gồm lực tối ưu và
nhịp độ điều trị lý tưởng vẫn chưa được xác định rõ ràng. Vai trò của hormon tăng trưởng đối với
sự phát triển các cấu trúc sọ mặt ở bệnh nhi mắc bệnh ung thư vẫn chưa được xác minh đầy đủ.
Bệnh nhi mắc bệnh ung thư có thể phát triển thêm loãng xương, và nhiều trường hợp được điều trị
bằng bisphosphonate; điều này dẫn đến thêm nhiều mối lo ngại trong vấn đề chăm sóc sức khỏe
răng miệng. Những vấn đề này được đào sâu, chi tiết hơn ở những nguồn thông tin khác.
Cấy ghép tế bào gốc tạo máu (Hematopoietic Stem Cell Transplantation - HSCT):
Cấy ghép tế bào gốc tạo máu (CGTBGTM- HSCT) vừa được sử dụng để thay thế tủy xương
cho các bệnh nhân mắc các rối loạn huyết học, các rối loạn miễn dịch bẩm sinh, rối loạn lipid máu
(lipidoses), bệnh chuyển hóa bẩm sinh (inborn errors of metabolism), vừa để hỗ trợ tủy xương để
có thể tăng liều lượng hóa trị và/hoặc xạ trị cho bệnh nhân mắc bệnh thuộc nhóm bướu đặc (solid
tumors). Tế bào gốc dùng trong CGTBGTM (HSCT) có thể được thu thập từ nhiều đợt hút tủy
xương từ xương mào chậu (iliac crest) và các xương khác, từ máu mạch ngoại biên, từ nhau thai
(placenta) hoặc máu từ dây rốn. Tế bào gốc có thể được thu thập từ tủy xương của chính người
bệnh (tự thân – autologous transplant), từ người hiến tặng có quan hệ với bệnh nhân hoặc từ một
người không quen biết (dị ghép – allogeneic transplant), từ anh/chị/em sinh đôi cùng trứng (đồng
ghép – syngeneic transplant), và từ động vật/giống loài khác (cấy ghép dị loài – xenogeneic). Xét
nghiệm kháng nguyên bạch cầu người (Human Leukocyte Antigen – HLA) được thực hiện nhằm
xác định các kháng nguyên nằm trên cánh ngắn của nhiễm sắc thể số 6 (short arm of chromosome
6) của người hiến tủy tiềm năng thuận hợp với ở người nhận (thuận hợp hoàn toàn hoặc nửa thuận
hợp). Vài ngày trước khi cấy ghép tủy, người bệnh được điều trị hóa trị liều cao độc lập hoặc được
kết hợp điều trị chiếu xạ toàn bộ cơ thể. Hiện tượng mọc ghép (engraftment) thường được thấy rõ
sau khoảng 20-30 ngày, đôi khi sớm hơn, được biểu hiện qua sự gia tăng của tế bào bạch cầu ngoại
vi và số lượng tiểu cầu; điều này được chứng thực bằng sự xuất hiện của tế bào của người hiến
tủy.
Các lưu ý trong việc chăm sóc sức khỏe răng miệng:
Hầu hết các nguyên tắc về chăm sóc sức khỏe răng miệng cho bệnh nhi được điều trị
CGTBGTM (HSCT) tương tự như những nguyên tắc được thảo luận trong phần “ung thư trong
nhi khoa” trước đó. Hai khác biệt chính bao gồm: (1) Trong điều trị CGTBGTM (HSCT), không
có giai đoạn nghỉ giữa các chu kỳ hóa trị để các thông số máu trở về giá trị bình thường, các giai
đoạn nghỉ giữa chu kỳ hóa trị chỉ có ở bệnh nhi không điều trị cấy ghép; (2) Có tình trạng ức chế
miễn dịch kéo dài sau cấy ghép, chức năng miễn dịch sẽ được khôi phục gần như hoàn toàn sau
khoảng 1 năm nếu không xuất hiện bệnh mảnh ghép chống ký chủ mạn tính (chronic graft-versus-
host disease) hoặc các biến chứng khác. Do đó, trước khi điều trị CGTBGTM, bệnh nhân cần được
điều trị nha khoa toàn diện để loại bỏ bệnh lý có thể dẫn đến các biến chứng trong và sau quá trình
cấy ghép.
Trong lâu dài, tần suất khám sức khỏe răng miệng sẽ thay đổi dự trên mực độ nghiệm trọng
của các vấn đề răng miệng, việc tuân thủ vệ sinh răng mệnh, và tình trạng sức khỏe tổng quát của
bệnh nhân. Việc chụp phim x-quang để kiểm tra sức khỏe răng miệng có thể được thực hiện thường
xuyên, tuy nhiên, những bệnh nhân suy giảm miễn dịch nghiêm trọng cần tránh các điều trị nha
khoa tự chọn, bao gồm cả điều trị dự phòng. Nếu có tình trạng cấp cứu về nha khoa trong khoảng
thời gian suy giảm chức năng miễn dịch nghiêm trọng, phải hội chẩn xin ý kiến của bác sĩ nội khoa
trước khi tiến hành bất kỳ điều trị nào. Những lưu ý trong điều trị chỉnh hình răng mặt cũng tương
tự như phần thảo luận trước đó.
Các biến chứng cấp tính và mạn tính của xạ trị và hóa trị:
Điều trị ung thư có thể gây ra nhiều vấn đề sức khỏe trong khoang miệng, làm suy giảm
chất lượng sống của trẻ và tăng chi phí trị liệu. Trong tất cả các biến chứng, viêm niêm mạc là
nhân tố phổ biến nhất của đau miệng trong điều trị ung thư và là biến chứng phổ biến nhất của
điều trị CGTBGTM. Các hóa chất được dùng trong thời kì chuẩn bị (preparative regimen) gây ảnh
hưởng lớn tới mô niêm mạc của hệ tiêu hóa, cản trở các lớp đáy (basal layer) thay thế các tế bào
ngoài cùng (superficial cells), dẫn đến viêm niêm mạc toàn phần (generalized mucositis). Sự hiện
diện và mức độ nghiêm trọng của tình trạng viêm niêm mạc có sự khác biệt lớn ở từng cá nhân, sự
thay đổi của biểu mô trở nên rõ ràng vào khoảng 4-7 ngày sau khi bắt đầu điều trị và thường kéo
dài từ 10 đến14 ngày. Việc kiểm soát tình trạng viêm niêm mạc hướng tới việc điều trị giảm nhẹ
các triệu chứng, ngăn ngừa nhiễm trùng và chấn thương. Viêm niêm mạc và các biến chứng cấp
tính, dài hạn do hóa trị và xạ trị được miêu tả chi tiết ở nhiều nguồn khác.
Sự hình thành của các dị dạng sọ mặt và/hoặc các khiếm khuyết về răng miệng (dental and
craniofacial abnormalities) là một vấn từ lâu đã được bác sĩ nha khoa bệnh nhi chú ý quan tâm đặc
biệt. Vào thời điểm bắt đầu quá trình trị liệu, trẻ cảng nhỏ tuổi (nhất là dưới 6 tuổi) thì có nguy cơ
càng cao về các gây xáo trộn, biến dị sọ mặt và răng miệng, chẳng hạn như thiếu răng bẩm sinh
(tooth agenesis), ngưng phát triển chân răng hoàn toàn hoặc bán phần, tạo thành các chân răng
mỏng, thuôn, đống chóp sớm, thân răng hình nón hoặc hình cầu, đục màu và thiểu sản ở men và
ngà, tình trạng răng nhỏ bất thường (microdontia), buồng tủy nở rộng, răng bò (taurodontism), bất
thường cắn khớp (abnormal occlusion). Không có sự bất thường về quá trình trưởng thành và mọc
răng của bộ răng vĩnh viễn ở các trẻ mắc bệnh ung thư máu được điều trị hóa trị, song tình trạng
răng mọc chậm có thể được phát hiện ở bệnh nhi. Việc tạo điều kiện thuận lợi trước điều trị
CGTBGTM (pre-HSCT conditioning) có ảnh hưởng tiêu cực đự phát triển kích thước dọc ở lồi
cầu cùng với chiều cao xương ổ răng và răng cối bị.
Cần theo dõi chặt chẽ các bệnh nhân từng bị viêm niêm mạc nặng hoặc viêm niêm mạc
mạn tính, vì có nguy cơ chuyển đổi niêm mạc thành khối u ác tính. Việc theo dõi cẩn thận tình
trạng khô miệng mạn tính và bệnh mảnh ghép chống ký chủ là vô cùng quan trọng.
You might also like
- Sach Mui Hong PDFDocument175 pagesSach Mui Hong PDFduy huynh100% (1)
- Viêm miệng là kiểu nhiễm virus phổ biến nhất ảnh hưởng tới miệngDocument3 pagesViêm miệng là kiểu nhiễm virus phổ biến nhất ảnh hưởng tới miệngAnh GiangNo ratings yet
- Chốc mépDocument1 pageChốc mépAnh Tuan LeNo ratings yet
- THỦY ĐẬUDocument37 pagesTHỦY ĐẬUEmma2 NguyễnNo ratings yet
- Bệnh Lý Niêm Mạc Miệng Do Vi NấmDocument31 pagesBệnh Lý Niêm Mạc Miệng Do Vi NấmTrịnh Xuân VinhNo ratings yet
- Bệnh Đau Mắt Đỏ 1 1Document4 pagesBệnh Đau Mắt Đỏ 1 1lamthikimdung1008No ratings yet
- SOIWRDocument3 pagesSOIWRDesign ProNo ratings yet
- Các Sang Thương Mô MềmDocument61 pagesCác Sang Thương Mô MềmQuân Trần ĐạoNo ratings yet
- Nấm da- Lang benDocument6 pagesNấm da- Lang benVinh PhamNo ratings yet
- Quai BịDocument24 pagesQuai BịQuoc Thinh100% (1)
- Thủy đậuDocument36 pagesThủy đậuPhan Văn NhanhNo ratings yet
- Các bệnh lý vùng miệng thường gặpDocument31 pagesCác bệnh lý vùng miệng thường gặpHUYNH TRINHNo ratings yet
- BHM 1Document42 pagesBHM 1Gián CornNo ratings yet
- Trực khuẩn ho gàDocument5 pagesTrực khuẩn ho gàNhàn TrầnNo ratings yet
- Viem Mieng - Y32Document34 pagesViem Mieng - Y32phamb6847No ratings yet
- Nguyên Nhân C A Viêm Nư UDocument19 pagesNguyên Nhân C A Viêm Nư UTrà My hiNo ratings yet
- Handout VMN HIVDocument6 pagesHandout VMN HIVLot TobNo ratings yet
- HerpesDocument32 pagesHerpesVinh HuyNo ratings yet
- Ly Thuyet Viem Mui Xoang CapDocument38 pagesLy Thuyet Viem Mui Xoang CapAn NguyễnNo ratings yet
- VADocument27 pagesVALâmNgânNo ratings yet
- Nhiễm Herpes SimplexDocument12 pagesNhiễm Herpes Simplexheodr03No ratings yet
- Viêm Răng Miệng Liên Quan Bệnh Toàn Thân, HIVDocument45 pagesViêm Răng Miệng Liên Quan Bệnh Toàn Thân, HIVPhạm Thành NamNo ratings yet
- Bao Cao Chuyen de TMH Viem Hong CapDocument26 pagesBao Cao Chuyen de TMH Viem Hong CapMai HàNo ratings yet
- Bệnh HerpesDocument2 pagesBệnh Herpesthiminhchau voNo ratings yet
- Kháng Sinh Trong RHM Cô VânDocument7 pagesKháng Sinh Trong RHM Cô Vân16YB- YKV LớpNo ratings yet
- Viêm kết mạcDocument39 pagesViêm kết mạcNguyễn Tấn ToànNo ratings yet
- Chuyên đề khe hở môi vòm miệng P.HOA SỬA 22.8Document31 pagesChuyên đề khe hở môi vòm miệng P.HOA SỬA 22.8nhoklontonNo ratings yet
- Bnhngoida22 6 2010 120919104531 Phpapp01Document149 pagesBnhngoida22 6 2010 120919104531 Phpapp01Triều LêNo ratings yet
- 6. Tay chân miệngDocument27 pages6. Tay chân miệngngocanhNo ratings yet
- Báo Cáo Nha ChuDocument30 pagesBáo Cáo Nha ChuphamnhuchauphuongNo ratings yet
- BỆNH SỞIDocument4 pagesBỆNH SỞIngohonganh.hmuNo ratings yet
- Ho GàDocument11 pagesHo GàOanh XuânNo ratings yet
- 2. Chốc-Ts Nuyên SaDocument18 pages2. Chốc-Ts Nuyên SaDương Khải MinhNo ratings yet
- Chuyên Đề: Viêm quanh răng có liên quan với các tình trạng toàn thânDocument42 pagesChuyên Đề: Viêm quanh răng có liên quan với các tình trạng toàn thânUMP-VNU K7RHMNo ratings yet
- Dấu Hiệu Khi Bị Dị Ứng Thuốc VinmecDocument1 pageDấu Hiệu Khi Bị Dị Ứng Thuốc Vinmechienpham110702No ratings yet
- (YhocData - Com) DAL CHUONG7 DAL 2.Hong+Ban+Da+DangDocument3 pages(YhocData - Com) DAL CHUONG7 DAL 2.Hong+Ban+Da+DangTuấn ĐìnhNo ratings yet
- Bài Giảng Hệ Tiêu Hóa RhmDocument122 pagesBài Giảng Hệ Tiêu Hóa RhmThu Hà ĐặngNo ratings yet
- TÀI LIỆU BỆNH DA LIỄU 1 1Document5 pagesTÀI LIỆU BỆNH DA LIỄU 1 1Nguyen Quynh AnhNo ratings yet
- Vi Khuẩn HP Có Nguy Hiểm Không VinmecDocument1 pageVi Khuẩn HP Có Nguy Hiểm Không VinmecTrang NguyễnNo ratings yet
- Văn Bản 2Document4 pagesVăn Bản 2nguyenhaphuonglinh2007No ratings yet
- NấmDocument1 pageNấmlethao20062001No ratings yet
- Truyền Nhiễm PHÁT BAN Ở TRẺ EM2015Document90 pagesTruyền Nhiễm PHÁT BAN Ở TRẺ EM2015Mynga NguyenNo ratings yet
- Ung thư hốc miệngDocument3 pagesUng thư hốc miệngNguyễn Quang HảiNo ratings yet
- 1.1.Định nghĩa ca bệnh:: 3. Đặc điểm dịch tễ học: Bệnh rất dễ lây từ người sang người do lây bằng đường hô hấp - KhảDocument4 pages1.1.Định nghĩa ca bệnh:: 3. Đặc điểm dịch tễ học: Bệnh rất dễ lây từ người sang người do lây bằng đường hô hấp - KhảHa HaNo ratings yet
- Điều trị các bệnh hô hấpDocument3 pagesĐiều trị các bệnh hô hấpOanh OanhNo ratings yet
- Chốc SVy5y6 NSA y5Document19 pagesChốc SVy5y6 NSA y5heodr03No ratings yet
- Chốc SVy5y6 NSA Y5Document19 pagesChốc SVy5y6 NSA Y5Lê Ngọc TrinhNo ratings yet
- Đề cương ôn tập học phần Da liễu lớp RHM - Google Tài liệuDocument8 pagesĐề cương ôn tập học phần Da liễu lớp RHM - Google Tài liệuPhuong Anh NguyenNo ratings yet
- 5. Sử dụng thuốc trong điều trị Nha khoa trẻ emDocument50 pages5. Sử dụng thuốc trong điều trị Nha khoa trẻ emKEY 1111No ratings yet
- Trần Phan Chung ThủyDocument45 pagesTrần Phan Chung Thủynthieu6464No ratings yet
- Benh Hoc Lang BenDocument11 pagesBenh Hoc Lang Benapi-26566692No ratings yet
- Benh Dau Mat Do Va Cach Phong ChongDocument4 pagesBenh Dau Mat Do Va Cach Phong ChongHùng NguyễnNo ratings yet
- Lao sơ nhiễmDocument33 pagesLao sơ nhiễmLâm Thị NguyênNo ratings yet
- PHÒNG BỆNH ĐAU MẮT ĐỎDocument2 pagesPHÒNG BỆNH ĐAU MẮT ĐỎ2054040059No ratings yet
- Bệnh Quai BịDocument25 pagesBệnh Quai BịPhạm Thanh Hương100% (1)
- Giáo Trình Dư C Lâm Sàng 2Document176 pagesGiáo Trình Dư C Lâm Sàng 2Nguyễn BìnhNo ratings yet
- Nha Chu 2Document21 pagesNha Chu 2tykay131201No ratings yet
- Zona thần kinh là gìDocument4 pagesZona thần kinh là gìTuan Anh LeNo ratings yet
- Đau mắt đỏDocument2 pagesĐau mắt đỏsuhye701No ratings yet