Professional Documents
Culture Documents
تبسيط لعملية المتابعة عن طريق المعايرة اللونية
تبسيط لعملية المتابعة عن طريق المعايرة اللونية
Uploaded by
chhaidar28Copyright:
Available Formats
You might also like
- درس و عفائس المعايرة اللونية 2020Document3 pagesدرس و عفائس المعايرة اللونية 2020المعالج الروحاني الشيخ سنديان الجزائريNo ratings yet
- ملخص شامل في الأسترةDocument7 pagesملخص شامل في الأسترةchahinez Mecherrak60% (5)
- الدرس 03Document8 pagesالدرس 03ayadilyes79No ratings yet
- الدرس 03Document7 pagesالدرس 03mekhadem rayaneNo ratings yet
- Examens Nationaux 2bac Science Mathematiques PC 2015 NormaleDocument17 pagesExamens Nationaux 2bac Science Mathematiques PC 2015 NormaleFatima Larhmicذڤ1قhNo ratings yet
- الامتحان الوطني في الفيزياء والكيمياء 2015 مسلك علوم رياضية الدورة العاديةDocument17 pagesالامتحان الوطني في الفيزياء والكيمياء 2015 مسلك علوم رياضية الدورة العاديةnasrelhassakNo ratings yet
- Alfiziaa Oalkimiaa Alom Riadhia 2017 Aldora Alaadia Altshih 3Document14 pagesAlfiziaa Oalkimiaa Alom Riadhia 2017 Aldora Alaadia Altshih 3bilal rojolaNo ratings yet
- الحلقة (7) درس المتابعة الزمنية عن طريق المعايرة اللونية PDFDocument3 pagesالحلقة (7) درس المتابعة الزمنية عن طريق المعايرة اللونية PDFu w uNo ratings yet
- درس المتابعة الزمنية عن طريق المعايرة اللونيةDocument3 pagesدرس المتابعة الزمنية عن طريق المعايرة اللونيةRedouane Reda83% (6)
- الدرس 06Document16 pagesالدرس 06ayadilyes79No ratings yet
- 32alfiziaa Oalkimiaa Alom Fiziaiia 2015 Aldora Alistdrakia Altshih 1Document7 pages32alfiziaa Oalkimiaa Alom Fiziaiia 2015 Aldora Alistdrakia Altshih 1Youssef YoussefNo ratings yet
- درس شامل في المتابعة الزمنيةDocument8 pagesدرس شامل في المتابعة الزمنيةBrahim YoucefNo ratings yet
- المعايرة 2020Document4 pagesالمعايرة 2020oukhitamazighNo ratings yet
- حل تمارين المعايرة اللونية 3 ثانويDocument10 pagesحل تمارين المعايرة اللونية 3 ثانويsafaamoudjari38No ratings yet
- سلسلة تمارين الوحدة الأولى 1Document1 pageسلسلة تمارين الوحدة الأولى 1picaking9No ratings yet
- تمارين الوحدة 01Document1 pageتمارين الوحدة 01MY GAMINGNo ratings yet
- Test of Significance in Multiple PDFDocument8 pagesTest of Significance in Multiple PDFMohamed AsimNo ratings yet
- تمرين 1-3Document2 pagesتمرين 1-3Hani StarkNo ratings yet
- 3as تصحيح إختبار الفصل الأولDocument5 pages3as تصحيح إختبار الفصل الأولKANIKI FFNo ratings yet
- تقويم الوحدة 2024Document4 pagesتقويم الوحدة 2024widad doudiNo ratings yet
- Bbl14bS MohamedDocument9 pagesBbl14bS MohamedrachidNo ratings yet
- ملخص درس النوى - الكتلة و الطاقةDocument1 pageملخص درس النوى - الكتلة و الطاقةbilalbenmchich10No ratings yet
- سلسلة تمارينDocument6 pagesسلسلة تمارينMalak ElaichouchiNo ratings yet
- سلسلة تمارين 2Document6 pagesسلسلة تمارين 2lisaNo ratings yet
- ملخص المكتسبات القبلية للسنة الثالثة ثانويDocument4 pagesملخص المكتسبات القبلية للسنة الثالثة ثانويTrainerYoucefDjouadjNo ratings yet
- ملزمة رياضيات ثالث متوسط رائد علي ج2Document242 pagesملزمة رياضيات ثالث متوسط رائد علي ج2Abdullah Esmail100% (1)
- تمارين الوحدة 01Document2 pagesتمارين الوحدة 01elandaloussimeriem59No ratings yet
- Alfiziaa Oalkimiaa Alom Riadhia 2013 Aldora Alistdrakia AltshihDocument12 pagesAlfiziaa Oalkimiaa Alom Riadhia 2013 Aldora Alistdrakia AltshihdrisshouariNo ratings yet
- تصحيح 2016Document8 pagesتصحيح 2016Tarik SouimdiNo ratings yet
- Corr Exam 05Document5 pagesCorr Exam 05Abdessalam BOUMARAFNo ratings yet
- العلاقة بين الأفراد الكيميائيةDocument3 pagesالعلاقة بين الأفراد الكيميائيةlynamellah415No ratings yet
- Dzexams Docs 3as 907348Document28 pagesDzexams Docs 3as 907348amelchahbaouiNo ratings yet
- الدرس 02Document5 pagesالدرس 02bouguerraceline0No ratings yet
- الدوال الاصلية والتكاملاتDocument2 pagesالدوال الاصلية والتكاملاتKhalil AkmoucheNo ratings yet
- 2016RDocument10 pages2016Ryasserhayati06No ratings yet
- - - - - - - - - الحلقة (10) تمرين حول المتابعة الزمنية عن طريق قياس الضغط PDFDocument5 pages- - - - - - - - الحلقة (10) تمرين حول المتابعة الزمنية عن طريق قياس الضغط PDFAbdou100% (1)
- - - - - - - - - الحلقة (10) تمرين حول المتابعة الزمنية عن طريق قياس الضغط PDFDocument5 pages- - - - - - - - الحلقة (10) تمرين حول المتابعة الزمنية عن طريق قياس الضغط PDFamina derkaouiNo ratings yet
- Physics 3se22 1trim d1Document4 pagesPhysics 3se22 1trim d1souissi souissiNo ratings yet
- Physics 3mtm22 1trim d4Document4 pagesPhysics 3mtm22 1trim d4Radovane PhysiqyeNo ratings yet
- سلسلة تمارين متعلقة بالمكتسبات القبليةDocument2 pagesسلسلة تمارين متعلقة بالمكتسبات القبليةBOUCHEFFA HalimNo ratings yet
- Alfrdh 2 Nmothj 3 Alfiziaa Oalkimiaa Thania Bak Alom Fiziaiia Aldora Alaola AltshihDocument6 pagesAlfrdh 2 Nmothj 3 Alfiziaa Oalkimiaa Thania Bak Alom Fiziaiia Aldora Alaola Altshihmimififi0208No ratings yet
- 8-1 مقاييس التشتت - 240515 - 071521Document9 pages8-1 مقاييس التشتت - 240515 - 071521BishrMushtaha1No ratings yet
- Dzexams 2am Mathematiques 931645Document6 pagesDzexams 2am Mathematiques 931645Ay MeNNo ratings yet
- تصحيح ف1 س3م2021Document2 pagesتصحيح ف1 س3م2021Nasser Eddine AbdouNo ratings yet
- تجميعية وثائق الأسبوع الثاني (فارغة)Document23 pagesتجميعية وثائق الأسبوع الثاني (فارغة)Mīšś KôükïtàNo ratings yet
- سلسلة مراجعة مكتسبات القبلية الجديدةDocument4 pagesسلسلة مراجعة مكتسبات القبلية الجديدةAbderrahmane henniNo ratings yet
- Alfiziaa Oalkimiaa Alom Fiziaiia 2010 Aldora Alaadia Altshih 3Document9 pagesAlfiziaa Oalkimiaa Alom Fiziaiia 2010 Aldora Alaadia Altshih 3Adil BahriNo ratings yet
- حلول تمارين السلسلة 1Document5 pagesحلول تمارين السلسلة 1Rania TataNo ratings yet
- Altrkiz Almoli Llanoaa Alkimiaiia Fi Mhlol Tshih Slsla Altmarin 2Document10 pagesAltrkiz Almoli Llanoaa Alkimiaiia Fi Mhlol Tshih Slsla Altmarin 2Ily asse Essay ahNo ratings yet
- سلسلة الوحدة 1 المتابعة الزمنيةDocument8 pagesسلسلة الوحدة 1 المتابعة الزمنيةMohamed Anis LounisNo ratings yet
- 7Document4 pages7samirus incNo ratings yet
- اختبار 2 عام 2024Document2 pagesاختبار 2 عام 2024abderrahmaneriad777No ratings yet
- 4 5879874055732990293Document5 pages4 5879874055732990293Loup le DésertNo ratings yet
- PhysicsDocument2 pagesPhysicsyacine yacineNo ratings yet
- الوحدة 01 Zoom معدلةDocument55 pagesالوحدة 01 Zoom معدلةabdelkaderheba563No ratings yet
- Corppcr 17Document11 pagesCorppcr 17اوىةNo ratings yet
- الامتحان الوطني في الفيزياء والكيمياء 2019 للمسالك العلمية الدورة الاستدراكيةDocument13 pagesالامتحان الوطني في الفيزياء والكيمياء 2019 للمسالك العلمية الدورة الاستدراكية05313893731llllNo ratings yet
- Kotobati - رواية مجبرونDocument64 pagesKotobati - رواية مجبرونdrenahmadyacoubNo ratings yet
- تمارين الأحماض و الأسسDocument1 pageتمارين الأحماض و الأسسmouad drouicheNo ratings yet
تبسيط لعملية المتابعة عن طريق المعايرة اللونية
تبسيط لعملية المتابعة عن طريق المعايرة اللونية
Uploaded by
chhaidar28Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
تبسيط لعملية المتابعة عن طريق المعايرة اللونية
تبسيط لعملية المتابعة عن طريق المعايرة اللونية
Uploaded by
chhaidar28Copyright:
Available Formats
ُ ُ
تركيزه -تبسيط لعملية املتابعة عن طريق املعايرة اللونية :نحدث تفاعل تام بين حجم 𝒍𝒎𝟎𝟓 = 𝟏 Vمن 𝑆2 𝑂82−
املولي 𝟏𝒄 مع حجم 𝑙𝑚 𝑉2 = 50من ) (𝑲+ + 𝑰−تركيزه املولي 𝟐𝒄 .
ُ
أسفله : -معادلة هذا التفاعل البطيئ موضح في جدول التقدم
2− −
معادلة التفاعل )𝑞𝑎(𝑆2 𝑂8 )𝑞𝑎(𝐼 + 2 = )𝑞𝑎(𝐼2 + )𝑞𝑎(2𝑆𝑂42−
الحالة التقدم كمي ـ ـ ـ ـ ــة امل ـ ـ ـ ـ ـ ـ ـ ـ ـ ـ ـ ـ ـ ــادة باملـ ـ ـ ـ ـ ـ ـ ـ ـ ـ ـ ـ ـ ـ ـ ـ ـ ـ ـ ـ ـ ـ ــول
االبتدائية 0 𝑐1 𝑉1 𝑐2 𝑉2 0 0
االنتقالية 𝑡𝑥 𝑡𝑥 𝑐1 𝑉1 − 𝑡𝑥 𝑐2 𝑉2 − 𝑡𝑥 𝑥
النهائية 𝑓𝑥 𝑓𝑥 𝑐1 𝑉1 − 𝑓𝑥 𝑐2 𝑉2 − 𝑓𝑥 𝑓𝑥
ُ
-الفكرة األساسية هي معرفة كمية املادة لثنائي اليود 𝑡) 𝑛(𝐼2في لحظات زمنية ُمختلفة وهذا بإستغالل اللون املميز لل ـ ( 𝐼2بني أو ُبني
ُمصفر أو أسمر ) ,ونعلم من جدول التقدم 𝑛(𝐼 ) = 𝑥 :إذن تتبع كمية مادة ثنائي اليود ُيمكننا من تتبع تقدم التفاعل 𝑥
𝑡 𝑡 2 𝑡
وعليه ُيمكننا رسم املنحنى )𝑡(𝑓 = 𝑡𝑥 ( إذن يكننا حساب سرعة أو كمية مادة أو تركيز ...في أي لحظة ما وهذا هو الهدف من
املتابعة )
-إذن كيف نقوم بذلك ـ ؟
-بإختصار ُيمكن توضيحها في الرسم التالي :نقوم بعملية املزج بين 𝑉1و 𝑉2ونكررها 05مرات ( أو أكثر) :
𝒏𝒊𝒎 𝟎𝟐 = 𝒕 𝒏𝒊𝒎 𝟓𝟏 = 𝒕 𝒏𝒊𝒎 𝟎𝟏 = 𝒕 𝒏𝒊𝒎 𝟓 = 𝒕 عند الدقيقة 𝒏𝒊𝒎 𝟎 = 𝒕
نكررالعملية نكررالعملية نكررالعملية نقوم بمزج 𝑉2و 𝑉1 نقوم بمزج 𝑉1 + 𝑉2
مرة أخرى .
ال وجود للــ 𝐼2ألن
التفاعل لم يبدأ والنواتج
بداية تشكل الـ 𝐼2مع تقدم التفاعل ويستمر في الظهور والتشكل معدومة
حتى يتوقف التفاعل 𝑓𝑥 = 𝑡𝑥 عندها يتوقف التفاعل ومنه تتوقف
زيادة كمية مادة الــ 𝐼2أي وصلنا إلى 𝑓) 𝑛(𝐼2
ترميز للــ 𝐼2وتزايد كمية مادتها بتطورالتفاعل .
نذكر بأن كمية المادة (عدد الموالت) ماهي إال عدد ألفراد -
الكيميائية نكتب 𝑙𝑜𝑚 𝟐 = ) 𝑛(𝐼2أي أن عدد أفراد الــ 𝐼2
هي :فرد 𝑁(𝐼2 ) = 𝟐 × 6,023 × 1023
-
الصفحة 1 األستاذ قطار أحمد يسين
ُ ُ
-ولتحديد كمية مادة ال ـ 𝐼2في املزيج ,في كل مرة ُنقوم بعملية املعايرة للمزيج بمحلول مناسب يتفاعل تفاعل أكسدة – إرجاع مع
ال ـ 𝐼 ونتوقف عن إضافة املحلول الذي ُنعاير به ( السحاحة) حتى يختفي اللون ُ
املميز لـل ـ ـ 𝐼 نهائيا ,وهي نقطة التكافؤ حيث تكون
2 2
املتفاعالت بنسب شروط ستوكيومترية .
ُ
-لكن مخبريا هذه الطريقة ال تستعمل ألنها تستهلك الكثير من الوقت و أحجام كبيرة من املحاليل ( تبذير) ,لذلك ـ جاءت فكرة تقسيم
ُ ُ
ُمحتوى االنابيب والتي نلخصها فيما يلي :نقوم عند اللحظة 𝑡 = 0بمزج 𝑉1 + 𝑉2ثم نقسم املزيج إلى 05انابيب( أو أكثر حسب
التجربة) :
نُقسمهُ المزيج عند اللحظة
𝟎 = 𝒕 إلى 5أنبوب
()1 ()2 ()3 ()4 ()5
𝒍𝒎𝟎𝟎𝟏 = 𝟐𝑽 𝑽𝟏 + ُ
بعد التقسيم نتحصل على 05أنابيب .كل أنبوب يحتوي على 𝑙𝑚 𝑉0 = 20
ُ
حجمه 𝑉0ونقوم بمعايرته بواسطة نأخذ في كل مرة أنبوب عند اللحظة : 𝑡 = 0
محلول يتفاعل تفاعل أكسدة – إرجاع مع ثنائي اليود ,
املحلول املناسب هنا هو ثيوكبريتات الصوديوم . 𝑆2 𝑂32−
-حيث يحدث التفاعل السريع : ()1 ()2 ()3 ()4 ()5
عند اللحظة 𝑛𝑖𝑚 : 𝑡 = 5
𝟐 𝑺𝟐 𝑶𝟐−
)𝒒𝒂(𝟑 = )𝒒𝒂(𝟐𝑰 + 𝑺𝟒 𝑶𝟐−
𝟔 + 𝟐𝑰−
)𝒒𝒂(
ُ
وهذا بإستعمال املعايرة اللونية حيث كل قطرة تسقط
من السحاحة تصل إلى حالتها النهائية بمجرد وصولها للبيشر ()2 ()3 ()4 ()5
𝟐− (سريع) . عند اللحظة 𝑛𝑖𝑚 : 𝑡 = 10
محلول الــ )𝒒𝒂(𝟑𝑶 𝟐𝑺 الذي
نعاير به تركي ُزهُ معلوم 𝟎𝑪
نضع قطرات من كاشف
مناسب ( صمغ النشاء)
ليتحول لون الـــ 𝟐𝑰 إلى ()3 ()4 ()5
األزرق الداكن وهو أوضح عند اللحظة 𝑛𝑖𝑚 : 𝑡 = 15
في المعايرة من اللون
البني أو األسمر
نضيف القليل من الماء
البارد +قطع جليد لتوقيف
التفاعل عند تلك اللحظة . ()4 ()5
وعند نقطة التكافؤ تكون املتفاعالت بنسب شروط عند اللحظة 𝑛𝑖𝑚 : 𝑡 = 20
) 𝑛′ (𝐼2 𝑛(𝑺𝟐 𝑶𝟐−
) 𝟑
= ستوكيومترية أي :
1 2
𝑬𝑽× 𝟎𝒄
= ) 𝑛′ (𝐼2 أي :
كمية مادة الـــ 𝟐𝑰 في 2
أنبوب واحد ( ألننا عايرنا
()5
أنبوب واحد فقط )
الصفحة 2 األستاذ قطار أحمد يسين
-نالحظ ان األنبوب رقم 05إستعملناه بعد مرور 20دقيقة و إنطالقا من معرفة كمية املادة املوجودة فيه ُ ,يمكننا إستنتاج كمية
املادة املتواجدة في املزيج عند هذه اللحظة .
ُ
◄عند التكافؤ ,تكون املتفاعالت بنسب شروط ستوكيومترية (إنطالقا من تفاعل املعايرة ) معناه :
𝑬𝑽× 𝟎𝒄 𝑬𝑽× 𝟎𝒄 ) 𝟐𝑰( 𝒏′ 𝒏(𝑺𝟐 𝑶𝟐−
) 𝟑 ) 𝟐𝑰( 𝒏′
= ) 𝟐𝑰( 𝒏′ = =
𝟐 𝟐 𝟏 𝟐 𝟏
حيث : 𝒏′ (𝑰𝟐 ) :هي كمية املادة لثنائي اليود املوجودة في أنبوب واحد .
education-onec-dz.blogspot.com
◄كتابة العالقة بداللة 𝒕) 𝟐𝑰( 𝒏 (كمية مادة ال ـ 𝟐𝑰 في املزيج ككل) ,نضرب الطرفين في عدد األنابيب ( 5أنبوب) :
𝑬𝑽× 𝟎𝒄
𝑬𝑽 × 𝟎𝒄 × 𝟓 𝒏 (𝑰𝟐 )𝒕 = 𝟐, × 𝟓 = ) 𝟐𝑰( 𝟓 × 𝒏′وبما أن 𝟓 × 𝒕) 𝟐𝑰( 𝒏 (𝑰𝟐 )𝒕 = 𝒏′
𝟐
𝒕) 𝟐𝑰( 𝒏
كمية املادة املوجودة في أنبوب واحد 𝟎𝑽 عند كل لحظة . 𝑛′ (𝐼2 )𝑡 = [𝐼2 ]𝑡 × 𝑉0
{ حيث أن } :
ُ ُ
كمية املادة املوجودة في املزيج الكلي قبل التقسيم 𝑻𝑽 عند كل لحظة . 𝑇𝑉 × 𝑡] 𝑛 (𝐼2 )𝑡 = [𝐼2
ُ
نفسه املوجود في املزيج عند لحظة زمنية , tحيث 𝑙𝑚 𝑉𝑇 = 100و 𝑙𝑚 𝑉0 = 20 -حيث أن التركيز 𝑡] [𝐼2املوجود في األنبوب
𝑬𝑽 × 𝟎𝒄 𝑬𝑽 × 𝟎𝒄 𝑬𝑽 × 𝟎𝒄 𝑬𝑽 × 𝟎𝒄
= ) 𝟐𝑰( ➔ 𝒏′ = [𝐼2 ]𝑡 × 𝑉0 = 𝑡] [𝐼2 = 𝑡] [𝐼2
𝟐 𝟐 𝟐𝑉0 𝟎𝟒
𝑬𝑽 × 𝟎𝒄 𝑬𝑽 × 𝟎𝒄 × 𝟓 𝟐,
= 𝑡] ➔ 𝒏 (𝑰𝟐 )𝒕 = 𝟐, 𝟓 × 𝒄𝟎 × 𝑽𝑬 [𝐼2 ]𝑡 × 𝑉𝑇 = 𝟐, 𝟓 × 𝒄𝟎 × 𝑽𝑬 [𝐼2 =
{ 𝟎𝟎𝟏 } 𝟎𝟒
𝑬𝑽× 𝟎𝒄
= 𝑡] [𝐼2 إذن عالقة ثنائي اليود هي نفسها :
𝟎𝟒
ُ
◄ بعد كل معايرة نسجل الحجم املضاف عند التكافؤ 𝐸 Vثم ندون النتائج في الجدول التالي بإستغالل العالقة 𝒕𝒙 = 𝒕) 𝟐𝑰( 𝒏 والعالقة
ُ
𝑬𝑽 × 𝟎𝒄 × 𝟓 𝒏 (𝑰𝟐 )𝒕 = 𝟐,حيث أن 𝑐0معلوم و 𝐸𝑉 نسجلها بعد كل عملية معايرة ونكمل الجدول .
)t (min 5 10 15 20
)V𝐸 (ml
)𝒍𝒐𝒎𝒎( 𝒕) 𝟐𝑰( 𝒏
)𝑙𝑜𝑚𝑚()𝑡(𝑥
◄ ُيمكننا إكمال الجدول أعاله إنطالقا من التعويض فقط في العالقة أعاله ُ
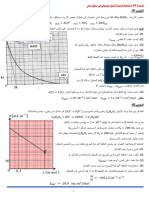
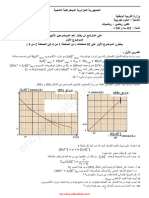
ومنه نستطيع رسم املنحنى )𝑡(𝑓 = 𝑡) 𝑛 (𝐼2أو
)𝑡(𝑓 = 𝑥 ( وبرسم أحد املنحنين نتمكن من متابعة هذا التحول الكيميائي)
الصفحة 3 األستاذ قطار أحمد يسين
ُ ملخص البروتوكول التجريبي :
◄ الهدف :التمكن من املتابعة الزمنية لتحول كيميائي
◄ األدوات واملواد املستعملة :بيشر ,سحاحة ُمدرجة ,ماصة عيارية ,أنابيب إختبار ,مخالط مغناطيس ي وقطعة مغناطيسية ,حامل ,
محلول نريد معايرته ,محلول نعاير به ,صمغ النشاء (أو التيودان) ,ماء بارد وجليد ,مؤقت (كرونومتر)
ُ
◄ الخطوات
ُ
• نأخذ في كل مرة عينة من املزيج التفاعلي حجمها V0
• نسكبها في كأس بيشر به جليد وماء بارد وبعض قطرات من صمغ النشاء
ُ
• ثم نعاير محتوى البيشر بمحلول مناسب معلوم التركيز حتى الوصول الى نقطة التكافؤ
• نكرر العملية في أزمنة مختلفة ونسجل في كل مرة VEالواجب للتكافؤ (نستعمل مؤقت)
ُ ملخص الرسم التجريبي للمتابعة عن طريق املعايرة اللونية :
ُ
ُ قــمع
املحلول الذي نعايربه
سحـاحة مدرجة
ثيوكبريتات الصوديوم
ُ ُ
قسمه ن
𝟐𝑽 𝑽𝟏 + إلى 05
حامل
أنابيب
حجم المــزيج قطرات من صمغ النشاء
+جليد +ماء بارد قضيب
حديد
مخالط
مغناطيس ي
ُ
حجمه 𝟎𝑽 ونقوم في كل لحظة زمنية نأخذ أنبوب إختبار
بتفريغه في البيشر ملعايرة ثنائي اليود املوجود فيه الذي
يتشكل بإستمرارا
الصفحة 4 األستاذ قطار أحمد يسين
اﻟﻤﻮﻗﻊ اﻷول ﻟﺘﺤﻀﻴﺮ اﻟﻔﺮوض واﻻﺧﺘبﺎرات ﻓﻲ اﻟﺠﺰاﺋﺮ
https://www.dzexams.com
https://www.dzexams.com/ar/0ap اﻟﻘﺴﻢ اﻟﺘﺤﻀﻴﺮي
https://www.dzexams.com/ar/1ap اﻟﺴﻨﺔ اﻷوﻟﻰ اﺑﺘﺪاﺋﻲ
https://www.dzexams.com/ar/2ap اﻟﺴﻨﺔ اﻟﺜﺎﻧ�ﺔ اﺑﺘﺪاﺋﻲ
https://www.dzexams.com/ar/3ap اﻟﺴﻨﺔ اﻟﺜﺎﻟﺜﺔ اﺑﺘﺪاﺋﻲ
https://www.dzexams.com/ar/4ap اﻟﺴﻨﺔ اﻟﺮابﻌﺔ اﺑﺘﺪاﺋﻲ
https://www.dzexams.com/ar/5ap اﻟﺴﻨﺔ اﻟﺨﺎﻣﺴﺔ اﺑﺘﺪاﺋﻲ
https://www.dzexams.com/ar/bep ﺷﻬﺎدة اﻟﺘﻌﻠ�ﻢ اﻻﺑﺘﺪاﺋﻲ
https://www.dzexams.com/ar/1am اﻟﺴﻨﺔ اﻷوﻟﻰ ﻣﺘﻮﺳﻂ
https://www.dzexams.com/ar/2am اﻟﺴﻨﺔ اﻟﺜﺎﻧ�ﺔ ﻣﺘﻮﺳﻂ
https://www.dzexams.com/ar/3am اﻟﺴﻨﺔ اﻟﺜﺎﻟﺜﺔ ﻣﺘﻮﺳﻂ
https://www.dzexams.com/ar/4am اﻟﺴﻨﺔ اﻟﺮابﻌﺔ ﻣﺘﻮﺳﻂ
https://www.dzexams.com/ar/bem ﺷﻬﺎدة اﻟﺘﻌﻠ�ﻢ اﻟﻤﺘﻮﺳﻂ
https://www.dzexams.com/ar/1as اﻟﺴﻨﺔ اﻷوﻟﻰ ﺛﺎﻧﻮي
https://www.dzexams.com/ar/2as اﻟﺴﻨﺔ اﻟﺜﺎﻧ�ﺔ ﺛﺎﻧﻮي
https://www.dzexams.com/ar/3as اﻟﺴﻨﺔ اﻟﺜﺎﻟﺜﺔ ﺛﺎﻧﻮي
https://www.dzexams.com/ar/bac ﺷﻬﺎدة اﻟبكﺎﻟﻮر�ﺎ
You might also like
- درس و عفائس المعايرة اللونية 2020Document3 pagesدرس و عفائس المعايرة اللونية 2020المعالج الروحاني الشيخ سنديان الجزائريNo ratings yet
- ملخص شامل في الأسترةDocument7 pagesملخص شامل في الأسترةchahinez Mecherrak60% (5)
- الدرس 03Document8 pagesالدرس 03ayadilyes79No ratings yet
- الدرس 03Document7 pagesالدرس 03mekhadem rayaneNo ratings yet
- Examens Nationaux 2bac Science Mathematiques PC 2015 NormaleDocument17 pagesExamens Nationaux 2bac Science Mathematiques PC 2015 NormaleFatima Larhmicذڤ1قhNo ratings yet
- الامتحان الوطني في الفيزياء والكيمياء 2015 مسلك علوم رياضية الدورة العاديةDocument17 pagesالامتحان الوطني في الفيزياء والكيمياء 2015 مسلك علوم رياضية الدورة العاديةnasrelhassakNo ratings yet
- Alfiziaa Oalkimiaa Alom Riadhia 2017 Aldora Alaadia Altshih 3Document14 pagesAlfiziaa Oalkimiaa Alom Riadhia 2017 Aldora Alaadia Altshih 3bilal rojolaNo ratings yet
- الحلقة (7) درس المتابعة الزمنية عن طريق المعايرة اللونية PDFDocument3 pagesالحلقة (7) درس المتابعة الزمنية عن طريق المعايرة اللونية PDFu w uNo ratings yet
- درس المتابعة الزمنية عن طريق المعايرة اللونيةDocument3 pagesدرس المتابعة الزمنية عن طريق المعايرة اللونيةRedouane Reda83% (6)
- الدرس 06Document16 pagesالدرس 06ayadilyes79No ratings yet
- 32alfiziaa Oalkimiaa Alom Fiziaiia 2015 Aldora Alistdrakia Altshih 1Document7 pages32alfiziaa Oalkimiaa Alom Fiziaiia 2015 Aldora Alistdrakia Altshih 1Youssef YoussefNo ratings yet
- درس شامل في المتابعة الزمنيةDocument8 pagesدرس شامل في المتابعة الزمنيةBrahim YoucefNo ratings yet
- المعايرة 2020Document4 pagesالمعايرة 2020oukhitamazighNo ratings yet
- حل تمارين المعايرة اللونية 3 ثانويDocument10 pagesحل تمارين المعايرة اللونية 3 ثانويsafaamoudjari38No ratings yet
- سلسلة تمارين الوحدة الأولى 1Document1 pageسلسلة تمارين الوحدة الأولى 1picaking9No ratings yet
- تمارين الوحدة 01Document1 pageتمارين الوحدة 01MY GAMINGNo ratings yet
- Test of Significance in Multiple PDFDocument8 pagesTest of Significance in Multiple PDFMohamed AsimNo ratings yet
- تمرين 1-3Document2 pagesتمرين 1-3Hani StarkNo ratings yet
- 3as تصحيح إختبار الفصل الأولDocument5 pages3as تصحيح إختبار الفصل الأولKANIKI FFNo ratings yet
- تقويم الوحدة 2024Document4 pagesتقويم الوحدة 2024widad doudiNo ratings yet
- Bbl14bS MohamedDocument9 pagesBbl14bS MohamedrachidNo ratings yet
- ملخص درس النوى - الكتلة و الطاقةDocument1 pageملخص درس النوى - الكتلة و الطاقةbilalbenmchich10No ratings yet
- سلسلة تمارينDocument6 pagesسلسلة تمارينMalak ElaichouchiNo ratings yet
- سلسلة تمارين 2Document6 pagesسلسلة تمارين 2lisaNo ratings yet
- ملخص المكتسبات القبلية للسنة الثالثة ثانويDocument4 pagesملخص المكتسبات القبلية للسنة الثالثة ثانويTrainerYoucefDjouadjNo ratings yet
- ملزمة رياضيات ثالث متوسط رائد علي ج2Document242 pagesملزمة رياضيات ثالث متوسط رائد علي ج2Abdullah Esmail100% (1)
- تمارين الوحدة 01Document2 pagesتمارين الوحدة 01elandaloussimeriem59No ratings yet
- Alfiziaa Oalkimiaa Alom Riadhia 2013 Aldora Alistdrakia AltshihDocument12 pagesAlfiziaa Oalkimiaa Alom Riadhia 2013 Aldora Alistdrakia AltshihdrisshouariNo ratings yet
- تصحيح 2016Document8 pagesتصحيح 2016Tarik SouimdiNo ratings yet
- Corr Exam 05Document5 pagesCorr Exam 05Abdessalam BOUMARAFNo ratings yet
- العلاقة بين الأفراد الكيميائيةDocument3 pagesالعلاقة بين الأفراد الكيميائيةlynamellah415No ratings yet
- Dzexams Docs 3as 907348Document28 pagesDzexams Docs 3as 907348amelchahbaouiNo ratings yet
- الدرس 02Document5 pagesالدرس 02bouguerraceline0No ratings yet
- الدوال الاصلية والتكاملاتDocument2 pagesالدوال الاصلية والتكاملاتKhalil AkmoucheNo ratings yet
- 2016RDocument10 pages2016Ryasserhayati06No ratings yet
- - - - - - - - - الحلقة (10) تمرين حول المتابعة الزمنية عن طريق قياس الضغط PDFDocument5 pages- - - - - - - - الحلقة (10) تمرين حول المتابعة الزمنية عن طريق قياس الضغط PDFAbdou100% (1)
- - - - - - - - - الحلقة (10) تمرين حول المتابعة الزمنية عن طريق قياس الضغط PDFDocument5 pages- - - - - - - - الحلقة (10) تمرين حول المتابعة الزمنية عن طريق قياس الضغط PDFamina derkaouiNo ratings yet
- Physics 3se22 1trim d1Document4 pagesPhysics 3se22 1trim d1souissi souissiNo ratings yet
- Physics 3mtm22 1trim d4Document4 pagesPhysics 3mtm22 1trim d4Radovane PhysiqyeNo ratings yet
- سلسلة تمارين متعلقة بالمكتسبات القبليةDocument2 pagesسلسلة تمارين متعلقة بالمكتسبات القبليةBOUCHEFFA HalimNo ratings yet
- Alfrdh 2 Nmothj 3 Alfiziaa Oalkimiaa Thania Bak Alom Fiziaiia Aldora Alaola AltshihDocument6 pagesAlfrdh 2 Nmothj 3 Alfiziaa Oalkimiaa Thania Bak Alom Fiziaiia Aldora Alaola Altshihmimififi0208No ratings yet
- 8-1 مقاييس التشتت - 240515 - 071521Document9 pages8-1 مقاييس التشتت - 240515 - 071521BishrMushtaha1No ratings yet
- Dzexams 2am Mathematiques 931645Document6 pagesDzexams 2am Mathematiques 931645Ay MeNNo ratings yet
- تصحيح ف1 س3م2021Document2 pagesتصحيح ف1 س3م2021Nasser Eddine AbdouNo ratings yet
- تجميعية وثائق الأسبوع الثاني (فارغة)Document23 pagesتجميعية وثائق الأسبوع الثاني (فارغة)Mīšś KôükïtàNo ratings yet
- سلسلة مراجعة مكتسبات القبلية الجديدةDocument4 pagesسلسلة مراجعة مكتسبات القبلية الجديدةAbderrahmane henniNo ratings yet
- Alfiziaa Oalkimiaa Alom Fiziaiia 2010 Aldora Alaadia Altshih 3Document9 pagesAlfiziaa Oalkimiaa Alom Fiziaiia 2010 Aldora Alaadia Altshih 3Adil BahriNo ratings yet
- حلول تمارين السلسلة 1Document5 pagesحلول تمارين السلسلة 1Rania TataNo ratings yet
- Altrkiz Almoli Llanoaa Alkimiaiia Fi Mhlol Tshih Slsla Altmarin 2Document10 pagesAltrkiz Almoli Llanoaa Alkimiaiia Fi Mhlol Tshih Slsla Altmarin 2Ily asse Essay ahNo ratings yet
- سلسلة الوحدة 1 المتابعة الزمنيةDocument8 pagesسلسلة الوحدة 1 المتابعة الزمنيةMohamed Anis LounisNo ratings yet
- 7Document4 pages7samirus incNo ratings yet
- اختبار 2 عام 2024Document2 pagesاختبار 2 عام 2024abderrahmaneriad777No ratings yet
- 4 5879874055732990293Document5 pages4 5879874055732990293Loup le DésertNo ratings yet
- PhysicsDocument2 pagesPhysicsyacine yacineNo ratings yet
- الوحدة 01 Zoom معدلةDocument55 pagesالوحدة 01 Zoom معدلةabdelkaderheba563No ratings yet
- Corppcr 17Document11 pagesCorppcr 17اوىةNo ratings yet
- الامتحان الوطني في الفيزياء والكيمياء 2019 للمسالك العلمية الدورة الاستدراكيةDocument13 pagesالامتحان الوطني في الفيزياء والكيمياء 2019 للمسالك العلمية الدورة الاستدراكية05313893731llllNo ratings yet
- Kotobati - رواية مجبرونDocument64 pagesKotobati - رواية مجبرونdrenahmadyacoubNo ratings yet
- تمارين الأحماض و الأسسDocument1 pageتمارين الأحماض و الأسسmouad drouicheNo ratings yet