Professional Documents
Culture Documents
تمرين شامل في الوحدة الأولى المتابعة الزمنية لتحول كيميائي
تمرين شامل في الوحدة الأولى المتابعة الزمنية لتحول كيميائي
Uploaded by
mlkmehdidCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
تمرين شامل في الوحدة الأولى المتابعة الزمنية لتحول كيميائي
تمرين شامل في الوحدة الأولى المتابعة الزمنية لتحول كيميائي
Uploaded by
mlkmehdidCopyright:
Available Formats
األستاذ :شنايت التمرين الشامل في وحدة المتابعة الزمنية لتحول كيميائي
بعد نهاية برنامج مادة العلوم الفيزيائية الخاص بتالميذ بكالوريا ،2024شعر التالميذ بضرورة إجراء مراجعة
شاملة في وحدة "المتابعة الزمنية لتحول كيميائي" نظرا ً لتعدد أفكارها ومرور فترة زمنية طويلة منذ دراستها،
لذلك قرر األستاذ تحضير مسألة شاملة نموذجية تتضمن جميع األفكار المحتملة في اِمتحان البكالوريا بترتيب مناسب ومساعد
على الفهم الجيد لهذه الوحدة.
قبل االنطالق في حل المسألة ،قام األستاذ باإلجابة عن أغلب األسئلة النظرية المتعلقة بالوحدة.
الجزء األول :األسئلة النظرية مع أجوبتها:
)1التقدم األعظمي 𝒙𝒂𝒎𝒙 :هو التقدم الذي من اجله تنعدم كمية مادة المتفاعل ال ُمحد( .يستخرج من جدول تقدم التفاعل).
)2التقدّم النّهائي 𝒇𝒙 :هو التقدم المالحظ تجريبيا (بيانيا) ،ويعرف بأنه التقدم الذي من أجله تتوقف الجملة عن التطور.
)3المؤكسد :هو كل فرد كيميائي قادر على اكتساب إلكترون أو أكثر خالل تفاعل كيميائي يرمز له بـ 𝑥𝑜.
)4المرجع :هو ك ّل فرد كيميائي قادر على فقد إلكترون أو أكثر خالل تفاعل كيميائي يرمز له بـ 𝑑𝑒𝑅.
)5تفاعل األكسدة :هو تفاعل كيميائي يتم فيه فقد إلكترون أو أكثر.
)6تفاعل اإلرجاع :هو تفاعل كيميائي يتم فيه اكتساب إلكترون أو أكثر.
التحول السريع :هو تفاعل آني (لحظي) ينتهي بمجرد مالمسة المتفاعالت لبعضها. ّ )7
التحول البطيء :هو تفاعل كيميائي يستغرق عدة ثواني ،دقائق ،ساعات. ّ )8
التحول البطيء جدّا :هو تفاعل كيميائي يستغرق عدة أيّام ،أسابيع ،أشهر ،سنوات وتعتبر الجملة عندها عاطلة كيميائيا. ّ )9
)10زمن نصف التفاعل 𝟐 :𝒕𝟏⁄هو الزمن الالزم لبلوغ التفاعل نصف تقدمه النّهائي 𝑓𝑥
𝑓𝑥
= ) 𝑥(𝑡1⁄2 إذن ∶
2
)11بعض استعماالت الـ 𝟐:𝒕𝟏⁄
الالزمة لتوقف التفاعل المدروس ) (≃ 7𝑡1⁄2 يُم ّكن الـ 𝑡1⁄2من تقدير المدّة الزمنية ّ
يُم ّكن الـ 𝑡1⁄2من المقارنة بين تفاعلين من حيث سرعة التفاعل.
التحول.
ّ يُم ّكن الـ 𝑡1⁄2من اختيار الطريقة المالئمة لتتبع التّطور الزمني لمجموعة أثناء
)12البروتوكول التجريبي للمتابعة الزمنية عن طريق قيس حجم غاز :بعد وضع لمتفاعالت في الدورق ،نسدّ بإحكام
بواسطة سدادة موصولة بأنبوب معكوف يمتد إلى أنبوب اختبار معكوس في الماء ،حيث يكون هذا األنبوب مدرجا لنقيس حجم
الغاز المنطلق نسدّ هذا األنبوب باألصبع ونخرجه من الماء
صلالمغمور فيه ،نكرر العملية في فترات زمنية مختلفة لنتح ّ
على جدول القياسات.
-باستعمال جدول التقدم ومعادلة التفاعل نربط التقدم )𝑡(𝑥
بالمقدار ال ُمقاس ))𝑡(𝑉( ونجد العالقة.
ّ
-انطالقا من العالقة نستنتج قيم 𝑥 في كل لحظة.
)13البروتوكول لتجريبي للمتابعة الزمنية عن طريق قيس ضغط غز منطلق:
-نضع المتفاعالت في حوجلة.
-نغلقها بإحكام بواسطة سدادة موصولة بجهاز قياس الضغط.
-عند قياس ضغط الغاز في لحظات زمنية مختلفة نتحصل على جدول للقياسات.
-من جدول تقدم التفاعل نربط المقدار الفيزيائي الضغط بالتقدم 𝑥 للتفاعل المدروس.
-من العالقة السابقة نستنتج قيم 𝑥 في ك ّل لحظة.
الصفحة | 1 بكالوريا 2024
األستاذ :شنايت التمرين الشامل في وحدة المتابعة الزمنية لتحول كيميائي
)14البروتوكول التجريبي عن طريق قياس الناقلية لمحلول شاردي:
-نضع المتفاعالت في بيشر.
-نغمر مسبار جهاز قياس الناقلية في المحلول الشاردي وذلك بعد ضبطه.
-نسجل قيم الناقلية في لحظات زمنية مختلفة.
-من جدول تقدم التفاعل نربط المقدار الفيزيائي الناقلية بالتقدم 𝑥 للتفاعل المدروس.
-من العالقة السابقة نستنتج قيم 𝑥 في ك ّل لحظة.
)15البروتوكول التجريبي عن طريق المعايرة اللونية:
-تقسيم المزيج االبتدائي إلى عدّة أنابيب متساوية الحجم .𝑉0
-في لحظات مختلفة … … . 𝑡3 , 𝑡2 , 𝑡1 :نأخذ أنبوبا ونضعه في بيشر يحتوي
على ماء بارد وجليد لتوقيف التفاعل في اللّحظة المعتبرة.
-نضع البيشر فوق مخالط مغناطيسي ونضيف له قليال من كاشف مناسب.
-نمأل السحاحة بالمحلول المعاير المعلوم التركيز ونسحح تدريجيا إلى غاية تغير
لون الكاشف
-نسجل 𝐸𝑉 الحجم الواجب للتكافؤ ونعيد العملية مع باقي األنابيب.
-باستعمال جدول تقدم التفاعل ومعادلة تفاعل المعايرة نربط التقدم )𝑡(𝑥
للتفاعل المدروس مع 𝐸𝑉 الحجم الالزم للحصول على التكافؤ.
)16الهدف من إضافة الماء والجليد قبل المعايرة :هو توقف التفاعل أو توقيف تطوره.
)17كيف نكشف عن التكافؤ :يتم الكشف عن التكافؤ :تغير لون الكاشف في المعايرة اللّونية
)18سرعة التفاعل :هي مقدار تغير تقدم التفاعل 𝑥 بالنسبة للزمن:
𝑥𝑑
=𝑣
𝑡𝑑
)19السرعة الحجمية للتفاعل :هي سرعة التفاعل في وحدة الحجم:
𝑥𝑑 1
𝑣𝑣𝑜𝑙 = .
𝑡𝑑 𝑉
)20سرعة تشكل فرد كيميائي :مقدار تغير كمية مادة الفرد المتشكل بالنسبة للزمن:
𝑛𝑑
=𝑣
𝑡𝑑
)21السرعة الحجمية لتشكل فرد كيميائي :هي سرعة تشكل فرد كيميائي في وحدة الحجم.
تتطور بها جملة كيميائية ويمكن أن يكون:ّ )22العامل الحركي :هو ك ّل مقدار يعمل على تغيير سرعة التفاعل التي
-سطح التالمس -الوسيط -التركيز االبتدائي للمتفاعالت. -درجة الحرارة.
)23الوساطة :هي عملية تأثير الوسيط على التفاعل الكيميائي وهي 3أنواع:
الطور (أي وسط سائل). وساطة متجانسة :الوسط التفاعلي والوسيط في نفس ّ
وساطة غير متجانسة :الوسط التفاعلي والوسيط طورين مختلفين (وسط صلب).
وساطة إنزيمية.
تحول كيميائي ،أو توقيفه ،أو تسريعه ،أو انطالقه. )24أهمية العوامل الحركية :للعوامل الحركية عدة أدوار :تبطئ ّ
)25التفسير المجهري للعوامل الحركية:
درجة الحرارة ↖ ⇐ 𝑪𝑬 ↖ ⇐ التصادمات الفعالة ↖ ⇐ 𝒗 ↖ ⇐ 𝟐↙ 𝒕𝟏/
التركيز االبتدائي ↖ ⇐ عدد األفراد الكيميائية ↖ ⇐ التصادمات الفعالة ↖ ⇐ 𝒗 ↖ ⇐ 𝟐↙ 𝒕𝟏/
وجود وسيط مناسب↖ ⇐ الطاقة الالزمة لحدوث التفاعل↙ ⇐التصادمات الفعالة ↖ ⇐ 𝑣 ↖ ⇐ ↙ 𝑡1/2
سطح التالمس ↖ ⇐ التصادمات الفعالة ↖ ⇐ 𝑣 ↖ ⇐ ↙ 𝑡1/2
الصفحة | 2 بكالوريا 2024
األستاذ :شنايت التمرين الشامل في وحدة المتابعة الزمنية لتحول كيميائي
الجزء الثاني :دراسة المتابعة الزمنية للتفاعل عن طريق قياس الحجم.
يتفاعل محلول حمض كلور الهيدروجين ) )𝑞𝑎( (𝐻3 𝑂+ (𝑎𝑞) + 𝐶𝑙 −مع األلمنيوم وفق معادلة تفاعل تام منتجا غاز ثنائي
الهيدروجين وشوارد األلمنيوم ) .(𝐴𝑙 3+
في اللحظة 𝑡 = 0ندخل عينة كتلتها 𝑔 𝑚 = 0,81من
حبيبات األلمنيوم في بالون (دورق) يحتوي على حجم
𝐿𝑚 𝑉 = 60من محلول حمض كلور الهيدروجين تركيزه المولي
.𝐶 = 0,18 𝑚𝑜𝑙. 𝐿−1نغلق البالون بسدادة مزودة بأنبوب انطالق
موصول بمقياس غاز مدرج ومنكس في حوض مائي لجمع الغاز الناتج
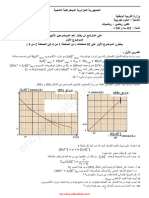
وقياس حجمه في لحظات مختلفة .النتائج المحصل عليها مكنتنا من رسم
البيان الممثل لتطور حجم الغاز المنطلق بداللة الزمن )𝑡(𝑓 = 𝑉𝐻2
ننمذج التفاعل الكيميائي الحادث بالمعادلة الكيميائية التالية:
+ 3+
)𝑞𝑎(𝑂 2𝐴𝑙(𝑠) + 6𝐻3 )𝑞𝑎(𝑙𝐴= 2 )𝑙(𝑂 + 3𝐻2 (𝑔) + 6𝐻2
)26وضح برسم تخطيطي التركيب المستعمل لقياس الحجم.
)27اكتب المعادلتين النصفيتين اإللكترونيتين لألكسدة واإلرجاع مع تحديد الثنائيتين )𝑑𝑒𝑅 (𝑂𝑥/المشاركتين في التفاعل.
)28أنشئ جدوال لتقدم التفاعل الكيميائي الحادث.
)29جد قيمة التقدم األعظمي 𝑥𝑎𝑚𝑥 ث ّم حدد المتفاعل المحد.
)30جد العالقة بين تقدم التفاعل )𝑡(𝑥 وحجم غاز ثنائي الهيدروجين الناتج )𝑡( .𝑉𝐻2
)31استنتج حجم غاز ثنائي الهيدروجين المنطلق عند نهاية التفاعل ) .𝑉𝑓 (𝐻2
)32بين أن حجم غاز ثنائي الهيدروجين المنطلق في زمن نصف التفاعل 𝑡1/2يعطى بالعالقة:
) 𝑉𝑓 (𝐻2
= ) 𝑉𝐻2 (𝑡1/2
2
ث ّم استنتج قيمة .𝑡1/2
)33بين أن سرعة التفاعل في اللحظة 𝑡 تعطى بالعالقة:
)𝑡( 1 𝑑𝑉𝐻2
=𝑣 .
𝑀𝑉3 𝑡𝑑
)34احسب قيمة هذه السرعة في اللحظة 𝑠.𝑡 = 300
)] +
𝑂 𝑚𝐴𝑙 = 𝑓([𝐻3 )35مثل بأكثر دقة ممكنة بيان كل من ) , 𝑚𝐴𝑙 = 𝑓(𝑉𝐻2
يعطى:
الحجم المولي في شروط التجربة𝑉𝑀 = 24 𝐿. 𝑚𝑜𝑙 −1 : 𝑙𝑜𝑚𝑀(𝐴𝑙) = 27 𝑔⁄
الصفحة | 3 بكالوريا 2024
األستاذ :شنايت التمرين الشامل في وحدة المتابعة الزمنية لتحول كيميائي
الجزء الثالث :دراسة المتابعة الزمنية للتفاعل عن طريق قياس الضغط.
التجربة األولى :نتابع التحول الكيميائي التام الحادث يبن معدن المغنزيوم )𝑔𝑀( ومحلول حمض كلور الهيدروجين
) .(𝐻3 𝑂+ , 𝐶𝑙 −الثنائيتان المتفاعلتان )𝑔𝑀 (𝑀𝑔2+ ⁄و ) .(𝐻3 𝑂+ ⁄𝐻2حضرنا محلوال ) (𝑆0لحمض كلور الهيدروجين
تركيزه المولي ،𝐶0في اللحظة 𝑡 = 0نضع شريطا من المغنزيوم كتلته 𝑔 𝑚0 = 13,2في إناء به حجم 𝐿 𝑉1 = 0,5من
المحلول ) .(𝑆0نمرر غاز الهيدروجين المتشكل في دورق حجمه 𝐿 𝑉 ′ = 1ودرجة الحرارة فيه 𝐾 .298
نزود الدورق بجهاز قياس الضغط ،مثلنا البيان )𝑡(𝑓 = ( 𝑃𝐻2الشكل .)1-
في نهاية التفاعل قمنا بوزن شريط المغنزيوم فوجدنا كتلته 𝑚.
)36ضع رسما تخطيطيا توضح فيه التركيب المستعمل لقياس الضغط.
)37اكتب معادلة التفاعل ،وأنشئ جدول تقدم التفاعل.
)38اكتب العالقة التي تجمع التقدم في اللحظة 𝑡 بضغط غاز الهيدروجين
،𝑃𝐻2ثم أوجد قيمة التقدم األعظمي.
)39احسب قيمة 𝐶0وقيمة الكتلة 𝑚.
)40احسب السرعة الحجمية للتفاعل في اللحظة .𝑡 = 0
)41ارسم بشكل تقريبي مع البيان السابق )𝑡(𝑔 = 𝑃𝐻2في حالة استعمال
نفس كمية المغنزيوم السابقة على شكل برادة.
𝑙𝐴𝑚 )42مثل بأكثر دقة ممكنة بيان كل من )𝑥(𝑓 = 𝑙𝐴𝑚 = 𝑓(𝑃𝐻2 ) ,
التجربة الثانية :نضع في دورق زجاجي حجما قيمته 𝐿𝑚 𝑉0 = 1000من محلول حمض كلور الماء
) (𝐻3 𝑂+ + 𝐶𝑙 −تركيزه المولي 𝐶0نصل الدورق إلى بالون زجاجي حجمه 𝐿 𝑉 = 1نلقي في الدورق كمية من
األلمنيوم كتلتها 𝑚 عند اللحظة .𝑡 = 0درجة الحرارة في البالون ثابتة وقيمتها 𝐾 𝑇 = 293
المعادلة المنمذجة للتفاعل الحاصل هي:
+ 3+
2𝐴𝑙(𝑠) + )𝑞𝑎(𝑂 6𝐻3 = )𝑞𝑎(𝑙𝐴2 𝑂 + 3𝐻2 (𝑔) + 6𝐻2
)43أنشئ جدوال لتقدم التفاعل الحادث.
)44بين أن ضغط غاز الهيدروجين في كل لحظة يعطى بالعالقة 𝑃(𝐻2 ) = 7.3 × 106 𝑥 :حيث 𝑥 هو تقدم التفاعل.
بواسطة برمجية مناسبة مكنت من الحصول على البيان )𝑡(𝑓 = 𝑦 (الشكل )5-حيث𝑦(𝑡) = 𝑛(𝐴𝑙) − 𝑛(𝐻2 ) :
باالستعانة بالبيان وجدول تقدم التفاعل جد:
)45التقدم األعظمي 𝑥𝑎𝑚𝑥.
)46أعظم قيمة 𝑥𝑎𝑚𝑃 للضغط في البالون.
)47المتفاعل المحد.
)48التركيز المولي .𝐶0
)49الكتلة 𝑚.
)50بين أنه عند زمن نصف التفاعل يكون:
𝑓𝑦
𝑙𝑜𝑚 𝑦(𝑡1⁄2 ) = + 0,1
2
1 )𝑡(𝑦𝑑
× 𝑣(𝑡) = − )51بين أن سرعة التفاعل تعطى بالعبارة:
5 𝑡𝑑
جد قيمتها في اللحظة.𝑡 = 6 min :
)52ارسم شكال تقريبيا لبيان )𝑡(𝑓 = ) .𝑃(𝐻2
ثابت الغازات 𝐼𝑆 .𝑅 = 8,31 𝑙𝑜𝑚𝑀(𝑀𝑔) = 24 𝑔⁄ 𝑙𝑜𝑚𝑀(𝐴𝑙) = 27 𝑔⁄ يعطى:
الصفحة | 4 بكالوريا 2024
األستاذ :شنايت التمرين الشامل في وحدة المتابعة الزمنية لتحول كيميائي
الجزء الرابع :دراسة المتابعة الزمنية للتفاعل عن طريق قياس الناقلية.
التجربة األولى :عند اللحظة 𝑡 = 0نضيف إلى بيشر يحتوي على حجم 𝐿𝑚 𝑉0 = 100من محلول كلور الهيدروجين
التحول الكيميائي التام بواسطة قياس
ّ تركيزه المولي 𝐶0كمية من مسحوق األلمنيوم كتلتها 𝑔𝑚 𝑚0 = 270ث ّم نتابع تطور
𝜎
الناقلية النوعية للمزيج التفاعلي وباستعمال نتائج القياس تمكنا من تمثيل البيان 𝑡 بداللة التقدم 𝑥 في الشكل ،3-والبيان 𝑡𝜎 𝜎0 −
𝜎0
بداللة الزمن 𝑡 في الشكل .4-
4
معادلة المنمذجة للتفاعل الحاصل هي:
+ 3+
2𝐴𝑙(𝑠) + )𝑞𝑎(𝑂 6𝐻3 = )𝑞𝑎(𝑙𝐴2 𝑂 + 3𝐻2 (𝑔) + 6𝐻2
)53اعتمادا على جدول التقدم حدّد المتفاعل المحدّ واستنتج قيمة التركيز المولي .𝐶0
)54أكتب عبارة الناقلية النوعية 𝜎0للمزيج عند اللحظة 𝑡 = 0ثم أحسب قيمتها.
)55أثبت أن عبارة الناقلية النوعية في اللحظة 𝑡 تعطى بالعالقة 𝜎(𝑡) = 𝜎0 + 𝐴𝑥 :حيث 𝑥 هو تقدم التفاعل و 𝐴 ثابت
يطلب تعيين قيمته.
)56أوجد عبارة الناقلية النوعية 𝑓𝜎 عند نهاية التفاعل.
)57أحسب قيمة الناقلية النوعية الشاردية لشاردة األلمنيوم . 𝜆𝐴𝑙3+
عرف السرعة الحجمية وبيّن أنّها تكتب على الشكل: ّ )58
) 𝑡𝜎 −1 𝑑(𝜎0 −
= 𝑙𝑜𝑣𝜈
𝑉 𝐴. 𝑡𝑑
ث ّم أحسب قيمتها عند اللحظة .𝑡 = 0
)59جد الناقلية النوعية النهائية للمزيج 𝑓𝜎.
)60بين أنه عند زمن نصف التفاعل ) (𝑡1⁄2تكون الناقلية النوعية للمزيج المتفاعل:
𝑓𝜎 𝜎0 +
= ) 𝜎(𝑡1⁄2
2
ثم استنتج زمن نصف التفاعل.
)61جد زمن نصف التفاعل بطريقة أخرى.
)62احسب السرعة الحجمية للتفاعل عند اللحظة .𝑡 = 0
𝑙𝐴𝑚 )63مثل بأكثر دقة ممكنة بيان كل من )𝜎(𝑓 = 𝑥 = 𝑓(𝜎) , 𝜎 = 𝑓(𝑥) ,
𝑙𝑜𝑚𝑀(𝐴𝑙) = 27 𝑔⁄ 𝜆(𝐻3 𝑂+ ) = 35 𝑚𝑆. 𝑚2 . 𝑚𝑜𝑙 −1 𝜆(𝐶𝑙 − ) = 7,36 𝑚𝑆. 𝑚2 . 𝑚𝑜𝑙 −1
الصفحة | 5 بكالوريا 2024
األستاذ :شنايت التمرين الشامل في وحدة المتابعة الزمنية لتحول كيميائي
التجربة الثانية :ندرس حركية التفاعل الحادث بين نوع كيميائي 𝐻𝐶𝑂𝑂𝐶𝐻2 𝐶𝐻3ومحلول الصودا ) (𝑁𝑎+ , 𝑂𝐻 −
عن طريق قياس ناقلية المزيج التفاعلي بداللة الزمن.
نحقق عند اللحظة 𝑡 = 0مزيجا من محلول الصودا حجمه 𝐿𝑚 𝑉0 = 200تركيزه المولي 𝑐0و 𝑙𝑜𝑚𝑚 𝑛0 = 2
من النوع الكيميائي ،𝐻𝐶𝑂𝑂𝐶𝐻2 𝐶𝐻3نعتبر حجم المزيج التفاعلي هو 𝐿𝑚 .𝑉 = 𝑉0 = 200
معادلة التفاعل التام المنمذج للتحول الحاصل هي:
− −
)𝑞𝑎(𝑂𝐻 𝐻𝐶𝑂𝑂𝐶𝐻2 𝐶𝐻3 (𝑙) + = )𝑞𝑎(𝑂𝑂𝐶𝐻 + )𝑞𝑎(𝐻𝑂 𝐶𝐻3 𝐶𝐻2
باستعمال برمجية مناسبة تحصلنا على المنحنيين الموضحين في الشكل4-
(تطور الناقلية بداللة تقدم التفاعل) والشكل( 5-تطور الناقلية بداللة الزمن).
)64هل التفاعل الكيميائي الحادث سريع أم بطيء؟ علل.
)65اذكر األنواع الكيميائية المسؤولة عن ناقلية المزيج التفاعلي.
)66أنشئ جدوال لتفدم التفاعل.
)67بين أن ناقلية المزيج التفاعلي في لحظة 𝑡 تكتب بالشكل:
𝐾
) 𝐺 = (𝜆𝐻𝐶𝑂𝑂− − 𝜆𝐻𝑂− )𝑥 + 𝐾. 𝑐0 (𝜆𝐻𝑂− + 𝜆𝑁𝑎+
𝑉
حيث 𝐾 :ثابت خلية قياس الناقلية.
الشكل )68اعتمادا على المنحنى (الشكل ،)4-جد قيمة كل من ثابت الخلية
𝐾 والتركيز المولي االبتدائي .𝑐0
)69انطالقا من المنحنيين السابقين ،جد التركيب المولي للمزيج
التفاعلي عند اللحظة 𝑛𝑖𝑚 .𝑡 = 15
)70بين أن عبارة السرعة الحجمية للتفاعل عند لحظة 𝑡 تكتب
بالشكل:
1 𝐺𝑑
= 𝑉𝑣 .
𝑡𝑑 ) 𝐾(𝜆𝐻𝐶𝑂𝑂− − 𝜆𝐻𝑂−
ثم احسب قيمة السرعة الحجمية للتفاعل عند اللحظة 𝑛𝑖𝑚 .𝑡 = 15
معطيات:
-الناقليات النوعية المولية الشاردية عند درجة الحرارة.25°𝐶 :
−
𝑂𝐻. -يهمل التركيز المولي لشوارد الهيدرونيوم 𝐻3 𝑂+أمام التركيز المولي لشوارد الهيدروكسيد
𝜆(𝑁𝑎+ ) = 5 𝑚𝑆. 𝑚2 . 𝑚𝑜𝑙 −1 𝜆(𝐻𝑂− ) = 20 𝑚𝑆. 𝑚2 . 𝑚𝑜𝑙 −1
𝜆(𝐻𝐶𝑂𝑂− ) = 5,5 𝑚𝑆. 𝑚2 . 𝑚𝑜𝑙 −1
الصفحة | 6 بكالوريا 2024
األستاذ :شنايت التمرين الشامل في وحدة المتابعة الزمنية لتحول كيميائي
الجزء الخامس :دراسة المتابعة الزمنية للتفاعل عن طريق قياس الكتلة.
+ −
)𝑞𝑎(𝑂 (𝐻3الذي )𝑞𝑎(𝑙𝐶 + التجربة :1لمتابعة تطور التحول الحادث بين معدن األلمنيوم 𝑙𝐴 ومحلول كلور الهيدروجين )
ينمذج بتفاعل كيميائي ذي المعادلة:
+ 3+
2𝐴𝑙(𝑠) + )𝑞𝑎(𝑂 6𝐻3 = )𝑞𝑎(𝑙𝐴2 𝑂 + 3𝐻2 (𝑔) + 6𝐻2
ندخل في اللحظة 𝑡 = 0صفيحة من األلمنيوم كتلتها 𝑔 𝑚 = 1,08بواسطة خيط داخل محلول حمض كلور الهيدروجين
حجمه 𝐿𝑚 𝑉 = 90تركيزه 𝐶 ومن لحظة إلى اخرى نخرج الصفيحة ونزنها ث ّم نعيدها إلى المحلول.
إن المنحنى البياني الموالي يمثل تغيرات كتلة صفيحة األلمنيوم بداللة الزمن )𝑡(𝑓 = 𝑚 ،نعتبر حجم الوسط التفاعلي ثابتا
خالل مدة التحول وأن درجة الحرارة ثابتة.
)71حدد الثنائيتين )𝑑𝑒𝑅 (𝑂𝑥 ⁄الداخلتان في التفاعل مع كتابة المعادلتين
النصفيتين.
)72أنشئ جدول تقدم التفاعل.
)73هل المزيج ستوكيومتري؟ حدد المتفاعل المحد.
)74أوجد التقدم األعظمي 𝑥𝑎𝑚𝑥 للتفاعل واستنتج قيمة التركيز المولي 𝐶.
)75باستعمال جدول تقدم التفاعل بين صحة العالقة:
] 𝑑𝑚 𝑀. 𝑉 𝑑[𝐻3 𝑂+ ] 𝑑[𝐻3 𝑂+
= × × = 0,81
𝑡𝑑 3 𝑡𝑑 𝑡𝑑
+
)𝑞𝑎(𝑂 (𝐻3في اللحظتين 𝑡 = 10 𝑚𝑖𝑛،𝑡 = 0 𝑚𝑖𝑛 :ماذا تالحظ؟ )76احسب السرعة الحجمية الختفاء شوارد )
)77بين أن كتلة األلمنيوم المتبقية في اللحظة ( 𝑡 = 𝑡1/2زمن نصف التفاعل) تعطى بالعبارة:
𝑓𝑚 𝑚0 +
= 𝑚𝑡1⁄2
2
حيث 𝑓𝑚 هي كتلة األلمنيوم المتبقية في الحالة النهائية .استنتج بيانيا قيمة .𝑡1/2
)78بين أن عبارة السرعة الحجمية للتفاعل تعطى بـ:
)𝑡(𝑚𝑑 1
𝑣𝑣𝑜𝑙 = −
𝑡𝑑 𝑀𝑉2
)79احسب قيمتها في اللحظة 𝑛𝑖𝑚.𝑡 = 3
3+
)80احسب عند 𝑛𝑖𝑚 𝑡 = 3كال من حجم الهيدروجين 𝑉𝐻2وتركيز شوارد األلمنيوم )𝑞𝑎(𝑙𝐴.
الصفحة | 7 بكالوريا 2024
األستاذ :شنايت التمرين الشامل في وحدة المتابعة الزمنية لتحول كيميائي
التجربة :2
المغنزيوم من المعادن ال ُم ْر ِجعَة التي تستعمل في الصناعات التَّحويليَّة لحماية علب المصبرات من التآكل.
يتفاعل معدن المغنيزيوم مع محلول حمض كلور الهيدروجين ،ويرافق التّفاعل انطالق غاز ثنائي الهيدروجين.
يهدف التمرين إلى دراسة حركية هذا التّحول.
يعطى ❖ :الكتلة المولية للمغنيزيوم𝑀(𝑀𝑔) = 24 𝑔. 𝑚𝑜𝑙 :
−1
❖ الحجم المولي للغاز في شروط التجربة𝑉𝑀 = 24 𝐿. 𝑚𝑜𝑙 −1 :
❖ نعتبر أن حجم المزيج التفاعلي يبقى ثابتا خالل مدة التحول ،وأن الغاز المنطلق غاز مثالي.
يُنَ ْمذَج التحول الكيميائي التام والبطيء الذي يحدث بين معدن المغنيزيوم )𝑠(𝑔𝑀 ومحلول حمض كلور الهيدروجين
+ −
)𝑞𝑎(𝑂 (𝐻3بتفاعل كيميائي معادلته: )𝑞𝑎(𝑙𝐶 + )
+ 2+
)𝑙(𝑂 𝑀𝑔(𝑠) + 2𝐻3 𝑂(𝑎𝑞) = 𝑀𝑔(𝑎𝑞) + 𝐻2 (𝑔) + 2𝐻2
❖ لدراسة هذا التحول الكيميائي ،ندخل عند اللحظة 𝑡 = 0في دورق ،شريط مغنزيوم كتلته ،𝑚0وحجما 𝐿𝑚 𝑉0 = 10
من محلول حمض كلور الهيدروجين ذي التركيز المولي ،𝐶0ثم نضيف الماء المقطر حتى يصبح حجم المحلول الممدد
𝐿𝑚 .𝑉𝑇 = 25نغلق الدورق بسدادة مزودة بأنبوب انطالق موصول إلى أنبوب مدرج ومنكس في حوض مائي.
)81استنتج الثنائيتان )𝑑𝑒𝑟 (𝑜𝑥 ⁄المشاركتين في التفاعل.
)82أنجز جدوال يصف تقدم التفاعل.
❖ مكنت القياسات التجريبية ،الحصول على المنحنى البياني الممثل لتغيرات كتلة المغنزيوم 𝑔𝑀𝑚 المتبقي بداللة الزمن
+
)𝑞𝑎(𝑂 [𝐻3بداللة تقدم التفاعل 𝑥( .الشكل.)6- (الشكل ،)5-والمنحنى البياني الممثل لتغيرات ]
)83حدد المتفاعل المحد ،ثم استنتج 𝑚0كتلة المغنزيوم المستعملة ،و ) 𝑉𝑓 (𝐻2حجم ثنائي الهيدروجين النهائي.
)84استنتج سلم الرسم الناقص في البيات )𝑡(𝑓 = 𝑔𝑀𝑚 الممثل في الشكل.5-
)85جد قيمة التركيز المولي 𝐶0لمحلول حمض كلور الهيدروجين المستعمل.
)86حدد زمن نصف التفاعل .𝑡1⁄2
)87بين أن عبارة السرعة الحجمية للتفاعل هي:
1 𝑔𝑀𝑚𝑑
𝑣𝑣𝑜𝑙 = − ×
)𝑔𝑀(𝑀 𝑉𝑇 . 𝑡𝑑
)88احسب قيمتها في اللحظة 𝑡 = 0بـ .𝑚𝑜𝑙. 𝐿−1 . 𝑚𝑖𝑛−1
)89استنتج السرعة الحجمية الختفاء شوارد الهيدرونيوم عند نفس اللحظة.
الصفحة | 8 بكالوريا 2024
األستاذ :شنايت التمرين الشامل في وحدة المتابعة الزمنية لتحول كيميائي
الجزء السادس :دراسة المتابعة الزمنية للتفاعل بواسطة المعايرة اللّونية
أوال :بعد إصابة أحد التالميذ بداء كورونا ) (𝐶𝑜𝑣𝑖𝑑19قرر األستاذ رفقة التالميذ تعقيم فناء المدرسة وبعض قاعات
التدريس بمحلول مطهر ومعقم يحتوي أساسا على ماء جافيل ،تعتبر شاردة الهيبوكلوريت 𝐶𝑙𝑂−الشاردة الفعالة في ماء
جافيل التي نحصل عليها من تفاعل غاز خطير عند استنشاقه حيث يسبب االختناق وهو غاز الكلور ) (𝐶𝑙2مع هيدروكسيد
الصوديوم وفق المعادلة التالية:
− − −
𝐻𝑂𝐶𝑙2 + 2 𝑙𝐶 = 𝐶𝑙𝑂 + 𝑂 + 𝐻2
تتفكك شاردة الهيبوكلوريت في وسط قاعدي ببطء وفق المعادلة:
2𝐶𝑙𝑂− = 2𝐶𝑙 − + 𝑂2
أخذ األستاذ قارورة ماء جافيل مكتوب عليها )𝑙(12°𝐶ℎ
مالحظة :الدرجة الكلورومترية لماء جافيل )𝐥𝐡𝐂 (°تمثل حجم غاز الكلور باللتر مقاس في الشرطين النظاميين الذي
يعطيه لتر من ماء جافيل.
قبل استعمال القارورة لتحضير المعقم أراد األستاذ التأكد من هذه الكتابة فقام بالتجربتين التاليتين:
التجربة :1قام بأخذ حجما 𝑉0من قارورة ماء جافيل ذات التركيز 𝐶0ومدده 10مرات للحصول على محلول )𝑆( حجمه
𝐿𝑚 𝑉 = 50وتركيزه 𝐶.
التجربة :2أخذ من المحلول )𝑆( بواسطة ماصة حجما 𝐿𝑚 𝑉1 = 10ونضعه في بيشر ،نضيف عند اللحظة
𝑡 = 0للبيشر حجما 𝐿𝑚 𝑉2 = 20من محلول يود البوتاسيوم ) (𝐾 + , 𝐼 −تركيزه المولي .𝐶2 = 0,1 𝑚𝑜𝑙. 𝐿−1
)90اذكر البروتوكول التجريبي لتحضير المحلول )𝑆(.
)91برهن أن الدرجة الكلورومترية°𝐶ℎ𝑙 = 𝐶0 . 𝑉𝑀 :
)92اكتب معادلة التفاعل التام الحاصل في التجربة .2
)93أنشئ جدول لتقدم التفاعل الحاصل في التجربة .2
نتابع هذا التفاعل بمعايرة ثنائي اليود الناتج من حين األخر بواسطة محلول مائي لثيوكبريتات الصوديوم
) (2𝑁𝑎+ + 𝑆2 𝑂32−تركيزه المولي ،𝐶3 = 88 𝑚𝑚𝑜𝑙. 𝐿−1ثم قمنا بتمثيل بيان تغيرات الحجم الالزم للتكافؤ عند
كل معايرة لثنائي اليود في المزيج بداللة الزمن.
)94اكتب معادلة تفاعل المعايرة.
)95حدد الخصائص التي يجب أن يتميز بها تفاعل المعايرة؟
)96اكتب عبارة كمية مادة اليود ) 𝑛(𝐼2بداللة الحجم الالزم
للتكافؤ 𝐸𝑉.
)97أوجد قيمة 𝑥𝑎𝑚𝑥 ،ثم استنتج المتفاعل المحد للتفاعل الحاصل
في التجربة .2
)98احسب التركيز المولي ] [𝐶𝑙𝑂−في المحلول )𝑆( ،ثم استنتج
التركيز المولي له قبل التمديد.
)99احسب الدرجة الكلورومترية لماء جافيل في القارورة ،هل حضر هذا المحلول حديثا؟
)100احسب السرعة الحجمية للتفاعل عند اللحظة 𝑛𝑖𝑚 .𝑡 = 4
)101لماذا ينصح صانعو ماء جافيل بعدم خلطه مع مواد منظفة أخرى ذات طبيعة حمضية؟
−
) 𝑙𝐶(𝐶𝑙𝑂 ⁄ − ) (𝐼2 ⁄𝐼 − ) (𝑆4 𝑂62− ⁄𝑆2 𝑂32− تعطى الثنائيات:
الصفحة | 9 بكالوريا 2024
األستاذ :شنايت التمرين الشامل في وحدة المتابعة الزمنية لتحول كيميائي
ثانيا :للماء األكسجيني 𝐻2 𝑂2أهمية بالغة ،فهو معالج للمياه المستعملة ومطهر للجروح ومعقم في الصناعات الغذائية ،الماء
األكسجيني يتفكك ذاتيا بتحول بطيء جدا في الشروط العادية معطيا غاز ثنائي األكسجين والماء وفقا للمعادلة المنمذجة للتفاعل
الكيميائي:
)𝑙(𝑂 2𝐻2 𝑂2 (𝑎𝑞) = 𝑂2 (𝑔) + 2𝐻2
)102ماذا نقصد بقولنا "يتفكك ذاتيا"؟
)103استخرج الثنائيات ) 𝑑𝑒𝑅 (𝑂𝑥⁄المشاركة في التفاعل.
لدراسة تطور التفكك الذاتي للماء األكسجيني بداللة الزمن ،نأخذ مجموعة
أنابيب اختبار يحتوي كل منها على حجم 𝐿𝑚 𝑉0 = 10من هذا المحلول
ونضعها عند اللحظة 𝑡 = 0في حمام مائي درجة حرارته ثابتة.
عند كل لحظة 𝑡 ،نفرغ أنبوبة اختبار في بيشر ونضيف إليه ماء وقطع
جليد وقطرات من حمض الكبريت المركز) (2𝐻3 𝑂+ + 𝑆𝑂42−ث ّم
نعاير المزيج بمحلول مائي لثاني كرومات البوتاسيوم
) (2𝐾 + + 𝐶𝑟2 𝑂72−تركيزه المولي 𝑐 = 0,1 𝑚𝑜𝑙. 𝐿−1فنحصل
في كل مرة على الحجم 𝐸𝑉 الالزم لبلوغ التكافؤ.
سمحت النتائج المحصل عليها برسم المنحنى الممثل في الشكل.
معادلة تفاعل المعايرة هي:
+ 3+
3𝐻2 𝑂2 (𝑎𝑞) + )𝑞𝑎( 𝐶𝑟2 𝑂72− + )𝑞𝑎(𝑂 8𝐻3 = 3𝑂2 (𝑔) + )𝑞𝑎(𝑟𝐶2 )𝑙(𝑂 + 15𝐻2
)104اكتب المعادلتين النصفيتين لألكسدة واإلرجاع الموافقتين لهذا التفاعل.
)105هل يمكن اعتبار حمض الكبريت كوسيط في هذا التفاعل؟ علّل.
)106هل يؤثر إضافة الماء وقطع الجليد على قيمة حجم التكافؤ 𝐸𝑉؟ لماذا؟
)107عبر عن التركيز المولي ] [𝐻2 𝑂2لمحلول الماء األكسجيني بداللة 𝑐 و 𝐸𝑉 و .𝑉0
)108القارورة التي أخذ منها الماء األكسجيني المستخدم في هذه التجربة كتب عليها الداللة )𝑉 (10أي( :كل 𝐿 1من
محلول الماء األكسجيني يحرر 𝐿 10من غاز ثنائي األكسجيني 𝑂2في الشرطين النظاميين).
-هل المحلول محضرا حديثا؟ علّل.
باالعتماد على المنحنى والعبارة المتوصل إليها في السؤال 2-جد:
)109زمن نصف التفاعل .𝑡1/2
)110عبارة السرعة الحجمية الختفاء )𝑞𝑎( 𝐻2 𝑂2بداللة 𝐸𝑉.
)111قيمة السرعة الحجمية الختفاء الماء األكسجيني عند اللحظتين 𝑠 .𝑡2 = 600𝑠،𝑡1 = 200ماذا تالحظ؟ علّل.
يعطى.𝑉𝑀 = 22,4 𝐿. 𝑚𝑜𝑙 −1 :
الصفحة | 10 بكالوريا 2024
األستاذ :شنايت التمرين الشامل في وحدة المتابعة الزمنية لتحول كيميائي
تصحيح الجزء الثاني :دراسة المتابعة الزمنية للتفاعل عن طريق قياس الحجم.
)26الرسم التخطيطي للتركيب المستعمل لقياس الحجم:
انظر السؤال 13في الجزء األول
)27المعادلتين النصفيتين:
3+ − 3+
= )𝑠(𝑙𝐴 )𝑞𝑎(𝑙𝐴 𝑒+ 3 )𝑞𝑎(𝑙𝐴( ) )𝑠(𝑙𝐴⁄
+ +
)𝑞𝑎(𝑂 2𝐻3 )𝑙(𝑂 + 2𝑒 − = 𝐻2 (𝑔) + 2𝐻2 )𝑞𝑎(𝑂 (𝐻3 ) )𝑔( ⁄𝐻2
)28جدول تقدم التفاعل:
+ 3+
المعادلة )𝑠(𝑙𝐴2 = )𝑞𝑎(𝑂 + 6𝐻3 )𝑙(𝑂 2𝐴𝑙(𝑎𝑞) + 3𝐻2 (𝐴𝑔) + 6𝐻2
التقدم الحالة كميات المادة )𝑙𝑜𝑚(
𝑥 = 0ابتدائية 0,03 1,08 × 10−2 0 0
بزيادة
−2
انتقالية 𝑥 𝑥0,03 − 2 𝑥1,08 × 10 − 6 𝑥2 𝑥3
−2
نهائية 𝑓𝑥 𝑓𝑥0,03 − 2 𝑓𝑥1,08 × 10 − 6 𝑓𝑥2 𝑓𝑥3
𝑙𝑜𝑚 𝑥𝑚𝑎𝑥 = 1,8 × 10−3المتفاعل المحد هو.𝐻3 𝑂+ : )29
𝑉𝐻2
=𝑥 )30
𝑀𝑉3
𝑉𝑓 (𝐻2 ) = 0,13 𝐿 )31
𝑥𝑎𝑚𝑥
= ) 𝑥(𝑡1⁄2 )32
2
) 3𝑉𝑀 . 𝑥𝑚𝑎𝑥 𝑉𝑓(𝐻2
= 𝑀𝑉𝑉𝐻2 (𝑡1⁄2 ) = 𝑥(𝑡1⁄2 ). 3 =
2 2
𝑠𝑡1⁄2 ≃ 300 قيمة :𝑡1⁄2
𝑥𝑑 𝑑 𝑉𝐻2
=𝑣 ) ( = )33
𝑡𝑑𝑀𝑉𝑑𝑡 3
1 𝑑𝑉𝐻2
=𝑣
𝑡𝑑 𝑀𝑉3
𝑠𝑣 = 2,0 × 10−6 𝑚𝑜𝑙 ⁄ )34
)35
الصفحة | 11 بكالوريا 2024
األستاذ :شنايت التمرين الشامل في وحدة المتابعة الزمنية لتحول كيميائي
تصحيح الجزء الثالث :دراسة المتابعة الزمنية للتفاعل عن طريق قياس الضغط.
التجربة :1
)36رسم تخطيطي للتركيب المستعمل لقياس الضغط.
انظر السؤال رقم 14في الجزء األول
)37معادلة التفاعل:
𝑀𝑔 = 𝑀𝑔2+ + 2𝑒 −
𝑂 2𝐻3 𝑂+ + 2𝑒 − = 𝐻2 + 2𝐻2
̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅̅
𝐻 𝑀𝑔 + 2𝐻 𝑂+ = 𝑀𝑔2+ + 𝑂 𝐻+ 2
)𝑠( )𝑞𝑎( 3 )𝑞𝑎( )𝑔( 2 )𝑙( 2
+ 2+
)𝑞𝑎(𝑂 𝑀𝑔(𝑠) + 2𝐻3 )𝑞𝑎(𝑔𝑀 = )𝑙(𝑂 + 𝐻2 (𝑔) + 2𝐻2
الحالة االبتدائية 𝑛0 𝑛1 0 0 بزيادة
الحالة االنتقالية 𝑥 𝑛0 − 𝑥𝑛1 − 2 𝑥 𝑥 بزيادة
الحالة النهائية 𝑓𝑥 𝑛0 − 𝑓𝑥𝑛1 − 2 𝑓𝑥 𝑓𝑥 بزيادة
)38عبارة )𝑡(𝑥 بداللة )𝑡(𝑃:
)𝑡( 𝑥(𝑡) = 𝑛𝐻2 من جدول تقدم التفاعل لدينا:
𝑃(𝑡)×𝑉 ′
= )𝑡( 𝑛𝐻2 من قانون الغازات المثالية:
𝑇𝑅
𝑉′
= )𝑡( 𝑥 )𝑡(𝑃 بالتساوي نجد:
𝑇𝑅
𝑉′ 10−3 𝑚3
= 𝑚𝑥 = 𝑥𝑎𝑚𝑃 × 1,24 × 105 ⇒ حساب 𝑚𝑥𝒙𝒎 = 𝟎, 𝟎𝟓 𝒎𝒐𝒍 :
𝑇𝑅 8,31×298
بما أنه تبقت كمية من المغنزيوم فإن 𝐻3 𝑂+هي المتفاعل المحد. )39حساب :𝐶0
𝑛1 − 2𝑥𝑚 = 0 𝑚𝑥→ 𝑛1 = 2 𝑚𝑥→ 𝐶0 . 𝑉1 = 2
2𝑥𝑚 2 × 0,05
= 𝐶0 = 𝐿= 0,2 𝑚𝑜𝑙 ⁄
𝑉1 0,5
𝑚 13,2
= 𝑚𝑥 𝑛𝑀𝑔 (𝑡𝑓 ) = 𝑛0 − 𝑥𝑚 = 0 − − 0,05 كذلك:
𝑀 24
𝑙𝑜𝑚 𝑛𝑀𝑔 (𝑡𝑓 ) = 0,550 − 0,050 = 0,5
𝑓𝑚
= ) 𝑓𝑡( 𝑔𝑀𝑛 𝑔 ⇒ 𝑚𝑓 = 𝑀 × 𝑛𝑀𝑔 (𝑡𝑓 ) = 24 × 0,5 = 12 وبما ّ
أن:
𝑀
)40السرعة الحجمية للتفاعل في اللحظة :𝑡 = 0
)𝑡(𝑥𝑑 1
× = )𝑡( 𝑙𝑜𝑣𝑣
𝑉1 𝑡𝑑
𝑉′ 𝑉′ )𝑡(𝑃𝑑
= )𝑡(𝑥 )𝑡(𝑃 . = )𝑡( 𝑙𝑜𝑣𝑣 ⇒ .
𝑇𝑅 𝑡𝑑 𝑅. 𝑇. 𝑉1
معامل توجيه المماس للبيان عند :𝑡 = 0
𝑑𝑃(0) (1,2 − 0) × 105
= 𝑛𝑖𝑚= 8 × 103 𝑃𝑎⁄
𝑡𝑑 )(15 − 0
1 10−3
= )𝑡( 𝑙𝑜𝑣𝑣 ⇒ ( ) × 8 × 103
0,5 8,31 × 298
𝑛𝑖𝑚 𝑣𝑣𝑜𝑙 (0) = 6,46 × 10−3 𝑚𝑜𝑙 ⁄𝐿.
الصفحة | 12 بكالوريا 2024
األستاذ :شنايت التمرين الشامل في وحدة المتابعة الزمنية لتحول كيميائي
)41البيان𝑃𝐻2 = 𝑔(𝑡) :
في حالة استعمال نفس كمية المغنزيوم على شكل برادة تزداد سرعة التحول وتنقص مدته.
)42
التجربة :2
يف انتظار إتمام كتابة الحل
تصحيح الجزء الرابع :دراسة المتابعة الزمنية للتفاعل عن طريق قياس الناقلية.
يف انتظار إتمام كتابة الحل
الصفحة | 13 بكالوريا 2024
األستاذ :شنايت التمرين الشامل في وحدة المتابعة الزمنية لتحول كيميائي
التجربة الثانية:
)63التفاعل الحادث بطيء ألن مدته تقدر بعدة دقائق (الشكل .)5
𝑎𝑁. +
)64األفراد الكيميائية المسؤولة عن الناقلية, 𝐻𝑂− , 𝐻𝐶𝑂𝑂− :
)65جدول تقدم التفاعل:
𝐻𝐶𝑂𝑂𝐶𝐻2 𝐶𝐻3 + = 𝐻𝑂− 𝐻𝐶𝑂𝑂− + 𝐻𝑂 𝐶𝐻3 𝐶𝐻2
الحالة االبتدائية 𝑛0 𝑉 𝐶0 . 0 0
الحالة االنتقالية 𝑥 𝑛0 − 𝑥 𝐶0 𝑉 − 𝑥 𝑥
الحالة النهائية 𝑓𝑥 𝑛0 − 𝑓𝑥 𝐶0 𝑉 − 𝑓𝑥 𝑓𝑥
)66عبارة الناقلية:
]− ]− ]+
; 𝜎𝐾 = 𝐺 𝑎𝑁[ 𝜎 = 𝜆𝐻𝐶𝑂𝑂− [𝐻𝐶𝑂𝑂 + 𝜆𝐻𝑂− [𝐻𝑂 + 𝜆𝑁𝑎+
)] 𝐺 = 𝐾 (𝜆𝐻𝐶𝑂𝑂− [𝐻𝐶𝑂𝑂− ] + 𝜆𝐻𝑂− [𝐻𝑂− ] + 𝜆𝑁𝑎+ [𝑁𝑎+
𝑥 𝑥 𝐶0 𝑉 −
𝐺 = 𝐾 (𝜆𝐻𝐶𝑂𝑂− + 𝜆𝐻𝑂− ) + 𝜆𝑁𝑎+ 𝐶0
𝑉 𝑉
𝐾
) 𝐺 = (𝜆𝐻𝐶𝑂𝑂− − 𝜆𝐻𝑂− )𝑥 + 𝐾𝐶0 (𝜆𝐻𝑂− + 𝜆𝑁𝑎+
𝑉
)67قيمة ثابت الخلية 𝐾 :من الشكل 𝐺 = 𝑎𝑥 + 𝑏 :4
𝑆 𝑏 = 2,5 × 10−3 و 𝑎 = −0,75 𝑆. 𝑚𝑜𝑙−1 حيث 𝑎 الميل
بالمطابقة مع العالقة النظرية:
𝑉𝑎 𝐾 2,5 × 10−3
=𝐾 ) 𝑎 = (𝜆𝐻𝐶𝑂𝑂− − 𝜆𝐻𝑂− = 𝐶0
) (𝜆𝐻𝐶𝑂𝑂− − 𝜆𝐻𝑂− 𝑉 ) 𝐾 (𝜆𝑁𝑎+ + 𝜆𝐻𝑂−
)68التركيب المولي للمزيج عند 𝑛𝑖𝑚 𝑡 = 15
𝑆𝑚 𝐺 = 1,6 يكون 𝑛𝑖𝑚 𝑡 = 15 من الشكل 5عند
𝑙𝑜𝑚𝑚 𝑥 = 1,2 يكون 𝑆𝑚 𝐺 = 1,6 من الشكل 4عند
لدينا 𝑙𝑜𝑚𝑚 𝑛0 = 2
= 𝐻𝐶𝑂𝑂𝐶𝐻2 𝐶𝐻3 + 𝐻𝑂− 𝐻𝑂 𝐻𝐶𝑂𝑂− + 𝐶𝐻3 𝐶𝐻2
𝑥 𝑛0 − 𝑥 𝐶0 𝑉 − 𝑥 𝑥
𝑛𝑖𝑚 𝑡 = 15
𝑙𝑜𝑚𝑚 0,8 𝑙𝑜𝑚𝑚 0,8 𝑙𝑜𝑚𝑚 1,2 𝑙𝑜𝑚𝑚 1,2
)69عبارة السرعة الحجمية للتفاعل:
𝑥𝑑 1
= 𝑉𝑣
𝑡𝑑 𝑉
𝐾
=𝐺 𝜆( ) − − 𝜆𝐻𝑂− )𝑥 + 𝐾 ∙ 𝐶0 (𝜆𝑁𝑎 + + 𝜆𝐻𝑂− لدينا ∶
𝑂𝑂𝐶𝐻 𝑉
) 𝐺 (𝑡 ) − 𝐾 ∙ 𝐶0 (𝜆𝑁𝑎+ + 𝜆𝐻𝑂− باالشتقاق ) 𝑡( 𝑥𝑑 1 ) 𝑡( 𝐺𝑑
= ) 𝑡( 𝑥 ⇒ = ∙
𝐾 𝑡𝑑 𝐾 𝑡𝑑
) (𝜆𝐻𝐶𝑂𝑂− − 𝜆𝐻𝑂− 𝜆( ) − − 𝜆𝐻𝑂−
𝑉 𝑂𝑂𝐶𝐻 𝑉
1 1 ) 𝑡( 𝐺𝑑 1 ) 𝑡( 𝐺𝑑
= 𝑉𝑣 ∙ ⇒ = 𝑉𝑣 ∙
𝜆( 𝐾 𝑉 ) − − 𝜆𝐻𝑂−
𝑡𝑑 𝑡𝑑 ) 𝐾 (𝜆𝐻𝐶𝑂𝑂− − 𝜆𝐻𝑂−
𝑂𝑂𝐶𝐻 𝑉
1 ) 𝑡( 𝐺𝑑
= 𝑉𝑣 ∙
𝑡𝑑 ) 𝐾 (𝜆𝐻𝐶𝑂𝑂− − 𝜆𝐻𝑂−
𝑡 𝐺𝑑( )
[ ] = −0,035 𝑚𝑠 ∙ 𝑚𝑖𝑛−1
𝑛𝑖𝑚 𝑑𝑡 15
𝟓 𝑮 = −𝟕𝟐𝟓𝒙 + 𝟐,
الصفحة | 14 بكالوريا 2024
األستاذ :شنايت التمرين الشامل في وحدة المتابعة الزمنية لتحول كيميائي
لكن يمكن استعمال عبارة البيان الخاص بالشكل .4
)𝒕(𝑮𝒅 𝟏 𝐺 2,5 −
𝒗𝑽 = − . ومنه ∶ =𝑥 وعليه ∶
𝒕𝒅 𝑽𝟓𝟐𝟕 725
في اللحظة 𝑛𝑖𝑚 𝑡 = 15تمثل ميل المماس:
1 0 − 2,15
𝑣𝑉 = − ×
725,02 (61 − 0)60
𝒔 𝒗𝑽 = 𝟒, 𝟎𝟓 × 𝟏𝟎−𝟔 𝒎𝒐𝒍⁄𝑳.
الصفحة | 15 بكالوريا 2024
األستاذ :شنايت التمرين الشامل في وحدة المتابعة الزمنية لتحول كيميائي
تصحيح الجزء الخامس :دراسة المتابعة الزمنية للتفاعل عن طريق قياس الكتلة.
التجربة األولى:
يف انتظار إتمام كتابة الحل
التجربة الثانية:
)81استنتاج الثنائيتان المشاركتين في التفاعل:
+ 2+
)𝑞𝑎(𝑂 (𝐻3 ) )𝑔( ⁄𝐻2 )𝑞𝑎(𝑔𝑀( ) )𝑠(𝑔𝑀⁄
)82جدول تقدم التفاعل:
+ 2+
المعادلة )𝑠(𝑔𝑀 + )𝑞𝑎(𝑂 2𝐻3 )𝑙(𝑂 = 𝑀𝑔(𝑎𝑞) + 𝐻2 (𝑔) + 2𝐻2
الحالة التقدم كميات المادة )𝑙𝑜𝑚(
𝑚0
ابتدائية 𝑥=0 = )𝑔𝑀( 𝑛0 𝑛0 = 𝐶0 . 𝑉0 0 0 بوفرة
𝑀
انتقالية 𝑥 𝑥 𝑛0 (𝑀𝑔) − 𝑥𝐶0 . 𝑉0 − 2 𝑥 𝑥 بوفرة
𝑥𝑎𝑚𝑥 = 𝑓𝑥 نهائية 𝑓𝑥 𝑛0 (𝑀𝑔) − 𝑓𝑥𝐶0 . 𝑉0 − 2 𝑓𝑥 𝑓𝑥 بوفرة
+
)𝑞𝑎(𝑂 [𝐻3وبما أن التحول تام فإن )𝑠(𝑔𝑀 هو )83تحديد المتفاعل المحد :من بيان الشكل ،6-وعند نهاية التفاعل ]
𝑓
المتفاعل المحد.
)84استنتاج )𝑔𝑀( 𝑀𝑔(𝑠) :𝑚0متفاعل محد
)𝑔𝑀( 𝑚0
= 𝑓𝑥 𝑛𝑓 (𝑀𝑔) = 𝑛0 (𝑀𝑔) − − 𝑥𝑓 = 0
)𝑔𝑀(𝑀
𝑓𝑥 × )𝑔𝑀(𝑀 = )𝑔𝑀( 𝑚0 ومنه ∶
𝑙𝑜𝑚 𝑥𝑓 = 1,5 𝑚𝑚𝑜𝑙 = 1,5 × 10−3 من بيان الشكل:6-
تطبيق عددي ∶ 𝑙𝑜𝑚 𝑚0 (𝑀𝑔) = 24 × 1,5 × 10−3نجد ∶ 𝑔𝑚 𝑚0 (𝑀𝑔) = 0,036 𝑔 = 36
)85استنتاج قيمة ) :𝑉𝑓 (𝐻2من جدول التقدم:
) 𝑉𝑓 (𝐻2
𝑓𝑥 𝑉𝑓 (𝐻2 ) = 𝑉𝑀 . ومن ∶ = ) 𝑛𝑓 (𝐻2 𝑓𝑥 = من جدول التقدم ∶
𝑀𝑉
نجد ∶ 𝐿𝑚 𝑉𝑓 (𝐻2 ) = 0,036 𝐿 = 36 𝑉𝑓 (𝐻2 ) = 24 × 1,5 × 10−3
الصفحة | 16 بكالوريا 2024
األستاذ :شنايت التمرين الشامل في وحدة المتابعة الزمنية لتحول كيميائي
)86استنتاج سلم الرسم:
36
1 cm → 9 mg → 𝑚𝑐 1أي ∶ ومنه يكون سلم الرسم ∶ 𝑔𝑚 𝑚0 (𝑀𝑔) = 36
4
)87إيجاد قيمة :𝐶0
+
𝐶0 𝑉0 )𝑞𝑎(𝑂 𝑉𝑇 . [𝐻3 ]
+ 0
)𝑞𝑎(𝑂 [𝐻3 = ] ⇒ = 𝐶0
0 𝑇𝑉 𝑉0
+ −2 −1
𝐿 [𝐻3 𝑂(𝑎𝑞) ] = 30 × 10 𝑚𝑜𝑙. ومن بيان الشكل ∶ 6 −
0
25 × 30 × 10−2
= 𝐶0 = 0,75 𝑚𝑜𝑙. 𝐿−1
10
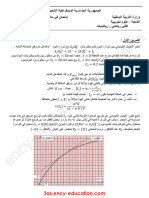
)88تحديد زمن نصف التفاعل :𝑡1⁄2من بيان الشكل5-
𝑚0 36
= )𝑔𝑀(𝑚 باإلسقاط نجد ∶ 𝑛𝑖𝑚𝑡1⁄2 = 5 = لما ∶ 𝑡 = 𝑡1⁄2فإن ∶ 𝑔𝑚 = 18
2 2
.aإثبات عبارة السرعة الحجمية للتفاعل:
)𝑡(𝑚 𝑚0 − 𝑥𝑑 1
= )𝑡( )𝑔𝑀(𝑛 𝑥(𝑡) = 𝑛0 − = 𝑙𝑜𝑣𝑣 حيث ∶ )𝑡(𝑥 𝑛(𝑀𝑔) (𝑡) = 𝑛0 −أي ∶
)𝑔𝑀(𝑀 𝑡𝑑 𝑇𝑉
)𝑡(𝑚 𝑚0 −
(𝑑 1 𝑀 ) )𝑡(𝑚𝑑 1
𝑙𝑜𝑣𝑣 = =−
𝑇𝑉 𝑡𝑑 𝑡𝑑 𝑀 𝑉𝑇 .
)89حساب قيمتها بوحدة 𝑚𝑜𝑙. 𝐿−1 . 𝑚𝑖𝑛−1لما :𝑡 = 0
𝑚𝑑 36 × 10−3
) ( =− = −4,8 × 10−3 𝑔. 𝑚𝑖𝑛−1
𝑑𝑡 𝑡=0 7,5
1
𝑣𝑣𝑜𝑙(𝑡=0) = − 𝟏× (−4,8 × 10−3 ) ⇒ 𝒗𝒗𝒐𝒍(𝒕=𝟎) = 𝟖 × 𝟏𝟎−𝟑 𝒎𝒐𝒍. 𝑳−𝟏 . 𝒎𝒊𝒏−
2,5 × 10−3 × 24
.iاستنتاج قيمة السرعة الحجمية الختفاء شوارد الهيدرونيوم عند اللحظة نفسها:
𝑣𝑣𝑜𝑙 (𝐻3 𝑂+ ) = 2 × 𝑣𝑣𝑜𝑙 = 2 × 8 × 10−3 حسب معادلة التفاعل فإن:
+ −3 −1 −1
𝑛𝑖𝑚 𝑣𝑣𝑜𝑙 (𝐻3 𝑂 ) = 16 × 10 𝑚𝑜𝑙. 𝐿 .
الصفحة | 17 بكالوريا 2024
األستاذ :شنايت التمرين الشامل في وحدة المتابعة الزمنية لتحول كيميائي
تصحيح الجزء السادس :دراسة المتابعة الزمنية للتفاعل بواسطة المعايرة اللّونية
أوال:
في انتظار إتمام كتابة الحل
ثانيا:
)102نقصد بقولنا "يتفكك ذاتيا" أن الماء األكسجيني مؤكسد في ثنائية ومرجع في ثنائية أخرى فيتفكك ذاتيا.
)103الثنائيات:
)𝑂 (𝐻2 𝑂2 ⁄𝐻2 , ) (𝑂2 ⁄𝐻2 𝑂2
)104المعادلتين النصفيتان:
+ −
𝑒𝐻2 𝑂2 (𝑎𝑞) + 2𝐻2 𝑂(𝑙) = 𝑂2 (𝑔) + 2𝐻3 𝑂(𝑎𝑞) + 2
+ 3+
)𝑞𝑎(𝑂 𝐶𝑟2 𝑂72− (𝑎𝑞) + 14𝐻3 )𝑞𝑎(𝑟𝐶+ 6𝑒 − = 2 )𝑙(𝑂 + 21𝐻2
+
)𝑞𝑎(𝑂 )𝐻3 )105ال يمكن اعتبار حمض الكبريت ) (2𝐻3 𝑂+ , 𝑆𝑂42−كوسيط ألنه استهلك في التفاعل (الشاردة
)106إضافة الماء وقطع الجليد ال تؤثر في قيمة 𝐸𝑉 ألن كمية الماء األكسجيني )𝑞𝑎( 𝐻2 𝑂2ال تتغير (التكافؤ يتعلق
بكمية المادة وليس التركيز).
)107عبارة التركيز المولي ] [𝐻2 𝑂2عند نقطة التكافؤ .جدول تقدم التفاعل( :يمكن عدم استعماله).
+ 3+
)𝑞𝑎(𝑂 3𝐻2 𝑂2 (𝑎𝑞) + 𝐶𝑟2 𝑂72− (𝑎𝑞) + 8𝐻3معادلة التفاعل )𝑞𝑎(𝑟𝐶= 3𝑂2 (𝑔) + 2 )𝑙(𝑂 + 15𝐻2
ابتدائية 0 𝑛1 𝑛2 0 0
انتقالية 𝑥 𝑥𝑛1 − 3 𝑥 𝑛2 − بوفرة 𝑥3 𝑥2 بوفرة
نهائية 𝑓𝑥 𝐸𝑥𝑛1 − 3 𝐸𝑥 𝑛2 − 𝐸𝑥3 𝐸𝑥2
عند نقطة التكافؤ المزيج ستوكيومتري.
𝑛1 𝑛2 [𝐻2 𝑂2 ]. 𝑉0 𝐸𝑉 3 × 𝐶.
= ⇒ 𝐸𝑉 = 𝐶. ⇒ = ] [𝐻2 𝑂2
3 1 3 𝑉0
)108صحة المعلومات المكتوبة على القارورة.
-حساب ] [𝐻2 𝑂2من البيان :عند 𝑡 = 0
لدينا𝑉𝐸0 = 6,2 × 4 𝑚𝑙 = 24,8 𝑚𝑙 :
بالتعويض في العبارة السابقة نجد:
3 × 0,1 × 24,8 × 10−3
= [𝐻2 𝑂2 ]0 𝐿= 0,74 𝑚𝑜𝑙 ⁄
10 × 10−3
الصفحة | 18 بكالوريا 2024
األستاذ :شنايت التمرين الشامل في وحدة المتابعة الزمنية لتحول كيميائي
-
-حساب التركيز من المعلومات المكتوبة :جدول التقدم للتفكك الذاتي للماء األكسجيني.
= )𝑞𝑎( 2𝐻2 𝑂2المعادلة 𝑂2 (𝑔) + )𝑙(𝑂 2𝐻2
ابتدائية 𝑛0 0 بوفرة
انتقالية 𝑥𝑛0 − 2 𝑥 بوفرة
نهائية 𝑥𝑎𝑚𝑥𝑛0 − 2 𝑥𝑎𝑚𝑥 بوفرة
عند تفاعل 𝐻2 𝑂2كليا نجد:
𝑛0 − 2𝑥𝑚𝑎𝑥 = 0 ⇒ 𝑥𝑎𝑚𝑥𝑛0 = 2
𝑉𝑂2
𝑥𝑎𝑚) 𝑛0 = 2𝑛0 (𝑂2 ⇒ × 𝐶. 𝑉 = 2
𝑚𝑉
𝑉10 20
× 𝐶. 𝑉 = 2 ⇒ =𝐶 𝐿= 0,892 𝑚𝑜𝑙 > 0,74 𝑚𝑜𝑙/
22,4 22,4
إذن المحلول غير حديث التحضير.
)109زمن نصف التفاعل:
𝑥𝑎𝑚𝑥 [𝐻2 𝑂2 ]0
⇒ 𝑡 = 𝑡1⁄2 = ) 𝑥(𝑡1⁄2 ⇒ [𝐻2 𝑂2 ]𝑡1⁄2 =
2 2
𝑉𝐸 (0) 24,8
= ) 𝑉𝐸 (𝑡1⁄2 = 𝐿𝑚 = 12,4
2 2
باإلسقاط على البيان نجد𝑡1⁄2 ≃ 300𝑠 :
)110عبارة السرعة الحجمية الختفاء 𝐻2 𝑂2بداللة 𝐸𝑉.
1 𝑑𝑛(𝐻2 𝑂2 ) ] 𝑑[𝐻2 𝑂2
𝑙𝑜𝑣𝑣 =− . =−
𝑉 𝑡𝑑 𝑡𝑑
𝐸𝑉 𝑑 3. 𝐶. 𝐸𝑉𝑑 𝐶3 3 × 0,1 𝐸𝑉𝑑
𝑙𝑜𝑣𝑣 ( =− )=− × =− ×
𝑡𝑑 𝑉0 𝑉0 𝑡𝑑 10 × 10−3 𝑡𝑑
)111قيمة السرعة الحجمية الختفاء . 𝐻2 𝑂2
-عند اللحظة 𝑠:𝑡1 = 200
𝑠 𝑣1 ≃ 1,10 × 10− 𝑚𝑜𝑙/𝐿.
-عند اللحظة 𝑠:𝑡1 = 600
𝑠 𝑣2 ≃ 0,44 × 10−5 𝑚𝑜𝑙/𝐿.
-نالحظ أن𝑣1 > 𝑣2 :
-التعليل :تتناقص السرعة بسبب تناقص التركيز المولي
للماء األكسجيني أثناء التفاعل.
الصفحة | 19 بكالوريا 2024
You might also like
- الأسئلة النظريةDocument10 pagesالأسئلة النظريةYeah Yeah100% (4)
- الأسئلة النظرية الوحدة الأولىDocument2 pagesالأسئلة النظرية الوحدة الأولىnourmalaklarbi29No ratings yet
- الوحدة 01 سلسلة المتابعة الزمنية عن طريق قياس الحجمDocument2 pagesالوحدة 01 سلسلة المتابعة الزمنية عن طريق قياس الحجمZizo Dark100% (2)
- سلسلة تمارينDocument6 pagesسلسلة تمارينMalak ElaichouchiNo ratings yet
- سلسلة تمارين 2Document6 pagesسلسلة تمارين 2lisaNo ratings yet
- وثيقة التلميذDocument3 pagesوثيقة التلميذIkram KimiNo ratings yet
- - - - - الحلقة (8) تمرين حول المتابعة الزمنية عن طريق المعايرة اللونيةDocument6 pages- - - - الحلقة (8) تمرين حول المتابعة الزمنية عن طريق المعايرة اللونيةAbdou0% (2)
- تجربة تعيين معمل الانتشارية السوائل م.احمد سالم البةعيشيDocument9 pagesتجربة تعيين معمل الانتشارية السوائل م.احمد سالم البةعيشيم.احمد سالمNo ratings yet
- 4 5879874055732990293Document5 pages4 5879874055732990293Loup le DésertNo ratings yet
- Physics 3se22 1trim d1Document4 pagesPhysics 3se22 1trim d1souissi souissiNo ratings yet
- Physics 3mtm22 1trim d4Document4 pagesPhysics 3mtm22 1trim d4Radovane PhysiqyeNo ratings yet
- سلسلة الوحدة 1 المتابعة الزمنيةDocument8 pagesسلسلة الوحدة 1 المتابعة الزمنيةMohamed Anis LounisNo ratings yet
- ________ (6) _____ ___ ________ _______ __ ____ ____ ________ (5)Document5 pages________ (6) _____ ___ ________ _______ __ ____ ____ ________ (5)mask blob 2No ratings yet
- الدرس 06Document16 pagesالدرس 06ayadilyes79No ratings yet
- Physics 3se20 1trim5Document3 pagesPhysics 3se20 1trim5louaiboualleg570No ratings yet
- بطاقة التلميذDocument1 pageبطاقة التلميذIkram KimiNo ratings yet
- PhysicsDocument2 pagesPhysicsyacine yacineNo ratings yet
- Exam 2021Document2 pagesExam 2021سمير دبيليNo ratings yet
- الوحدة 01 سلسلة تمارين حصص zoomDocument4 pagesالوحدة 01 سلسلة تمارين حصص zoomferiel taibiNo ratings yet
- الدرس 03Document8 pagesالدرس 03ayadilyes79No ratings yet
- الدرس 03Document7 pagesالدرس 03mekhadem rayaneNo ratings yet
- ملخّص شامل حول الوحدة 01 بكالوريا 2024Document6 pagesملخّص شامل حول الوحدة 01 بكالوريا 2024kdsfghjhfvcfvNo ratings yet
- ملخّص شامل حول الوحدة 01 بكالوريا 2024Document6 pagesملخّص شامل حول الوحدة 01 بكالوريا 2024hamoudiali19200No ratings yet
- الحلقة (7) درس المتابعة الزمنية عن طريق المعايرة اللونية PDFDocument3 pagesالحلقة (7) درس المتابعة الزمنية عن طريق المعايرة اللونية PDFu w uNo ratings yet
- درس المتابعة الزمنية عن طريق المعايرة اللونيةDocument3 pagesدرس المتابعة الزمنية عن طريق المعايرة اللونيةRedouane Reda83% (6)
- هندسة تفاعلاتDocument7 pagesهندسة تفاعلاتعبدوNo ratings yet
- ملخص المكتسبات القبلية للسنة الثالثة ثانويDocument4 pagesملخص المكتسبات القبلية للسنة الثالثة ثانويTrainerYoucefDjouadjNo ratings yet
- الوثيقة 1Document1 pageالوثيقة 1Soumia KerdNo ratings yet
- جميع الأسئلة النظرية و التعريفات للوحدة 01 باك المتابعة الزمنية لتحول كيميائي في وسط مائيDocument10 pagesجميع الأسئلة النظرية و التعريفات للوحدة 01 باك المتابعة الزمنية لتحول كيميائي في وسط مائيmayssabl47No ratings yet
- Cours - 7 - Thermodynamique (2022-2023)Document10 pagesCours - 7 - Thermodynamique (2022-2023)Farouk FeddaNo ratings yet
- Bbl14bS MohamedDocument9 pagesBbl14bS MohamedrachidNo ratings yet
- - - - - - - - - الحلقة (10) تمرين حول المتابعة الزمنية عن طريق قياس الضغط PDFDocument5 pages- - - - - - - - الحلقة (10) تمرين حول المتابعة الزمنية عن طريق قياس الضغط PDFamina derkaouiNo ratings yet
- - - - - - - - - الحلقة (10) تمرين حول المتابعة الزمنية عن طريق قياس الضغط PDFDocument5 pages- - - - - - - - الحلقة (10) تمرين حول المتابعة الزمنية عن طريق قياس الضغط PDFAbdou100% (1)
- تمرين 1-3Document2 pagesتمرين 1-3Hani StarkNo ratings yet
- Dzexams Docs 3as 907324Document11 pagesDzexams Docs 3as 907324Chahinez BenameurNo ratings yet
- جميع الأسئلة النظرية و التعريفات لكل الوحدات 2Document10 pagesجميع الأسئلة النظرية و التعريفات لكل الوحدات 2morailiknoorNo ratings yet
- امتحان تجريبي في الفيزياء مع التصحيح PDFDocument10 pagesامتحان تجريبي في الفيزياء مع التصحيح PDFzakkou100% (6)
- جميع الأسئلة النظرية و التعريفات لكل الوحداتDocument10 pagesجميع الأسئلة النظرية و التعريفات لكل الوحداتUsb UsbNo ratings yet
- الوحدة 01 سلسلة 02 السنة ثالثةDocument1 pageالوحدة 01 سلسلة 02 السنة ثالثةÊš Pőîř100% (1)
- سلسلة تمارين الوحدة الأولى 1Document1 pageسلسلة تمارين الوحدة الأولى 1picaking9No ratings yet
- الاختبار الاول ثانوية بونور 2021-2022Document1 pageالاختبار الاول ثانوية بونور 2021-2022Daya Lebaili100% (1)
- هندسة تفاعلاتDocument10 pagesهندسة تفاعلاتعبدوNo ratings yet
- Bb13B AflouDocument4 pagesBb13B AflouProfchaari SciencesNo ratings yet
- Contr 1ér S 1-2 2bacDocument7 pagesContr 1ér S 1-2 2bacbalawisolaymanNo ratings yet
- التتبع الزمني لتحول كيميائيDocument8 pagesالتتبع الزمني لتحول كيميائيYou ZbirNo ratings yet
- فروض الفيزياء والكيمياء الثانية باك علوم فيزيائية الدورة الاولى المرحلة 1 النموذج 5Document4 pagesفروض الفيزياء والكيمياء الثانية باك علوم فيزيائية الدورة الاولى المرحلة 1 النموذج 5Amine taikNo ratings yet
- Exercices PC 2bac 0013Document8 pagesExercices PC 2bac 0013aharrar jamilaNo ratings yet
- المقرونة تمارينDocument8 pagesالمقرونة تمارينayoubberramram5No ratings yet
- دوسية الفصل الثاني توجيهيDocument137 pagesدوسية الفصل الثاني توجيهيHamzeh MansourNo ratings yet
- Altholat Alkimiaiia Almqrona Baltfaalat HMDH Qaada Slsla Altmarin 3 2Document2 pagesAltholat Alkimiaiia Almqrona Baltfaalat HMDH Qaada Slsla Altmarin 3 2muka fihNo ratings yet
- Acide BaseDocument2 pagesAcide Baseayman lamzouriNo ratings yet
- سلسلة تمارينDocument5 pagesسلسلة تمارينayadilyes79No ratings yet
- سلسلة تمارين 1Document5 pagesسلسلة تمارين 1lisaNo ratings yet
- ExamsDocument1 pageExamsyacine yacineNo ratings yet
- Physics 3se22 1trim2Document2 pagesPhysics 3se22 1trim2yacine yacineNo ratings yet
- وثيقة الأستاذDocument2 pagesوثيقة الأستاذIkram KimiNo ratings yet
- Dzexams Docs 3as 904241Document224 pagesDzexams Docs 3as 904241amine mansouriNo ratings yet
- سلسلة تمارين بالحل المفصل في 6 وحداتDocument223 pagesسلسلة تمارين بالحل المفصل في 6 وحداتjkruege1No ratings yet
- Acfrogc9pxi4 N0bgzwxfdiabmiljk5egaqcwadleehiy16u Fzalf U7nhyqwjayfd36crgv7agtcvlz4lg7pfr8r Wqku7lerlalfll Pppoknefwhjtecij7jdpy6e71nqlkjleks7nceh 39Document223 pagesAcfrogc9pxi4 N0bgzwxfdiabmiljk5egaqcwadleehiy16u Fzalf U7nhyqwjayfd36crgv7agtcvlz4lg7pfr8r Wqku7lerlalfll Pppoknefwhjtecij7jdpy6e71nqlkjleks7nceh 39Mohamed NachafNo ratings yet