Professional Documents
Culture Documents
0 ratings0% found this document useful (0 votes)
6 viewsمعادلات الباب الخامس فى الكيمياء للثانوية العامة - الامتحان التعليمى
معادلات الباب الخامس فى الكيمياء للثانوية العامة - الامتحان التعليمى
Uploaded by
manarsehiem1Copyright:
© All Rights Reserved
Available Formats
Download as PDF, TXT or read online from Scribd
You might also like
- كيمياء رموز العناصر والصيغ الكيميائيةDocument3 pagesكيمياء رموز العناصر والصيغ الكيميائيةammar Mhd100% (1)
- هام جداً ٢Document80 pagesهام جداً ٢sohalasayd mohmedNo ratings yet
- مخطط معادلات الحديد 3ث TOOPSEC@ ❤️⚠️Document1 pageمخطط معادلات الحديد 3ث TOOPSEC@ ❤️⚠️the662hey100% (1)
- وضح بالمعادلات الكيمائية كيف تحصل علي كل ما يأتي مع ذكر شروط التفاعلDocument2 pagesوضح بالمعادلات الكيمائية كيف تحصل علي كل ما يأتي مع ذكر شروط التفاعلshadymekNo ratings yet
- مراجعة امتحان الكيمياء للصف الثالث الثانوي PDFDocument18 pagesمراجعة امتحان الكيمياء للصف الثالث الثانوي PDFhamdy kassem100% (1)
- Corrections of Science 230403 075841Document3 pagesCorrections of Science 230403 075841Abir OmarNo ratings yet
- التدرب على موازنة المعادلات (Www.pc1.Ma)Document1 pageالتدرب على موازنة المعادلات (Www.pc1.Ma)Choâyb ZetiliNo ratings yet
- بسم الله الرحمن الرحيمDocument1 pageبسم الله الرحمن الرحيمkhaledthewhite268No ratings yet
- التحليل الكيميائيDocument6 pagesالتحليل الكيميائيEslamSalehNo ratings yet
- ملزمة الكيمياء ثالث متوسط قاسم عجرشDocument97 pagesملزمة الكيمياء ثالث متوسط قاسم عجرشaldawwdybdallh675No ratings yet
- D&F HsDocument2 pagesD&F HsNityam shahNo ratings yet
- استخلاص الحديد2Document1 pageاستخلاص الحديد2Basmah AlhajNo ratings yet
- 3AS U01 - E5 - Exercice 007Document3 pages3AS U01 - E5 - Exercice 007Halim GHazaouetNo ratings yet
- التأسيس كما يجب أن يكون تامر البطشDocument30 pagesالتأسيس كما يجب أن يكون تامر البطشMohamed Samir100% (1)
- LLLLLLLLLLLLLLLLLLLLLLKKKKKKKKKKKKKKKDocument37 pagesLLLLLLLLLLLLLLLLLLLLLLKKKKKKKKKKKKKKKahmad DavudNo ratings yet
- التدرب على موزانة معادلات الأكسدة و الإرجاعDocument1 pageالتدرب على موزانة معادلات الأكسدة و الإرجاعOmaima AliNo ratings yet
- ملخص الكشف عن الشقوق الحامضيةDocument4 pagesملخص الكشف عن الشقوق الحامضيةEzdeen Al-moflhiNo ratings yet
- أفكار الباب الثانىDocument4 pagesأفكار الباب الثانىHassan MesbahNo ratings yet
- التفاعلات الكيميائيةDocument4 pagesالتفاعلات الكيميائيةm.zdekNo ratings yet
- Dzexams Docs 1as 906426Document2 pagesDzexams Docs 1as 906426simousimgsmNo ratings yet
- , ; ا اMD م<P ا لو<Q RHAأDocument2 pages, ; ا اMD م<P ا لو<Q RHAأanwarnoro23No ratings yet
- Boiler 2023Document9 pagesBoiler 2023Abdallah AbdallahNo ratings yet
- ArDocument2 pagesArYoussef MoujahidNo ratings yet
- ورق عمل أسئلة وإجابة 8Document5 pagesورق عمل أسئلة وإجابة 8chem4samiNo ratings yet
- كاربؤن لةبريَكى تةواولةهةوادا دةسوتيَت دوانةئؤكسيدى كاربؤن دروستDocument1 pageكاربؤن لةبريَكى تةواولةهةوادا دةسوتيَت دوانةئؤكسيدى كاربؤن دروستMuhammad XalilNo ratings yet
- ملخص المادة وتحولاتها لـ 4 متوسطDocument2 pagesملخص المادة وتحولاتها لـ 4 متوسطmaamar SebbarNo ratings yet
- معادلات الخامسDocument11 pagesمعادلات الخامسSameh AbdelkhalekNo ratings yet
- Cacl + (NH) Co Caco + 2Nh CL: 2 (Aq) 4 2 3 (Aq) 3 (S) 4 (Aq)Document8 pagesCacl + (NH) Co Caco + 2Nh CL: 2 (Aq) 4 2 3 (Aq) 3 (S) 4 (Aq)Abanoub NabilNo ratings yet
- المحاليل المائيةDocument2 pagesالمحاليل المائيةoutemy20006042100% (1)
- التفاعلات الكيميائيةDocument23 pagesالتفاعلات الكيميائيةehagar60No ratings yet
- 10دفترDocument44 pages10دفترHealthyATP 100No ratings yet
- تأثير المحاليل الحمضية و القاعدية على الفلزات PDFDocument1 pageتأثير المحاليل الحمضية و القاعدية على الفلزات PDFوليد الادوزيNo ratings yet
- Mol 2Document1 pageMol 2oussama kherboucheNo ratings yet
- Dzexams Docs 4am 905807Document2 pagesDzexams Docs 4am 905807Souhed BouchelouiNo ratings yet
- كيمياء ترشيحي - 240602 - 110903Document30 pagesكيمياء ترشيحي - 240602 - 110903rabi3a.laiilaNo ratings yet
- روائز الكشف عن بعض الأيوناتDocument3 pagesروائز الكشف عن بعض الأيوناتReddahi BrahimNo ratings yet
- ورقة عمل في أساسيات الكيمياءDocument15 pagesورقة عمل في أساسيات الكيمياءmeltayeb2002No ratings yet
- Y3,4Document30 pagesY3,4Elostaz Educational ChannelNo ratings yet
- كيمياء امتحان 60 نقطةDocument10 pagesكيمياء امتحان 60 نقطةSwee TyNo ratings yet
- شرح وتلخيص الوحدة الثالثة (الحموض والقواعد) كيمياء 12Document63 pagesشرح وتلخيص الوحدة الثالثة (الحموض والقواعد) كيمياء 12Issa ShuqairNo ratings yet
- الكشف عن الشقوق الحامضية والقاعدية للأملاح البسيطةDocument30 pagesالكشف عن الشقوق الحامضية والقاعدية للأملاح البسيطةSarbast Khoshnaw100% (2)
- تحويلات و تعليلات العضويةDocument33 pagesتحويلات و تعليلات العضويةMahmoud MarwanNo ratings yet
- كيمياء أولى ثانوى 2018معدلDocument88 pagesكيمياء أولى ثانوى 2018معدلAnonymous LqAsrY4Hp100% (2)
- Ar Fertilizer IMDocument167 pagesAr Fertilizer IMMostafa FawzyNo ratings yet
- ملخص كيمياء معملDocument8 pagesملخص كيمياء معملzachariakeshlafNo ratings yet
- مهم جدااااااااااااااااااااDocument9 pagesمهم جدااااااااااااااااااااRania A.AbougalalaNo ratings yet
- جميع تحويلات الكيمياء العضوية للصف الثالث الثانوي 2017 - مذكرة دوت كومDocument29 pagesجميع تحويلات الكيمياء العضوية للصف الثالث الثانوي 2017 - مذكرة دوت كومbelal rashadNo ratings yet
- 3trim Sem Physique2Document1 page3trim Sem Physique2Hàtim MadridNo ratings yet
- بنك دوائر الكيمياء الوزاري جيل 2005Document100 pagesبنك دوائر الكيمياء الوزاري جيل 2005tareqxpertNo ratings yet
- ورقة عمل تأكسد واختزال 2004Document7 pagesورقة عمل تأكسد واختزال 2004hanoodeh.mmNo ratings yet
- ProcedesDocument3 pagesProcedeshabelamine820No ratings yet
- التحولات السريعة والتحولات البطيئةDocument4 pagesالتحولات السريعة والتحولات البطيئةالغزيزال الحسن EL GHZIZAL Hassane100% (3)
- المجموعات الذريةDocument1 pageالمجموعات الذريةredmercury8048% (21)
- تقويم تشخيصي مع الحل في العلوم الفيزيائية و التكنولوجيا 44Document2 pagesتقويم تشخيصي مع الحل في العلوم الفيزيائية و التكنولوجيا 44Maroua ChaNo ratings yet
- بحث صيغ الأملاح المائية الطالب محمد بن يحيى ال ملوذDocument6 pagesبحث صيغ الأملاح المائية الطالب محمد بن يحيى ال ملوذj1rb707No ratings yet
- ورقة عمل المراجعة التوجيهي ف1 14Document5 pagesورقة عمل المراجعة التوجيهي ف1 14ahmad bahaNo ratings yet
- Yf 2Document28 pagesYf 2Elostaz Educational ChannelNo ratings yet
- تمرين في الأكسدة و الإرجاعDocument2 pagesتمرين في الأكسدة و الإرجاعabderachid041107No ratings yet
معادلات الباب الخامس فى الكيمياء للثانوية العامة - الامتحان التعليمى
معادلات الباب الخامس فى الكيمياء للثانوية العامة - الامتحان التعليمى
Uploaded by
manarsehiem10 ratings0% found this document useful (0 votes)
6 views2 pagesOriginal Title
معادلات الباب الخامس فى الكيمياء للثانوية العامة _ الامتحان التعليمى
Copyright
© © All Rights Reserved
Available Formats
PDF, TXT or read online from Scribd
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
© All Rights Reserved
Available Formats
Download as PDF, TXT or read online from Scribd
Download as pdf or txt
0 ratings0% found this document useful (0 votes)
6 views2 pagesمعادلات الباب الخامس فى الكيمياء للثانوية العامة - الامتحان التعليمى
معادلات الباب الخامس فى الكيمياء للثانوية العامة - الامتحان التعليمى
Uploaded by
manarsehiem1Copyright:
© All Rights Reserved
Available Formats
Download as PDF, TXT or read online from Scribd
Download as pdf or txt
You are on page 1of 2
1
CoCl2 .6H2 O CoCl2 + 6H2 O ك لوري د اللوبلت
II
وردى فاتح ازرق
عممية التحميص - 1جتفيف اخلام وزيادة نصبة احلديد
FeCO3 FeO + CO2 , 4FeO + O2 2Fe 2O3
2Fe 2O3 .3H2O 2Fe 2O3 + 3H2O
- 2أكصدة الشوائب-:
S + O2 SO2 , 4P + 5O2 2P 2O5
] 1دور فحم الكوك فى الفرن العاىل
C + O2 CO2 , C + CO2 2CO
اعلى مو ْ 700
3CO +Fe 2O3 اختسال خام اهليناتيت فى الفرى العاىل 2Fe + 3CO2
م
[ ] 2التخمص من الشوائب -:دور احلجر اجلريى فى الفرن العاىل-:
CaCO3 CaO + CO2
CaO + SiO2 CaSiO3 شليلات كالصيوم
3CaO + P 2O5 فوشفات كالصيوم Ca3(PO4)2 خبث
CaO + Al2O3 ألوميهات كالصيوم Ca(AlO2)2
اختزال خام اهليناتيت فى فرن مدركس
2Fe 2O3 + 3CO + 3H2 4Fe + 3CO2 + 3H2O
خواص احلديد
3Fe + 2O2 Fe3O4 [ ] 1تأثري اهلواء الصاخو-:
3Fe + 4H2O Fe 3O4 + 4H2 [ ] 2أثــر الـنـاء-:
.
2Fe + 3Cl2 2FeCl3 [ ] 3مـع الـللــــور ( الفلـــــس )-:
Fe + S FeS [ ] 4مع اللربيت ( الفلــــــس )-:
Fe + 2HCl dil FeCl2 + H2 [ ] 5مع األمح اض -:أوالً :ـ األمحاض املخففة
dil
Fe + H2SO4 FeSO4 + H2
Fe + 4HNO3 dil Fe(NO3)3 + 2H2O + NO
ثانياً :ـ األمحاض املركسة-:
3Fe + 8H2SO4 conc. / hot FeSO4 + Fe 2(SO4)3 + 4SO2 + 8H2O
حتضري اكسيد احلديد II
[ ] 1بتصخني أوكصاالت احلديد )-: (II
COO
تصخني مبعسل عو اهلواء Fe FeO + CO + CO2
COO
[ ] 2باختسال األكاشيد األعلى باهليدروجني أو أول أكصيد اللربوى-:
400:700 0c
Fe 2O3 + H2 2FeO + H2O
400:700 0c
2
Fe 3O4 + H2 3FeO + H2O
خ واص اك سيد احل دي د
II
4FeO + O2 2Fe 2O3 [ ] 1ت أث ري اهل واء ال صاخو-:
dil
FeO + H2SO4 FeSO4 + H2O [ ] 2مع األمح اض امل خففة
حتضري اكسيد احلديد III
FeCl3 + Fe(OH)3 + 3NH4Cl [] 1
اعلى مو ْ 200م 3NH4OH
2Fe(OH)3 Fe 2O3 + 3H2O
2FeSO4 Fe 2O3 + SO2 + SO3 2
خواص اكسيد احلديد III
Fe 2O3 + 3H2SO4 conc. / hot Fe2(SO4)3 + 3H2O
Fe O + 6HCl conc. / hot
2 3 2FeCl + 3H O 3 2
حتضري اكسيد احلديداملغناطيسى
230:300 0c
3Fe 2O3 + CO )2Fe O -: (III3 4 [ ] 1باختسال أكصيد حديد
0
c +CO2
[ ] 2مو احلديد املصخو لدرجة االمحرار بفعل اهلواء أو خبار املاء
3Fe + 2O2 Fe 3O4 , 3Fe + 4H2O Fe 3O4 + 4H2
خواص اكسيد احلديداملغناطيسى
2Fe 3O4 + 1
2 O2 3Fe 2O3 [ ] 1مع اهلواء الصاخو
[ ] 2مع األمحاض املركسة الصاخهة-:
conc. / hot
Fe 3O4 + 4H2SO4 FeSO4 + Fe 2(SO4)3 + 4H2 O
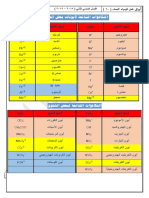
[أ] اللشف عو كاتيوى احلديد )-: (Fe 2+) (II
FeSO4 + 2NaOH Fe(OH)2 + Na2SO4
راشب أبيض خمضر
FeCl2 + 2NaOH Fe(OH)2 + 2NaCl
[ب] اللشف عو كاتيوى احلديد )-: (Fe 3+) (III
Fe 2(SO4)3 + 6NH4OH 2Fe(OH)3 + 3(NH4)2 SO4
FeCl3 + 3NH4OH Fe(OH)3 + 3NH4Cl
راشب بهى حمنر
م وق ع االم تحاى ال –
تعلينىجلنيع امل راح ل ال درا شية فى مجيع امل واد
www.exam-eg.com
You might also like
- كيمياء رموز العناصر والصيغ الكيميائيةDocument3 pagesكيمياء رموز العناصر والصيغ الكيميائيةammar Mhd100% (1)
- هام جداً ٢Document80 pagesهام جداً ٢sohalasayd mohmedNo ratings yet
- مخطط معادلات الحديد 3ث TOOPSEC@ ❤️⚠️Document1 pageمخطط معادلات الحديد 3ث TOOPSEC@ ❤️⚠️the662hey100% (1)
- وضح بالمعادلات الكيمائية كيف تحصل علي كل ما يأتي مع ذكر شروط التفاعلDocument2 pagesوضح بالمعادلات الكيمائية كيف تحصل علي كل ما يأتي مع ذكر شروط التفاعلshadymekNo ratings yet
- مراجعة امتحان الكيمياء للصف الثالث الثانوي PDFDocument18 pagesمراجعة امتحان الكيمياء للصف الثالث الثانوي PDFhamdy kassem100% (1)
- Corrections of Science 230403 075841Document3 pagesCorrections of Science 230403 075841Abir OmarNo ratings yet
- التدرب على موازنة المعادلات (Www.pc1.Ma)Document1 pageالتدرب على موازنة المعادلات (Www.pc1.Ma)Choâyb ZetiliNo ratings yet
- بسم الله الرحمن الرحيمDocument1 pageبسم الله الرحمن الرحيمkhaledthewhite268No ratings yet
- التحليل الكيميائيDocument6 pagesالتحليل الكيميائيEslamSalehNo ratings yet
- ملزمة الكيمياء ثالث متوسط قاسم عجرشDocument97 pagesملزمة الكيمياء ثالث متوسط قاسم عجرشaldawwdybdallh675No ratings yet
- D&F HsDocument2 pagesD&F HsNityam shahNo ratings yet
- استخلاص الحديد2Document1 pageاستخلاص الحديد2Basmah AlhajNo ratings yet
- 3AS U01 - E5 - Exercice 007Document3 pages3AS U01 - E5 - Exercice 007Halim GHazaouetNo ratings yet
- التأسيس كما يجب أن يكون تامر البطشDocument30 pagesالتأسيس كما يجب أن يكون تامر البطشMohamed Samir100% (1)
- LLLLLLLLLLLLLLLLLLLLLLKKKKKKKKKKKKKKKDocument37 pagesLLLLLLLLLLLLLLLLLLLLLLKKKKKKKKKKKKKKKahmad DavudNo ratings yet
- التدرب على موزانة معادلات الأكسدة و الإرجاعDocument1 pageالتدرب على موزانة معادلات الأكسدة و الإرجاعOmaima AliNo ratings yet
- ملخص الكشف عن الشقوق الحامضيةDocument4 pagesملخص الكشف عن الشقوق الحامضيةEzdeen Al-moflhiNo ratings yet
- أفكار الباب الثانىDocument4 pagesأفكار الباب الثانىHassan MesbahNo ratings yet
- التفاعلات الكيميائيةDocument4 pagesالتفاعلات الكيميائيةm.zdekNo ratings yet
- Dzexams Docs 1as 906426Document2 pagesDzexams Docs 1as 906426simousimgsmNo ratings yet
- , ; ا اMD م<P ا لو<Q RHAأDocument2 pages, ; ا اMD م<P ا لو<Q RHAأanwarnoro23No ratings yet
- Boiler 2023Document9 pagesBoiler 2023Abdallah AbdallahNo ratings yet
- ArDocument2 pagesArYoussef MoujahidNo ratings yet
- ورق عمل أسئلة وإجابة 8Document5 pagesورق عمل أسئلة وإجابة 8chem4samiNo ratings yet
- كاربؤن لةبريَكى تةواولةهةوادا دةسوتيَت دوانةئؤكسيدى كاربؤن دروستDocument1 pageكاربؤن لةبريَكى تةواولةهةوادا دةسوتيَت دوانةئؤكسيدى كاربؤن دروستMuhammad XalilNo ratings yet
- ملخص المادة وتحولاتها لـ 4 متوسطDocument2 pagesملخص المادة وتحولاتها لـ 4 متوسطmaamar SebbarNo ratings yet
- معادلات الخامسDocument11 pagesمعادلات الخامسSameh AbdelkhalekNo ratings yet
- Cacl + (NH) Co Caco + 2Nh CL: 2 (Aq) 4 2 3 (Aq) 3 (S) 4 (Aq)Document8 pagesCacl + (NH) Co Caco + 2Nh CL: 2 (Aq) 4 2 3 (Aq) 3 (S) 4 (Aq)Abanoub NabilNo ratings yet
- المحاليل المائيةDocument2 pagesالمحاليل المائيةoutemy20006042100% (1)
- التفاعلات الكيميائيةDocument23 pagesالتفاعلات الكيميائيةehagar60No ratings yet
- 10دفترDocument44 pages10دفترHealthyATP 100No ratings yet
- تأثير المحاليل الحمضية و القاعدية على الفلزات PDFDocument1 pageتأثير المحاليل الحمضية و القاعدية على الفلزات PDFوليد الادوزيNo ratings yet
- Mol 2Document1 pageMol 2oussama kherboucheNo ratings yet
- Dzexams Docs 4am 905807Document2 pagesDzexams Docs 4am 905807Souhed BouchelouiNo ratings yet
- كيمياء ترشيحي - 240602 - 110903Document30 pagesكيمياء ترشيحي - 240602 - 110903rabi3a.laiilaNo ratings yet
- روائز الكشف عن بعض الأيوناتDocument3 pagesروائز الكشف عن بعض الأيوناتReddahi BrahimNo ratings yet
- ورقة عمل في أساسيات الكيمياءDocument15 pagesورقة عمل في أساسيات الكيمياءmeltayeb2002No ratings yet
- Y3,4Document30 pagesY3,4Elostaz Educational ChannelNo ratings yet
- كيمياء امتحان 60 نقطةDocument10 pagesكيمياء امتحان 60 نقطةSwee TyNo ratings yet
- شرح وتلخيص الوحدة الثالثة (الحموض والقواعد) كيمياء 12Document63 pagesشرح وتلخيص الوحدة الثالثة (الحموض والقواعد) كيمياء 12Issa ShuqairNo ratings yet
- الكشف عن الشقوق الحامضية والقاعدية للأملاح البسيطةDocument30 pagesالكشف عن الشقوق الحامضية والقاعدية للأملاح البسيطةSarbast Khoshnaw100% (2)
- تحويلات و تعليلات العضويةDocument33 pagesتحويلات و تعليلات العضويةMahmoud MarwanNo ratings yet
- كيمياء أولى ثانوى 2018معدلDocument88 pagesكيمياء أولى ثانوى 2018معدلAnonymous LqAsrY4Hp100% (2)
- Ar Fertilizer IMDocument167 pagesAr Fertilizer IMMostafa FawzyNo ratings yet
- ملخص كيمياء معملDocument8 pagesملخص كيمياء معملzachariakeshlafNo ratings yet
- مهم جدااااااااااااااااااااDocument9 pagesمهم جدااااااااااااااااااااRania A.AbougalalaNo ratings yet
- جميع تحويلات الكيمياء العضوية للصف الثالث الثانوي 2017 - مذكرة دوت كومDocument29 pagesجميع تحويلات الكيمياء العضوية للصف الثالث الثانوي 2017 - مذكرة دوت كومbelal rashadNo ratings yet
- 3trim Sem Physique2Document1 page3trim Sem Physique2Hàtim MadridNo ratings yet
- بنك دوائر الكيمياء الوزاري جيل 2005Document100 pagesبنك دوائر الكيمياء الوزاري جيل 2005tareqxpertNo ratings yet
- ورقة عمل تأكسد واختزال 2004Document7 pagesورقة عمل تأكسد واختزال 2004hanoodeh.mmNo ratings yet
- ProcedesDocument3 pagesProcedeshabelamine820No ratings yet
- التحولات السريعة والتحولات البطيئةDocument4 pagesالتحولات السريعة والتحولات البطيئةالغزيزال الحسن EL GHZIZAL Hassane100% (3)
- المجموعات الذريةDocument1 pageالمجموعات الذريةredmercury8048% (21)
- تقويم تشخيصي مع الحل في العلوم الفيزيائية و التكنولوجيا 44Document2 pagesتقويم تشخيصي مع الحل في العلوم الفيزيائية و التكنولوجيا 44Maroua ChaNo ratings yet
- بحث صيغ الأملاح المائية الطالب محمد بن يحيى ال ملوذDocument6 pagesبحث صيغ الأملاح المائية الطالب محمد بن يحيى ال ملوذj1rb707No ratings yet
- ورقة عمل المراجعة التوجيهي ف1 14Document5 pagesورقة عمل المراجعة التوجيهي ف1 14ahmad bahaNo ratings yet
- Yf 2Document28 pagesYf 2Elostaz Educational ChannelNo ratings yet
- تمرين في الأكسدة و الإرجاعDocument2 pagesتمرين في الأكسدة و الإرجاعabderachid041107No ratings yet