Professional Documents
Culture Documents
Sol BAC BLANC 2023 2024 TM M
Sol BAC BLANC 2023 2024 TM M
Uploaded by
oldgloryrayOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Sol BAC BLANC 2023 2024 TM M
Sol BAC BLANC 2023 2024 TM M
Uploaded by
oldgloryrayCopyright:
Available Formats
األستاذ :بوزيان زكرياء الشعب :تقني رياضي ورياضي اإلجابة النموذجية بكالوريا تجريبي 2024
العالمة
عناصر اإلجابة
مجزأة مجموعة
الموضوع األول
التمرين األول 04( :نقاط)
.1.1 .1التعريفات:
0.75 3x0.25
*نظائر مشعة :أنوية غير مستقرة لنفس العنصر الكيميائي لها نفس العدد الذري وتختلف في العدد الكتلي،
تتفكك تلقائيا إلى أنوية اكثر استق ار ار مع اصدار اشعاعات.
*النواة * : ZA Xهي نواة مثارة (لها فائض في الطاقة) ينتج عنها اشعاع غاما .
، 131مع تحديد نمط التفكك ورمز النواة البنت الناتجة:
.2.1معادلة تفكك اليود 53 I
0.75
-بما أنه يحدث تحول نيترون إلى بروتون فإن نمط التفكك هو ، −وعليه:
3x0.25
131 * A 0
53 I → Z X + −1e
A = 131وعليه النواة البنت الناتجة54 Xe :
* 131
بتطبيق قانون االنحفاظ لصوديZ = 54 :
131 * 131 0
53 I → 54 Xe + −1e +
0.25 0.25 .1.2 .2كتابة عبارة قانون النشاط اإلشعاعي ) A ( t ) = A0 .e− .t : A( t
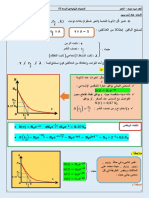
.2.2تعريف زمن نصف العمر ، t1/2وتحديد قيمته بيانيا:
*تعريف زمن نصف العمر :هو الزمن الالزم لتفكك نصف عدد األنوية المشعة االبتدائية
N
0.5 2x0.25 . N ( t1/2 ) = 0
2
15
4,6 10
= ) ، N d ( t1/2باإلسقاط نجدt1/2 = 8 jours : *تحديد قيمته= 2,3 1015 noyaux :
2
.3.2حساب N0عدد األنوية االبتدائية في العينة:
0.5 0.5 A0 t1/2 . A0 8 24 3600 9,28 109
= N0 = = = 9,25 1015 noyaux
ln 2 ln 2
.4.2استخراج ) N0 ( inject1عدد األنوية االبتدائية في الجرعة األولى ،وحساب نشاطها اإلبتدائي:
0.5
0.5 من البيان نجد أنN 0 ( inject1) = 4,6 1015 noyaux :
وعليهA0 ( inject1) = .N 0 ( inject1) = 4,61 109 Bq :
.5.2حساب قيمة : t2
N ( inject 2 )
N0 ( inject1) = N0 ( inject 2 ) .e−.t2 → t2 = 1/2 ln 0
t
0.75 ln 2 N0 ( inject1)
0.5
t N − N0 ( inject1)
→ t2 = 1/2 ln 0 = 3h
ln 2 N0 ( inject1)
صفحة 1من 11
األستاذ :بوزيان زكرياء الشعب :تقني رياضي ورياضي تابع لإلجابة النموذجية للبكالوريا التجريبي 2024
التمرين الثاني 04( :نقاط)
-الجزء األول:
.1تذكير بمميزات الثقل Pودافعة أرخميدس :
دافعة أرخميدس الثقل P
0.5
0.5 مركز عطالة الجملة مركز عطالة الجملة المبدأ
شاقولي شاقولي الحامل
نحو األعلى نحو مركز األرض االتجاه
= f .V .g P = m.g الشدة
.2المقارنة بين شدة الثقل وشدة دافعة أرخميدس:
0.5 2x0.25 .Vb . g 1,234 4 10 3
= = = 3,085 → P
P m. g 1,6 10 3
بما أن Pفإن الجملة تتحرك نحو األعلى.
-الجزء الثاني:
.1توضيح سبب اعتبار أن حركة المغامر سقوط حر:
0.25 كثافة الهواء صغيرة في هذه المرحلة مما يجعل قوى االحتكاك ودافعة أرخميدس مهملة أمام ثقل
المغامر ولوازمه.
.1.2 .2تحديد زمن السقوط خالل هذه المرحلة:
-الجملة :المغامر ولوازمه
-المرجع :سطحي أرضي نعتبره عطالي.
-بتطبيق القانون الثاني لنيوتن على مركز عطالة الجملة:
0.25 0.25 F ext = m.a → P = m.a → a = g
= a y = g → v y = g.t → y
1 2
2
) (
بإسقاط العبارة الشعاعية في المعلم g .t : O, j
vy
=t وعليه= 30,55s :
g
1 2
0.25 0.25 =d .2.2المسافة المقطوعة خالل هذه المرحلةg .t = 4526,5 m :
2
-الجزء الثالث:
.1التحليل البعدي لـ : k
0.25 0.25
=k
f
= → k
f m. a M . L .T −2
= = =
M
−2
v2 v 2
v2
L 2 .T L
منه وحدة kهي kg.m−1
صفحة 2من 11
األستاذ :بوزيان زكرياء الشعب :تقني رياضي ورياضي تابع لإلجابة النموذجية للبكالوريا التجريبي 2024
.2إثبات المعادلة التفاضلية للسرعة:
-المرجع :سطحي أرضي نعتبره غاليليا.
-الجملة :كرة.
بتطبيق القانون الثاني لنيوتن على مركز عطالة الجملة:
F ext = m.a → P + f = m.a
) (
0.5 2x0.25
بإسقاط العبارة الشعاعية على المحور : Oz
dv dv k 2
m.g0 − k .v 2 = m. → + v = g0
dt dt m
وعليه= 3,9 10−3 m−1 ; B = 9,8 m.s −2 :
k
=A
m
0.25 0.25 .1.3 .3تحديد الزمن التقريبي لبلوغ السرعة الحديةt f 7 s :
0.25 0.25 .2.3الزمن المميز للحركة :اعتمادا على مماس t = 0نجد = 1,875s :
.3.3تسارع مركز عطالة المغامر عند اللحظة t = 0بطريقتين مختلفتين:
0 − 85,83
*الطريقة األولى−19 m.s −2 :
dv
= a0 =
dt t =0 4,5 − 0
0.5 2x0.25
*الطريقة الثانية:
2
−3
309 103
2
a0 = g0 − A v0 = 9,8 − 3,9 10 = −18,93 m.s −2 −19 m.s −2
3600
.4.3إثبات عبارة الزمن المميز للحركة :
0.25
0.25
-معادلة المماس عند ، v = a0 .t + v0 : t = 0وعند اللحظة t = نعلم أن ، v = vlimوعليه:
v −v
vlim = a0 . + v0 → = lim 0
a0
(
a m.s −2 ) .5.3الشكل التقريبي لتغيرات تسارع
مركز عطالة المغامر بداللة الزمن:
)t (s
0.25 0.25
−19
صفحة 3من 11
األستاذ :بوزيان زكرياء الشعب :تقني رياضي ورياضي تابع لإلجابة النموذجية للبكالوريا التجريبي 2024
التمرين الثالث 06( :نقاط)
R
i أوال :دراسة الدارة ) : ( RC
uR 1
0.75 3x0.25
E
.1تمثيل الدارة الكهربائية:
uC C
.2إيجاد المعادلة التفاضلية التي يحققها التوتر الكهربائي uCبين طرفي المكثفة:
0.5 0.5 بتطبيق قانون جمع التوترات:
) duC ( t
uC ( t ) + uR ( t ) = E uC ( t ) + R1 i ( t ) = E uC ( t ) + R1C =E
dt
.3إيجاد قيمة كل من 1و : E
j ) duC ( t
1 2x0.5 a = tan و b = ( uc ) duc =0 uC ( t ) = a + bحيث : معادلة البيان:
dt
i dt
1 = a = 2 ms ) du ( t
uC ( t ) = E − R1C Cوبالمطابقة المعادلتين ،نجد : نظريا :من السؤال ، 2.نجد :
E =b=9 V dt
ثانيا :دراسة الدارة ) : ( RL
.1دور الصمام :نعم للصمام دور في هذا الجزء من الدارة الكهربائية.
0.5 0.5
أثناء فتح القاطعة الوشيعة تتحرض ذاتيا فيتولد تيار متحرض ،الهواء يتميز بمقاومة كبيرة األمر الذي
يجعل التوتر الكهربائي بين فكي القاطعة كبير جدا مما يؤدي إلى حدوث ش اررة كهربائية وجود الصمام لمنع
حدوث الش اررة الكهربائية وبالتالي حماية التجهيز من اإلتالف.
.2ارفاق كل بيان بالتوتر الموافق له:
0.75 3x0.25 التعليل التوتر الموافق رمز البيان
uR = 0
ub a
t =0i =0 1
ub = r I 0
uR1 b
.3تبيان كيفية ربط راسم االهتزاز بالدارة:
Y 2
R
0.5 0.5
E (L,r
)
الضغط على الزر Y INV
0.5 2x0.25 .4إيجاد قيمة كل من Eو 1' = 0, 2 ms ، E = 9 V : '1
ثالثا :تأثير قيمة مقاومة الناقل األومي على ثابت الزمن
-تحديد البيان لكل حالة واستنتاج تأثير مقاومة الناقل األومي على ثابت الزمن لكل حالة:
صفحة 4من 11
األستاذ :بوزيان زكرياء الشعب :تقني رياضي ورياضي تابع لإلجابة النموذجية للبكالوريا التجريبي 2024
تحديد البيان الموافق لكل حالة :
التعليل الحالة رمز البيان
0.5 2x0.25
= ثابت الزمن يتناقص بازدياد المقاومة
L
R+r RL )(1
= RCثابت الزمن يزداد بازدياد المقاومة RC )( 2
رابعا :استثمار النتائج
.1إيجاد قيمة Cواستنتاج قيمة المقاومة : R1
0.5 2x0.25 j
a = C = tan = 4, 7 F حيث 4, 6 − 4,8 : البيان ) = a R : ( 2
i
1
= 1 = R1 C R1 *قيمة المقاومة : R1لدينا = 425
C
.2جد مميزات الوشيعة:
L
= = 3, 6 ms
0.5 R = 0 r = 25
= نأخذ من البيان ): (1 لدينا
2x0.25 r L
R = 50 = 1, 2 ms = L L = 0, 09 H R+r
50 + r
التمرين التجريبي 06( :نقاط)
-الجزء األول:
.1تعريف الحمض حسب برونشتد :هو كل فرد كيميائي قادر على تحرير بروتون H +خالل
0.25 0.25
تفاعل كيميائي.
0.5 2x0.25 .2تحديد احداثيات نقطة التكافؤ :باالعتماد على طريقة المماسين )E (14 mL ;8,4
.3استنتاج قيمة التركيز المولي C1للمحلول ) : ( S1
CB .VB, E
0.5 0.5 = C1 عند نقطة التكافؤ= 0,014 mol.L−1 :
V1
0.25 0.25 .4تحديد الكاشف الملون المناسب لهذه المعايرة :الفينول فتالين أن . 8,0 pH E 10,0
( )
.5استنتاج قيمة ثابت الحموضة pKaللثنائية : CH 3COOH / CH 3COO −
V
0.25 0.25
عند نقطة نصف التكافؤ V1/2 = b, E = 7 mLباإلسقاط على منحنى الشكل 8.نجدpKa = 4,8 :
2
-الجزء الثاني:
.1رسم تخطيطي للتركيب التجريبي المستعمل:
0.5
0.5
.2حساب التركيز المولي C0للمحلول التجاري ) = 1,4 mol.L−1 : ( S0
0.5 0.5 10.d . p
= C0
M
صفحة 5من 11
األستاذ :بوزيان زكرياء الشعب :تقني رياضي ورياضي تابع لإلجابة النموذجية للبكالوريا التجريبي 2024
.3جدول تقدم التفاعل:
المعادلة = CO32– + 2 CH3COOH CO2 + 2 CH3COO– + H2O
الحالة التقدم كميات المادة ) ( mol
0.75 3x0.25
ابتدائية 0 n1 n0 0 0
وسطية x n1 − x n0 − 2 x x 2x بوفرة
نهائية xf n1 − x f n0 − 2 x f xf 2x f
.4عبارة تقدم التفاعل xبداللة T ، R ،VPو : P
V
بتطبيق قانون الغازات المثالية. P = n.RT → x = P P :
PV
0.5 0.5 RT
10−3
=x التطبيق العددي P = 4 10−7 P :
)8,31 ( 25 + 273
.5استخراج قيمة التقدم النهائي ، x fوتبيان أن التفاعل تام:
من البيان Pf = 350 hPaوعليهx f = 4 10−7 350 102 = 0,014 mol :
0.5 0.5
من جدول تقدم التفاعلn f ( HA) = C0V0 − 2 x f = 0 mol :
وعليه بما أن n f ( HA) = 0 molفإن التفاعل تام.
.6تعريف السرعة الحجمية للتفاعل ،وكتابة عبارتها بداللة : P
1 dx
= . vVol *تعريف السرعة الحجمية للتفاعل :هي سرعة التفاعل في وحدة الحجوم
0.5 0.5 VS dt
*عبارة السرعة الحجمية للتفاعل بداللة الضغط : P
4 10−7 dP
= 4 10−7
dx dP
= vVol منه: باشتقاق عبارة ، xtنجد:
VS dt dt dt
.7حساب قيمة السرعة الحجمية للتفاعل عند : t = 0
0.5 0.5
= vVol t =0
4 10−7
( 350 − 0 ) 102
9,33 10−2 mol.L−1.min −1
50 10−3 3−0
.8تعريف زمن نصف التفاعل ، t1/2وتحديد قيمته:
xf
0.5
2x0.25 = . xt1/ 2 هو الزمن الالزم لبلوغ تقدم التفاعل نصف تقدمه النهائي
2
Pf
= ) P ( t1/2باإلسقاط على المنحنى ،نجدt1/2 = 1,95min : = 175 hPa
2
A O الموضوع الثاني
0.5 )(S التمرين األول 04( :نقاط)
2x0.2
5 -حركة الجسم على المسار ) : ( AB
B .1تمثيل القوى المؤثرة على الجسم ) ( Sفي موضع كيفي:
صفحة 6من 11
األستاذ :بوزيان زكرياء الشعب :تقني رياضي ورياضي تابع لإلجابة النموذجية للبكالوريا التجريبي 2024
.2إيجاد عبارة vBبداللة gو : r
بتطبيق مبدأ انحفاظ الطاقة للجملة السابقة:
0.5
) (
0.5 0 1 2
Ec A + W P = EcB → m .g.r = m vB → vB = 2 g.r
2
.3تبيان عبارة فعل السطح : R
A O -الجملة :الجسم ) . ( S
-المرجع :سطحي أرضي نعتبره عطالي.
)(S
0.75 -بتطبيق القانون الثاني لنيوتن على مركز عطالة الجملة:
0.75
B
F ext = m.a → P + R = m.a
بإسقاط العبارة الشعاعية على المحور الناظمي:
v2 v2 2.g. r
R − P = m B → R = m B + P = m + m.g → R = 3.m.g
r r r
-حركة الجسم في الهواء:
.1استنتاج المعادالت الزمنية للموضع ) x ( tو ) : y ( t
0.5 0.5
v x = vB x = vB .t
v = g .t → انطالقا من العبارة الشعاعية للسرعة ، vنجد1 2 :
y y = g .t
2
.2تحديد قيمة كل من vBو : g
2x025
2x0.25 *سرعة الجسم عند الموضع : Bاعتمادا على البيانية للشكل ،3.نجد vB = 2 m.s −1 :
*تسارع الجاذبية األرضية : gاعتمادا على البيانية للشكل ،2.نجد g = 5 → g = 10 m.s −2 :
1
2
2
vB
0.5 0.5 = vB = g.r → r .3حساب rنصف قطر المسار الدائري ) = 0,2 m : ( AB
2g
.4تعيين فاصلة نقطة سقوط الجسم على اللوح:
0.5 1 2h
0.5 = h = g.t 2 → t = 0,6 s → x = 2 0,6 = 1,2 m
2 g
0.25 0.25 .5حساب قيمة فعل السطح Rعند الموضع R = 3 0,1 10 = 3 N : B
التمرين الثاني 04( :نقاط)
.1تحديد قيمتي xو : Z
0.5
2x0.25 238 + x = 241 x = 3
→ بتطبيق قانوني االنحفاظ لصودي:
92 = Z − 2 Z = 94
صفحة 7من 11
األستاذ :بوزيان زكرياء الشعب :تقني رياضي ورياضي تابع لإلجابة النموذجية للبكالوريا التجريبي 2024
.2شكل الطاقة المحررة :ح اررية وحركية.
0.25 0..25
: 241
.3حساب النقص الكتلي لألنوية 39Yو Z Pu
98
0.5
2x0.25 m 98 ) ( 98
) (
*النقص في كتلة نواة 39Y = 39.m p + 59.m p − m 39Y = 0,8940 u : 39Y
98
(
El 241 *النقص في كتلة نواة ) = 7,544 241 = 1,9518u : 241Pu
(
m 241
= Z Pu ) Z Pu
931,5 931,5
Z
: 241
.4مقارنة استقرار األنوية 39Yو Z Pu
98
0.5 = 1
( ) = 0,8940 931,5 = 8,497 MeV / n
El 98
39Y
0.5 A 98
= 2
(
El 241
Z Pu ) = 7,544 MeV / n
A
98هي األكثر استق اررا.
بما أن 1 2إذن النواة 39Y
.5حساب الطاقة المحررة عن انشطار نواة من البلوتونيوم :241
( ) ( ) ( )
0.5 0.5
Elib = El 141 98
55 Cs + El m 39Y − El
241
Z Pu = 183,774 MeV
.6استنتاج الطاقة المحررة عن كتلة m = 2 gمن البلوتونيوم :241
0.5 0.5
m 2 6,02 1023 183,774
= ET = N A Elib = 9,18 1023 MeV
M 241
Z Pu( ) 241
.1.7 .7حساب مقدار الطاقة الكلية التي يحررها انشطار كتلة m = 3 kgمن البلوتونيوم :241
0.5 0.5
9,18 1023 3000
= E 'T = 1,377 1027 MeV
2
.2.7استنتاج مقدار الطاقة الضائعة داخل مفاعل الغواصة:
0.5 EPer = E 'T − P t = 1,377 1027 1,6 10−13 − 25 106 30 24 3600
0.5
→ EPer = 1,55 1014 J
P t
0.25 0.25 =r .3.7حساب مردود المفاعل 100 = 29,4% :
E 'T
التمرين الثالث 06( :نقاط)
-الجزء األول:
.1أهمية الجسر الملحي :يعمل على غلق الدارة الكهربائية ،ويضمن التوازن الكهربائي في العمود.
صفحة 8من 11
األستاذ :بوزيان زكرياء الشعب :تقني رياضي ورياضي تابع لإلجابة النموذجية للبكالوريا التجريبي 2024
.2كتابة المعادالت النصفية الحادثة عند كل مسرى ،واستنتاج قطبية العمود:
0.5 2x0.25 Cu 2+ + 2e− = Cu
Al = Al 3+ + 3e−
*المسرى السالب :األلمنيوم *المسرى الموجب :النحاس
( )
.1.3 .3حساب كمية المادة االبتدائية ) n0 ( Alو : n0 Cu 2 +
( )
0.5 2x0.25
= 3,7 10−2 mol n0 Cu 2+ = Cu 2+ .V = 2,5 10−2 mol
m1
= ) n0 ( Al ;
) M ( Al 0
.2.3إكمال الجدول ،واستنتاج قيمة التقدم األعظمي : xmax
معادلة التفاعل 3 Cu2+ + 2 Al = 3 Cu + 2 Al3+
0.75
3x0.25 الحالة التقدم كمية المادة ) ( mol
االبتدائية 0 2,5 10−2 3,7 10−2 14 10−2 2,5 10−2
أثناء التحول x 2,5 10−2 − 3x 3,7 10−2 − 2x 14 10−2 + 3x 2,5 10−2 + 2x
بما أن التفاعل تام:
نفرض أن Alمتفاعل محد نفرض أن Cu 2+متفاعل محد
3,7 10−2 2,5 10−2
= ) xm ( 2 = 18,5 10−3 mol = )xm (1 = 8,33 10−3 mol
2 3
بما أن ) xm ( 2) xm (1فإن xmax = 8,33 10−3 mol
0.25 0.25 .3.3حساب كمية الكهرباء األعظمية:
Qmax = z.xmax .F = 6 8,33 10−3 96500 = 4823,07 C
.4.3حساب التغير في كتلة مسرى النحاس:
0.25 0.25
m ( Cu ) = 3xmax .M ( Cu ) = 3 8,33 10−3 63,5 = 1,58 g
-الجزء الثاني:
0.5
.1تبيان أن التفاعل حمض – أساس:
0.5 C13 H18O2 = C13 H17O2 − + H +
HO− + H + = C13 H17O2 − + H 2O
ألنه حدث انتقال بروتون H +من الحمض C13 H18O2إلى األساس . HO −
.2جدول تقدم التفاعل ،وتبيان أن C13 H18O2متفاعل محد:
معادلة التفاعل C13H18O2 + –HO = –C13H17O2 + H2O
0.75 3x0.25 الحالة التقدم كمية المادة ) ( mol
نهائية xf n0 − x f CB .V − x f xf xf
صفحة 9من 11
األستاذ :بوزيان زكرياء الشعب :تقني رياضي ورياضي تابع لإلجابة النموذجية للبكالوريا التجريبي 2024
بما أن الكاشف فينول فتالين أخذ اللون األزرق دليل على المحلول أساسي ،وعليه C13 H18O2متفاعل
محد.
0.5 0.5
( )
.3كتابة عبارة n HO −المتبقية في المزيج بداللة V ، Cbو ) : n0 (C13H18O2
بما أن C13 H18O2متفاعل محد فإن n0 = x fوعليهn ( HO − ) = CB .V − n0 :
.1.4 .4كتابة معادلة تفاعل المعايرة ،وتبيان أنه تفاعل تام:
0.5 0.5 ) HO− ( aq ) + H3O+ ( aq ) = 2H 2O(l
1
= Kبما أن K 104فإن تفاعل المعايرة تام. = 1014
HO . H 3O
− +
f f
.2.4تحديد حجم التكافؤ ، VA, Eواستنتاج كمية مادة شوارد HO −المعايرة:
اعتمادا على طريقة المماسين VA, E = 25 mL :وعليه:
0.5 0.5
n ( HO − ) = C A .VA, E = 5 10−4 mol.L−1
.3.4حساب كتلة الحمض C13 H18O2الموجود في القرص ،واستنتاج نسبته الكتلية:
0.5
2x0.25 n0 = CB .V − n ( HO − ) = 3,5 10−2 0,1 − 5 10−4 = 3 10−3 mol
→ m0 = n0 .M = 0,618 g
m0 0,618
=P = 100 100 = 67,17%
m 0,920
التمرين التجريبي 06( :نقاط)
.Iغلق القاطعة:
1 2x0.5 .1حساب شدة التيار األعظمي ،ثم استنتاج قيمة الطاقة المغناطيسية في الوشيعة:
E 1
I '0 = = 0,06 A → Eb ( ) = L.I '02 = 1,8 10−4 J
R 2
.2حساب الطاقة المغناطيسية في الوشيعة في النظام الدائم:
1 2x0.5 E 1
= I0 = 0,05 A → Eb ( ) = L.I 02 = 1,25 10−4 J
R+r 2
.IIدراسة غلق القاطعة للوشيعة ) : ( b2
.1تحديد أهمية النواة الحديدية :الرفع من ذاتية الوشيعة (الفعل التحريضي)
0.25 0.25
.2إيجاد المعادلة التفاضلية المميزة لشدة التيار:
0.75 0..75 di di R + r E
ub + u R = E → L ' + r.i + R.i = E → + = i بتطبيق قانون جمع التوترات:
dt dt 'L 'L
.1.3 .3إيجاد عبارة ثابت الزمن :
باشتقاق عبارة ) i (tوتعويضها في المعادلة التفاضلية ،نجد:
صفحة 10من 11
األستاذ :بوزيان زكرياء الشعب :تقني رياضي ورياضي تابع لإلجابة النموذجية للبكالوريا التجريبي 2024
t t t t
I 0 − R + r
e +
−
I 0 − I 0 .e
E I −
= → 0e − R + r −
I 0 .e +
( R + r ) I0 = E
L L L L L
0.75 0.75
t 0
− 1
R + r ( R + r ) I0 − E L
→ I 0e − + = = 0 →
L L R+r
.2.3تأكد من تجانس مع الزمن:
u t
0.5 0.5
L L i
= منه متجانس مع الزمن ووحدته ) . ( s = → = = t = T
RT R u
i
) di (
: .1.4 .4تبيان عبارة
dt
t
di ( t ) I 0 − di ( ) I 0 − I ) di ( E. RT
0.75 0.75 → = e → = e = 0,37 0 = 0,37
dt dt dt L '. RT
) di ( E. RT ) di ( E
→ = 0,37 → = 0,37
dt L '. RT dt 'L
.2.4استنتاج قيمة ' Lوثابت الزمن :
= 5 10−3 s
0.5 di E E 6 L
2x0.25 = '= → L = = = 0,6 H ;
' dt t =0 L di 10 R+r
dt t =0
مالحظة :يمكن توظيف عبارة السؤال (.)1.4
.5تحديد الشكل المناسب :هو الشكل9.
0.5 0.5
عند اللحظة ، t = 0وبتطبيق قانون جمع التوتراتub ( 0) + uR ( 0) = 0 → ub ( 0) = −uR ( 0) :
صفحة 11من 11
You might also like
- Bac2023 Physics MTM CorrectionDocument11 pagesBac2023 Physics MTM Correctionveterinaire37No ratings yet
- Correction Bac Physics Math 2023Document11 pagesCorrection Bac Physics Math 2023daya bouNo ratings yet
- Correction Bac Se Physique 2017Document9 pagesCorrection Bac Se Physique 2017Yacine Ben BrahimNo ratings yet
- Correction Bac Se Physique 2017Document9 pagesCorrection Bac Se Physique 2017Alaa Eddine NouiNo ratings yet
- الإجابة النموذجية وسلم التنقيطDocument5 pagesالإجابة النموذجية وسلم التنقيطKHALED KHALEDNo ratings yet
- تصحيح الموضوع الأولDocument7 pagesتصحيح الموضوع الأولYacine AmraneNo ratings yet
- فرض محروس رقم 3 الدورة الأولى ع ف 2012 2013 2 1Document2 pagesفرض محروس رقم 3 الدورة الأولى ع ف 2012 2013 2 1المتفوق في المعلومياتNo ratings yet
- Exo TerminalDocument11 pagesExo TerminalshadowNo ratings yet
- 8Document2 pages8e.maskarNo ratings yet
- EXO de Physique Nucleaire 2bac PC/SMDocument4 pagesEXO de Physique Nucleaire 2bac PC/SMHAKIM ELOUARDE100% (2)
- فرض محروس 1 الدورة 2Document2 pagesفرض محروس 1 الدورة 2Mouhibi AbdellahNo ratings yet
- lateur1الأختبار الثاني 2008-2009 الجزائرDocument2 pageslateur1الأختبار الثاني 2008-2009 الجزائرassembleur7777100% (1)
- PDF Walido 1631808330Document7 pagesPDF Walido 1631808330Nor HanNo ratings yet
- _Document25 pages_Mouhand MhendNo ratings yet
- التتبع الزمني الموجات الضوئية و الصوتيةDocument2 pagesالتتبع الزمني الموجات الضوئية و الصوتيةYassineNo ratings yet
- 2xp Xam Watani 2011 Dawra 3adiyaDocument12 pages2xp Xam Watani 2011 Dawra 3adiyaassad saisNo ratings yet
- تصحيح-المقترح-رقم-01-علوم-تجريبيةDocument4 pagesتصحيح-المقترح-رقم-01-علوم-تجريبيةdzphysique48No ratings yet
- Dzexams Docs 3as 907323Document6 pagesDzexams Docs 3as 907323Mãrch MelløNo ratings yet
- Sujet_09_Bac2024Document4 pagesSujet_09_Bac2024dzphysique48No ratings yet
- ملخص البيانات في النوويDocument5 pagesملخص البيانات في النوويLamia LamiaNo ratings yet
- (simplex) حل السلسلة رقم 03 طريقةDocument4 pages(simplex) حل السلسلة رقم 03 طريقةMelki Ameur100% (1)
- 06 2b Prof Soufiane ChakirDocument3 pages06 2b Prof Soufiane ChakirAbderrazak AFERYADNo ratings yet
- UntitledDocument2 pagesUntitledothman HassounNo ratings yet
- ExPhyCorr U6Document15 pagesExPhyCorr U6chahinez MecherrakNo ratings yet
- موضوع_المراجعة-الشاملةDocument5 pagesموضوع_المراجعة-الشاملةdzphysique48No ratings yet
- تصحيح اختبار فيزياء - شعبة ع تجDocument12 pagesتصحيح اختبار فيزياء - شعبة ع تجBerragouba BerragoubaNo ratings yet
- Bbl14MTM BrahimDocument8 pagesBbl14MTM Brahimعبد العزيز مروىNo ratings yet
- Phy3 Serie 3Document4 pagesPhy3 Serie 3جمال سينغNo ratings yet
- M2EMB-modelisation FinanciereDocument2 pagesM2EMB-modelisation Financieremohrez2002No ratings yet
- الحركة،مبدأ القصـ, الذرة 1Document3 pagesالحركة،مبدأ القصـ, الذرة 1assurance.ilham.zitouniNo ratings yet
- 31RRDocument3 pages31RRChaimaa BaghdadiNo ratings yet
- فرض محروس 2 ع رDocument1 pageفرض محروس 2 ع رMajed GharibNo ratings yet
- سلسلة تمارين 4Document2 pagesسلسلة تمارين 4soulato47No ratings yet
- الاجابة النموذجية مع سلم التنقيطDocument8 pagesالاجابة النموذجية مع سلم التنقيطal maktabaNo ratings yet
- - www.svt: ةظحللا دنع t =4ms نوكي،: u =1V يلاتلابو: E (t) = ⁶ نيتظحللا نيب ةيئابرهكلا ةقاطلا ريغت t و tDocument4 pages- www.svt: ةظحللا دنع t =4ms نوكي،: u =1V يلاتلابو: E (t) = ⁶ نيتظحللا نيب ةيئابرهكلا ةقاطلا ريغت t و tIssam IssamNo ratings yet
- فرض محروس رقم 1 في مادة الفيزياء والكيمياء 2015 2016 السنة الثانية بكالوريا علوم رياضية الدورة الثانية من إنجاز الأستاذ رشيد جنكلDocument2 pagesفرض محروس رقم 1 في مادة الفيزياء والكيمياء 2015 2016 السنة الثانية بكالوريا علوم رياضية الدورة الثانية من إنجاز الأستاذ رشيد جنكلTahiri MehdiNo ratings yet
- 8-اختبار الابار الغازية (تابع الجريان المتتابع)Document10 pages8-اختبار الابار الغازية (تابع الجريان المتتابع)Oussama ChabbiNo ratings yet
- تصحيح إمتحان رياضيات-2021Document5 pagesتصحيح إمتحان رياضيات-2021soumaya guittNo ratings yet
- Math M Bac2017 CorrectionDocument9 pagesMath M Bac2017 Correctionlamichi boudjemaaNo ratings yet
- 265Document2 pages265e.maskarNo ratings yet
- DS1S2SVT 2013 - 2Document2 pagesDS1S2SVT 2013 - 2SiMo ElbNo ratings yet
- 3AS U02 - E3 - Cour-Exe 02 PDFDocument22 pages3AS U02 - E3 - Cour-Exe 02 PDFAmina ZouaouiNo ratings yet
- ـ نشاط عينة مشعDocument4 pagesـ نشاط عينة مشعHicham MarzouqNo ratings yet
- ـ نشاط عينة مشعDocument4 pagesـ نشاط عينة مشعHicham MarzouqNo ratings yet
- ـ نشاط عينة مشعDocument4 pagesـ نشاط عينة مشعHicham MarzouqNo ratings yet
- ـ نشاط عينة مشعDocument4 pagesـ نشاط عينة مشعHicham MarzouqNo ratings yet
- السلسلة 1 لمقياس احصاء3 السنة 2 مالية ومحاسبةDocument1 pageالسلسلة 1 لمقياس احصاء3 السنة 2 مالية ومحاسبةGraZerFFNo ratings yet
- سلسلسة رقم 3 الدورة الأولى التحولات النووية 2014 2015Document3 pagesسلسلسة رقم 3 الدورة الأولى التحولات النووية 2014 2015debbab Ahmed mrhbaNo ratings yet
- سلسلسة رقم 3 الدورة الأولى التحولات النووية 2014 2015Document3 pagesسلسلسة رقم 3 الدورة الأولى التحولات النووية 2014 2015debbab Ahmed mrhbaNo ratings yet
- Math4 - MshLa2y - Lec 4 (Wave&heat)Document16 pagesMath4 - MshLa2y - Lec 4 (Wave&heat)ahmedhusseinkamelNo ratings yet
- التوزنات الكيميائية و التحولات النووية 5Document1 pageالتوزنات الكيميائية و التحولات النووية 5Yassine100% (2)
- التوزنات الكيميائية و التحولات النووية 5Document1 pageالتوزنات الكيميائية و التحولات النووية 5YassineNo ratings yet
- TD UdDocument2 pagesTD UdboustakatbNo ratings yet
- تصحيح البكالوريا التجريبية علوم تجريبية 2020 2021Document11 pagesتصحيح البكالوريا التجريبية علوم تجريبية 2020 2021dzphysique48No ratings yet
- الطاقة الكامنة الفتلية-عمل مخبريDocument3 pagesالطاقة الكامنة الفتلية-عمل مخبريLynda LiliNo ratings yet
- Dzexams 3as Physique d2 20201 1502131Document7 pagesDzexams 3as Physique d2 20201 1502131yacine yacineNo ratings yet
- نص الموضوع 04Document4 pagesنص الموضوع 04Ana Oum AwladiNo ratings yet
- 2 BacDocument3 pages2 BacF-e FaresNo ratings yet
- c1 s2 PC TC Ar 20152016 Prof - Rabia (1) (WWW - Pc1.ma)Document2 pagesc1 s2 PC TC Ar 20152016 Prof - Rabia (1) (WWW - Pc1.ma)hppc07157No ratings yet