Professional Documents
Culture Documents
Bài 9-10 Nhóm 4- Tổ 5- Nguyễn Quốc Hưng-Nguyễn Phan Hồng Ngọc-Trương Thị Mỹ Thanh
Bài 9-10 Nhóm 4- Tổ 5- Nguyễn Quốc Hưng-Nguyễn Phan Hồng Ngọc-Trương Thị Mỹ Thanh
Uploaded by
chau9804Copyright:
Available Formats
You might also like
- Bài 8Document8 pagesBài 8Trần Thuý Quỳnh100% (1)
- Báo Cáo Thí Nghiệm Hóa Vô Cơ Bài 8Document7 pagesBáo Cáo Thí Nghiệm Hóa Vô Cơ Bài 8Hà Thế VinhNo ratings yet
- Bài 10Document5 pagesBài 10Vũ lê Minh PhongNo ratings yet
- Báo cáo thí nghiệm Bài 5Document5 pagesBáo cáo thí nghiệm Bài 5Tường Vy Bùi ĐỗNo ratings yet
- Bài 10Document7 pagesBài 10doannga2702No ratings yet
- Báo Cáo TN Hóa Vô Cơ Bài 5Document4 pagesBáo Cáo TN Hóa Vô Cơ Bài 5Huỳnh Diễm QuyNo ratings yet
- NHẬN BIẾT CÁC CHẤT HỮU CƠDocument4 pagesNHẬN BIẾT CÁC CHẤT HỮU CƠQuan DaoNo ratings yet
- BÁO CÁO THÍ NGHIỆM HVC BÀI 1Document7 pagesBÁO CÁO THÍ NGHIỆM HVC BÀI 1Tường Vy Bùi ĐỗNo ratings yet
- báo cáo cuối bài 1Document5 pagesbáo cáo cuối bài 1Huong NguyenNo ratings yet
- Bài 2 Kim Loại Kiềm ThổDocument7 pagesBài 2 Kim Loại Kiềm ThổHan NgNo ratings yet
- Tổng Ôn Phần Tự Luận (Full Dạng Theo Ma Trận)Document6 pagesTổng Ôn Phần Tự Luận (Full Dạng Theo Ma Trận)vvctriNo ratings yet
- Đáp Án Thi TH Chuyên Hoá Lam Sơn 2024 2025Document6 pagesĐáp Án Thi TH Chuyên Hoá Lam Sơn 2024 2025hoangdungdtdNo ratings yet
- BÁO CÁO THÍ NGHIỆM BÀI 12 1Document11 pagesBÁO CÁO THÍ NGHIỆM BÀI 12 1Thanh NghiNo ratings yet
- Bài 7Document12 pagesBài 7Khánh LươngNo ratings yet
- Chương 3 - Phân KaliDocument19 pagesChương 3 - Phân KaliHậu NguyễnNo ratings yet
- 027 Chuyên Đề 27 Các Dạng Bài Tập KLK - KLKTDocument29 pages027 Chuyên Đề 27 Các Dạng Bài Tập KLK - KLKTnguyenthithaomy291005No ratings yet
- PEA GEN 2 Chuyên đề mẫu môn HóaDocument16 pagesPEA GEN 2 Chuyên đề mẫu môn HóaHợp NguyễnNo ratings yet
- Đề Cương TT Hoá Phân Tích 1Document10 pagesĐề Cương TT Hoá Phân Tích 1Vĩnh ThuầnNo ratings yet
- Tinh Khu Cua HCLDocument60 pagesTinh Khu Cua HCLLê Phú QuốcNo ratings yet
- CHUẨN BỊ BÀI THÍ NGHIỆM SỐ 1Document4 pagesCHUẨN BỊ BÀI THÍ NGHIỆM SỐ 122128139No ratings yet
- Báo Cáo TH C Hành Hóa Dư C - Bài 1 - Nhóm 3Document6 pagesBáo Cáo TH C Hành Hóa Dư C - Bài 1 - Nhóm 3Nguyễn Hoàng LêNo ratings yet
- Báo Cáo Thí Nghiệm Bài 1Document7 pagesBáo Cáo Thí Nghiệm Bài 1nguyendinhgiahuy2206No ratings yet
- BÁO CÁO THÍ NGHIỆM BÀI 1Document8 pagesBÁO CÁO THÍ NGHIỆM BÀI 1468nhatNo ratings yet
- Đề thi HSG Thai Binh 07-08Document4 pagesĐề thi HSG Thai Binh 07-08dtg0909No ratings yet
- Hoa Phan Tich 1Document10 pagesHoa Phan Tich 1QuiLeNo ratings yet
- Ôn Tap Theo Chu de Hoa 11-Hk1-2022 - Phung DangDocument7 pagesÔn Tap Theo Chu de Hoa 11-Hk1-2022 - Phung DangMinh Nguyễn LêNo ratings yet
- Bài 4Document15 pagesBài 4Vy PhamNo ratings yet
- Bài 9 §1. Xác Định Hàm Lượng Amoni Trong Đất Bằng Phương Pháp So Màu Với Thuốc Thư Nessle 9.1. Nguyên TắcDocument5 pagesBài 9 §1. Xác Định Hàm Lượng Amoni Trong Đất Bằng Phương Pháp So Màu Với Thuốc Thư Nessle 9.1. Nguyên TắcLong PhạmNo ratings yet
- Tailieumienphi - VN Tuyen Tap 10 Nam de Thi Olympic 30 4 Mon Hoa Hoc 10Document34 pagesTailieumienphi - VN Tuyen Tap 10 Nam de Thi Olympic 30 4 Mon Hoa Hoc 10Long Nguyễn ThếNo ratings yet
- Báo Cáo TH C Hành Hóa 6 Chinh SuaDocument10 pagesBáo Cáo TH C Hành Hóa 6 Chinh SuaQuangNo ratings yet
- Ôn Tập TH Hóa Vô CơDocument24 pagesÔn Tập TH Hóa Vô Cơphùng lê tuấnNo ratings yet
- Bai 34 Crom Va Hop Chat Cua CromDocument28 pagesBai 34 Crom Va Hop Chat Cua CromB22DCDT058Nguyễn Tiến DũngNo ratings yet
- HN 2022HDC - de Chinh ThucDocument8 pagesHN 2022HDC - de Chinh ThucNhật Minh NguyễnNo ratings yet
- BCN2 THHDocument14 pagesBCN2 THHTran Quynh TrangNo ratings yet
- Ly Thuyet Crom - TTDocument4 pagesLy Thuyet Crom - TTThị Thùy Dương PhanNo ratings yet
- BÀI 5 TH Hóa Vô CơDocument6 pagesBÀI 5 TH Hóa Vô CơMỹ Như Lê NguyễnNo ratings yet
- Báo Cáo Tn Bài 2: Dung Dịch: 1. Kết Quả Thí Nghiệm: A. Tích số tan: 1. Điều kiện hình thành tủaDocument5 pagesBáo Cáo Tn Bài 2: Dung Dịch: 1. Kết Quả Thí Nghiệm: A. Tích số tan: 1. Điều kiện hình thành tủaNgọc TrânNo ratings yet
- Bac Ninh 16-17Document5 pagesBac Ninh 16-17Nguyễn Đăng Nhật MinhNo ratings yet
- TĂNG GIẢM KHỐI LƯỢNGDocument9 pagesTĂNG GIẢM KHỐI LƯỢNGbi_hpu2No ratings yet
- ôn tập hóa đại cươngDocument18 pagesôn tập hóa đại cươngPhương ThảoNo ratings yet
- Trinhdinhngoc N06 Bai7Document7 pagesTrinhdinhngoc N06 Bai7Trịnh Đình NgọcNo ratings yet
- Baocao TN Hoa - CNSHDocument18 pagesBaocao TN Hoa - CNSHnmai87733No ratings yet
- Hà Nội 2018- Giải chi tiếtDocument7 pagesHà Nội 2018- Giải chi tiếtDiễm NguyễnNo ratings yet
- Demo 8-10Document9 pagesDemo 8-10Võ Phát ĐạtNo ratings yet
- De Hoc Sinh Gioi Cap Truong Hoa Hoc 10 Nam 2020 2021 Truong THPT Minh Chau Hung YenDocument7 pagesDe Hoc Sinh Gioi Cap Truong Hoa Hoc 10 Nam 2020 2021 Truong THPT Minh Chau Hung YenLê Mạnh DũngNo ratings yet
- CK Che Bien KS 1 16012023Document18 pagesCK Che Bien KS 1 16012023Trịnh HuyNo ratings yet
- On Tap Chuong CSiDocument8 pagesOn Tap Chuong CSiPhạm Xuân ĐồngNo ratings yet
- THÍ NGHIỆM HÓA VÔ CƠ BÀI 6Document2 pagesTHÍ NGHIỆM HÓA VÔ CƠ BÀI 6Chanh Tran100% (3)
- báo cáo Hóa vô cơ thí nghiệmDocument34 pagesbáo cáo Hóa vô cơ thí nghiệmTRƯƠNG Châu KhánhNo ratings yet
- Bai 1-ND2Document6 pagesBai 1-ND2namphamthanh69No ratings yet
- Báo Cáo Thí Nghiệm Bài 10Document6 pagesBáo Cáo Thí Nghiệm Bài 10drjg7v45840% (1)
- Tiên L 20 21Document6 pagesTiên L 20 21Cường PhạmNo ratings yet
- 43 - KCL - 01.12.2023Document8 pages43 - KCL - 01.12.2023Tâm NguyễnNo ratings yet
- Bài thí nghiệm Vô cơ - Điện hóaDocument10 pagesBài thí nghiệm Vô cơ - Điện hóasan chueNo ratings yet
- Ly Thuyet Va Bai Tap Ve Muoi 1Document3 pagesLy Thuyet Va Bai Tap Ve Muoi 1Trần Khải Phương 9/2No ratings yet
- h9. Tphcm. 2016-2017.tran Le Lieu ThanhDocument8 pagesh9. Tphcm. 2016-2017.tran Le Lieu ThanhHOÀNG VIỆT William NguyễnNo ratings yet
- Nhom 5 K2Cr2O7Document32 pagesNhom 5 K2Cr2O7Vũ HạNo ratings yet
- Ly Thuyet Va Bai Tap Ve Muoi 1Document3 pagesLy Thuyet Va Bai Tap Ve Muoi 138.Lê Thị Mai PhươngNo ratings yet
Bài 9-10 Nhóm 4- Tổ 5- Nguyễn Quốc Hưng-Nguyễn Phan Hồng Ngọc-Trương Thị Mỹ Thanh
Bài 9-10 Nhóm 4- Tổ 5- Nguyễn Quốc Hưng-Nguyễn Phan Hồng Ngọc-Trương Thị Mỹ Thanh
Uploaded by
chau9804Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Bài 9-10 Nhóm 4- Tổ 5- Nguyễn Quốc Hưng-Nguyễn Phan Hồng Ngọc-Trương Thị Mỹ Thanh
Bài 9-10 Nhóm 4- Tổ 5- Nguyễn Quốc Hưng-Nguyễn Phan Hồng Ngọc-Trương Thị Mỹ Thanh
Uploaded by
chau9804Copyright:
Available Formats
BÁO CÁO THÍ NGHIỆM HÓA VÔ CƠ_602033
N08 ngày 6/4/2024
1) Vũ Nguyễn Ngọc Châu - 62200227
2) Lê Hoàng Anh - 62200053
Bài 9: CÁC NGUYÊN TỐ PHÂN NHÓM VIB-CRÔM
I) DỤNG CỤ HÓA CHẤT
DỤNG CỤ HÓA CHẤT
-Cối và chày -K2Cr2O7 khan, dung dịch
-Chén niken -Carbon khan
-Đèn cồn -Nước cất
-Becher -Axit H2SO4, HCl
-Đũa thủy tinh -Dung dịch cồn 95o
-Ống nghiệm -CrCl3 khan
-Giá đỡ -Dung dịch NaOH
-Pipet -Dung dịch muối NaNO2
-Thao nước
-Lò nung
II) THÍ NGHIỆM
TN Quy trình-Hiện tượng Hình ảnh
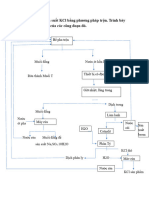
TN1: Điều chế và tính - 2,55g K2Cr2O7 và 0,98g C cho vào cối trộn 2,55g K2Cr2O7
chất của Oxit crom. và nghiền mịn hỗn hợp
- Cho hỗn hợp vào chén Niken đốt trên đèn
cồn khoảng 10 phút,nung ở 600oC trong 1
giờ.
- Để nguội, hòa tan sản phẩm trong nước, lọc,
sấy khô, cân.
- Trộn và nghiền mịn nhằm tăng diện tích 0,98g C
tiếp xúc, tăng tốc dộ phản ứng
- PTHH:
2C + K2Cr2O7 CO + K2CO3 + Cr2O3 (to)
- Sản phẩm thu được là Cr2O3 có màu lục sẫm
- Tính toán: 2,55
nK2Cr2O7 =
39.2+52.2+16.7
17
= mol Trộn và nghiền mịn
1960
nC = 0,98 = 49
mol
12 600 17 49
Ta có nK2Cr2O7 < nC/2 ( < ) nên tính
1960 1200
theo nK2Cr2O7
=> nCr2O3 = 17 mol
1960
17.( 52.2+16.3)
=> mCr2O3 lý thuyết = = 1,318g Cho vào chén Niken đốt trên
1960
đèn cồn
Ta có: mCr2O3 thực tế = 0.95 g
Hiệu suất
mlt.100% 0.95 .100%
H= mtt = 1,318 = 72%
Hỗn hợp sau nung
Hòa tan, lọc thu sản phẩm
Sấy, cân sản phẩm: m=0.95 g
TN2: Điều chế phèn - Hòa tan 5g K2Cr2O7 với 25ml nước cất, 5 g K2Cr2O7 hòa tan với
Crom. khuấy đều 25ml nước cất
Cr2(SO4)3.K2SO4.24H2O - Cho từng giọt đến 5ml H2SO4 đậm đặc vào
becher, lắc đều, để nguội, ngâm vào chậu
nước
- Cho từ từ 3ml cồn 95oC vào, lắc đều, để
nguội rồi làm lạnh bằng nước đá đến khi tinh
thể phèn xuất hiện, lọc chân không, cân, tính
hiệu suất
- Màu cam là màu của dung dịch K2Cr2O7 Thêm 5ml H2SO4 đậm đặc
- Khi cho H2SO4 đặc dung dịch đậm màu
hơn, có tỏa nhiệt
- PTHH:
K2Cr2O7 + H2SO4 K2SO4 +2CrO3 + H2O
- Giải thích: H2SO4 đặc và CrO3 lấy nước của
dung dịch làm màu đậm hơn
Thêm 3ml cồn 95o
- Khi để nguội cho thêm cồn dung dịch
chuyển sang màu xanh đậm, khí sốc mùi
chua
-PTHH: 2CrO3 + 3H2SO4 + 2C2H5OH
Cr2(SO4)3 + CH3CHO + CH3COOH + 5H2O
- Giải thích: mùi sốc là mùi của CH 3CHO,
mùi chua là CH3COOH, màu xanh là màu
của Cr3+ Làm lạnh
-Tinh thể thu được có màu xanh đen
-Trong dung dịch có mặt 2 muối Cr2(SO4)3
và K2SO4. Sản phẩm kết tinh thu được là
phèn crom Cr2(SO4)3.K2SO4.24H2O
- PTHH:
Cr2(SO4)3 + K2SO4 + 24H2O
Cr2(SO4)3.K2SO4.24H2O
TN3: Tính chất các hợp -Lấy 1 ít tinh thể CrCl3 cho vào 1 ống Dung dịch CrCl3
3+
chất Cr . nghiệm, hòa tan CrCl3 trong nước lạnh, ta
thấy dung dịch
màu xanh lá.
-Nhỏ từ từ dung dịch NaOH loãng vừa đủ
vào ,xuất hiện kết tủa xám trắng và dung
dịch nhạt dân.
-Khi cho dung dịch CrCl3 tác dụng với NaOH
ta thu được kết tủa màu xanh xám. Đó là màu
của Cr3+ CrCl3 + NaOH
CrCl3 + 3NaOH → Cr(OH)3 + 3NaCl
-Lấy kết tủa cho vào 2 ống nghiệm khác
nhau:
Ống 1: thử tác dụng với acid HCl loãng , kết
tủa tan, dung dịch màu xanh dương.
Cr(OH)3 + 3HCl → CrCl3 + 3H2O
Ống 2: thử tác dụng với lượng dư
NaOH loãng,kết tủa tan dung dịch màu
xanh lá. Cr(OH)3 + 3NaOH →
Na3[Cr(OH)6] Ống 1
Kết luận: Cr(OH)3 có tính lưỡng tính
Ống 2:
You might also like
- Bài 8Document8 pagesBài 8Trần Thuý Quỳnh100% (1)
- Báo Cáo Thí Nghiệm Hóa Vô Cơ Bài 8Document7 pagesBáo Cáo Thí Nghiệm Hóa Vô Cơ Bài 8Hà Thế VinhNo ratings yet
- Bài 10Document5 pagesBài 10Vũ lê Minh PhongNo ratings yet
- Báo cáo thí nghiệm Bài 5Document5 pagesBáo cáo thí nghiệm Bài 5Tường Vy Bùi ĐỗNo ratings yet
- Bài 10Document7 pagesBài 10doannga2702No ratings yet
- Báo Cáo TN Hóa Vô Cơ Bài 5Document4 pagesBáo Cáo TN Hóa Vô Cơ Bài 5Huỳnh Diễm QuyNo ratings yet
- NHẬN BIẾT CÁC CHẤT HỮU CƠDocument4 pagesNHẬN BIẾT CÁC CHẤT HỮU CƠQuan DaoNo ratings yet
- BÁO CÁO THÍ NGHIỆM HVC BÀI 1Document7 pagesBÁO CÁO THÍ NGHIỆM HVC BÀI 1Tường Vy Bùi ĐỗNo ratings yet
- báo cáo cuối bài 1Document5 pagesbáo cáo cuối bài 1Huong NguyenNo ratings yet
- Bài 2 Kim Loại Kiềm ThổDocument7 pagesBài 2 Kim Loại Kiềm ThổHan NgNo ratings yet
- Tổng Ôn Phần Tự Luận (Full Dạng Theo Ma Trận)Document6 pagesTổng Ôn Phần Tự Luận (Full Dạng Theo Ma Trận)vvctriNo ratings yet
- Đáp Án Thi TH Chuyên Hoá Lam Sơn 2024 2025Document6 pagesĐáp Án Thi TH Chuyên Hoá Lam Sơn 2024 2025hoangdungdtdNo ratings yet
- BÁO CÁO THÍ NGHIỆM BÀI 12 1Document11 pagesBÁO CÁO THÍ NGHIỆM BÀI 12 1Thanh NghiNo ratings yet
- Bài 7Document12 pagesBài 7Khánh LươngNo ratings yet
- Chương 3 - Phân KaliDocument19 pagesChương 3 - Phân KaliHậu NguyễnNo ratings yet
- 027 Chuyên Đề 27 Các Dạng Bài Tập KLK - KLKTDocument29 pages027 Chuyên Đề 27 Các Dạng Bài Tập KLK - KLKTnguyenthithaomy291005No ratings yet
- PEA GEN 2 Chuyên đề mẫu môn HóaDocument16 pagesPEA GEN 2 Chuyên đề mẫu môn HóaHợp NguyễnNo ratings yet
- Đề Cương TT Hoá Phân Tích 1Document10 pagesĐề Cương TT Hoá Phân Tích 1Vĩnh ThuầnNo ratings yet
- Tinh Khu Cua HCLDocument60 pagesTinh Khu Cua HCLLê Phú QuốcNo ratings yet
- CHUẨN BỊ BÀI THÍ NGHIỆM SỐ 1Document4 pagesCHUẨN BỊ BÀI THÍ NGHIỆM SỐ 122128139No ratings yet
- Báo Cáo TH C Hành Hóa Dư C - Bài 1 - Nhóm 3Document6 pagesBáo Cáo TH C Hành Hóa Dư C - Bài 1 - Nhóm 3Nguyễn Hoàng LêNo ratings yet
- Báo Cáo Thí Nghiệm Bài 1Document7 pagesBáo Cáo Thí Nghiệm Bài 1nguyendinhgiahuy2206No ratings yet
- BÁO CÁO THÍ NGHIỆM BÀI 1Document8 pagesBÁO CÁO THÍ NGHIỆM BÀI 1468nhatNo ratings yet
- Đề thi HSG Thai Binh 07-08Document4 pagesĐề thi HSG Thai Binh 07-08dtg0909No ratings yet
- Hoa Phan Tich 1Document10 pagesHoa Phan Tich 1QuiLeNo ratings yet
- Ôn Tap Theo Chu de Hoa 11-Hk1-2022 - Phung DangDocument7 pagesÔn Tap Theo Chu de Hoa 11-Hk1-2022 - Phung DangMinh Nguyễn LêNo ratings yet
- Bài 4Document15 pagesBài 4Vy PhamNo ratings yet
- Bài 9 §1. Xác Định Hàm Lượng Amoni Trong Đất Bằng Phương Pháp So Màu Với Thuốc Thư Nessle 9.1. Nguyên TắcDocument5 pagesBài 9 §1. Xác Định Hàm Lượng Amoni Trong Đất Bằng Phương Pháp So Màu Với Thuốc Thư Nessle 9.1. Nguyên TắcLong PhạmNo ratings yet
- Tailieumienphi - VN Tuyen Tap 10 Nam de Thi Olympic 30 4 Mon Hoa Hoc 10Document34 pagesTailieumienphi - VN Tuyen Tap 10 Nam de Thi Olympic 30 4 Mon Hoa Hoc 10Long Nguyễn ThếNo ratings yet
- Báo Cáo TH C Hành Hóa 6 Chinh SuaDocument10 pagesBáo Cáo TH C Hành Hóa 6 Chinh SuaQuangNo ratings yet
- Ôn Tập TH Hóa Vô CơDocument24 pagesÔn Tập TH Hóa Vô Cơphùng lê tuấnNo ratings yet
- Bai 34 Crom Va Hop Chat Cua CromDocument28 pagesBai 34 Crom Va Hop Chat Cua CromB22DCDT058Nguyễn Tiến DũngNo ratings yet
- HN 2022HDC - de Chinh ThucDocument8 pagesHN 2022HDC - de Chinh ThucNhật Minh NguyễnNo ratings yet
- BCN2 THHDocument14 pagesBCN2 THHTran Quynh TrangNo ratings yet
- Ly Thuyet Crom - TTDocument4 pagesLy Thuyet Crom - TTThị Thùy Dương PhanNo ratings yet
- BÀI 5 TH Hóa Vô CơDocument6 pagesBÀI 5 TH Hóa Vô CơMỹ Như Lê NguyễnNo ratings yet
- Báo Cáo Tn Bài 2: Dung Dịch: 1. Kết Quả Thí Nghiệm: A. Tích số tan: 1. Điều kiện hình thành tủaDocument5 pagesBáo Cáo Tn Bài 2: Dung Dịch: 1. Kết Quả Thí Nghiệm: A. Tích số tan: 1. Điều kiện hình thành tủaNgọc TrânNo ratings yet
- Bac Ninh 16-17Document5 pagesBac Ninh 16-17Nguyễn Đăng Nhật MinhNo ratings yet
- TĂNG GIẢM KHỐI LƯỢNGDocument9 pagesTĂNG GIẢM KHỐI LƯỢNGbi_hpu2No ratings yet
- ôn tập hóa đại cươngDocument18 pagesôn tập hóa đại cươngPhương ThảoNo ratings yet
- Trinhdinhngoc N06 Bai7Document7 pagesTrinhdinhngoc N06 Bai7Trịnh Đình NgọcNo ratings yet
- Baocao TN Hoa - CNSHDocument18 pagesBaocao TN Hoa - CNSHnmai87733No ratings yet
- Hà Nội 2018- Giải chi tiếtDocument7 pagesHà Nội 2018- Giải chi tiếtDiễm NguyễnNo ratings yet
- Demo 8-10Document9 pagesDemo 8-10Võ Phát ĐạtNo ratings yet
- De Hoc Sinh Gioi Cap Truong Hoa Hoc 10 Nam 2020 2021 Truong THPT Minh Chau Hung YenDocument7 pagesDe Hoc Sinh Gioi Cap Truong Hoa Hoc 10 Nam 2020 2021 Truong THPT Minh Chau Hung YenLê Mạnh DũngNo ratings yet
- CK Che Bien KS 1 16012023Document18 pagesCK Che Bien KS 1 16012023Trịnh HuyNo ratings yet
- On Tap Chuong CSiDocument8 pagesOn Tap Chuong CSiPhạm Xuân ĐồngNo ratings yet
- THÍ NGHIỆM HÓA VÔ CƠ BÀI 6Document2 pagesTHÍ NGHIỆM HÓA VÔ CƠ BÀI 6Chanh Tran100% (3)
- báo cáo Hóa vô cơ thí nghiệmDocument34 pagesbáo cáo Hóa vô cơ thí nghiệmTRƯƠNG Châu KhánhNo ratings yet
- Bai 1-ND2Document6 pagesBai 1-ND2namphamthanh69No ratings yet
- Báo Cáo Thí Nghiệm Bài 10Document6 pagesBáo Cáo Thí Nghiệm Bài 10drjg7v45840% (1)
- Tiên L 20 21Document6 pagesTiên L 20 21Cường PhạmNo ratings yet
- 43 - KCL - 01.12.2023Document8 pages43 - KCL - 01.12.2023Tâm NguyễnNo ratings yet
- Bài thí nghiệm Vô cơ - Điện hóaDocument10 pagesBài thí nghiệm Vô cơ - Điện hóasan chueNo ratings yet
- Ly Thuyet Va Bai Tap Ve Muoi 1Document3 pagesLy Thuyet Va Bai Tap Ve Muoi 1Trần Khải Phương 9/2No ratings yet
- h9. Tphcm. 2016-2017.tran Le Lieu ThanhDocument8 pagesh9. Tphcm. 2016-2017.tran Le Lieu ThanhHOÀNG VIỆT William NguyễnNo ratings yet
- Nhom 5 K2Cr2O7Document32 pagesNhom 5 K2Cr2O7Vũ HạNo ratings yet
- Ly Thuyet Va Bai Tap Ve Muoi 1Document3 pagesLy Thuyet Va Bai Tap Ve Muoi 138.Lê Thị Mai PhươngNo ratings yet